鲁科版高中化学必修一第一章第三节常用的物理量物质的量第三课时课件
文档属性
| 名称 | 鲁科版高中化学必修一第一章第三节常用的物理量物质的量第三课时课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-24 00:00:00 | ||
图片预览







文档简介
(共26张PPT)
第三节 化学中常用的物理量
——物质的量
第3课时 物质的量浓度
鲁科版2019必修第一册
第一章 认识化学科学
回顾旧知
你曾学过的表示溶液浓度的物理量是什么?
溶质的质量分数(ω)=
溶质的质量
溶液的质量
×100%
溶质的质量
溶质的质量+溶剂的质量
×100%
=
活动·探究 配制一定物质的量浓度的溶液
实验目的
实验室计划配制0.1L的NaCl溶液,其中溶质的物质的量为0.04mol。请你利用实验室的固体氯化钠完成任务。
检验程序:加水→塞瓶塞→倒立→查漏→正立,瓶塞旋转180°→倒立→查漏。
具体方法是:往瓶内加水,塞好瓶塞(瓶口和瓶塞要干,且不涂任何油脂等),用食指顶住瓶塞,另一只手托住瓶底把瓶倒立过来,观察瓶塞周围是否有水漏出,如不漏水,把瓶塞旋转180°塞紧,仍把瓶倒立过来,再检查是否漏水,经检查不漏水的容量瓶才能使用
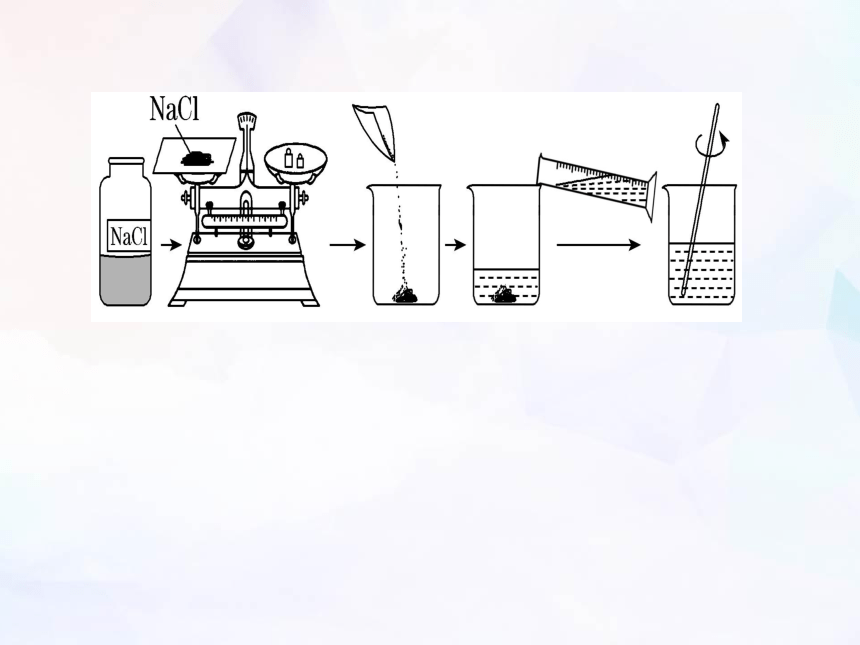
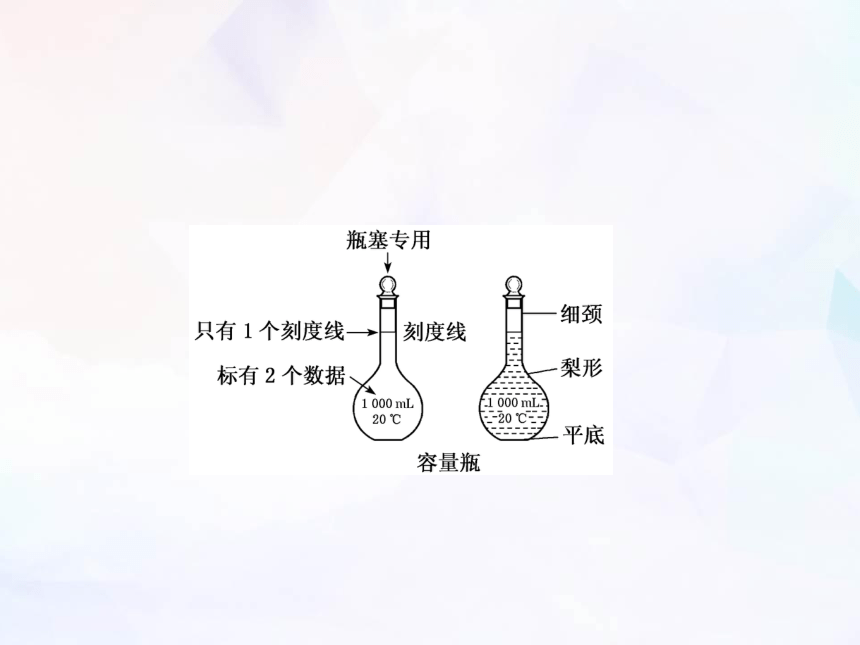
实验仪器
实验步骤
装瓶贴签 (容量瓶不能长期储存溶液)
误差分析
V
m
对浓度的影响
因变量
可能引起误差的一些操作
偏低
增大
—
定容时仰视读刻度
偏高
减小
—
定容时俯视读刻度
偏低
增大
—
定容摇匀时液面下降再加水
偏低
—
减小
定容时,水加多后用滴管吸出
偏高
减小
—
未恢复至室温就注入定容
偏低
—
减小
未洗涤烧杯和玻璃棒
偏低
—
减小
向容量瓶转移液体时有少量液体流出
无影响
不变
不变
移液前容量瓶内有少量水
配制过程误差分析
偏低
—
减小
称NaOH时用滤纸
偏低
—
减小
称量时间过长
称量过程误差分析
新知学习 物质的量浓度
单位体积溶液所含溶质B的物质的量叫做溶质B的物质的量浓度
符号:cB 单位:mol·L-1 或 mol·m-3
注意:体积是溶液的!!!
2、表达式:
cB=
溶质B的物质的量(mol)
溶液的体积(L)
1、定义:
nB
V
cB=
nB
cB
V=
nB =
cB×V
V溶液 ≠ V溶剂
V溶液 ≠ V溶剂 + V溶质
新知学习 与物质的量浓度相关的计算
与表达式相关的计算
nB
V
cB=
nB
cB
V=
nB =
cB×V
例1.(1) 将 1 mol NaOH 溶解并加水至 500 mL,则 c(NaOH)为多少
(2) 100 mL 2 mol·L-1的NaCl溶液,含有 NaCl 的物质的量为多少?
c(NaOH) = n(NaOH) / V = 1 mol ÷ 0.5 L = 2 mol·L-1
n(NaCl) = c(NaCl)V = 2 mol·L-1 × 0.1 L = 0.2 mol
学
例2.将标准状况下体积为V L的HCl气体溶于1 L水中,所得溶液的密度为ρ g·cm-3,试计算该溶液的物质的量浓度。(书写计算过程)
标况下气体溶质溶于水后其物质的量浓度的计算
浓溶液稀释问题
(1)溶质的物质的量不变:c(浓)·V(浓)=c(稀)·V(稀)
(2)溶质的质量不变:m(浓)·w(浓)=m(稀)·w(稀)
(3)溶液的质量守恒:m(稀)=m(浓)+m(水)
【例3】将5 mol·L-1 的盐酸10 mL稀释到200 mL,其物质的量浓度为多少?
5mol/L ×10mL= c2 ×200mL
c2 = 0.25 mol·L-1
物质的量浓度cB与质量分数w的换算
例4.市售浓硫酸中溶质的质量分数为98%,密度为1.84 g·cm-3。计算市售浓硫酸中硫酸的物质的量浓度为 。
先计算出1 000 mL浓硫酸中含硫酸的质量,1 000 mL×1.84 g·cm-3×98%=1 803.2 g,将其换算成硫酸的物质的量,1 803.2 g÷98 g·mol-1=18.4 mol,市售浓硫酸中硫酸的物质的量浓度为18.4 mol·L-1。
18.4 mol·L-1
由“定义式”出发:物质的量浓度的表达式为cB,由此知,欲求cB,先求nB及V。设溶液体积为1 L,则:
cB=
cB
课堂小结
第三节 化学中常用的物理量
——物质的量
第3课时 物质的量浓度
鲁科版2019必修第一册
第一章 认识化学科学
回顾旧知
你曾学过的表示溶液浓度的物理量是什么?
溶质的质量分数(ω)=
溶质的质量
溶液的质量
×100%
溶质的质量
溶质的质量+溶剂的质量
×100%
=
活动·探究 配制一定物质的量浓度的溶液
实验目的
实验室计划配制0.1L的NaCl溶液,其中溶质的物质的量为0.04mol。请你利用实验室的固体氯化钠完成任务。
检验程序:加水→塞瓶塞→倒立→查漏→正立,瓶塞旋转180°→倒立→查漏。
具体方法是:往瓶内加水,塞好瓶塞(瓶口和瓶塞要干,且不涂任何油脂等),用食指顶住瓶塞,另一只手托住瓶底把瓶倒立过来,观察瓶塞周围是否有水漏出,如不漏水,把瓶塞旋转180°塞紧,仍把瓶倒立过来,再检查是否漏水,经检查不漏水的容量瓶才能使用
实验仪器
实验步骤
装瓶贴签 (容量瓶不能长期储存溶液)
误差分析
V
m
对浓度的影响
因变量
可能引起误差的一些操作
偏低
增大
—
定容时仰视读刻度
偏高
减小
—
定容时俯视读刻度
偏低
增大
—
定容摇匀时液面下降再加水
偏低
—
减小
定容时,水加多后用滴管吸出
偏高
减小
—
未恢复至室温就注入定容
偏低
—
减小
未洗涤烧杯和玻璃棒
偏低
—
减小
向容量瓶转移液体时有少量液体流出
无影响
不变
不变
移液前容量瓶内有少量水
配制过程误差分析
偏低
—
减小
称NaOH时用滤纸
偏低
—
减小
称量时间过长
称量过程误差分析
新知学习 物质的量浓度
单位体积溶液所含溶质B的物质的量叫做溶质B的物质的量浓度
符号:cB 单位:mol·L-1 或 mol·m-3
注意:体积是溶液的!!!
2、表达式:
cB=
溶质B的物质的量(mol)
溶液的体积(L)
1、定义:
nB
V
cB=
nB
cB
V=
nB =
cB×V
V溶液 ≠ V溶剂
V溶液 ≠ V溶剂 + V溶质
新知学习 与物质的量浓度相关的计算
与表达式相关的计算
nB
V
cB=
nB
cB
V=
nB =
cB×V
例1.(1) 将 1 mol NaOH 溶解并加水至 500 mL,则 c(NaOH)为多少
(2) 100 mL 2 mol·L-1的NaCl溶液,含有 NaCl 的物质的量为多少?
c(NaOH) = n(NaOH) / V = 1 mol ÷ 0.5 L = 2 mol·L-1
n(NaCl) = c(NaCl)V = 2 mol·L-1 × 0.1 L = 0.2 mol
学
例2.将标准状况下体积为V L的HCl气体溶于1 L水中,所得溶液的密度为ρ g·cm-3,试计算该溶液的物质的量浓度。(书写计算过程)
标况下气体溶质溶于水后其物质的量浓度的计算
浓溶液稀释问题
(1)溶质的物质的量不变:c(浓)·V(浓)=c(稀)·V(稀)
(2)溶质的质量不变:m(浓)·w(浓)=m(稀)·w(稀)
(3)溶液的质量守恒:m(稀)=m(浓)+m(水)
【例3】将5 mol·L-1 的盐酸10 mL稀释到200 mL,其物质的量浓度为多少?
5mol/L ×10mL= c2 ×200mL
c2 = 0.25 mol·L-1
物质的量浓度cB与质量分数w的换算
例4.市售浓硫酸中溶质的质量分数为98%,密度为1.84 g·cm-3。计算市售浓硫酸中硫酸的物质的量浓度为 。
先计算出1 000 mL浓硫酸中含硫酸的质量,1 000 mL×1.84 g·cm-3×98%=1 803.2 g,将其换算成硫酸的物质的量,1 803.2 g÷98 g·mol-1=18.4 mol,市售浓硫酸中硫酸的物质的量浓度为18.4 mol·L-1。
18.4 mol·L-1
由“定义式”出发:物质的量浓度的表达式为cB,由此知,欲求cB,先求nB及V。设溶液体积为1 L,则:
cB=
cB
课堂小结
