人教版(2019)高中化学必修二 8.1.1 自然资源的开发利用 课件(共25张PPT)
文档属性
| 名称 | 人教版(2019)高中化学必修二 8.1.1 自然资源的开发利用 课件(共25张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 24.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-25 00:00:00 | ||
图片预览





文档简介
(共25张PPT)
人教版(2019)·必修第二册
第一课时 金属矿物的开发利用
第八章 化学与可持续发展
第一节 自然资源的开发利用
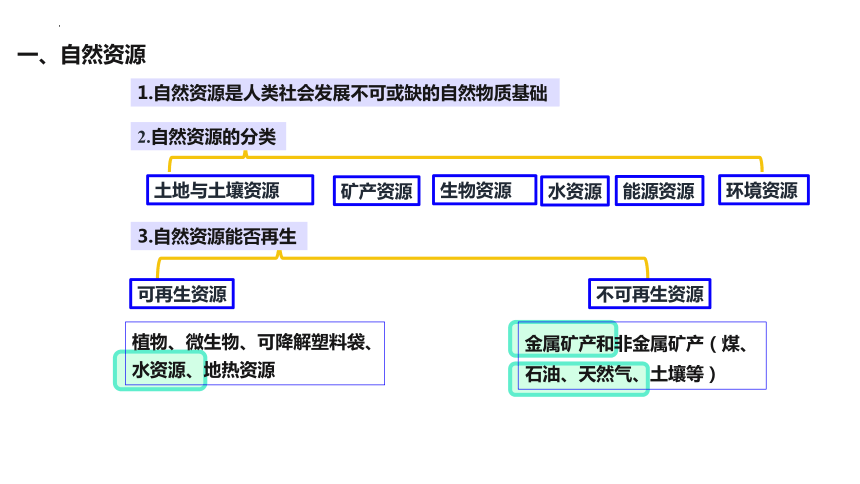
一、自然资源
1.自然资源是人类社会发展不可或缺的自然物质基础
2.自然资源的分类
土地与土壤资源
矿产资源
生物资源
水资源
能源资源
环境资源
3.自然资源能否再生
可再生资源
不可再生资源
植物、微生物、可降解塑料袋、水资源、地热资源
金属矿产和非金属矿产(煤、石油、天然气、土壤等)
二、金属矿物的开发利用
1.金属元素在自然界的存在
⑴游离态:
少数不活泼金属
铂矿
银
陨铁
金矿
⑵化合态:
绝大多数金属以矿物质形式存在
蓝铜矿
赤铁矿
赤铜矿
钨矿
铝矿
孔雀石
铅锌矿
菱镁矿
黄铜矿
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
如图表示金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发利用的大致年限。
约10000年前
约6000年前
约6000年前
约2500年前
约200年前
为什么地壳中铝的含量比铁和铜高,但使用的时间却晚得太多?
金属越活泼,冶炼时所需条件要求越高,在人类历史上出现相对晚一些。
思考2
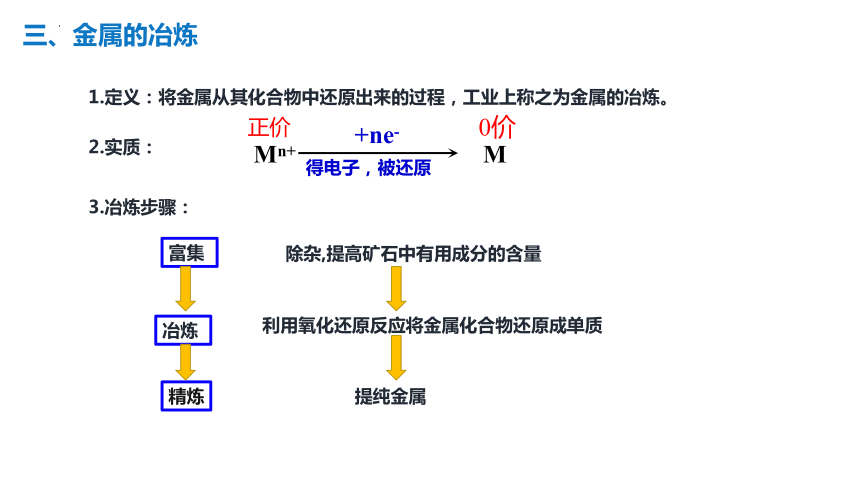
三、金属的冶炼
1.定义:将金属从其化合物中还原出来的过程,工业上称之为金属的冶炼。
2.实质:
Mn+ M
+ne-
得电子,被还原
3.冶炼步骤:
富集
除杂,提高矿石中有用成分的含量
利用氧化还原反应将金属化合物还原成单质
提纯金属
冶炼
精炼
正价
0价
三、金属的冶炼
4.方法
三、金属的冶炼
①物理法——富集法
淘金原理:
金的密度比沙大
金在自然界中以游离态存在。
“沙里淘金”有诗为证:
“千淘万漉虽辛苦,吹尽狂沙始到金”
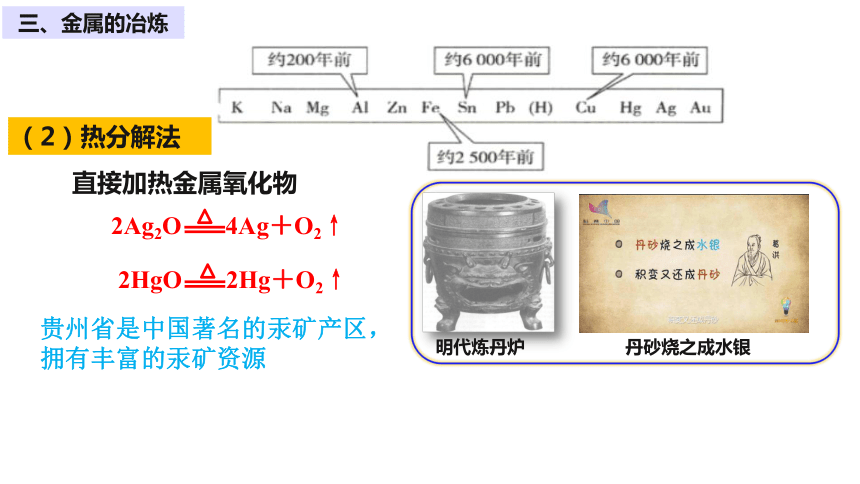
三、金属的冶炼
(2)热分解法
明代炼丹炉
丹砂烧之成水银
直接加热金属氧化物
2HgO 2Hg+O2↑
2Ag2O 4Ag+O2↑
贵州省是中国著名的汞矿产区,
拥有丰富的汞矿资源
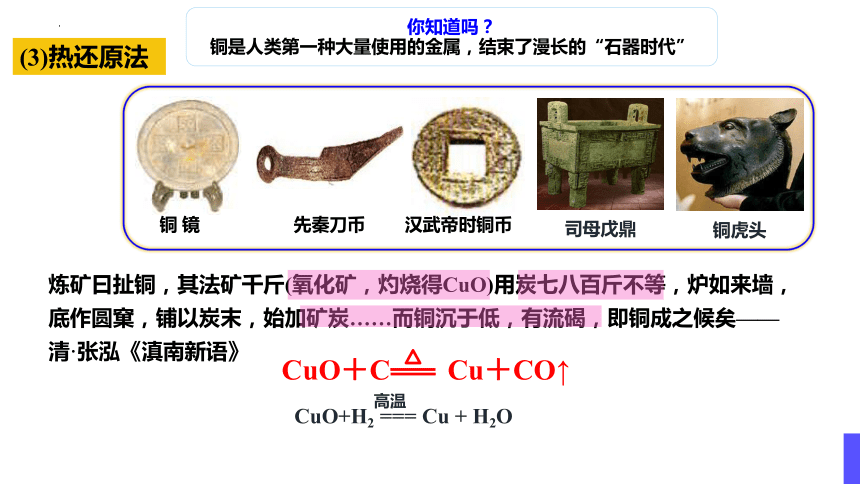
炼矿曰扯铜,其法矿千斤(氧化矿,灼烧得CuO)用炭七八百斤不等,炉如来墙,底作圆窠,铺以炭末,始加矿炭……而铜沉于低,有流碣,即铜成之候矣——清·张泓《滇南新语》
你知道吗?
铜是人类第一种大量使用的金属,结束了漫长的“石器时代”
铜 镜
汉武帝时铜币
先秦刀币
司母戊鼎
铜虎头
CuO+C Cu+CO↑
(3)热还原法
CuO+H2 === Cu + H2O
高温
2PbS+3O2 2PbO+2SO2
高温
①富集:将方铅矿(PbS)进行浮选
②焙烧:
③制粗铅:PbO+C Pb+CO↑; PbO+CO Pb+CO2
高温
高温
铅的冶炼大致过程如下:
我国是世界铅生产和铅消费的最大国,
铅的冶炼方法:成本高、污染严重
单质 Sn的制备:
将SnO2与焦炭充分混合后,于惰性气氛中加热至800℃,由于固体之间反应慢,未明显发生反应。若通入空气在800℃下, SnO2能迅速被还原为单质 Sn。
(3)热还原法
②铁的冶炼(高炉炼铁)
Fe2O3+3CO === 2Fe + 3CO2
高温
常用的还原剂有:
CO、H2、C(焦炭)、活泼金属
(3)热还原法
①剧烈反应,火星四射。
②放出大量的热,纸漏斗下端被烧穿,有红热熔融物落入细沙上,冷却后变为黑色固体。
实验现象
2Al+Fe2O3 === 2Fe+Al2O3
高温
(3)热还原法——铝热反应
【问题1】铝热反应需要高温条件,是否还需要持续加热?
铝热反应为放热反应,放出的热可以维持反应继续进行,因此不需要持续加热。
2Al+Fe2O3 === 2Fe+Al2O3
高温
铝热剂(混合物)
(3)热还原法——铝热反应
2Al+Fe2O3 === 2Fe+Al2O3
高温
铝热剂(混合物)
【问题2】在实验中,镁条、氯酸钾的作用是什么?引发反应的操作是什么?
C镁条是引燃剂,氯酸钾为助燃剂;
点燃镁条,促使氯酸钾分解,释放出氧气,使镁条更剧烈燃烧,单位时间内放出更多热量,从而引发Al和Fe2O3发生反应。
【问题3】细沙的作用是什么?
①防止蒸发皿炸裂
②防止生成的熔融物溅出。
(3)热还原法——铝热反应
铝热反应
铝单质做还原剂冶炼高熔点,且活动性比铝弱的金属(Fe、V、Cr、Mn等)
铝热剂:铝粉和金属氧化物 (V2O5/Cr2O3/MnO2/FexOy等)的混合物
Fe2O3+2Al 2Fe + Al2O3
高温
3MnO2+4Al 3Mn+ 2Al2O3
高温
Cr2O3+2Al 2Cr + Al2O3
高温
3Co3O4+8Al 9Co + 4Al2O3
高温
3V2O5+10Al 6V+ 5Al2O3
高温
置换反应
① 冶炼高熔点金属,如铬、锰、钨、钒等
【铝热反应的应用】
【铝热反应的应用】
② 金属焊接,如焊接钢轨
将两个铁轨缝隙处套上模具,预热,加入铝热剂(铁氧化物与铝单质混合固体),然后等待其反应,放出大量热,生成铁水(液态铁)流进缝隙,冷却,打磨。
你知道吗?
拿破仑大帝喜欢炫耀自己。每次宴会,餐桌上的用具几乎全是用银制成的,唯有他自己用的那一个碗
却是铝制品。为什么贵为法国皇帝用色泽要暗得多的铝碗呢?
1827年,德国化学家维勒用金属钾制得了铝
1854 年,法国的德维尔用金属钠制得铝
到19世纪末,铝的价格发生了成千倍的跌落!
1886年发明了一种炼铝的方法。
电解法
置换反应
三、金属的冶炼
(4)电解法
MgCl2 (熔融) ==== Mg + Cl2 ↑
电解
2NaCl (熔融) ==== 2Na+Cl2 ↑
电解
2Al2O3 (熔融) ====== 4Al + 3O2 ↑
电解
冰晶石
加入冰晶石(Na3AlF6)能够溶解氧化铝而又能降低其熔点,且冰晶石在电解温度下不被分解,并有足够的流动性,有利于电解
——适用于很活泼的金属(K Ca Na Mg Al )
思考2
结合下列表格物质的熔、沸点数据分析,为什么冶炼镁时,选择MgCl2而不是MgO?为什么冶炼铝时,选择Al2O3而不是AlCl3?
物质 MgO Al2O3 MgCl2 AlCl3
熔点/℃ 2 852 2 054 714 190(以分子形式存在)
沸点/℃ 3 600 2 980 1 412 180
MgO熔点高,耗能多;
AlCl3的沸点比熔点低,易升华,是共价化合物,熔融状态下不导电。
电解法制备此类金属,能否在水溶液中进行
不能,因为此类金属的活动性强,阳离子的氧化性弱于水电离的氢离子,根据氧化还原反应的先后规律,轮不到它们得电子被还原。
2NaCl+2H2O ==== 2NaOH+H2↑+Cl2↑
电解
思考3
三、金属的冶炼
(5)其他的冶炼方法
Fe+CuSO4===FeSO4+Cu
湿法炼铜
火法炼铜
Cu2S+O2 === 2Cu+SO2
高温
火烧孔雀石炼铜
Cu2(OH)2CO3 === 2CuO + H2O + CO2↑
高温
C + 2CuO === CO2 ↑ + 2Cu
难挥发性物质制备易挥发性的物质
Na+KCl (熔融) === NaCl+K↑
人类很早就发现,孔雀石在熊熊燃烧的树木中灼烧,树木余烬里会有一种红色光亮的金属凝固出来。
Cu2(OH)2CO3
孔雀石
K Ca Na Mg Al ︱ Zn Fe Sn Pb (H) Cu ︱ Hg Ag ︱Pt Au
电解法
热还原法
热分解法
物理法
4.方法
三、金属的冶炼
金属冶炼方法的选择取决于:金属的活泼性
需要利用电能提供电子
强还原剂提供电子
自身氧化还原
单质
金属活动性逐渐减弱
金属简单阳离子的得电子能力逐渐增强
课堂思考
你想到了什么?
请将你的想法与同学交流
计算表明,生产1mol铝消耗的电能至少为1.8×106J,回收铝质饮料罐得到铝与从铝土矿制铝相比,前者的能耗仅为后者的3%~5%。通过对上述数据的分析和比较,结合图8-1和图8-2,你想到了什么?请将你的想法与同学交流。
计算表明,生产1mol铝消耗的电能至少为1.8×106J,回收铝质饮料罐得到铝与从铝土矿制铝相比,前者的能耗仅为后者的3%~5%。通过对上述数据的分析和比较,结合图8-1和图8-2,你想到了什么?请将你的想法与同学交流。
启示1:从铝土矿制铝消耗的能量要远远高于回收铝质饮料罐得到铝消耗的能量,可知在实际生产过程中必须考虑投入与产出,要考虑成本。
启示2:加强旧金属的回收和再利用是合理开发和利用金属资源的重要途径。要树立金属垃圾也是一种宝贵资源的理念。在日常生活中,要大力倡导金属垃圾的分类回收和再利用,养成自觉珍惜自然资源、节约资源、爱惜环境和保护环境的意识。
课堂思考
计算表明,生产1mol铝消耗的电能至少为1.8×106J,回收铝质饮料罐得到铝与从铝土矿制铝相比,前者的能耗仅为后者的3%~5%。通过对上述数据的分析和比较,结合图8-1和图8-2,你想到了什么?请将你的想法与同学交流。
启示3:实际工业生产中,从金属矿物到纯净金属的冶炼过程是一个复杂的过程,往往涉及许多其他物质和反应,在得到所需产品的同时,也会产生废弃物。因此必须考虑废弃物的处理和生产对环境的影响,形成绿色化学观念和可持续发展意识。
课堂思考
【习题】铝土矿中除Al2O3外常含有杂质Fe2O3 、SiO2,怎样从铝土矿中获得铝单质呢?
Al2O3
Fe2O3
SiO2
NaOH
溶液
Fe2O3
Na[Al(OH)4] Na2SiO3
NaOH
盐酸
H2SiO3
NaCl AlCl3
氨水
Al(OH)3
过滤
过滤
过滤
NH4Cl
NaCl
Al2O3
Al
电解
加热
方案一:碱溶法
①
②
③
④
⑤
[Al(OH)4] + 4H+ === Al3++4H2O
Al3++3NH3·H2O === Al(OH)3↓+3NH4+
Al2O3 + 2OH + 3H2O === 2[Al(OH)4]
SiO2 + 2OH === SiO32- + H2O
SiO32- + 2H+ === H2SiO3↓ + H2O
强酸制弱酸
Al2O3
Fe2O3
SiO2
SiO2
AlCl3
FeCl3
HCl
Fe(OH)3
Na[Al(OH)4]
NaCl
NaOH
CO2
Al(OH)3
NaHCO3
NaCl
盐酸
过滤
NaOH
溶液
过滤
过滤
Al2O3
Al
电解
加热
【习题】铝土矿中除Al2O3外常含有杂质Fe2O3 、SiO2,怎样从铝土矿中获得铝单质呢?
方案二:酸溶法
①
②
③
④
⑤
[Al(OH)4] + CO2 === Al(OH)3↓ + HCO3-
Al3++4OH === [Al(OH)4]
Al2O3+6H+ === 2Al3++3H2O
2Al2O3 (熔融) ====== 4Al + 3O2 ↑
电解
冰晶石
强酸制弱酸
人教版(2019)·必修第二册
第一课时 金属矿物的开发利用
第八章 化学与可持续发展
第一节 自然资源的开发利用
一、自然资源
1.自然资源是人类社会发展不可或缺的自然物质基础
2.自然资源的分类
土地与土壤资源
矿产资源
生物资源
水资源
能源资源
环境资源
3.自然资源能否再生
可再生资源
不可再生资源
植物、微生物、可降解塑料袋、水资源、地热资源
金属矿产和非金属矿产(煤、石油、天然气、土壤等)
二、金属矿物的开发利用
1.金属元素在自然界的存在
⑴游离态:
少数不活泼金属
铂矿
银
陨铁
金矿
⑵化合态:
绝大多数金属以矿物质形式存在
蓝铜矿
赤铁矿
赤铜矿
钨矿
铝矿
孔雀石
铅锌矿
菱镁矿
黄铜矿
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
如图表示金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发利用的大致年限。
约10000年前
约6000年前
约6000年前
约2500年前
约200年前
为什么地壳中铝的含量比铁和铜高,但使用的时间却晚得太多?
金属越活泼,冶炼时所需条件要求越高,在人类历史上出现相对晚一些。
思考2
三、金属的冶炼
1.定义:将金属从其化合物中还原出来的过程,工业上称之为金属的冶炼。
2.实质:
Mn+ M
+ne-
得电子,被还原
3.冶炼步骤:
富集
除杂,提高矿石中有用成分的含量
利用氧化还原反应将金属化合物还原成单质
提纯金属
冶炼
精炼
正价
0价
三、金属的冶炼
4.方法
三、金属的冶炼
①物理法——富集法
淘金原理:
金的密度比沙大
金在自然界中以游离态存在。
“沙里淘金”有诗为证:
“千淘万漉虽辛苦,吹尽狂沙始到金”
三、金属的冶炼
(2)热分解法
明代炼丹炉
丹砂烧之成水银
直接加热金属氧化物
2HgO 2Hg+O2↑
2Ag2O 4Ag+O2↑
贵州省是中国著名的汞矿产区,
拥有丰富的汞矿资源
炼矿曰扯铜,其法矿千斤(氧化矿,灼烧得CuO)用炭七八百斤不等,炉如来墙,底作圆窠,铺以炭末,始加矿炭……而铜沉于低,有流碣,即铜成之候矣——清·张泓《滇南新语》
你知道吗?
铜是人类第一种大量使用的金属,结束了漫长的“石器时代”
铜 镜
汉武帝时铜币
先秦刀币
司母戊鼎
铜虎头
CuO+C Cu+CO↑
(3)热还原法
CuO+H2 === Cu + H2O
高温
2PbS+3O2 2PbO+2SO2
高温
①富集:将方铅矿(PbS)进行浮选
②焙烧:
③制粗铅:PbO+C Pb+CO↑; PbO+CO Pb+CO2
高温
高温
铅的冶炼大致过程如下:
我国是世界铅生产和铅消费的最大国,
铅的冶炼方法:成本高、污染严重
单质 Sn的制备:
将SnO2与焦炭充分混合后,于惰性气氛中加热至800℃,由于固体之间反应慢,未明显发生反应。若通入空气在800℃下, SnO2能迅速被还原为单质 Sn。
(3)热还原法
②铁的冶炼(高炉炼铁)
Fe2O3+3CO === 2Fe + 3CO2
高温
常用的还原剂有:
CO、H2、C(焦炭)、活泼金属
(3)热还原法
①剧烈反应,火星四射。
②放出大量的热,纸漏斗下端被烧穿,有红热熔融物落入细沙上,冷却后变为黑色固体。
实验现象
2Al+Fe2O3 === 2Fe+Al2O3
高温
(3)热还原法——铝热反应
【问题1】铝热反应需要高温条件,是否还需要持续加热?
铝热反应为放热反应,放出的热可以维持反应继续进行,因此不需要持续加热。
2Al+Fe2O3 === 2Fe+Al2O3
高温
铝热剂(混合物)
(3)热还原法——铝热反应
2Al+Fe2O3 === 2Fe+Al2O3
高温
铝热剂(混合物)
【问题2】在实验中,镁条、氯酸钾的作用是什么?引发反应的操作是什么?
C镁条是引燃剂,氯酸钾为助燃剂;
点燃镁条,促使氯酸钾分解,释放出氧气,使镁条更剧烈燃烧,单位时间内放出更多热量,从而引发Al和Fe2O3发生反应。
【问题3】细沙的作用是什么?
①防止蒸发皿炸裂
②防止生成的熔融物溅出。
(3)热还原法——铝热反应
铝热反应
铝单质做还原剂冶炼高熔点,且活动性比铝弱的金属(Fe、V、Cr、Mn等)
铝热剂:铝粉和金属氧化物 (V2O5/Cr2O3/MnO2/FexOy等)的混合物
Fe2O3+2Al 2Fe + Al2O3
高温
3MnO2+4Al 3Mn+ 2Al2O3
高温
Cr2O3+2Al 2Cr + Al2O3
高温
3Co3O4+8Al 9Co + 4Al2O3
高温
3V2O5+10Al 6V+ 5Al2O3
高温
置换反应
① 冶炼高熔点金属,如铬、锰、钨、钒等
【铝热反应的应用】
【铝热反应的应用】
② 金属焊接,如焊接钢轨
将两个铁轨缝隙处套上模具,预热,加入铝热剂(铁氧化物与铝单质混合固体),然后等待其反应,放出大量热,生成铁水(液态铁)流进缝隙,冷却,打磨。
你知道吗?
拿破仑大帝喜欢炫耀自己。每次宴会,餐桌上的用具几乎全是用银制成的,唯有他自己用的那一个碗
却是铝制品。为什么贵为法国皇帝用色泽要暗得多的铝碗呢?
1827年,德国化学家维勒用金属钾制得了铝
1854 年,法国的德维尔用金属钠制得铝
到19世纪末,铝的价格发生了成千倍的跌落!
1886年发明了一种炼铝的方法。
电解法
置换反应
三、金属的冶炼
(4)电解法
MgCl2 (熔融) ==== Mg + Cl2 ↑
电解
2NaCl (熔融) ==== 2Na+Cl2 ↑
电解
2Al2O3 (熔融) ====== 4Al + 3O2 ↑
电解
冰晶石
加入冰晶石(Na3AlF6)能够溶解氧化铝而又能降低其熔点,且冰晶石在电解温度下不被分解,并有足够的流动性,有利于电解
——适用于很活泼的金属(K Ca Na Mg Al )
思考2
结合下列表格物质的熔、沸点数据分析,为什么冶炼镁时,选择MgCl2而不是MgO?为什么冶炼铝时,选择Al2O3而不是AlCl3?
物质 MgO Al2O3 MgCl2 AlCl3
熔点/℃ 2 852 2 054 714 190(以分子形式存在)
沸点/℃ 3 600 2 980 1 412 180
MgO熔点高,耗能多;
AlCl3的沸点比熔点低,易升华,是共价化合物,熔融状态下不导电。
电解法制备此类金属,能否在水溶液中进行
不能,因为此类金属的活动性强,阳离子的氧化性弱于水电离的氢离子,根据氧化还原反应的先后规律,轮不到它们得电子被还原。
2NaCl+2H2O ==== 2NaOH+H2↑+Cl2↑
电解
思考3
三、金属的冶炼
(5)其他的冶炼方法
Fe+CuSO4===FeSO4+Cu
湿法炼铜
火法炼铜
Cu2S+O2 === 2Cu+SO2
高温
火烧孔雀石炼铜
Cu2(OH)2CO3 === 2CuO + H2O + CO2↑
高温
C + 2CuO === CO2 ↑ + 2Cu
难挥发性物质制备易挥发性的物质
Na+KCl (熔融) === NaCl+K↑
人类很早就发现,孔雀石在熊熊燃烧的树木中灼烧,树木余烬里会有一种红色光亮的金属凝固出来。
Cu2(OH)2CO3
孔雀石
K Ca Na Mg Al ︱ Zn Fe Sn Pb (H) Cu ︱ Hg Ag ︱Pt Au
电解法
热还原法
热分解法
物理法
4.方法
三、金属的冶炼
金属冶炼方法的选择取决于:金属的活泼性
需要利用电能提供电子
强还原剂提供电子
自身氧化还原
单质
金属活动性逐渐减弱
金属简单阳离子的得电子能力逐渐增强
课堂思考
你想到了什么?
请将你的想法与同学交流
计算表明,生产1mol铝消耗的电能至少为1.8×106J,回收铝质饮料罐得到铝与从铝土矿制铝相比,前者的能耗仅为后者的3%~5%。通过对上述数据的分析和比较,结合图8-1和图8-2,你想到了什么?请将你的想法与同学交流。
计算表明,生产1mol铝消耗的电能至少为1.8×106J,回收铝质饮料罐得到铝与从铝土矿制铝相比,前者的能耗仅为后者的3%~5%。通过对上述数据的分析和比较,结合图8-1和图8-2,你想到了什么?请将你的想法与同学交流。
启示1:从铝土矿制铝消耗的能量要远远高于回收铝质饮料罐得到铝消耗的能量,可知在实际生产过程中必须考虑投入与产出,要考虑成本。
启示2:加强旧金属的回收和再利用是合理开发和利用金属资源的重要途径。要树立金属垃圾也是一种宝贵资源的理念。在日常生活中,要大力倡导金属垃圾的分类回收和再利用,养成自觉珍惜自然资源、节约资源、爱惜环境和保护环境的意识。
课堂思考
计算表明,生产1mol铝消耗的电能至少为1.8×106J,回收铝质饮料罐得到铝与从铝土矿制铝相比,前者的能耗仅为后者的3%~5%。通过对上述数据的分析和比较,结合图8-1和图8-2,你想到了什么?请将你的想法与同学交流。
启示3:实际工业生产中,从金属矿物到纯净金属的冶炼过程是一个复杂的过程,往往涉及许多其他物质和反应,在得到所需产品的同时,也会产生废弃物。因此必须考虑废弃物的处理和生产对环境的影响,形成绿色化学观念和可持续发展意识。
课堂思考
【习题】铝土矿中除Al2O3外常含有杂质Fe2O3 、SiO2,怎样从铝土矿中获得铝单质呢?
Al2O3
Fe2O3
SiO2
NaOH
溶液
Fe2O3
Na[Al(OH)4] Na2SiO3
NaOH
盐酸
H2SiO3
NaCl AlCl3
氨水
Al(OH)3
过滤
过滤
过滤
NH4Cl
NaCl
Al2O3
Al
电解
加热
方案一:碱溶法
①
②
③
④
⑤
[Al(OH)4] + 4H+ === Al3++4H2O
Al3++3NH3·H2O === Al(OH)3↓+3NH4+
Al2O3 + 2OH + 3H2O === 2[Al(OH)4]
SiO2 + 2OH === SiO32- + H2O
SiO32- + 2H+ === H2SiO3↓ + H2O
强酸制弱酸
Al2O3
Fe2O3
SiO2
SiO2
AlCl3
FeCl3
HCl
Fe(OH)3
Na[Al(OH)4]
NaCl
NaOH
CO2
Al(OH)3
NaHCO3
NaCl
盐酸
过滤
NaOH
溶液
过滤
过滤
Al2O3
Al
电解
加热
【习题】铝土矿中除Al2O3外常含有杂质Fe2O3 、SiO2,怎样从铝土矿中获得铝单质呢?
方案二:酸溶法
①
②
③
④
⑤
[Al(OH)4] + CO2 === Al(OH)3↓ + HCO3-
Al3++4OH === [Al(OH)4]
Al2O3+6H+ === 2Al3++3H2O
2Al2O3 (熔融) ====== 4Al + 3O2 ↑
电解
冰晶石
强酸制弱酸
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
