2026届高考生物一轮复习:ATP是细胞内的能量通货 课件(30张)
文档属性
| 名称 | 2026届高考生物一轮复习:ATP是细胞内的能量通货 课件(30张) |  | |
| 格式 | pptx | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2025-08-25 07:24:10 | ||
图片预览


文档简介
(共30张PPT)
ATP是细胞内的能量通货
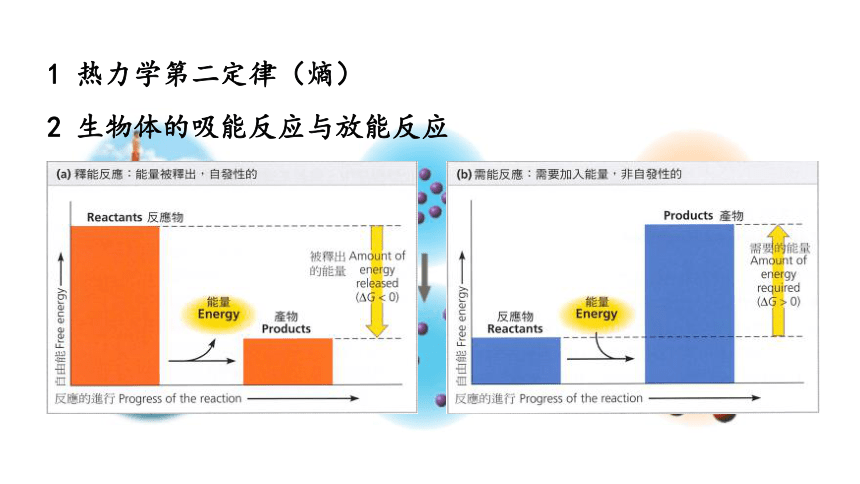
1 热力学第二定律(熵)
2 生物体的吸能反应与放能反应
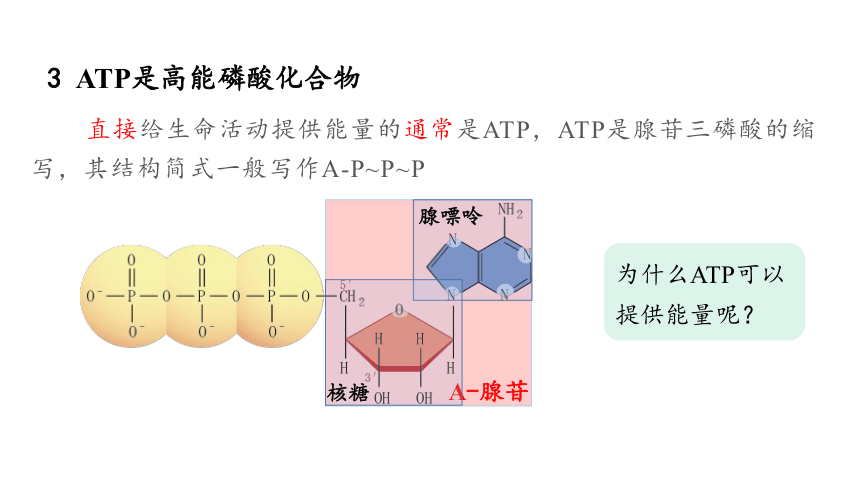
直接给生命活动提供能量的通常是ATP,ATP是腺苷三磷酸的缩写,其结构简式一般写作A-P~P~P
为什么ATP可以提供能量呢?
腺嘌呤
A-腺苷
3 ATP是高能磷酸化合物
核糖
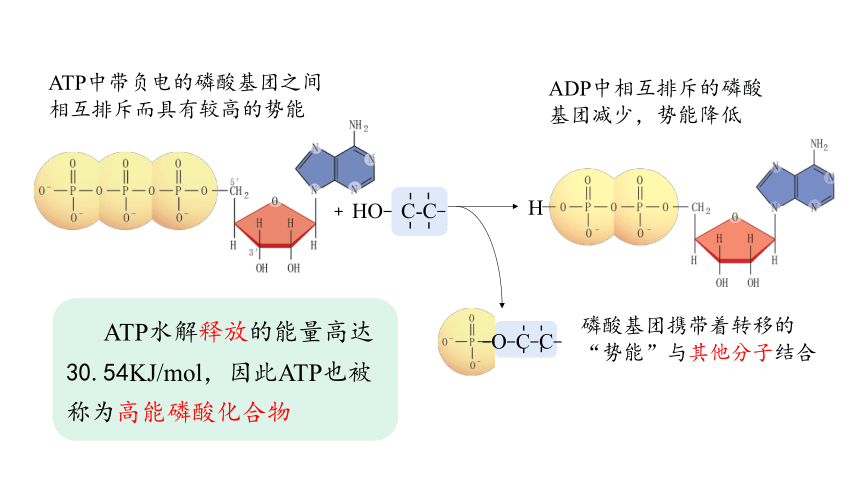
ATP中带负电的磷酸基团之间相互排斥而具有较高的势能
ADP中相互排斥的磷酸基团减少,势能降低
+ HO- C-C-
-O-C-C-
磷酸基团携带着转移的“势能”与其他分子结合
H
ATP水解释放的能量高达30.54KJ/mol,因此ATP也被称为高能磷酸化合物
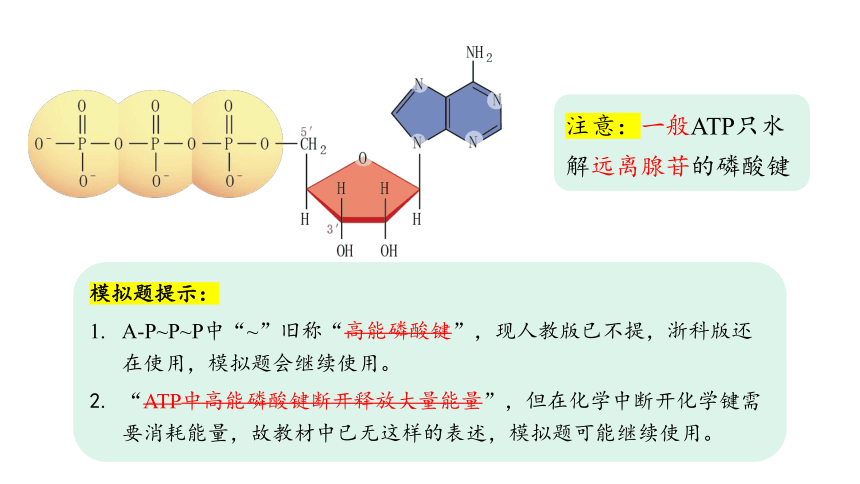
模拟题提示:
A-P~P~P中“~”旧称“高能磷酸键”,现人教版已不提,浙科版还在使用,模拟题会继续使用。
“ATP中高能磷酸键断开释放大量能量”,但在化学中断开化学键需要消耗能量,故教材中已无这样的表述,模拟题可能继续使用。
注意:一般ATP只水解远离腺苷的磷酸键
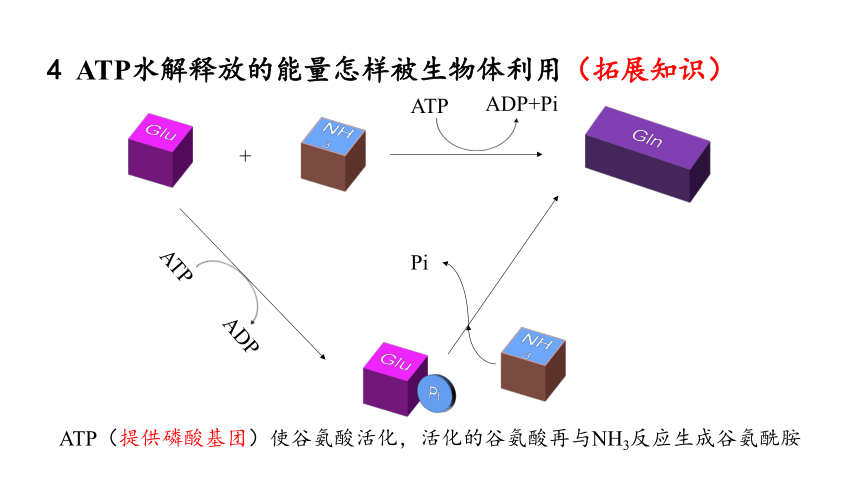
4 ATP水解释放的能量怎样被生物体利用(拓展知识)
Glu
+
ATP
NH3
Gln
Glu
Pi
ADP+Pi
ATP
ADP
Pi
NH3
ATP(提供磷酸基团)使谷氨酸活化,活化的谷氨酸再与NH3反应生成谷氨酰胺
P
Ca2+
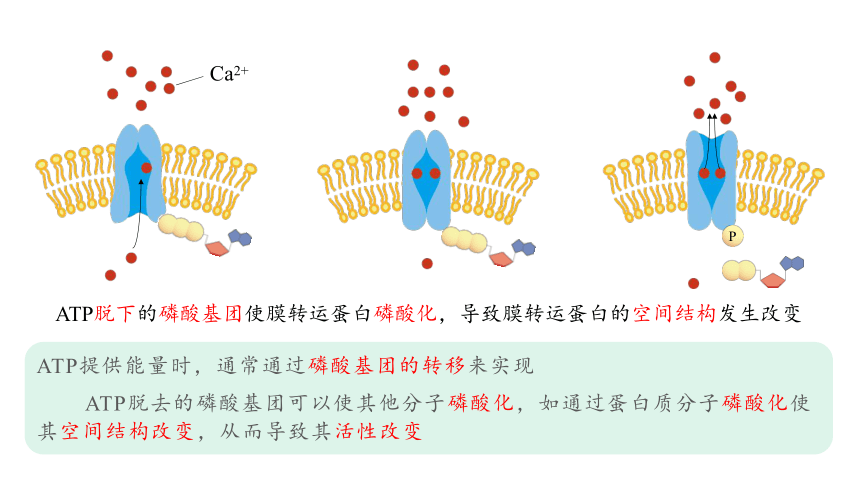
ATP脱下的磷酸基团使膜转运蛋白磷酸化,导致膜转运蛋白的空间结构发生改变
ATP提供能量时,通常通过磷酸基团的转移来实现
ATP脱去的磷酸基团可以使其他分子磷酸化,如通过蛋白质分子磷酸化使其空间结构改变,从而导致其活性改变
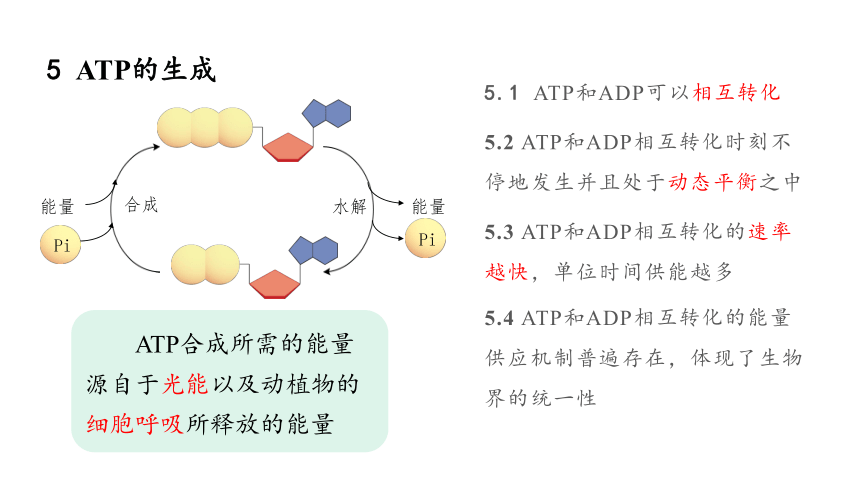
5 ATP的生成
5.1 ATP和ADP可以相互转化
5.2 ATP和ADP相互转化时刻不停地发生并且处于动态平衡之中
5.3 ATP和ADP相互转化的速率越快,单位时间供能越多
5.4 ATP和ADP相互转化的能量供应机制普遍存在,体现了生物界的统一性
Pi
能量
Pi
能量
水解
合成
ATP合成所需的能量源自于光能以及动植物的细胞呼吸所释放的能量
吸
能
反
应
能量
能量
水解
合成
放
能
反
应
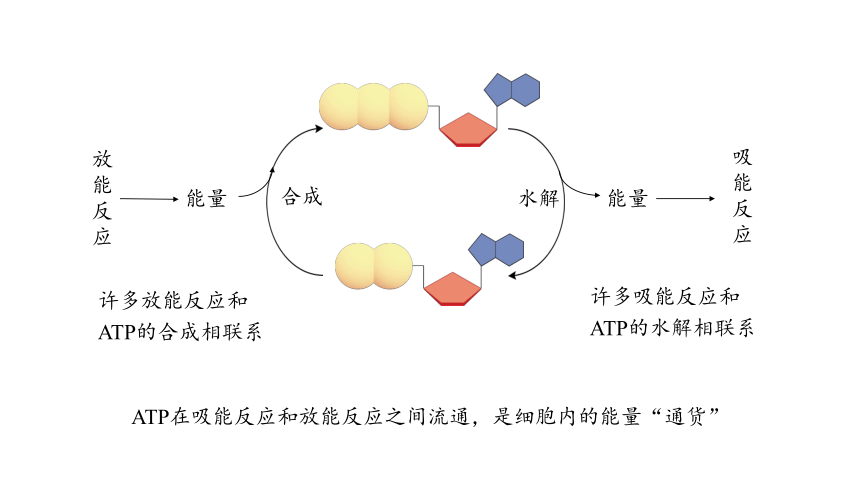
许多放能反应和ATP的合成相联系
许多吸能反应和ATP的水解相联系
ATP在吸能反应和放能反应之间流通,是细胞内的能量“通货”
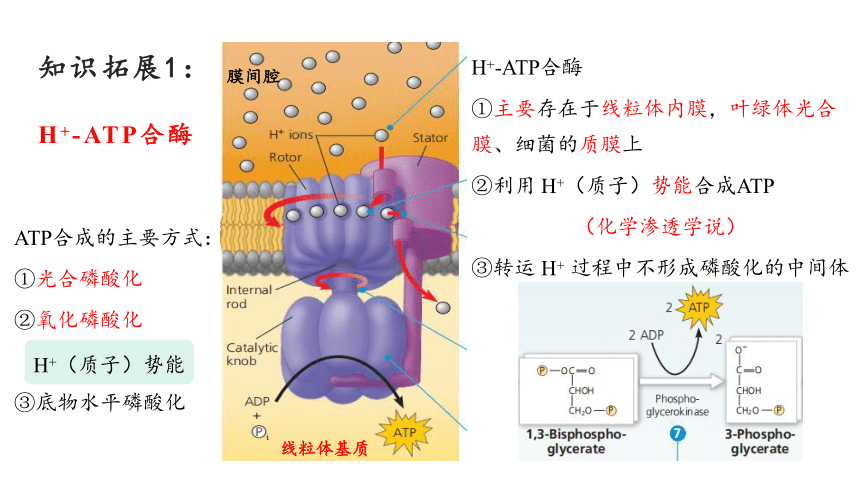
知识拓展1:
H+-ATP合酶
H+-ATP合酶
①主要存在于线粒体内膜,叶绿体光合膜、细菌的质膜上
②利用 H+(质子)势能合成ATP
(化学渗透学说)
③转运 H+ 过程中不形成磷酸化的中间体
线粒体基质
膜间腔
ATP合成的主要方式:
①光合磷酸化
②氧化磷酸化
③底物水平磷酸化
H+(质子)势能
提示:
ATP是主要的直接能源物质,但不是唯一的,GTP、CTP、dNTP等也常用于不同的代谢活动。
6 ATP用作直接能源物质,这主要源于:
6.1 ATP具有较高的转移势能
6.2 ATP在消耗后可以快速重新生成
……
银烛秋光冷画屏,轻罗小扇扑流萤。
天阶夜色凉如水,卧看牵牛织女星。
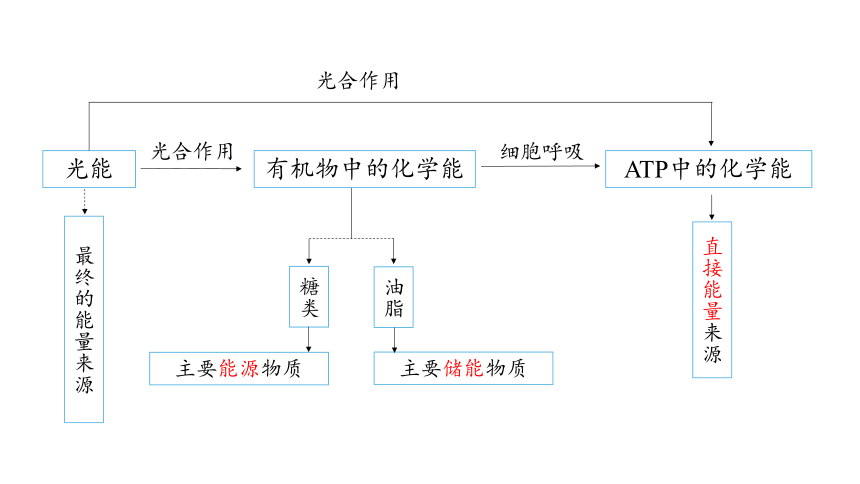
糖类
光能
ATP中的化学能
最终的能量来源
直接能量来源
主要能源物质
有机物中的化学能
光合作用
光合作用
细胞呼吸
油脂
主要储能物质
课件引用图片仅用于教学用途
第7讲 酶是生物催化剂
1 酶的发现史
酿酒与生命活动无关
巴斯德:酿酒需活的酵母参与
李比希:
酿酒是酵母死亡后释放的物质引起的
其它实验:
大量的酶是蛋白质,酿酒酶为蛋白质
萨姆纳:
脲酶是蛋白质
切赫和奥特曼:
部分RNA具有酶活性
酿酒发酵液中发现酵母
酿酒是什么回事呢?
毕希纳:
活酵母细胞产生能引起发酵的物质
2 酶的概念
2.1 酶是活细胞产生的具有生物催化活性的有机物,其中绝大多数酶是蛋白质,少部分酶是RNA。
细胞内产生的酶可以在细胞内/外发生作用,如鹰和人的消化酶。
2.2 酶的组成和类型
{
单纯酶:
结合酶:
酶蛋白对辅助因子有高度的选择性
水解产物仅有氨基酸或核糖核苷酸
全酶 = 酶蛋白 + 辅助因子(P71)(辅酶与辅基)
酶与底物结合
形成酶-底物复合物
复合物发生一定的形态变化
底物变成产物
产物从复合物上脱离
酶分子
恢复原状
诱导—契合学说
3 酶的催化学说
锁钥学说
中间产物学说
4 酶的催化机理
降低化学反应活化能
反应物
产物
活化能是指分子从常态转变为容易发生化学反应的活化状态所需的能量。
处于不同能量状态的分子数
分子能态
酶不能增加反应物分子的能量,但可以降低化学反应活化能【容易发生化学反应的活跃状态所需的最低能量】,从而使处于容易发生化学反应的活跃状态的反应物分子增多。
拓展知识1:酶降低化学反应活化能,促进反应进行的本质?
EA′有酶时,容易发生化学反应的活跃状态所需的最低能量
常温且无酶存在时,容易发生化学反应的活跃状态分子数
EA′无酶时,容易发生化学反应的活跃状态所需的最低能量
常温,有酶存在增加的容易发生化学反应的活跃状态分子数
处于不同能量状态的分子数
分子能态
升高温度可以提高反应物分子的能量水平,使处于容易发生化学反应的活跃状态的分子增多。
EA: 容易发生化学反应的活跃状态所需的最低能量
T1下容易发生化学反应的活跃状态分子数
升温至T2,增加的容易发生化学反应的活跃状态分子数
拓展知识2:为什么加热可以促进化学反应的进行?
概念:单位酶在单位时间内底物减少的量或产物增加的量表示。
5 酶的催化活性
6 酶催化效应的特点
6.1 专一性
6.1.1 只有特定形状的底物才能和酶结合
6.1.2 一种酶只能催化一种或一类化合物的反应
绝对专一性、相对专一性、键的专一性
(如:过氧化氢酶、胰蛋白酶、外切蛋白酶)
N
C
精氨酸
赖氨酸
胰蛋白酶
胰蛋白酶
胰蛋白酶能切开特定氨基酸(碱性氨基酸)羧基形成的肽键
6.2 高效性
E1:无催化剂
E2:+无机催化剂
E3:+有机催化剂(酶)
与无机催化剂相比,酶能更显著地降低反应的活化能,从而使反应更有效地进行
能量
反应历程
E1
E2
E3
H2O2
H2O+1/2O2
6.3 易受环境因素影响
6.3.1 温度
6.3.2 pH值
6.3.3 ...
胃蛋白酶
胰蛋白酶
注意:
①温度的图像与pH值的不一致性
②最适宜条件不一定是一个点,可能是一个区间
注意: 温度对酶促反应速率的影响的两个方面
① 温度升高,反应物分子所具有的能量增加,反应速度加快。【a】
② 酶分子本身具有热变性,会随温度的升高而发生空间结构的改变。温度升的越高,酶变性的速率越快,升到一定程度,酶将完全失活。【b】
③ 曲线c 是曲线a 与曲线b 的综合
注意: 1.低温会使酶活性降低,但不会破坏酶分子的结构,温度适宜时,酶的催化作用可以恢复。
2.低温下酶空间结构稳定,所以酶一般在低温条件下保存。
活性位点有两个
关键的氨基酸参
与催化淀粉的水解
7.1 激活调节
激活剂,指能使无活性的酶形成有活性的酶,或能提高酶活性的一类物质。
如Cl-是唾液淀粉酶的激活剂
7.2 抑制调节
7.2.1 不可逆抑制
7.2.2 可逆抑制
如重金属
竞争性抑制剂
非竞争性抑制剂
7 酶活性的调控(拓展知识3)
有活性
无活性
竞争性抑制剂
非竞争性抑制剂
抑制剂
╳
酶促反应调节示意图:
可逆性抑制剂与不可逆性抑制剂影响酶促反应曲线图解读
8 酶促反应的实验探究注意事项
证明酶具有专一性应该怎么做?
验证酶具有专一性应该怎么做?
酶1
酶2
酶3
酶…
底物1
底物2
底物3
底物…
需测试所有酶和所有底物的反应,即只有完全归纳,才能证明酶的专一性
若酶具有专一性,则
淀粉酶具有专一性
蔗糖酶具有专一性
淀粉酶能催化淀粉的水解,不能催化蔗糖的水解
淀粉酶能催化淀粉的水解,而蔗糖酶不能
实验验证
推论
推论
淀粉酶+淀粉
淀粉酶+蔗糖
实验验证
淀粉酶+淀粉
蔗糖酶+淀粉
模拟题提示:
模拟题把验证和证明混用,但我们要严于律己,规范自己的表述。
8.1 专一性实验
8.1.1 实验探究分组:酶相同,底物不同;底物相同,酶不同。
8.1.2 鉴定试剂与底物的选择,如试剂是本尼迪特就不能选择过氧化氢为底物。
8.1.3 异常阳性反应的可能原因:酶不纯或底物不纯。
8.1.4 其他细节:如唾液稀释200倍,淀粉用0.3%氯化钠溶解等。
8.2 探究pH对过氧化氢酶的影响
为什们要将滤纸片贴在上壁?增加滤纸片会有什么效果?为什么每次实验完要反复冲洗?淀粉为什么不能作为反应底物?
8.3 酶高效性实验
制匀浆(鸡肝或马铃薯)的目的;试管加塞;产物量与反应物量的关系曲线图等
酶
活化能
能障
高效性
专一性
作用条件温和
有机物
生理条件
酶的活性
pH
温度
是
降低
具有以下特性
也称
一般为
具有高的
主要影响因素
ATP是细胞内的能量通货
1 热力学第二定律(熵)
2 生物体的吸能反应与放能反应
直接给生命活动提供能量的通常是ATP,ATP是腺苷三磷酸的缩写,其结构简式一般写作A-P~P~P
为什么ATP可以提供能量呢?
腺嘌呤
A-腺苷
3 ATP是高能磷酸化合物
核糖
ATP中带负电的磷酸基团之间相互排斥而具有较高的势能
ADP中相互排斥的磷酸基团减少,势能降低
+ HO- C-C-
-O-C-C-
磷酸基团携带着转移的“势能”与其他分子结合
H
ATP水解释放的能量高达30.54KJ/mol,因此ATP也被称为高能磷酸化合物
模拟题提示:
A-P~P~P中“~”旧称“高能磷酸键”,现人教版已不提,浙科版还在使用,模拟题会继续使用。
“ATP中高能磷酸键断开释放大量能量”,但在化学中断开化学键需要消耗能量,故教材中已无这样的表述,模拟题可能继续使用。
注意:一般ATP只水解远离腺苷的磷酸键
4 ATP水解释放的能量怎样被生物体利用(拓展知识)
Glu
+
ATP
NH3
Gln
Glu
Pi
ADP+Pi
ATP
ADP
Pi
NH3
ATP(提供磷酸基团)使谷氨酸活化,活化的谷氨酸再与NH3反应生成谷氨酰胺
P
Ca2+
ATP脱下的磷酸基团使膜转运蛋白磷酸化,导致膜转运蛋白的空间结构发生改变
ATP提供能量时,通常通过磷酸基团的转移来实现
ATP脱去的磷酸基团可以使其他分子磷酸化,如通过蛋白质分子磷酸化使其空间结构改变,从而导致其活性改变
5 ATP的生成
5.1 ATP和ADP可以相互转化
5.2 ATP和ADP相互转化时刻不停地发生并且处于动态平衡之中
5.3 ATP和ADP相互转化的速率越快,单位时间供能越多
5.4 ATP和ADP相互转化的能量供应机制普遍存在,体现了生物界的统一性
Pi
能量
Pi
能量
水解
合成
ATP合成所需的能量源自于光能以及动植物的细胞呼吸所释放的能量
吸
能
反
应
能量
能量
水解
合成
放
能
反
应
许多放能反应和ATP的合成相联系
许多吸能反应和ATP的水解相联系
ATP在吸能反应和放能反应之间流通,是细胞内的能量“通货”
知识拓展1:
H+-ATP合酶
H+-ATP合酶
①主要存在于线粒体内膜,叶绿体光合膜、细菌的质膜上
②利用 H+(质子)势能合成ATP
(化学渗透学说)
③转运 H+ 过程中不形成磷酸化的中间体
线粒体基质
膜间腔
ATP合成的主要方式:
①光合磷酸化
②氧化磷酸化
③底物水平磷酸化
H+(质子)势能
提示:
ATP是主要的直接能源物质,但不是唯一的,GTP、CTP、dNTP等也常用于不同的代谢活动。
6 ATP用作直接能源物质,这主要源于:
6.1 ATP具有较高的转移势能
6.2 ATP在消耗后可以快速重新生成
……
银烛秋光冷画屏,轻罗小扇扑流萤。
天阶夜色凉如水,卧看牵牛织女星。
糖类
光能
ATP中的化学能
最终的能量来源
直接能量来源
主要能源物质
有机物中的化学能
光合作用
光合作用
细胞呼吸
油脂
主要储能物质
课件引用图片仅用于教学用途
第7讲 酶是生物催化剂
1 酶的发现史
酿酒与生命活动无关
巴斯德:酿酒需活的酵母参与
李比希:
酿酒是酵母死亡后释放的物质引起的
其它实验:
大量的酶是蛋白质,酿酒酶为蛋白质
萨姆纳:
脲酶是蛋白质
切赫和奥特曼:
部分RNA具有酶活性
酿酒发酵液中发现酵母
酿酒是什么回事呢?
毕希纳:
活酵母细胞产生能引起发酵的物质
2 酶的概念
2.1 酶是活细胞产生的具有生物催化活性的有机物,其中绝大多数酶是蛋白质,少部分酶是RNA。
细胞内产生的酶可以在细胞内/外发生作用,如鹰和人的消化酶。
2.2 酶的组成和类型
{
单纯酶:
结合酶:
酶蛋白对辅助因子有高度的选择性
水解产物仅有氨基酸或核糖核苷酸
全酶 = 酶蛋白 + 辅助因子(P71)(辅酶与辅基)
酶与底物结合
形成酶-底物复合物
复合物发生一定的形态变化
底物变成产物
产物从复合物上脱离
酶分子
恢复原状
诱导—契合学说
3 酶的催化学说
锁钥学说
中间产物学说
4 酶的催化机理
降低化学反应活化能
反应物
产物
活化能是指分子从常态转变为容易发生化学反应的活化状态所需的能量。
处于不同能量状态的分子数
分子能态
酶不能增加反应物分子的能量,但可以降低化学反应活化能【容易发生化学反应的活跃状态所需的最低能量】,从而使处于容易发生化学反应的活跃状态的反应物分子增多。
拓展知识1:酶降低化学反应活化能,促进反应进行的本质?
EA′有酶时,容易发生化学反应的活跃状态所需的最低能量
常温且无酶存在时,容易发生化学反应的活跃状态分子数
EA′无酶时,容易发生化学反应的活跃状态所需的最低能量
常温,有酶存在增加的容易发生化学反应的活跃状态分子数
处于不同能量状态的分子数
分子能态
升高温度可以提高反应物分子的能量水平,使处于容易发生化学反应的活跃状态的分子增多。
EA: 容易发生化学反应的活跃状态所需的最低能量
T1下容易发生化学反应的活跃状态分子数
升温至T2,增加的容易发生化学反应的活跃状态分子数
拓展知识2:为什么加热可以促进化学反应的进行?
概念:单位酶在单位时间内底物减少的量或产物增加的量表示。
5 酶的催化活性
6 酶催化效应的特点
6.1 专一性
6.1.1 只有特定形状的底物才能和酶结合
6.1.2 一种酶只能催化一种或一类化合物的反应
绝对专一性、相对专一性、键的专一性
(如:过氧化氢酶、胰蛋白酶、外切蛋白酶)
N
C
精氨酸
赖氨酸
胰蛋白酶
胰蛋白酶
胰蛋白酶能切开特定氨基酸(碱性氨基酸)羧基形成的肽键
6.2 高效性
E1:无催化剂
E2:+无机催化剂
E3:+有机催化剂(酶)
与无机催化剂相比,酶能更显著地降低反应的活化能,从而使反应更有效地进行
能量
反应历程
E1
E2
E3
H2O2
H2O+1/2O2
6.3 易受环境因素影响
6.3.1 温度
6.3.2 pH值
6.3.3 ...
胃蛋白酶
胰蛋白酶
注意:
①温度的图像与pH值的不一致性
②最适宜条件不一定是一个点,可能是一个区间
注意: 温度对酶促反应速率的影响的两个方面
① 温度升高,反应物分子所具有的能量增加,反应速度加快。【a】
② 酶分子本身具有热变性,会随温度的升高而发生空间结构的改变。温度升的越高,酶变性的速率越快,升到一定程度,酶将完全失活。【b】
③ 曲线c 是曲线a 与曲线b 的综合
注意: 1.低温会使酶活性降低,但不会破坏酶分子的结构,温度适宜时,酶的催化作用可以恢复。
2.低温下酶空间结构稳定,所以酶一般在低温条件下保存。
活性位点有两个
关键的氨基酸参
与催化淀粉的水解
7.1 激活调节
激活剂,指能使无活性的酶形成有活性的酶,或能提高酶活性的一类物质。
如Cl-是唾液淀粉酶的激活剂
7.2 抑制调节
7.2.1 不可逆抑制
7.2.2 可逆抑制
如重金属
竞争性抑制剂
非竞争性抑制剂
7 酶活性的调控(拓展知识3)
有活性
无活性
竞争性抑制剂
非竞争性抑制剂
抑制剂
╳
酶促反应调节示意图:
可逆性抑制剂与不可逆性抑制剂影响酶促反应曲线图解读
8 酶促反应的实验探究注意事项
证明酶具有专一性应该怎么做?
验证酶具有专一性应该怎么做?
酶1
酶2
酶3
酶…
底物1
底物2
底物3
底物…
需测试所有酶和所有底物的反应,即只有完全归纳,才能证明酶的专一性
若酶具有专一性,则
淀粉酶具有专一性
蔗糖酶具有专一性
淀粉酶能催化淀粉的水解,不能催化蔗糖的水解
淀粉酶能催化淀粉的水解,而蔗糖酶不能
实验验证
推论
推论
淀粉酶+淀粉
淀粉酶+蔗糖
实验验证
淀粉酶+淀粉
蔗糖酶+淀粉
模拟题提示:
模拟题把验证和证明混用,但我们要严于律己,规范自己的表述。
8.1 专一性实验
8.1.1 实验探究分组:酶相同,底物不同;底物相同,酶不同。
8.1.2 鉴定试剂与底物的选择,如试剂是本尼迪特就不能选择过氧化氢为底物。
8.1.3 异常阳性反应的可能原因:酶不纯或底物不纯。
8.1.4 其他细节:如唾液稀释200倍,淀粉用0.3%氯化钠溶解等。
8.2 探究pH对过氧化氢酶的影响
为什们要将滤纸片贴在上壁?增加滤纸片会有什么效果?为什么每次实验完要反复冲洗?淀粉为什么不能作为反应底物?
8.3 酶高效性实验
制匀浆(鸡肝或马铃薯)的目的;试管加塞;产物量与反应物量的关系曲线图等
酶
活化能
能障
高效性
专一性
作用条件温和
有机物
生理条件
酶的活性
pH
温度
是
降低
具有以下特性
也称
一般为
具有高的
主要影响因素
同课章节目录
