人教版选择性必修三 1.1.1 分子动理论的基本内容(一)课件(共26张PPT)
文档属性
| 名称 | 人教版选择性必修三 1.1.1 分子动理论的基本内容(一)课件(共26张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 18.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2025-08-26 00:00:00 | ||
图片预览







文档简介
(共26张PPT)
第一章 分子动理论
分子动理论的基本内容(一)
置身花海,为什么能够闻到这沁人心脾的香味呢
真香啊!
古希腊学者德谟克利特作出了解释:“花的原子” 飘到了人们鼻子里。
热学就是研究物质热运动规律及其应用的一门学科,是物理学的一个重要组成部分。
“花的原子”究竟是怎么运动的?
热运动
2
知道两种分子模型,体会建立模型在研究物理问题中的作用。
1
认识物体是由大量分子组成的。
重点
重难点
3
知道阿伏加德罗常数及其意义,会用阿伏加德罗常数进行计算或估算。
重点
物体是由大量分子组成的
一
视频:树叶内部的“宇宙”
构成物体的微小分子到底小到什么程度?我们该如何观察与计量呢?
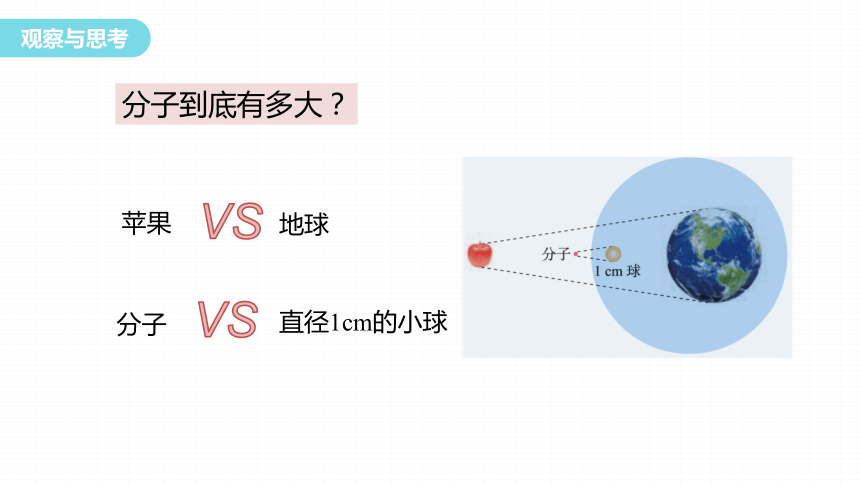
分子到底有多大?
苹果
地球
VS
分子
直径1cm的小球
VS
DNA分子结构图
氯化钠晶体结构图
(1)在研究物体的热运动性质和规律时,把组成物体的分子、原子或者离子统称为热学上的分子。
显微镜下的远古细胞
放大上亿倍的蛋白质分子结构模型
物体是由大量分子组成的
电子扫描隧道显微镜
(放大几亿倍)
(2)观察方法:用肉眼和高倍的光学显微镜都无法看到,只有用扫描隧道显微镜才能观察到物质表面原子的排列。
我国科学家用扫描隧道显微镜拍摄的石墨表面原子的排布
图中的每个亮斑都是一个碳原子
怎样才能看到分子?
(3)分子大小:多数分子直径的数量级为10-10 m。
除一些有机物质的大分子外
分子如何计量?
请回忆:
(2)是怎样定义的该量的?
(1)高中化学的哪一个量是联系宏观与微观世界的桥梁?
(2)数值:
1 mol的任何物质都有相同的粒子数
是微观世界的一个重要常数,是联系微观物理量和宏观物理量的桥梁。
(3)意义:
(1)定义:
NA=6.02×1023 mol-1
微观 宏观
NA
桥梁
阿伏加德罗常数
宏观量与微观量
微观量
m0 —分子质量
V0—分子体积
d —分子直径
V —物体体积
Vmol —摩尔体积
m —物体的质量
Mmol —摩尔质量
ρ — 物体的密度
宏观量
分子质量:
1mol物质的体积:
分子平均占有的体积:
1.已知水的摩尔质量为M,摩尔体积为Vmol,则一个水分子的质量为多大?假设水分子是一个挨着一个排列的,一个水分子的体积为多大?质量为m的水中含有水分子个数为多少?(已知阿伏加德罗常数为NA)
NA
2.若已知水的密度为ρ,则水的摩尔质量M与水的摩尔体积Vmol满足什么关系?
Vmol=或M=ρVmol
3.利用m0=和V0=能否估算氢气中氢气分子的质量和体积?
可以估算氢气分子的质量,不能估算氢气分子的体积,因为气体分子间不是紧密排列的。
1.仅利用下列某一组数据,可以计算出阿伏加德罗常数的是
A.水的密度和水的摩尔质量
B.水分子的体积和水分子的质量
C.水的摩尔质量和水分子的体积
D.水的摩尔质量和水分子的质量
√
由NA==知(其中m0、V0分别是一个水分子的质量和体积),D正确,A、B、C错误。
2.阿伏加德罗常量是NA,铜的摩尔质量是M,铜的密度是ρ,试推算出:
(1)1 m3铜所含的原子数目的表达式;
(2)1个铜原子占有体积大小的表达式。
答案 1 m3铜的物质的量n=(mol), 所以1 m3铜所含原子的数目的表达式 N=nNA=;
答案 1个铜原子占有的体积等于摩尔体积除以阿伏加德罗常量,则1个铜原子占有体积大小的表达式V=。
两种分子模型
二
d
d
d
d
固体和液体可看作一个一个紧挨着的球形分子排列而成的,忽略分子间空隙,如图所示。已知水的摩尔体积为Vmol,阿伏加德罗常数为NA,则一个水分子的直径为多大?
分子的直径
1.球模型
d
d=
V0=
V0=π()3
气体分子间的空隙很大,把气体分成若干个小立方体,气体分子位于每个小立方体的中心,如图所示。表示什么含义?若令d3=,d表示什么含义,能否表示气体分子的大小?
表示一个气体分子平均占有的空间
d
d
2.立方体模型
d表示相邻两个气体分子的平均距离,不能表示气体分子的大小
d
3.(2024·济南市高二期末)二氧化碳海洋封存技术能将二氧化碳封存在海底。研究发现,当水深超过2 500 m时,二氧化碳会变成近似固体的硬胶体。标准状态下二氧化碳气体的密度为ρ,二氧化碳的摩尔质量为M,NA表示阿伏加德罗常数,二氧化碳分子可近似看作直径为D的球体。则标准状态下体积为V的二氧化碳气体变成硬胶体后的体积为
A.NA B.NA C.NA D.NA
√
标准状态下体积为V的二氧化碳气体的质量m=ρV,二氧化碳的分子数为n=NA,二氧化碳气体变成硬胶体后,硬胶体的体积为V0=n·π()3,解得V0=NA,故选D。
4.(来自教材)标准状态下氧气分子间的平均距离是多少?氧气的摩尔质量为3.2×10-2 kg/mol,1 mol气体处于标准状态时的体积为2.24×10-2 m3,阿伏加德罗常数NA=6×1023 mol-1。
答案 3.3×10-9 m
每个氧气分子占有的体积V0== m3≈3.7×10-26 m3
将每个氧气分子占有的空间看成立方体,立方体的边长即氧气分子间的平均距离,由a3=V0
得a=≈ m≈3.3×10-9 m。
拓展1 由例4中的物理量求出氧气在标准状态下的密度。
答案 1.43 kg/m3
ρ== kg/m3≈1.43 kg/m3。
拓展2 在标准状态下体积为1 m3的氧气中含有多少个氧气分子?
答案 2.69×1025个
n=·NA=×6.02×1023个=2.69×1025个。
分子动理论的基本内容(一)
阿伏加德罗常数
1. 阿伏加德罗常数NA=6.02×1023 mol-1
2.微观量与宏观量的桥梁
1.球体模型(固体、液体)
2.立方体模型(气体)
两种分子模型
课堂总结
Keep Thinking!
第一章 分子动理论
分子动理论的基本内容(一)
置身花海,为什么能够闻到这沁人心脾的香味呢
真香啊!
古希腊学者德谟克利特作出了解释:“花的原子” 飘到了人们鼻子里。
热学就是研究物质热运动规律及其应用的一门学科,是物理学的一个重要组成部分。
“花的原子”究竟是怎么运动的?
热运动
2
知道两种分子模型,体会建立模型在研究物理问题中的作用。
1
认识物体是由大量分子组成的。
重点
重难点
3
知道阿伏加德罗常数及其意义,会用阿伏加德罗常数进行计算或估算。
重点
物体是由大量分子组成的
一
视频:树叶内部的“宇宙”
构成物体的微小分子到底小到什么程度?我们该如何观察与计量呢?
分子到底有多大?
苹果
地球
VS
分子
直径1cm的小球
VS
DNA分子结构图
氯化钠晶体结构图
(1)在研究物体的热运动性质和规律时,把组成物体的分子、原子或者离子统称为热学上的分子。
显微镜下的远古细胞
放大上亿倍的蛋白质分子结构模型
物体是由大量分子组成的
电子扫描隧道显微镜
(放大几亿倍)
(2)观察方法:用肉眼和高倍的光学显微镜都无法看到,只有用扫描隧道显微镜才能观察到物质表面原子的排列。
我国科学家用扫描隧道显微镜拍摄的石墨表面原子的排布
图中的每个亮斑都是一个碳原子
怎样才能看到分子?
(3)分子大小:多数分子直径的数量级为10-10 m。
除一些有机物质的大分子外
分子如何计量?
请回忆:
(2)是怎样定义的该量的?
(1)高中化学的哪一个量是联系宏观与微观世界的桥梁?
(2)数值:
1 mol的任何物质都有相同的粒子数
是微观世界的一个重要常数,是联系微观物理量和宏观物理量的桥梁。
(3)意义:
(1)定义:
NA=6.02×1023 mol-1
微观 宏观
NA
桥梁
阿伏加德罗常数
宏观量与微观量
微观量
m0 —分子质量
V0—分子体积
d —分子直径
V —物体体积
Vmol —摩尔体积
m —物体的质量
Mmol —摩尔质量
ρ — 物体的密度
宏观量
分子质量:
1mol物质的体积:
分子平均占有的体积:
1.已知水的摩尔质量为M,摩尔体积为Vmol,则一个水分子的质量为多大?假设水分子是一个挨着一个排列的,一个水分子的体积为多大?质量为m的水中含有水分子个数为多少?(已知阿伏加德罗常数为NA)
NA
2.若已知水的密度为ρ,则水的摩尔质量M与水的摩尔体积Vmol满足什么关系?
Vmol=或M=ρVmol
3.利用m0=和V0=能否估算氢气中氢气分子的质量和体积?
可以估算氢气分子的质量,不能估算氢气分子的体积,因为气体分子间不是紧密排列的。
1.仅利用下列某一组数据,可以计算出阿伏加德罗常数的是
A.水的密度和水的摩尔质量
B.水分子的体积和水分子的质量
C.水的摩尔质量和水分子的体积
D.水的摩尔质量和水分子的质量
√
由NA==知(其中m0、V0分别是一个水分子的质量和体积),D正确,A、B、C错误。
2.阿伏加德罗常量是NA,铜的摩尔质量是M,铜的密度是ρ,试推算出:
(1)1 m3铜所含的原子数目的表达式;
(2)1个铜原子占有体积大小的表达式。
答案 1 m3铜的物质的量n=(mol), 所以1 m3铜所含原子的数目的表达式 N=nNA=;
答案 1个铜原子占有的体积等于摩尔体积除以阿伏加德罗常量,则1个铜原子占有体积大小的表达式V=。
两种分子模型
二
d
d
d
d
固体和液体可看作一个一个紧挨着的球形分子排列而成的,忽略分子间空隙,如图所示。已知水的摩尔体积为Vmol,阿伏加德罗常数为NA,则一个水分子的直径为多大?
分子的直径
1.球模型
d
d=
V0=
V0=π()3
气体分子间的空隙很大,把气体分成若干个小立方体,气体分子位于每个小立方体的中心,如图所示。表示什么含义?若令d3=,d表示什么含义,能否表示气体分子的大小?
表示一个气体分子平均占有的空间
d
d
2.立方体模型
d表示相邻两个气体分子的平均距离,不能表示气体分子的大小
d
3.(2024·济南市高二期末)二氧化碳海洋封存技术能将二氧化碳封存在海底。研究发现,当水深超过2 500 m时,二氧化碳会变成近似固体的硬胶体。标准状态下二氧化碳气体的密度为ρ,二氧化碳的摩尔质量为M,NA表示阿伏加德罗常数,二氧化碳分子可近似看作直径为D的球体。则标准状态下体积为V的二氧化碳气体变成硬胶体后的体积为
A.NA B.NA C.NA D.NA
√
标准状态下体积为V的二氧化碳气体的质量m=ρV,二氧化碳的分子数为n=NA,二氧化碳气体变成硬胶体后,硬胶体的体积为V0=n·π()3,解得V0=NA,故选D。
4.(来自教材)标准状态下氧气分子间的平均距离是多少?氧气的摩尔质量为3.2×10-2 kg/mol,1 mol气体处于标准状态时的体积为2.24×10-2 m3,阿伏加德罗常数NA=6×1023 mol-1。
答案 3.3×10-9 m
每个氧气分子占有的体积V0== m3≈3.7×10-26 m3
将每个氧气分子占有的空间看成立方体,立方体的边长即氧气分子间的平均距离,由a3=V0
得a=≈ m≈3.3×10-9 m。
拓展1 由例4中的物理量求出氧气在标准状态下的密度。
答案 1.43 kg/m3
ρ== kg/m3≈1.43 kg/m3。
拓展2 在标准状态下体积为1 m3的氧气中含有多少个氧气分子?
答案 2.69×1025个
n=·NA=×6.02×1023个=2.69×1025个。
分子动理论的基本内容(一)
阿伏加德罗常数
1. 阿伏加德罗常数NA=6.02×1023 mol-1
2.微观量与宏观量的桥梁
1.球体模型(固体、液体)
2.立方体模型(气体)
两种分子模型
课堂总结
Keep Thinking!
同课章节目录
- 第一章 分子动理论
- 1 分子动理论的基本内容
- 2 实验:用油膜法估测油酸分子的大小
- 3 分子运动速率分布规律
- 4 分子动能和分子势能
- 第二章 气体、固体和液体
- 1 温度和温标
- 2 气体的等温变化
- 3 气体的等压变化和等容变化
- 4 固体
- 5 液体
- 第三章 热力学定律
- 1 功、热和内能的改变
- 2 热力学第一定律
- 3 能量守恒定律
- 4 热力学第二定律
- 第四章 原子结构和波粒二象性
- 1 普朗克黑体辐射理论
- 2 光电效应
- 3 原子的核式结构模型
- 4 氢原子光谱和玻尔的原子模型
- 5 粒子的波动性和量子力学的建立
- 第五章 原子核
- 1 原子核的组成
- 2 放射性元素的衰变
- 3 核力与结合能
- 4 核裂变与核聚变
- 5 “基本”粒子
