人教版(2019)高中化学选择性必修一 1.1 反应热、热化学方程式书写 课件(共40张PPT)
文档属性
| 名称 | 人教版(2019)高中化学选择性必修一 1.1 反应热、热化学方程式书写 课件(共40张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-27 00:00:00 | ||
图片预览









文档简介
(共40张PPT)
第一章 化学反应的热效应
第一节 反应热
01
反应热 焓变
③ 酸碱
中和反应
①燃烧
④ 大部分
化合反应
②金属与水
/酸反应
⑤ 铝热
反应
化学反应过程中伴随着能量变化,通常体现为热量变化。
常见的放热反应:
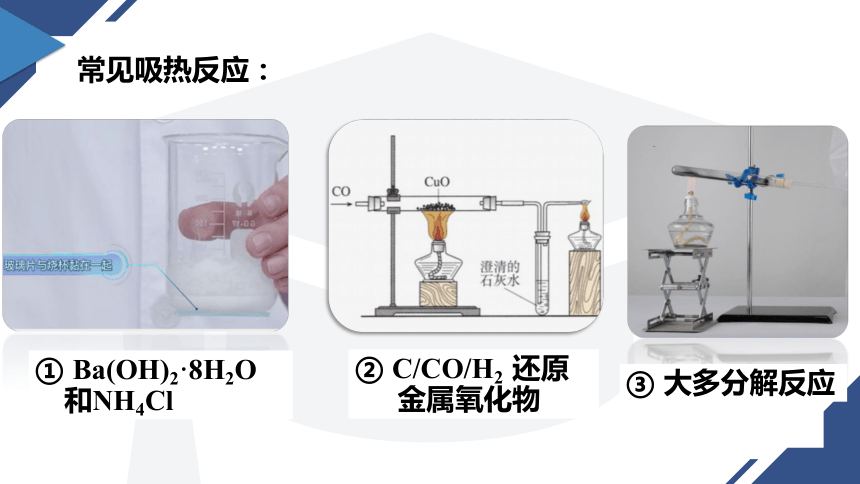
常见吸热反应:
① Ba(OH)2·8H2O
和NH4Cl
② C/CO/H2 还原
金属氧化物
③ 大多分解反应
KMnO4
反应热 焓变
一、
(1)反应热:在等温条件下,化学反应体系向环境释放或从环境吸收的热量,称为化学反应的热效应,简称反应热。
注意:等温条件指的是反应前后体系温度相等
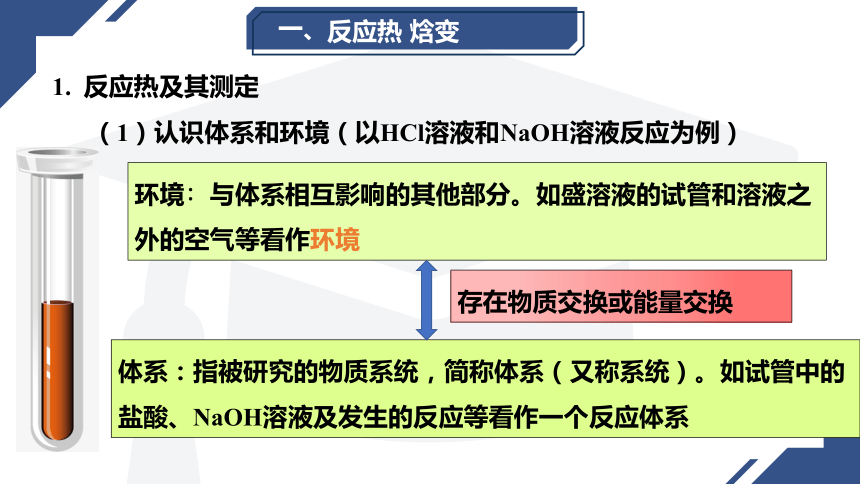
环境∶与体系相互影响的其他部分。如盛溶液的试管和溶液之外的空气等看作环境
体系:指被研究的物质系统,简称体系(又称系统)。如试管中的盐酸、NaOH溶液及发生的反应等看作一个反应体系
存在物质交换或能量交换
(1)认识体系和环境(以HCl溶液和NaOH溶液反应为例)
反应热 焓变
一、
1. 反应热及其测定
许多反应热可以通过量热计直接测定
反应热的测定工具
反应热 焓变
一、
(3)反应热的测定
中和反应反应热的测定
反应热 焓变
一、
(3)反应热的测定
例如,盐酸与NaOH溶液反应的过程中会放出热量,导致体系与环境之间的温度产生差异。
在反应前后,如果环境的温度没有变化,则反应放出的热量就会使体系的温度升高,这时可以根据测得的体系的温度变化和有关物质的比热容等来计算反应热
计算公式:Q = c · m ·(t2-t1)
c:比热容
m:体系的质量
t1、t2:反应前和反应后体系的温度
Q:放出的热量
步骤二:用另一个量筒量取50 mL 0.55 mol/L NaOH溶液,用温度计测量并记录NaOH溶液的温度(数据填入下表)。
为了保证HCl被完全中和
步骤一:用量筒量取50 mL 0.50 mol/L盐酸,打开杯盖,倒入量热计的内筒,盖上杯盖,插入温度计,测量并记录盐酸的温度(数据填入下表)。用水把温度计上的酸冲洗干净,擦干备用。
中和反应反应热的测定
反应热 焓变
一、
(3)反应热的测定
步骤四:重复上述步骤两次。
为了减小误差
步骤三:打开杯盖,将量筒中的NaOH溶液迅速倒入量热计的内筒,立即盖上杯盖,插入温度计,用搅拌器匀速搅拌。密切关注温度变化,将最高温度记为反应后体系的温度(t2)。
中和反应反应热的测定
反应热 焓变
一、
(3)反应热的测定
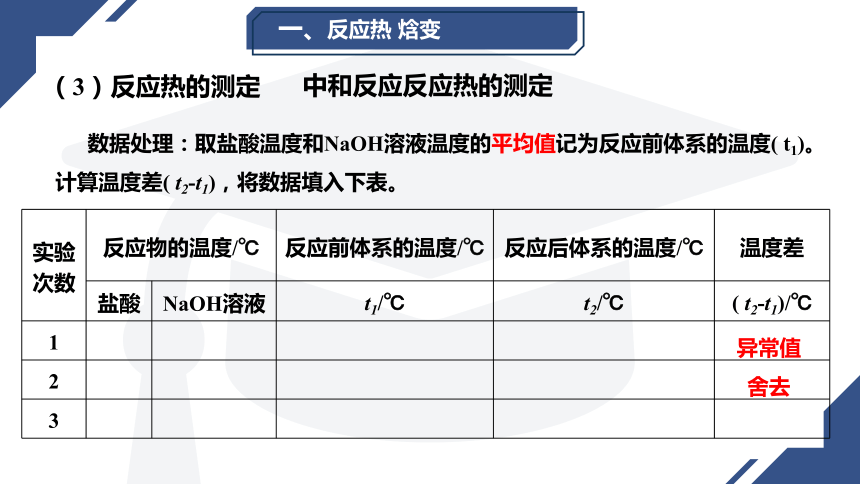
数据处理:取盐酸温度和NaOH溶液温度的平均值记为反应前体系的温度( t1)。计算温度差( t2-t1),将数据填入下表。
实验次数 反应物的温度/℃ 反应前体系的温度/℃ 反应后体系的温度/℃ 温度差
盐酸 NaOH溶液 t1/℃ t2/℃ ( t2-t1)/℃
1
2
3
中和反应反应热的测定
反应热 焓变
一、
(3)反应热的测定
异常值舍去
为了计算简便,可以近似地认为实验所用酸、碱稀溶液的密度、比热容与水的相同,并忽略量热计的比热容,则:
① 50 mL 0.50 mol/L 盐酸的质量 m1=50 g, 50 mL 0.55 mol/L NaOH 溶液的质量m2=50 g;
②反应后生成的溶液的比热容c=4.18 J/(g· ℃ ), 50 mL 0.50 mol/L盐酸与 50 mL 0.55 mol/L NaOH溶液发生中和反应时放出的热量为:(m1+m2)· c· (t2-t1)=_________________
③生成1 mol H2O时放出的热量为______________。
取三次测量所得温度差的平均值作为计算依据。
根据温度差和比热容等计算反应热。
多次计算求平均值以减小实验误差
中和反应反应热的测定
反应热 焓变
一、
(3)反应热的测定
使反应物迅速混合,使反应充分进行,保持体系的温度均匀。
测量反应前后体系的温度
反应容器
减少热量散失,
降低实验误差。
减少热量散失,降低实验误差。
量热计
注意:1. 该实验中只用一个温度计,每次测量完温度后,必须用水洗净并用滤纸擦干后再使用
2. 在测量反应混合液的温度时要随时读取温度值,并记录最高温度值。
大量实验测得在25℃和101kPa下,________跟_______的______溶液发生中和反应生成_____________时所释放的热量为 57.3 kJ。
强酸
强碱
稀
1mol水
HCl
NaOH
HNO3
Ba(OH)2
H2SO4
HNO3
NH3·H2O
Ba(OH)2
CH3COOH
NaOH
×
×
×
中和反应反应热的测定
试判断下列酸碱稀溶液发生中和反应生成1mol水的反应热是否为57.3kJ/mol
等压
研究表明,等压条件下进行的化学反应(严格地说,对反应体系做功还有限定,中学阶段一般不考虑),其反应热等于反应的焓变,用符号ΔH表示
化学反应为什么会产生反应热?
体系
内能改变
产生
反应热
反应热
(焓变)
反应热 焓变
一、
2、焓变
(1)焓的定义:为了描述等压条件下的反应热,科学上引入了一个与内能有关的物理量(无法直接测量)
符号:H 单位:kJ·mol-1
影响因素:
反应物本身的性质
物质的状态:气态(g) > 液态(l)>固态(s)温度:T↑→H↑
压强:P↑→H↑
反应热 焓变
一、
(2)焓变的定义:研究表明,等压条件下进行的化学反应(严格地说,对反应体系做功还有限定,中学阶段一般不考虑),其反应热等于反应的焓变,用符号ΔH表示
2、焓变
ΔH=H生成物-H反应物
kJ/mol 或 kJ mol-1
单位:
数学表达式:
反应热 焓变
一、
(3)从宏观角度分析焓变
2、焓变
放热反应
∑H (反应物)> ∑H(生成物)
吸热反应
∑H (反应物) < ∑H(生成物)
(体系焓降低)
(体系焓升高)
H < 0
H > 0
反应热 焓变
一、
(4)从微观角度分析焓变
2、焓变
反应物
生成物
键断裂
键生成
原子重新组合
吸收能量
放出能量
化学反应的实质:旧的化学键断裂和新的化学键形成过程。
H(估算)=∑E (反应物键能)-∑E (生成物键能)
【例1】依据信息估算2 mol H2(g) 和1 mol O2(g) 反应生成2 mol H2O(g) 的反应热 H=?
H(估算)= ∑E (反应物键能)-∑E (生成物键能)
=2×436 kJ/mol+498 kJ/mol-4×463.4 kJ/mol
= 483.6 kJ/mol
2H2(g) + O2(g) 2H2O(g) H=?
2H2
O2
4H
2O
2H2O
1 mol H2(g)中的H-H键断裂吸收436 kJ能量
1 mol O2(g)中的化学键断裂吸收498 kJ能量
形成H2O(g)中1 mol H-O键释放463.4 kJ能量
反应热 焓变 焓
概念
符号
单位 数值
联系 注意 反应热、焓、焓变的比较
在等温条件下,化学反应体系向环境释放或从环境吸收的热量
化学反应中生成物的总焓与反应物的总焓之差
物质所具有的能量
等压条件下的反应热为ΔH
ΔH
H
kJ/mol
正值表示反应吸热;负值表示反应放热
只有正值
反应热=焓变(等压);ΔH=H(生成物)-H(反成物)
任何化学反应都有反应热。
物质三态之间变化的焓变不能叫反应热,反应热是化学反应的焓变。
A.每生成2个AB分子吸收(a-b)kJ热量
B.该反应热ΔH=+(a-b)kJ·mol-1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量
1.化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,下列叙述中正确的是( )
B
【课堂练习】
2.已知 C(石墨,s)= C(金刚石,s)ΔH = +1.9kJ/mol 判断石墨、金刚石哪个更稳定?
金刚石
石墨
物质能量、键能与稳定性的关系:
1.键能越大,破坏该化学键需要的能量越高,该化学键越难断裂,所以物质越稳定。
2.物质能量越低,物质越稳定。
石墨更稳定
3.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:下列说法正确的是( )
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
C
4.SF6是一种优良的绝缘气体,分子结构中只存在S—F。已知:1 mol S(s)转化为气态硫原子吸收能量280 kJ,断裂1 mol F—F、S—F需吸收的能量分别为160 kJ、330 kJ。则反应S(s)+3F2(g)===SF6(g)的反应热ΔH为( )
A.-1 780 kJ·mol-1 B.-1 220 kJ·mol-1
C.-450 kJ·mol-1 D.+430 kJ·mol-1
B
5.下表是部分化学键的键能数据:
(1)已知1 mol白磷燃烧生成P4O10(s)的反应热ΔH=-2 982 kJ·mol-1,白磷(P4)、P4O6、P4O10结构如图所示,则上表中x=________。
(2)0.5 mol白磷(P4)与O2完全反应生成固态P4O6放出的热量为________ kJ。
585
819
化学键 P—P P—O O==O P==O
键能/(kJ·mol-1) 198 360 498 x
02
热化学方程式
热化学方程式
二、
1.概念:
2.意义:
H2(g)+I2(g) ====== 2HI(g) △H=-14.9kJ/mol
200℃
101kPa
物质状态
温度和压强
能量变化
表示:在200℃、101 kPa时,1 mol气态H2与1 mol气态I2完全反应生成2mol气态HI,放出14.9kJ的热量。
表明反应所释放或吸收的热量的化学方程式
能表示实际参加反应物质的量和反应热的关系
对于 25℃(298K) 101kPa时进行的反应可不注明
热化学方程式
二、
观察以上三个热化学方程式,试总结书写时应该注意的事项
H2(g) + O2(g) H2O(l) H2= 285.8 kJ/mol
H2(g) + O2(g) H2O(g) H1= 241.8 kJ/mol
2H2(g) + O2(g) 2H2O(g) H3= 483.6 kJ/mol
2H2O(g) 2H2(g) + O2(g) H4=+483.6 kJ/mol
①标明各物质的聚集状态(s-固体、l-液体、g-气体、aq-溶液)
②化学计量数不表示分子数或原子个数,仅表示物质的量(可以是整数,也可以是分数), H数值与化学计量数相对应,正逆反应的ΔH绝对值相等,符号相反
③一般不写反应条件,需注明反应的温度、压强(250C ,101kPa时可不注明)
阅读教材P9,思考:ΔH 中的单位mol-1代表什么含义?
【例1】依据反应事实,写出下列反应的热化学方程式(常温下)
HCl(aq) + NaOH(aq) NaCl(aq) + H2O(l) H= 57.3 kJ/mol
1 L 1 mol/L HCl和 1 L 1 mol/L NaOH溶液恰好完全反应放出57.3 kJ的热量
01
1 mol N2(g)与适量H2(g)反应,生成NH3(g),放出92.2 kJ热量
02
1 mol Cu(s)与适量O2(g)反应,生成CuO(s),放出157 kJ热量
03
N2(g) + 3H2(g) 2NH3(g) H= 92.2 kJ/mol
Cu(s) + O2(g) CuO(s) H= 157 kJ/mol
1
2
【课堂练习】
B.NaOH(aq)+HCl(aq) NaCl(aq)+H2O(l) ΔH=+57.3 kJ/mol
A.C2H5OH+3O2 2CO2+3H2O ΔH=-1 366.8 kJ/mol
判断下列热化学方程式中书写是否正确,说明错误原因
C.S(s)+O2(g) SO2(g) ΔH=-296.8 kJ/mol
D.2NO(g)+O2(g) 2NO2(g) ΔH=-116.2 kJ
×
×
√
×
热化学方程式
二、
3. 热化学方程式正误判断方法
放热反应一定为“—”,吸热反应一定为“+”
单位一般为“kJ·mol-1”,易写错成“kJ”或漏写
物质的状态必须正确,特别是溶液中的反应易写错
反应热的数值必须与热化学方程式的化学计量数相对应。当反应逆向进行时,其反应热与正反应的反应热数值相等,符号相反
一审“+” “-”
二审单位
三审状态
四审数值对应性
五审是否符合概念
如表示燃烧热、中和反应反应热的热化学方程式是否正确
03
燃烧热
燃烧热
三、
1、定义:101 kPa时,1 mol纯物质完全燃烧生成指定产物时所放出的热量,
单位为kJ/mol
注意:
碳元素变为CO2(g) 、氢元素变为H2O(l)、硫元素变为SO2(g)、氮元素变为N2(g)等
例如:
H2(g) + O2(g) H2O(l) H2= 285.8 kJ/mol
1
2
H2(g) + O2(g) H2O(g) H1= 241.8 kJ/mol
1
2
哪个表示的是氢气的燃烧热的热化学方程式?
2H2(g) + O2(g) 2H2O(l) H3= 571.6 kJ/mol
燃烧热
三、
2、燃烧热的热化学方程式正误判断方法
一看
可燃物的化学计量数是否为1
二看
三看
元素完全燃烧生成的物质是否为指定产物
ΔH的数值和单位是否正确
例:0.3mol的气态高能燃料乙炔(C2H2)在氧气中完全燃烧,生成气态CO2和液态水,放出389.88kJ热量,其燃烧的热化学方程式_________________________________
其燃烧热为 ______________________
表示燃烧热的热化学方程式为_____________________________________________
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H= -2599.2kJ/mol
1299.6kJ/mol
C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l) △H= -1299.6kJ/mol
【例1】依据反应事实,按要求写出下列反应的热化学方程式(常温下)
8 g CH4完全燃烧,放出445.0 kJ热量,写出其燃烧热的热化学方程式
01
1 mol 气态丙烷在O2(g)中燃烧,生成CO2(g)和H2O(l),放出2219.9 kJ热量,
写出其燃烧的热化学方程式
02
煤气的主要成分为CO和H2,常温下14 g CO完全燃烧,放出141.5 kJ热量写出
其燃烧的热化学方程式
03
CH4(g) + 2O2(g) CO2(g) + 2H2O(l) H= 890 kJ/mol
C3H8(g) + 5O2(g) 3CO2(g) + 4H2O(l) H= 2219.9 kJ/mol
1
2
CO(g) + O2(g) CO2(g) H= 283 kJ/mol
2CO(g) + O2(g) 2CO2(g) H= 566 kJ/mol
某些物质的燃烧热(25 ℃,101 kPa) 名称 化学式 ΔH kJ/mol 名称 化学式 ΔH
kJ/mol
石墨 C(s) -393.5 乙烷 C2H6(g) -1559.8
金刚石 C(s) -395.0 乙烯 C2H4(g) -1411.0
氢气 H2(g) -285.8 乙炔 C2H2(g) -1299.6
一氧化碳 CO(g) -283.0 乙醇 C2H5OH(l) -1366.8
甲烷 CH4(g) -890.31 丙烷 C3H8(g) -2219.9
甲醇 CH3OH(l) -726.51 苯 C6H6(l) -3267.5
长征五号B运载火箭是专门为中国载人航天工程空间站建设而研制的一型新型运载火箭,以液态氧和液态氢作为火箭推进剂燃料,结合下表解释原因并写出热化学方程式。
某些物质的燃烧热(25 ℃,101 kPa) 名称 化学式 ΔH/kJ/mol 名称 化学式 ΔH/kJ/mol
石墨 C(s) -393.5 乙烷 C2H6(g) -1559.8
金刚石 C(s) -395.0 乙烯 C2H4(g) -1411.0
氢气 H2(g) -285.8 乙炔 C2H2(g) -1299.6
一氧化碳 CO(g) -283.0 乙醇 C2H5OH(l) -1366.8
甲烷 CH4(g) -890.31 丙烷 C3H8(g) -2219.9
甲醇 CH3OH(l) -726.51 苯 C6H6(l) -3267.5
火箭推进剂燃料的选择
H2(g) + O2(g) H2O(l) H= 285.8 kJ/mol
1
2
H2(g) + O2(g) H2O(g) H= 241.8 kJ/mol
1
2
单位质量产生热量: ≈ 13.4 kJ/g
241.8 kJ
2 g+16 g
1.已知下列两个热化学方程式:
2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
C3H8(g)+5O2(g)===3CO2(g)+4H2O(l) ΔH=-2 220 kJ·mol-1
请根据上面两个热化学方程式,回答下列问题:
(1)H2的燃烧热为________________,C3H8的燃烧热为________________。
(2)1 mol H2和2 mol C3H8组成的混合气体完全燃烧释放的热量为____________。
(3)现有H2和C3H8的混合气体共5 mol,完全燃烧时放热3 846.75 kJ,则在混合气体中H2和C3H8的体积比是________。
285.8 kJ·mol-1
2 220 kJ·mol-1
4 725.8 KJ
3:1
2.已知:
H+(aq)+OH-(aq)===H2O(l) ΔH1=-57.3 kJ·mol-1
1/2H2SO4(浓,aq)+NaOH(aq)===1/2Na2SO4(aq)+H2O(l) ΔH2=m kJ·mol-1
下列说法正确的是( )
A.上述热化学方程式中的化学计量数表示物质的量
B.ΔH1<ΔH2
C.ΔH2=-57.3 kJ·mol-1
D.|ΔH1|>|ΔH2|
A
第一章 化学反应的热效应
第一节 反应热
01
反应热 焓变
③ 酸碱
中和反应
①燃烧
④ 大部分
化合反应
②金属与水
/酸反应
⑤ 铝热
反应
化学反应过程中伴随着能量变化,通常体现为热量变化。
常见的放热反应:
常见吸热反应:
① Ba(OH)2·8H2O
和NH4Cl
② C/CO/H2 还原
金属氧化物
③ 大多分解反应
KMnO4
反应热 焓变
一、
(1)反应热:在等温条件下,化学反应体系向环境释放或从环境吸收的热量,称为化学反应的热效应,简称反应热。
注意:等温条件指的是反应前后体系温度相等
环境∶与体系相互影响的其他部分。如盛溶液的试管和溶液之外的空气等看作环境
体系:指被研究的物质系统,简称体系(又称系统)。如试管中的盐酸、NaOH溶液及发生的反应等看作一个反应体系
存在物质交换或能量交换
(1)认识体系和环境(以HCl溶液和NaOH溶液反应为例)
反应热 焓变
一、
1. 反应热及其测定
许多反应热可以通过量热计直接测定
反应热的测定工具
反应热 焓变
一、
(3)反应热的测定
中和反应反应热的测定
反应热 焓变
一、
(3)反应热的测定
例如,盐酸与NaOH溶液反应的过程中会放出热量,导致体系与环境之间的温度产生差异。
在反应前后,如果环境的温度没有变化,则反应放出的热量就会使体系的温度升高,这时可以根据测得的体系的温度变化和有关物质的比热容等来计算反应热
计算公式:Q = c · m ·(t2-t1)
c:比热容
m:体系的质量
t1、t2:反应前和反应后体系的温度
Q:放出的热量
步骤二:用另一个量筒量取50 mL 0.55 mol/L NaOH溶液,用温度计测量并记录NaOH溶液的温度(数据填入下表)。
为了保证HCl被完全中和
步骤一:用量筒量取50 mL 0.50 mol/L盐酸,打开杯盖,倒入量热计的内筒,盖上杯盖,插入温度计,测量并记录盐酸的温度(数据填入下表)。用水把温度计上的酸冲洗干净,擦干备用。
中和反应反应热的测定
反应热 焓变
一、
(3)反应热的测定
步骤四:重复上述步骤两次。
为了减小误差
步骤三:打开杯盖,将量筒中的NaOH溶液迅速倒入量热计的内筒,立即盖上杯盖,插入温度计,用搅拌器匀速搅拌。密切关注温度变化,将最高温度记为反应后体系的温度(t2)。
中和反应反应热的测定
反应热 焓变
一、
(3)反应热的测定
数据处理:取盐酸温度和NaOH溶液温度的平均值记为反应前体系的温度( t1)。计算温度差( t2-t1),将数据填入下表。
实验次数 反应物的温度/℃ 反应前体系的温度/℃ 反应后体系的温度/℃ 温度差
盐酸 NaOH溶液 t1/℃ t2/℃ ( t2-t1)/℃
1
2
3
中和反应反应热的测定
反应热 焓变
一、
(3)反应热的测定
异常值舍去
为了计算简便,可以近似地认为实验所用酸、碱稀溶液的密度、比热容与水的相同,并忽略量热计的比热容,则:
① 50 mL 0.50 mol/L 盐酸的质量 m1=50 g, 50 mL 0.55 mol/L NaOH 溶液的质量m2=50 g;
②反应后生成的溶液的比热容c=4.18 J/(g· ℃ ), 50 mL 0.50 mol/L盐酸与 50 mL 0.55 mol/L NaOH溶液发生中和反应时放出的热量为:(m1+m2)· c· (t2-t1)=_________________
③生成1 mol H2O时放出的热量为______________。
取三次测量所得温度差的平均值作为计算依据。
根据温度差和比热容等计算反应热。
多次计算求平均值以减小实验误差
中和反应反应热的测定
反应热 焓变
一、
(3)反应热的测定
使反应物迅速混合,使反应充分进行,保持体系的温度均匀。
测量反应前后体系的温度
反应容器
减少热量散失,
降低实验误差。
减少热量散失,降低实验误差。
量热计
注意:1. 该实验中只用一个温度计,每次测量完温度后,必须用水洗净并用滤纸擦干后再使用
2. 在测量反应混合液的温度时要随时读取温度值,并记录最高温度值。
大量实验测得在25℃和101kPa下,________跟_______的______溶液发生中和反应生成_____________时所释放的热量为 57.3 kJ。
强酸
强碱
稀
1mol水
HCl
NaOH
HNO3
Ba(OH)2
H2SO4
HNO3
NH3·H2O
Ba(OH)2
CH3COOH
NaOH
×
×
×
中和反应反应热的测定
试判断下列酸碱稀溶液发生中和反应生成1mol水的反应热是否为57.3kJ/mol
等压
研究表明,等压条件下进行的化学反应(严格地说,对反应体系做功还有限定,中学阶段一般不考虑),其反应热等于反应的焓变,用符号ΔH表示
化学反应为什么会产生反应热?
体系
内能改变
产生
反应热
反应热
(焓变)
反应热 焓变
一、
2、焓变
(1)焓的定义:为了描述等压条件下的反应热,科学上引入了一个与内能有关的物理量(无法直接测量)
符号:H 单位:kJ·mol-1
影响因素:
反应物本身的性质
物质的状态:气态(g) > 液态(l)>固态(s)温度:T↑→H↑
压强:P↑→H↑
反应热 焓变
一、
(2)焓变的定义:研究表明,等压条件下进行的化学反应(严格地说,对反应体系做功还有限定,中学阶段一般不考虑),其反应热等于反应的焓变,用符号ΔH表示
2、焓变
ΔH=H生成物-H反应物
kJ/mol 或 kJ mol-1
单位:
数学表达式:
反应热 焓变
一、
(3)从宏观角度分析焓变
2、焓变
放热反应
∑H (反应物)> ∑H(生成物)
吸热反应
∑H (反应物) < ∑H(生成物)
(体系焓降低)
(体系焓升高)
H < 0
H > 0
反应热 焓变
一、
(4)从微观角度分析焓变
2、焓变
反应物
生成物
键断裂
键生成
原子重新组合
吸收能量
放出能量
化学反应的实质:旧的化学键断裂和新的化学键形成过程。
H(估算)=∑E (反应物键能)-∑E (生成物键能)
【例1】依据信息估算2 mol H2(g) 和1 mol O2(g) 反应生成2 mol H2O(g) 的反应热 H=?
H(估算)= ∑E (反应物键能)-∑E (生成物键能)
=2×436 kJ/mol+498 kJ/mol-4×463.4 kJ/mol
= 483.6 kJ/mol
2H2(g) + O2(g) 2H2O(g) H=?
2H2
O2
4H
2O
2H2O
1 mol H2(g)中的H-H键断裂吸收436 kJ能量
1 mol O2(g)中的化学键断裂吸收498 kJ能量
形成H2O(g)中1 mol H-O键释放463.4 kJ能量
反应热 焓变 焓
概念
符号
单位 数值
联系 注意 反应热、焓、焓变的比较
在等温条件下,化学反应体系向环境释放或从环境吸收的热量
化学反应中生成物的总焓与反应物的总焓之差
物质所具有的能量
等压条件下的反应热为ΔH
ΔH
H
kJ/mol
正值表示反应吸热;负值表示反应放热
只有正值
反应热=焓变(等压);ΔH=H(生成物)-H(反成物)
任何化学反应都有反应热。
物质三态之间变化的焓变不能叫反应热,反应热是化学反应的焓变。
A.每生成2个AB分子吸收(a-b)kJ热量
B.该反应热ΔH=+(a-b)kJ·mol-1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量
1.化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,下列叙述中正确的是( )
B
【课堂练习】
2.已知 C(石墨,s)= C(金刚石,s)ΔH = +1.9kJ/mol 判断石墨、金刚石哪个更稳定?
金刚石
石墨
物质能量、键能与稳定性的关系:
1.键能越大,破坏该化学键需要的能量越高,该化学键越难断裂,所以物质越稳定。
2.物质能量越低,物质越稳定。
石墨更稳定
3.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:下列说法正确的是( )
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
C
4.SF6是一种优良的绝缘气体,分子结构中只存在S—F。已知:1 mol S(s)转化为气态硫原子吸收能量280 kJ,断裂1 mol F—F、S—F需吸收的能量分别为160 kJ、330 kJ。则反应S(s)+3F2(g)===SF6(g)的反应热ΔH为( )
A.-1 780 kJ·mol-1 B.-1 220 kJ·mol-1
C.-450 kJ·mol-1 D.+430 kJ·mol-1
B
5.下表是部分化学键的键能数据:
(1)已知1 mol白磷燃烧生成P4O10(s)的反应热ΔH=-2 982 kJ·mol-1,白磷(P4)、P4O6、P4O10结构如图所示,则上表中x=________。
(2)0.5 mol白磷(P4)与O2完全反应生成固态P4O6放出的热量为________ kJ。
585
819
化学键 P—P P—O O==O P==O
键能/(kJ·mol-1) 198 360 498 x
02
热化学方程式
热化学方程式
二、
1.概念:
2.意义:
H2(g)+I2(g) ====== 2HI(g) △H=-14.9kJ/mol
200℃
101kPa
物质状态
温度和压强
能量变化
表示:在200℃、101 kPa时,1 mol气态H2与1 mol气态I2完全反应生成2mol气态HI,放出14.9kJ的热量。
表明反应所释放或吸收的热量的化学方程式
能表示实际参加反应物质的量和反应热的关系
对于 25℃(298K) 101kPa时进行的反应可不注明
热化学方程式
二、
观察以上三个热化学方程式,试总结书写时应该注意的事项
H2(g) + O2(g) H2O(l) H2= 285.8 kJ/mol
H2(g) + O2(g) H2O(g) H1= 241.8 kJ/mol
2H2(g) + O2(g) 2H2O(g) H3= 483.6 kJ/mol
2H2O(g) 2H2(g) + O2(g) H4=+483.6 kJ/mol
①标明各物质的聚集状态(s-固体、l-液体、g-气体、aq-溶液)
②化学计量数不表示分子数或原子个数,仅表示物质的量(可以是整数,也可以是分数), H数值与化学计量数相对应,正逆反应的ΔH绝对值相等,符号相反
③一般不写反应条件,需注明反应的温度、压强(250C ,101kPa时可不注明)
阅读教材P9,思考:ΔH 中的单位mol-1代表什么含义?
【例1】依据反应事实,写出下列反应的热化学方程式(常温下)
HCl(aq) + NaOH(aq) NaCl(aq) + H2O(l) H= 57.3 kJ/mol
1 L 1 mol/L HCl和 1 L 1 mol/L NaOH溶液恰好完全反应放出57.3 kJ的热量
01
1 mol N2(g)与适量H2(g)反应,生成NH3(g),放出92.2 kJ热量
02
1 mol Cu(s)与适量O2(g)反应,生成CuO(s),放出157 kJ热量
03
N2(g) + 3H2(g) 2NH3(g) H= 92.2 kJ/mol
Cu(s) + O2(g) CuO(s) H= 157 kJ/mol
1
2
【课堂练习】
B.NaOH(aq)+HCl(aq) NaCl(aq)+H2O(l) ΔH=+57.3 kJ/mol
A.C2H5OH+3O2 2CO2+3H2O ΔH=-1 366.8 kJ/mol
判断下列热化学方程式中书写是否正确,说明错误原因
C.S(s)+O2(g) SO2(g) ΔH=-296.8 kJ/mol
D.2NO(g)+O2(g) 2NO2(g) ΔH=-116.2 kJ
×
×
√
×
热化学方程式
二、
3. 热化学方程式正误判断方法
放热反应一定为“—”,吸热反应一定为“+”
单位一般为“kJ·mol-1”,易写错成“kJ”或漏写
物质的状态必须正确,特别是溶液中的反应易写错
反应热的数值必须与热化学方程式的化学计量数相对应。当反应逆向进行时,其反应热与正反应的反应热数值相等,符号相反
一审“+” “-”
二审单位
三审状态
四审数值对应性
五审是否符合概念
如表示燃烧热、中和反应反应热的热化学方程式是否正确
03
燃烧热
燃烧热
三、
1、定义:101 kPa时,1 mol纯物质完全燃烧生成指定产物时所放出的热量,
单位为kJ/mol
注意:
碳元素变为CO2(g) 、氢元素变为H2O(l)、硫元素变为SO2(g)、氮元素变为N2(g)等
例如:
H2(g) + O2(g) H2O(l) H2= 285.8 kJ/mol
1
2
H2(g) + O2(g) H2O(g) H1= 241.8 kJ/mol
1
2
哪个表示的是氢气的燃烧热的热化学方程式?
2H2(g) + O2(g) 2H2O(l) H3= 571.6 kJ/mol
燃烧热
三、
2、燃烧热的热化学方程式正误判断方法
一看
可燃物的化学计量数是否为1
二看
三看
元素完全燃烧生成的物质是否为指定产物
ΔH的数值和单位是否正确
例:0.3mol的气态高能燃料乙炔(C2H2)在氧气中完全燃烧,生成气态CO2和液态水,放出389.88kJ热量,其燃烧的热化学方程式_________________________________
其燃烧热为 ______________________
表示燃烧热的热化学方程式为_____________________________________________
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H= -2599.2kJ/mol
1299.6kJ/mol
C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l) △H= -1299.6kJ/mol
【例1】依据反应事实,按要求写出下列反应的热化学方程式(常温下)
8 g CH4完全燃烧,放出445.0 kJ热量,写出其燃烧热的热化学方程式
01
1 mol 气态丙烷在O2(g)中燃烧,生成CO2(g)和H2O(l),放出2219.9 kJ热量,
写出其燃烧的热化学方程式
02
煤气的主要成分为CO和H2,常温下14 g CO完全燃烧,放出141.5 kJ热量写出
其燃烧的热化学方程式
03
CH4(g) + 2O2(g) CO2(g) + 2H2O(l) H= 890 kJ/mol
C3H8(g) + 5O2(g) 3CO2(g) + 4H2O(l) H= 2219.9 kJ/mol
1
2
CO(g) + O2(g) CO2(g) H= 283 kJ/mol
2CO(g) + O2(g) 2CO2(g) H= 566 kJ/mol
某些物质的燃烧热(25 ℃,101 kPa) 名称 化学式 ΔH kJ/mol 名称 化学式 ΔH
kJ/mol
石墨 C(s) -393.5 乙烷 C2H6(g) -1559.8
金刚石 C(s) -395.0 乙烯 C2H4(g) -1411.0
氢气 H2(g) -285.8 乙炔 C2H2(g) -1299.6
一氧化碳 CO(g) -283.0 乙醇 C2H5OH(l) -1366.8
甲烷 CH4(g) -890.31 丙烷 C3H8(g) -2219.9
甲醇 CH3OH(l) -726.51 苯 C6H6(l) -3267.5
长征五号B运载火箭是专门为中国载人航天工程空间站建设而研制的一型新型运载火箭,以液态氧和液态氢作为火箭推进剂燃料,结合下表解释原因并写出热化学方程式。
某些物质的燃烧热(25 ℃,101 kPa) 名称 化学式 ΔH/kJ/mol 名称 化学式 ΔH/kJ/mol
石墨 C(s) -393.5 乙烷 C2H6(g) -1559.8
金刚石 C(s) -395.0 乙烯 C2H4(g) -1411.0
氢气 H2(g) -285.8 乙炔 C2H2(g) -1299.6
一氧化碳 CO(g) -283.0 乙醇 C2H5OH(l) -1366.8
甲烷 CH4(g) -890.31 丙烷 C3H8(g) -2219.9
甲醇 CH3OH(l) -726.51 苯 C6H6(l) -3267.5
火箭推进剂燃料的选择
H2(g) + O2(g) H2O(l) H= 285.8 kJ/mol
1
2
H2(g) + O2(g) H2O(g) H= 241.8 kJ/mol
1
2
单位质量产生热量: ≈ 13.4 kJ/g
241.8 kJ
2 g+16 g
1.已知下列两个热化学方程式:
2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
C3H8(g)+5O2(g)===3CO2(g)+4H2O(l) ΔH=-2 220 kJ·mol-1
请根据上面两个热化学方程式,回答下列问题:
(1)H2的燃烧热为________________,C3H8的燃烧热为________________。
(2)1 mol H2和2 mol C3H8组成的混合气体完全燃烧释放的热量为____________。
(3)现有H2和C3H8的混合气体共5 mol,完全燃烧时放热3 846.75 kJ,则在混合气体中H2和C3H8的体积比是________。
285.8 kJ·mol-1
2 220 kJ·mol-1
4 725.8 KJ
3:1
2.已知:
H+(aq)+OH-(aq)===H2O(l) ΔH1=-57.3 kJ·mol-1
1/2H2SO4(浓,aq)+NaOH(aq)===1/2Na2SO4(aq)+H2O(l) ΔH2=m kJ·mol-1
下列说法正确的是( )
A.上述热化学方程式中的化学计量数表示物质的量
B.ΔH1<ΔH2
C.ΔH2=-57.3 kJ·mol-1
D.|ΔH1|>|ΔH2|
A
