人教版(2019)高中化学选择性必修一 1.1.1 反应热 焓变 课件(共23张PPT)
文档属性
| 名称 | 人教版(2019)高中化学选择性必修一 1.1.1 反应热 焓变 课件(共23张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 7.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-27 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
选择性必修1
第一章 化学反应的热效应
第一节 反应热
第1课时 反应热 焓变
开矿爆破
利用乙炔焰切割金属
能量变化
物质
变化
基础
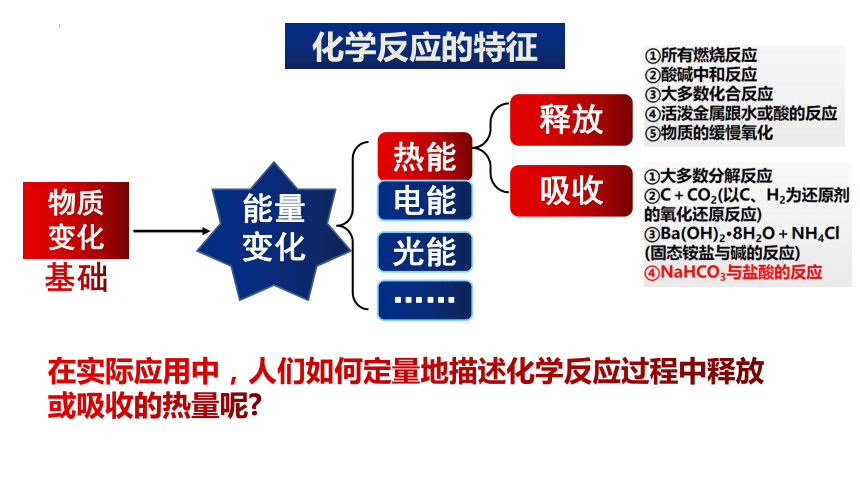
化学反应的特征
热能
电能
光能
……
吸收
释放
在实际应用中,人们如何定量地描述化学反应过程中释放或吸收的热量呢
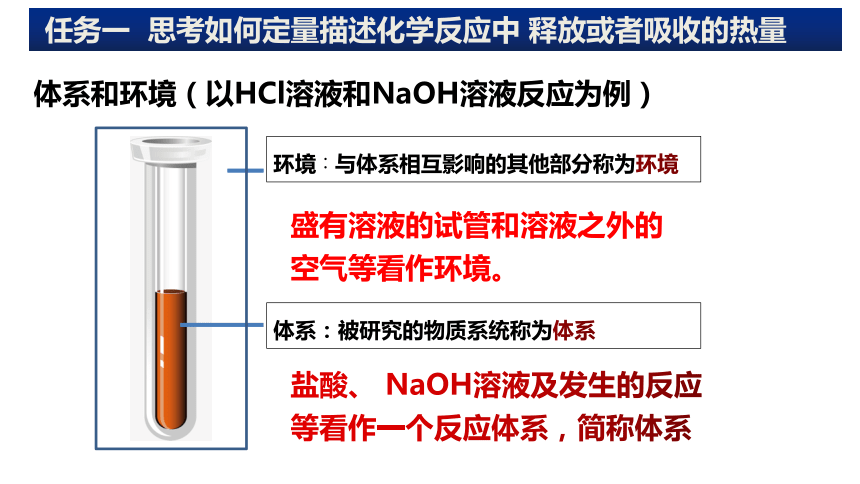
环境∶与体系相互影响的其他部分称为环境
体系:被研究的物质系统称为体系
体系和环境(以HCl溶液和NaOH溶液反应为例)
任务一 思考如何定量描述化学反应中 释放或者吸收的热量
盐酸、 NaOH溶液及发生的反应等看作一个反应体系,简称体系
盛有溶液的试管和溶液之外的空气等看作环境。
反应热
在等温条件下,化学反应体系向环境释放或从环境吸收的热量,称为化学反应的热效应,简称反应热。
等温:指化学反应发生后,使反应后体系的温度恢复到反应前体系的温度,即反应前后体系的温度相等。
任务一 思考如何定量描述化学反应中 释放或者吸收的热量
热量
指因温度不同而在体系与环境之间交换或传递的能量
许多反应热可以通过量热计直接测定。
保温杯式量热计
原理:根据体系的温度的变化和有关物质的比热容等来计算
Q = c . m . △t
比热容
质量
温度的变化量
任务一 思考如何定量描述化学反应中 释放或者吸收的热量
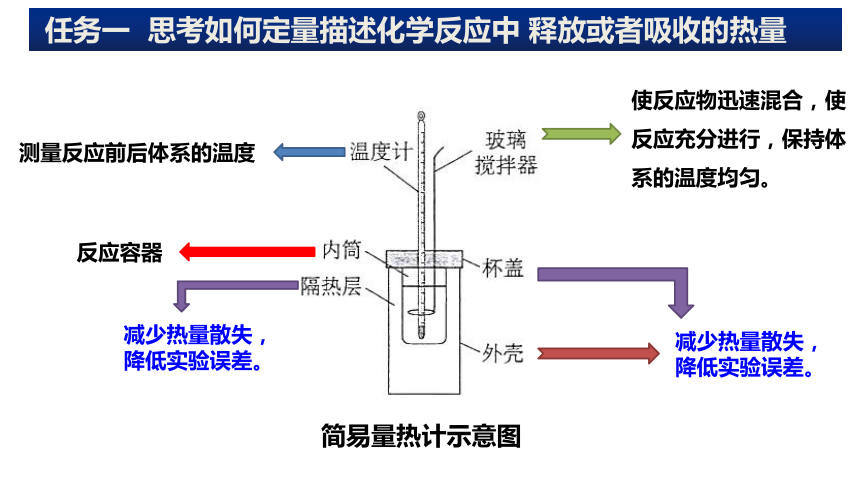
使反应物迅速混合,使反应充分进行,保持体系的温度均匀。
测量反应前后体系的温度
反应容器
减少热量散失,
降低实验误差。
减少热量散失,降低实验误差。
任务一 思考如何定量描述化学反应中 释放或者吸收的热量
简易量热计示意图
在测定中和反应的反应热时,应该测量哪些数据 如何根据测得的数据计算反应热
1. 反应前体系温度 2. 反应后的体系温度
3. 体系的比热容 4. 体系的质量
为了计算简便,可以近似地认为实验所用酸、碱稀溶液的密度、比热容与水的相同,并忽略量热计的比热容,则:
①50 mL 0.50 mol/L盐酸的质量m1=50 g, 50 mL 0.55 mol/L NaOH溶液的质量m2=50 g。
②反应后生成的溶液的比热容c=4.18 J/(g . 0C)。
50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液发生中和反应时放出的热量为:
Q=c·m·△t
任务一 思考如何定量描述化学反应中 释放或者吸收的热量
【实验测量】
(1)反应物温度的测量
①用量筒量取50mL0.50mol/L盐酸,打开杯盖,倒入量热计的内筒中,盖上杯盖,插入温度计,测量并记录盐酸的温度(数据填入下表)。用水把温度计上的酸冲洗干净,擦干备用。
②用另一个量简量取50mL0.55mol/L.NaOH溶液,用温度计测量并记录NaOH溶液的温度(数据填入下表)。
(2)反应后体系温度的测量
打开杯盖,将量筒中的NaOH溶液迅速倒入量热计的内简中,立即盖上杯盖,插入温度计,用玻璃搅拌器匀速搅拌。密切关注温度变化,将最高温度记为反应后体系的温度(t2)。
(3)重复上述步骤(l)至步骤(2)两次。
1.实验中是否可以更换温度计?
不能,会存在仪器误差
2.能否测完酸后直接测量碱的温度?
不能,残留的酸与碱反应,造成酸碱消耗,热量损失。测定一种溶液后必须用水冲洗干净并用滤纸擦干再测别的溶液。
3.能否将NaOH分多次倒入热量计中?
为了保证盐酸完全被中和
不能,操作时动作要快,尽量减少热量的散失
4.为什么NaOH的浓度稍稍比酸大?
5.玻璃搅拌棒能否用金属搅拌棒代替?
不能。原因是金属质搅拌器易导热,
造成实验过程中热量损失。
数据处理:
某小组用50 mL 0.5 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液进行实验。
实验次数 反应物的温度/℃ 反应前体系的温度 反应后体系的温度 温度差
盐酸 NaOH溶液 t1/℃ t2/℃ (t2-t1)/℃
1 25.0 25.2 _____ 28.5 ____
2 24.9 25.1 _____ 28.3 ____
3 25.6 25.4 _____ 29.0 ____
25.1
3.4
3.3
25.0
25.5
3.5
(2)取三次测量所得温度差的平均值作为计算依据。
(3)根据温度差和比热容等计算反应热。
设溶液的密度均为1 g·cm-3,反应后溶液的比热容c=4.18 J·g-1·℃-1,则反应放出的热量Q=cmΔt=c·[m(盐酸)+m(NaOH溶液)]·(t2-t1)≈
kJ,那么生成1 mol H2O放出的热量为 = = 。
特别提醒 大量实验测得,在25 ℃和101 kPa下,强酸的稀溶液与强碱的稀溶液发生中和反应生成1 mol H2O时,放出57.3 kJ的热量。
1.42
56.8 kJ
中和反应反应热(中和热)
中和热定义:在稀溶液中,强酸跟强碱发生中和反应,生成1mol水时的反应热叫做中和热。稀硫酸与稀NaOH溶液反应的中和热_____57.5kJ/mol浓硫酸与稀NaOH溶液反应的中和热_____57.5kJ/mol醋酸与稀的NaOH溶液反应的中和热_____57.5kJ/mol稀硫酸与稀的Ba(OH)2溶液反应的中和热_____57.5kJ/mol实质:H++ OH-= H2O反应生成1mol水产生的热量=><>【思考讨论】
中和反应热测定实验中产生实验误差的原因有哪些?
上述过程中,提高测定反应热准确度的措施有哪些?
【注意事项】
使用同一支温度计,测定一种溶液温度后温度计必须用水冲洗干净并用滤纸擦干
减少热量损失:量热过程中操作要快(将NaOH溶液迅速倒入量热计内筒,立即盖上杯盖);量热计杯盖上的孔不要太大,能正好使温度计和玻璃搅拌器通过即可;
操作规范、读数准确。
注意事项 ①防止热量散失的方法:
a.两个烧杯口要相平;b.在两个烧杯之间填充碎泡沫塑料或碎纸片;c.用玻璃搅拌器搅拌,而不能用金属棒(丝)搅拌;
②加过量碱液使酸完全反应,碱过量对中和热测定没有影响;
③数据处理时,相差较大的数据可能是偶然误差引起的,应舍去。
任务二 探究化学反应中为什么会有反应热
内能是体系内物质的各种能量的总和
其受温度、压强和物质的聚集状态等影响
化学反应前后体系的内能(符号为U)发生了变化。
焓变( H ): H= H生成物- H反应物
单位: kJ/mol 或 kJ mol-1
等压条件下,反应热等于焓变。
在科学研究和生产实践中,化学反应通常是在等压条件下进行的。为了描述等压条件下的反应热,科学上引入了一个与内能有关的物理量——焓(符号为H)
任务二 探究化学反应中为什么会有反应热
产生
反应热
体系
内能改变
等压
反应热
(焓变)
任务二 探究化学反应中为什么会有反应热
宏观分析
放热反应
吸热反应
H (反应物)> H(生成物)
H (反应物)< H(生成物)
任务二 探究化学反应中为什么会有反应热
任务二 探究化学反应中为什么会有反应热
微观分析
=679kJ
=862kJ
△H
=-184.6kJ/mol
△H=H生成物 – H反应物 = E吸-E放<0
放热反应
化学键的断裂和形成是化学反应中能量变化的主要原因。
用“-”表示
任务二 探究化学反应中为什么会有反应热
微观分析
△H=H生成物 – H反应物 = E吸-E放>0
吸热反应
用“+”表示
例1.(1)在25 °C和101 kPa下,1 molH2与1 mol Cl2反应生成2 mol HCl时放出184.6 kJ的热量,则该反应的反应热为:_________________
(2)在25 ° C和101 kPa下,1 mol C(如无特别说明,C均指石墨)与1 mol H20(g)反应,生成1 mol CO和1 mol H2,需要吸收131.5 kJ的热量,则该反应的反应热为:________________________
△H= -184.6 kJ/mol
△H= +131.5 kJ/mol
例1.(3)如图所示反应N2(g) + O2(g) = 2NO(g) △H=__________,生成1molNO时,△H=__________,反应_____(放热或吸热)
(4)稀盐酸与稀NaOH溶液反应生成2mol水,△H=__________,表示中和热时△H=_______________
+180kJ/mol
+90kJ/mol
吸热
-114.6kJ/mol
-57.3kJ/mol
H+(aq)+OH-(aq)=H2O (l) △H= -57.3 kJ/mol
B
课堂小结
选择性必修1
第一章 化学反应的热效应
第一节 反应热
第1课时 反应热 焓变
开矿爆破
利用乙炔焰切割金属
能量变化
物质
变化
基础
化学反应的特征
热能
电能
光能
……
吸收
释放
在实际应用中,人们如何定量地描述化学反应过程中释放或吸收的热量呢
环境∶与体系相互影响的其他部分称为环境
体系:被研究的物质系统称为体系
体系和环境(以HCl溶液和NaOH溶液反应为例)
任务一 思考如何定量描述化学反应中 释放或者吸收的热量
盐酸、 NaOH溶液及发生的反应等看作一个反应体系,简称体系
盛有溶液的试管和溶液之外的空气等看作环境。
反应热
在等温条件下,化学反应体系向环境释放或从环境吸收的热量,称为化学反应的热效应,简称反应热。
等温:指化学反应发生后,使反应后体系的温度恢复到反应前体系的温度,即反应前后体系的温度相等。
任务一 思考如何定量描述化学反应中 释放或者吸收的热量
热量
指因温度不同而在体系与环境之间交换或传递的能量
许多反应热可以通过量热计直接测定。
保温杯式量热计
原理:根据体系的温度的变化和有关物质的比热容等来计算
Q = c . m . △t
比热容
质量
温度的变化量
任务一 思考如何定量描述化学反应中 释放或者吸收的热量
使反应物迅速混合,使反应充分进行,保持体系的温度均匀。
测量反应前后体系的温度
反应容器
减少热量散失,
降低实验误差。
减少热量散失,降低实验误差。
任务一 思考如何定量描述化学反应中 释放或者吸收的热量
简易量热计示意图
在测定中和反应的反应热时,应该测量哪些数据 如何根据测得的数据计算反应热
1. 反应前体系温度 2. 反应后的体系温度
3. 体系的比热容 4. 体系的质量
为了计算简便,可以近似地认为实验所用酸、碱稀溶液的密度、比热容与水的相同,并忽略量热计的比热容,则:
①50 mL 0.50 mol/L盐酸的质量m1=50 g, 50 mL 0.55 mol/L NaOH溶液的质量m2=50 g。
②反应后生成的溶液的比热容c=4.18 J/(g . 0C)。
50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液发生中和反应时放出的热量为:
Q=c·m·△t
任务一 思考如何定量描述化学反应中 释放或者吸收的热量
【实验测量】
(1)反应物温度的测量
①用量筒量取50mL0.50mol/L盐酸,打开杯盖,倒入量热计的内筒中,盖上杯盖,插入温度计,测量并记录盐酸的温度(数据填入下表)。用水把温度计上的酸冲洗干净,擦干备用。
②用另一个量简量取50mL0.55mol/L.NaOH溶液,用温度计测量并记录NaOH溶液的温度(数据填入下表)。
(2)反应后体系温度的测量
打开杯盖,将量筒中的NaOH溶液迅速倒入量热计的内简中,立即盖上杯盖,插入温度计,用玻璃搅拌器匀速搅拌。密切关注温度变化,将最高温度记为反应后体系的温度(t2)。
(3)重复上述步骤(l)至步骤(2)两次。
1.实验中是否可以更换温度计?
不能,会存在仪器误差
2.能否测完酸后直接测量碱的温度?
不能,残留的酸与碱反应,造成酸碱消耗,热量损失。测定一种溶液后必须用水冲洗干净并用滤纸擦干再测别的溶液。
3.能否将NaOH分多次倒入热量计中?
为了保证盐酸完全被中和
不能,操作时动作要快,尽量减少热量的散失
4.为什么NaOH的浓度稍稍比酸大?
5.玻璃搅拌棒能否用金属搅拌棒代替?
不能。原因是金属质搅拌器易导热,
造成实验过程中热量损失。
数据处理:
某小组用50 mL 0.5 mol·L-1的盐酸与50 mL 0.55 mol·L-1的NaOH溶液进行实验。
实验次数 反应物的温度/℃ 反应前体系的温度 反应后体系的温度 温度差
盐酸 NaOH溶液 t1/℃ t2/℃ (t2-t1)/℃
1 25.0 25.2 _____ 28.5 ____
2 24.9 25.1 _____ 28.3 ____
3 25.6 25.4 _____ 29.0 ____
25.1
3.4
3.3
25.0
25.5
3.5
(2)取三次测量所得温度差的平均值作为计算依据。
(3)根据温度差和比热容等计算反应热。
设溶液的密度均为1 g·cm-3,反应后溶液的比热容c=4.18 J·g-1·℃-1,则反应放出的热量Q=cmΔt=c·[m(盐酸)+m(NaOH溶液)]·(t2-t1)≈
kJ,那么生成1 mol H2O放出的热量为 = = 。
特别提醒 大量实验测得,在25 ℃和101 kPa下,强酸的稀溶液与强碱的稀溶液发生中和反应生成1 mol H2O时,放出57.3 kJ的热量。
1.42
56.8 kJ
中和反应反应热(中和热)
中和热定义:在稀溶液中,强酸跟强碱发生中和反应,生成1mol水时的反应热叫做中和热。稀硫酸与稀NaOH溶液反应的中和热_____57.5kJ/mol浓硫酸与稀NaOH溶液反应的中和热_____57.5kJ/mol醋酸与稀的NaOH溶液反应的中和热_____57.5kJ/mol稀硫酸与稀的Ba(OH)2溶液反应的中和热_____57.5kJ/mol实质:H++ OH-= H2O反应生成1mol水产生的热量=><>【思考讨论】
中和反应热测定实验中产生实验误差的原因有哪些?
上述过程中,提高测定反应热准确度的措施有哪些?
【注意事项】
使用同一支温度计,测定一种溶液温度后温度计必须用水冲洗干净并用滤纸擦干
减少热量损失:量热过程中操作要快(将NaOH溶液迅速倒入量热计内筒,立即盖上杯盖);量热计杯盖上的孔不要太大,能正好使温度计和玻璃搅拌器通过即可;
操作规范、读数准确。
注意事项 ①防止热量散失的方法:
a.两个烧杯口要相平;b.在两个烧杯之间填充碎泡沫塑料或碎纸片;c.用玻璃搅拌器搅拌,而不能用金属棒(丝)搅拌;
②加过量碱液使酸完全反应,碱过量对中和热测定没有影响;
③数据处理时,相差较大的数据可能是偶然误差引起的,应舍去。
任务二 探究化学反应中为什么会有反应热
内能是体系内物质的各种能量的总和
其受温度、压强和物质的聚集状态等影响
化学反应前后体系的内能(符号为U)发生了变化。
焓变( H ): H= H生成物- H反应物
单位: kJ/mol 或 kJ mol-1
等压条件下,反应热等于焓变。
在科学研究和生产实践中,化学反应通常是在等压条件下进行的。为了描述等压条件下的反应热,科学上引入了一个与内能有关的物理量——焓(符号为H)
任务二 探究化学反应中为什么会有反应热
产生
反应热
体系
内能改变
等压
反应热
(焓变)
任务二 探究化学反应中为什么会有反应热
宏观分析
放热反应
吸热反应
H (反应物)> H(生成物)
H (反应物)< H(生成物)
任务二 探究化学反应中为什么会有反应热
任务二 探究化学反应中为什么会有反应热
微观分析
=679kJ
=862kJ
△H
=-184.6kJ/mol
△H=H生成物 – H反应物 = E吸-E放<0
放热反应
化学键的断裂和形成是化学反应中能量变化的主要原因。
用“-”表示
任务二 探究化学反应中为什么会有反应热
微观分析
△H=H生成物 – H反应物 = E吸-E放>0
吸热反应
用“+”表示
例1.(1)在25 °C和101 kPa下,1 molH2与1 mol Cl2反应生成2 mol HCl时放出184.6 kJ的热量,则该反应的反应热为:_________________
(2)在25 ° C和101 kPa下,1 mol C(如无特别说明,C均指石墨)与1 mol H20(g)反应,生成1 mol CO和1 mol H2,需要吸收131.5 kJ的热量,则该反应的反应热为:________________________
△H= -184.6 kJ/mol
△H= +131.5 kJ/mol
例1.(3)如图所示反应N2(g) + O2(g) = 2NO(g) △H=__________,生成1molNO时,△H=__________,反应_____(放热或吸热)
(4)稀盐酸与稀NaOH溶液反应生成2mol水,△H=__________,表示中和热时△H=_______________
+180kJ/mol
+90kJ/mol
吸热
-114.6kJ/mol
-57.3kJ/mol
H+(aq)+OH-(aq)=H2O (l) △H= -57.3 kJ/mol
B
课堂小结
