人教版(2019)高中化学选择性必修一 1.2 反应热的计算、盖斯定律 课件(共22张PPT)
文档属性
| 名称 | 人教版(2019)高中化学选择性必修一 1.2 反应热的计算、盖斯定律 课件(共22张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 709.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-28 00:00:00 | ||
图片预览





文档简介
(共22张PPT)
盖斯定律、反应热的计算
第一章 化学反应的热效应
第二节 反应热的计算
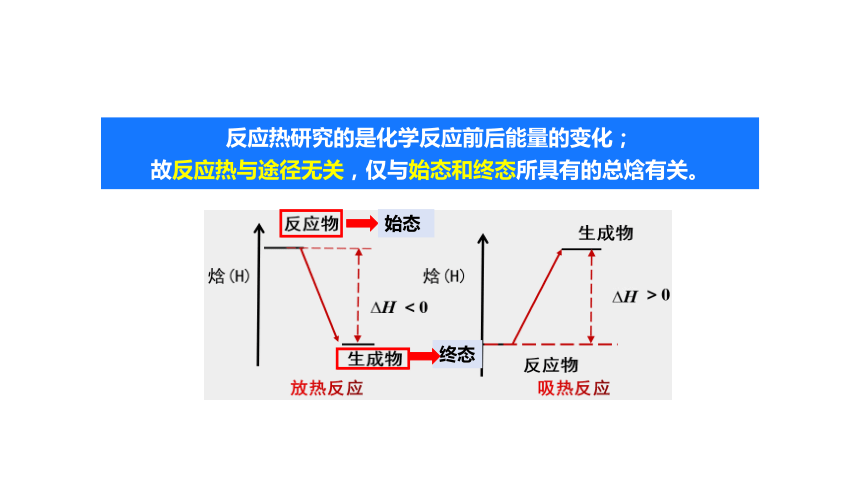
反应热研究的是化学反应前后能量的变化;
故反应热与途径无关,仅与始态和终态所具有的总焓有关。
始态
终态
盖斯定律
环节一:盖斯定律
1.盖斯定律的内容
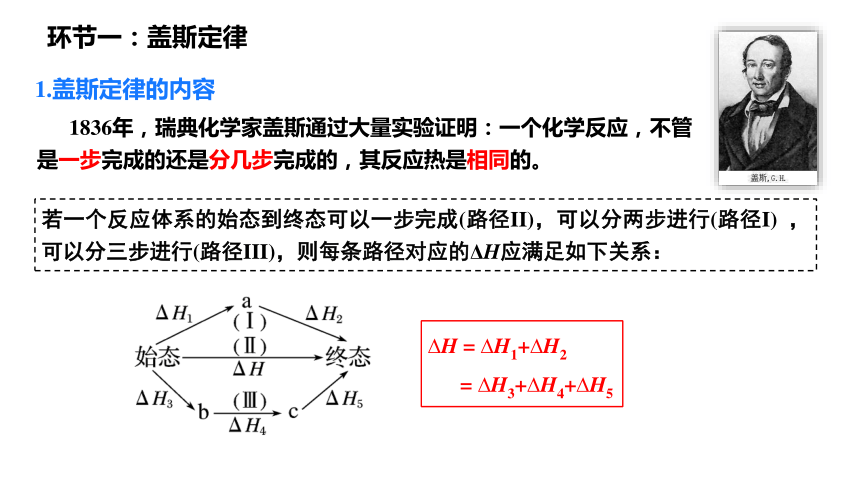
1836年,瑞典化学家盖斯通过大量实验证明:一个化学反应,不管是一步完成的还是分几步完成的,其反应热是相同的。
若一个反应体系的始态到终态可以一步完成(路径II),可以分两步进行(路径I) ,可以分三步进行(路径III),则每条路径对应的ΔH应满足如下关系:
H = H1+ H2
= H3+ H4+ H5
环节一:盖斯定律
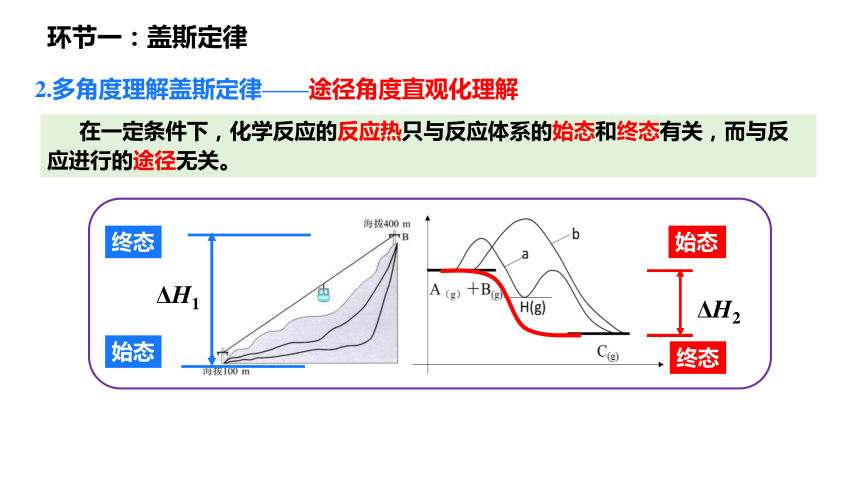
2.多角度理解盖斯定律——途径角度直观化理解
ΔH1
ΔH2
终态
始态
始态
终态
在一定条件下,化学反应的反应热只与反应体系的始态和终态有关,而与反应进行的途径无关。
环节一:盖斯定律
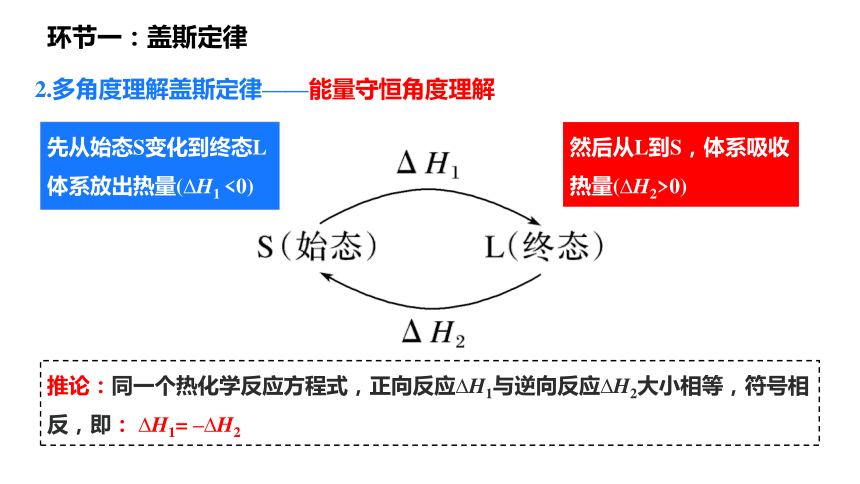
2.多角度理解盖斯定律——能量守恒角度理解
先从始态S变化到终态L 体系放出热量( H1 <0)
然后从L到S,体系吸收热量( H2>0)
推论:同一个热化学反应方程式,正向反应 H1与逆向反应 H2大小相等,符号相反,即: H1= – H2
环节一:盖斯定律
3.盖斯定律的意义
盖斯定律的提出,为反应热的研究提供了极大的方便,使一些不易测定或无法测定的化学反应的反应热可以通过推算间接求得
H = H1+ H2
= H3+ H4+ H5
H2 = H H1
?
若反应物A变为生成物D有两种途径:
(1)由A直接变成D,反应热为ΔH;
(2)由A经过B变成C,再由C变成D,每步的反应热分别为ΔH1、ΔH2、ΔH3。
ΔH=ΔH1+ΔH2+ΔH3
【方法总结】利用盖斯定律解题的常用方法——虚拟路径法
环节一:盖斯定律
【例1】已知:
Ⅰ. C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
Ⅱ. CO(g)+ 1/2 O2(g)===CO2(g) ΔH2=-283.0 kJ·mol-1
根据上述两个反应,能计算C(s)+ 1/2 O2(g)===CO(g)的反应热ΔH3吗?
环节一:盖斯定律
反应C(s)+1/2 O2(g)===CO2(g)的途径可设计为:
则ΔH3=ΔH1-ΔH2=-110.5 kJ·mol-1
环节一:盖斯定律
【方法总结】利用盖斯定律解题的常用方法——加和法
(1)唯一入手:
目标热化学方程式中的物质,在已知热化学方程式中仅出现一次。
(2)调整系数:
热化学方程式同乘以某一个数时,反应热的数值也必须乘上该数。
(3)同加异减:
目标热化学方程式中的物质与已知热化学方程式中的物质,若在热化学方程式等号的同侧,则相加,反之,则相减,同时ΔH的符号也相应加减。
环节一:盖斯定律
(1)定:确定待求反应的热化学方程式。
(2)找:找出待求热化学方程式中只在已知化学方程式中出现一次的物质。
(3)调:依据该物质调整已知化学方程式的方向(同侧相加,异侧相减)和化学计量数,每个已知化学方程式只能调整一次。
(4)算:ΔH与化学方程式一一对应调整和运算。
【方法总结】根据盖斯定律计算反应热的步骤
【例1】已知:
Ⅰ. C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
Ⅱ. CO(g)+ 1/2 O2(g)===CO2(g) ΔH2=-283.0 kJ·mol-1
根据上述两个反应,能计算C(s)+ 1/2 O2(g)===CO(g)的反应热ΔH3吗?
环节一:盖斯定律
【练习1】如何计算甲烷不完全燃烧的反应热呢?
环节一:盖斯定律
CO(g) + 2H2O(l) + 1/2O2(g)
CH4(g) + 2O2(g)
CO2(g) + 2H2O(l)
始态
终态
ΔH2
ΔH1
ΔH3
③ CO (g) + 1/2O2 (g) = CO2 (g) ΔH3= 283.0 kJ/mol
①CH4 (g) + 2O2 (g) = CO2 (g) + 2H2O(l) ΔH1= 890.3 kJ/mol
② CH4 (g) + 3/2O2 (g) = CO (g) + 2H2O(l) ΔH2= ?
CH4 (g) + 3/2O2 (g) = CO (g) + 2H2O(l) ΔH2= 607.3kJ/mol
【练习1】如何计算甲烷不完全燃烧的反应热呢?
环节一:盖斯定律
③ CO (g) + 1/2O2 (g) = CO2 (g) ΔH3= 283.0 kJ/mol
①CH4 (g) + 2O2 (g) = CO2 (g) + 2H2O(l) ΔH1= 890.3 kJ/mol
② CH4 (g) + 3/2O2 (g) = CO (g) + 2H2O(l) ΔH2= ?
ΔH2 = ΔH1 ΔH3
= 890.3 kJ/mol ( 283.0kJ/mol)
= 607.3kJ/mol
② = ① ③
【练习2】(2024·上海徐汇区高二质检)已知热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l) ΔH1=-Q1 kJ/mol
S(s)+O2(g)===SO2(g) ΔH2=-Q2 kJ/mol
则2H2S(g)+O2(g)===2S(s)+2H2O(l)的焓变ΔH3(单位为kJ/mol)为( )
A.-Q1-2Q2 B.-Q2-2Q1
C.-Q1+2Q2 D.-Q2+2Q1
环节一:盖斯定律
√
反应热的计算
环节二:反应热的计算
【题型1】利用热化学方程式进行相关量的计算
环节二:反应热的计算
【例1】(选择性必修1第15页例题1)黄铁矿(主要成分为FeS2)的燃烧是工业上制硫酸时得到SO2的途径之一,反应的化学方程式为:
4FeS2+11O2===2Fe2O3+8SO2
在25℃和101kPa时,1 mol FeS2(s)完全燃烧生成Fe2O3(s)和SO2(g)时放出853kJ的热量。这些热量(工业中叫做“废热”)在生产过程中得到了充分利用,大大降低了生产成本,对于节约资源、能源循环利用具有重要意义。
(1)请写出FeS2燃烧的热化学方程式。
(2)计算理论上1kg黄铁矿(FeS2的含量为90%)完全燃烧放出的热量。
环节二:反应热的计算
【题型2】根据盖斯定律计算
【例2】已知25 ℃时,相关物质的燃烧热数据如下表:
物质 H2(g) C(石墨,s) C6H6(l)
燃烧热ΔH/(kJ·mol-1) -285.8 -393.5 -3 267.5
25 ℃时,H2(g)和C(石墨,s)反应生成C6H6(l)的热化学方程式为
________________________________________________________________________
3H2(g)+6C(石墨,s)===C6H6(l) ΔH=+49.1 kJ·mol-1
环节二:反应热的计算
【题型3】根据燃烧热计算
可燃物完全燃烧产生的热量=可燃物的物质的量×燃烧热
【例3】已知:甲烷气体燃烧的热化学方程式为CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1。320 g “可燃冰”(分子式为CH4·8H2O)释放的甲烷气体完全燃烧生成二氧化碳气体和液态水时放出的热量为多少?
320 g CH4·8H2O中甲烷的物质的量为2 mol,2 mol甲烷气体完全燃烧生成二氧化碳气体和液态水时放出的热量为1 780.6 kJ。
环节二:反应热的计算
【题型4】根据键能计算
ΔH = ∑E吸 - ∑E放=∑(反应物的键能)-∑(生成物的键能)
【例4】已知①C(s)+H2O(g)===CO(g)+H2(g) ΔH1=a kJ·mol-1;
②2C(s)+O2(g)===2CO(g) ΔH2=-220 kJ·mol-1。
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。其中H—H、O===O和O—H的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,a为多少?
环节二:反应热的计算
【题型5】根据图像计算
盖斯定律、反应热的计算
第一章 化学反应的热效应
第二节 反应热的计算
反应热研究的是化学反应前后能量的变化;
故反应热与途径无关,仅与始态和终态所具有的总焓有关。
始态
终态
盖斯定律
环节一:盖斯定律
1.盖斯定律的内容
1836年,瑞典化学家盖斯通过大量实验证明:一个化学反应,不管是一步完成的还是分几步完成的,其反应热是相同的。
若一个反应体系的始态到终态可以一步完成(路径II),可以分两步进行(路径I) ,可以分三步进行(路径III),则每条路径对应的ΔH应满足如下关系:
H = H1+ H2
= H3+ H4+ H5
环节一:盖斯定律
2.多角度理解盖斯定律——途径角度直观化理解
ΔH1
ΔH2
终态
始态
始态
终态
在一定条件下,化学反应的反应热只与反应体系的始态和终态有关,而与反应进行的途径无关。
环节一:盖斯定律
2.多角度理解盖斯定律——能量守恒角度理解
先从始态S变化到终态L 体系放出热量( H1 <0)
然后从L到S,体系吸收热量( H2>0)
推论:同一个热化学反应方程式,正向反应 H1与逆向反应 H2大小相等,符号相反,即: H1= – H2
环节一:盖斯定律
3.盖斯定律的意义
盖斯定律的提出,为反应热的研究提供了极大的方便,使一些不易测定或无法测定的化学反应的反应热可以通过推算间接求得
H = H1+ H2
= H3+ H4+ H5
H2 = H H1
?
若反应物A变为生成物D有两种途径:
(1)由A直接变成D,反应热为ΔH;
(2)由A经过B变成C,再由C变成D,每步的反应热分别为ΔH1、ΔH2、ΔH3。
ΔH=ΔH1+ΔH2+ΔH3
【方法总结】利用盖斯定律解题的常用方法——虚拟路径法
环节一:盖斯定律
【例1】已知:
Ⅰ. C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
Ⅱ. CO(g)+ 1/2 O2(g)===CO2(g) ΔH2=-283.0 kJ·mol-1
根据上述两个反应,能计算C(s)+ 1/2 O2(g)===CO(g)的反应热ΔH3吗?
环节一:盖斯定律
反应C(s)+1/2 O2(g)===CO2(g)的途径可设计为:
则ΔH3=ΔH1-ΔH2=-110.5 kJ·mol-1
环节一:盖斯定律
【方法总结】利用盖斯定律解题的常用方法——加和法
(1)唯一入手:
目标热化学方程式中的物质,在已知热化学方程式中仅出现一次。
(2)调整系数:
热化学方程式同乘以某一个数时,反应热的数值也必须乘上该数。
(3)同加异减:
目标热化学方程式中的物质与已知热化学方程式中的物质,若在热化学方程式等号的同侧,则相加,反之,则相减,同时ΔH的符号也相应加减。
环节一:盖斯定律
(1)定:确定待求反应的热化学方程式。
(2)找:找出待求热化学方程式中只在已知化学方程式中出现一次的物质。
(3)调:依据该物质调整已知化学方程式的方向(同侧相加,异侧相减)和化学计量数,每个已知化学方程式只能调整一次。
(4)算:ΔH与化学方程式一一对应调整和运算。
【方法总结】根据盖斯定律计算反应热的步骤
【例1】已知:
Ⅰ. C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
Ⅱ. CO(g)+ 1/2 O2(g)===CO2(g) ΔH2=-283.0 kJ·mol-1
根据上述两个反应,能计算C(s)+ 1/2 O2(g)===CO(g)的反应热ΔH3吗?
环节一:盖斯定律
【练习1】如何计算甲烷不完全燃烧的反应热呢?
环节一:盖斯定律
CO(g) + 2H2O(l) + 1/2O2(g)
CH4(g) + 2O2(g)
CO2(g) + 2H2O(l)
始态
终态
ΔH2
ΔH1
ΔH3
③ CO (g) + 1/2O2 (g) = CO2 (g) ΔH3= 283.0 kJ/mol
①CH4 (g) + 2O2 (g) = CO2 (g) + 2H2O(l) ΔH1= 890.3 kJ/mol
② CH4 (g) + 3/2O2 (g) = CO (g) + 2H2O(l) ΔH2= ?
CH4 (g) + 3/2O2 (g) = CO (g) + 2H2O(l) ΔH2= 607.3kJ/mol
【练习1】如何计算甲烷不完全燃烧的反应热呢?
环节一:盖斯定律
③ CO (g) + 1/2O2 (g) = CO2 (g) ΔH3= 283.0 kJ/mol
①CH4 (g) + 2O2 (g) = CO2 (g) + 2H2O(l) ΔH1= 890.3 kJ/mol
② CH4 (g) + 3/2O2 (g) = CO (g) + 2H2O(l) ΔH2= ?
ΔH2 = ΔH1 ΔH3
= 890.3 kJ/mol ( 283.0kJ/mol)
= 607.3kJ/mol
② = ① ③
【练习2】(2024·上海徐汇区高二质检)已知热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l) ΔH1=-Q1 kJ/mol
S(s)+O2(g)===SO2(g) ΔH2=-Q2 kJ/mol
则2H2S(g)+O2(g)===2S(s)+2H2O(l)的焓变ΔH3(单位为kJ/mol)为( )
A.-Q1-2Q2 B.-Q2-2Q1
C.-Q1+2Q2 D.-Q2+2Q1
环节一:盖斯定律
√
反应热的计算
环节二:反应热的计算
【题型1】利用热化学方程式进行相关量的计算
环节二:反应热的计算
【例1】(选择性必修1第15页例题1)黄铁矿(主要成分为FeS2)的燃烧是工业上制硫酸时得到SO2的途径之一,反应的化学方程式为:
4FeS2+11O2===2Fe2O3+8SO2
在25℃和101kPa时,1 mol FeS2(s)完全燃烧生成Fe2O3(s)和SO2(g)时放出853kJ的热量。这些热量(工业中叫做“废热”)在生产过程中得到了充分利用,大大降低了生产成本,对于节约资源、能源循环利用具有重要意义。
(1)请写出FeS2燃烧的热化学方程式。
(2)计算理论上1kg黄铁矿(FeS2的含量为90%)完全燃烧放出的热量。
环节二:反应热的计算
【题型2】根据盖斯定律计算
【例2】已知25 ℃时,相关物质的燃烧热数据如下表:
物质 H2(g) C(石墨,s) C6H6(l)
燃烧热ΔH/(kJ·mol-1) -285.8 -393.5 -3 267.5
25 ℃时,H2(g)和C(石墨,s)反应生成C6H6(l)的热化学方程式为
________________________________________________________________________
3H2(g)+6C(石墨,s)===C6H6(l) ΔH=+49.1 kJ·mol-1
环节二:反应热的计算
【题型3】根据燃烧热计算
可燃物完全燃烧产生的热量=可燃物的物质的量×燃烧热
【例3】已知:甲烷气体燃烧的热化学方程式为CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1。320 g “可燃冰”(分子式为CH4·8H2O)释放的甲烷气体完全燃烧生成二氧化碳气体和液态水时放出的热量为多少?
320 g CH4·8H2O中甲烷的物质的量为2 mol,2 mol甲烷气体完全燃烧生成二氧化碳气体和液态水时放出的热量为1 780.6 kJ。
环节二:反应热的计算
【题型4】根据键能计算
ΔH = ∑E吸 - ∑E放=∑(反应物的键能)-∑(生成物的键能)
【例4】已知①C(s)+H2O(g)===CO(g)+H2(g) ΔH1=a kJ·mol-1;
②2C(s)+O2(g)===2CO(g) ΔH2=-220 kJ·mol-1。
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。其中H—H、O===O和O—H的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,a为多少?
环节二:反应热的计算
【题型5】根据图像计算
