课题2 原子结构 第1课时 原子的构成与相对原子质量 课件(共32张PPT)2025-2026学年人教版九年级化学上册
文档属性
| 名称 | 课题2 原子结构 第1课时 原子的构成与相对原子质量 课件(共32张PPT)2025-2026学年人教版九年级化学上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-27 00:00:00 | ||
图片预览






文档简介
(共32张PPT)
第三单元 物质构成的奥秘
课题2
原子结构
(第1课时)
九年级化学 上册·人教版2024
学习内容导览
相对原子质量
2
原子的构成
1
1.了解原子结构模型的发展历程,能利用科学家的研究成果认识原子的构成。
2.了解原子的构成及构成粒子之间的关系。
3.认识相对原子质量的含义和使用方法。
明·教学目标
引·新课导入
原子是化学变化中的最小粒子,单个原子是不是就是一个简单的实心球体?是否由一些更小的微粒构成?
原子的构成
01
一、原子的构成
探·知识奥秘
1. 原子模型的演变
(1)道尔顿原子模型
1808年,道尔顿提出了原子论。认为原子是坚实的、不可再分的实心球体。
道尔顿(1766—1844)
一、原子的构成
探·知识奥秘
1. 原子模型的演变
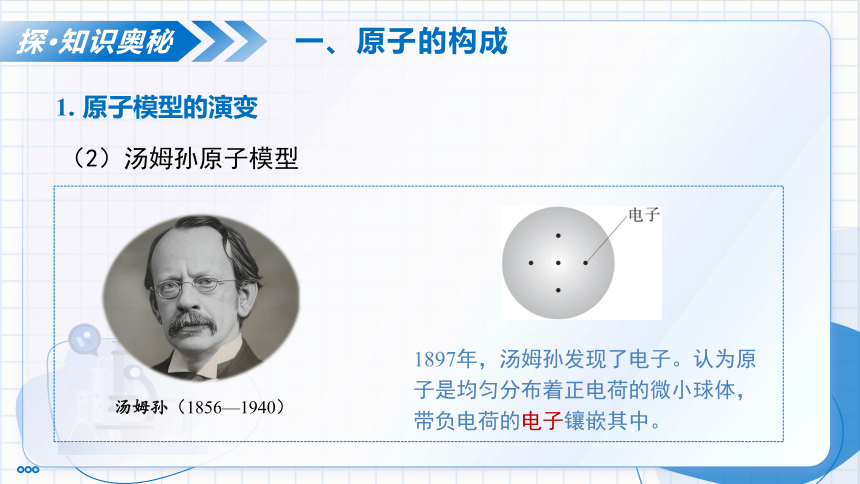
(2)汤姆孙原子模型
1897年,汤姆孙发现了电子。认为原子是均匀分布着正电荷的微小球体,带负电荷的电子镶嵌其中。
汤姆孙(1856—1940)
一、原子的构成
探·知识奥秘
1. 原子模型的演变
(3)卢瑟福原子模型
1911年,卢瑟福提出了原子的“核式结构模型”。认为原子中带正电荷部分的体积很小,但几乎占有全部质量,电子在原子核外运动。
卢瑟福(1871-1937)
一、原子的构成
探·知识奥秘
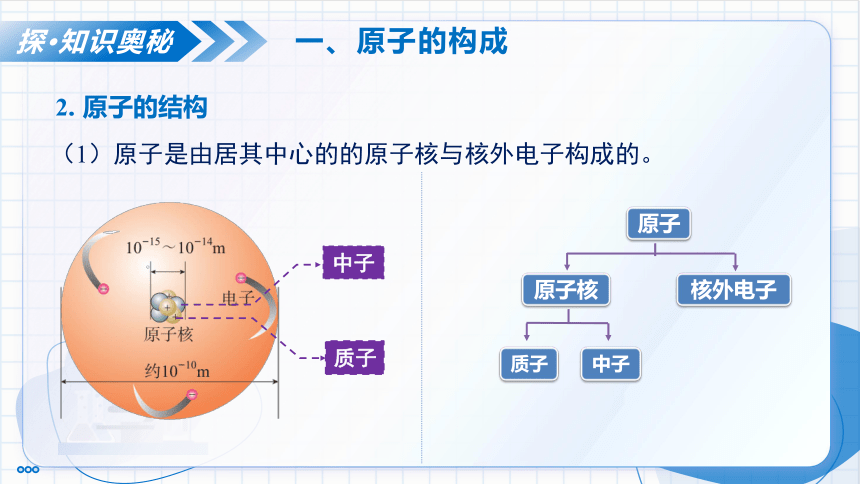
2. 原子的结构
(1)原子是由居其中心的的原子核与核外电子构成的。
中子
质子
原子
原子核
核外电子
质子
中子
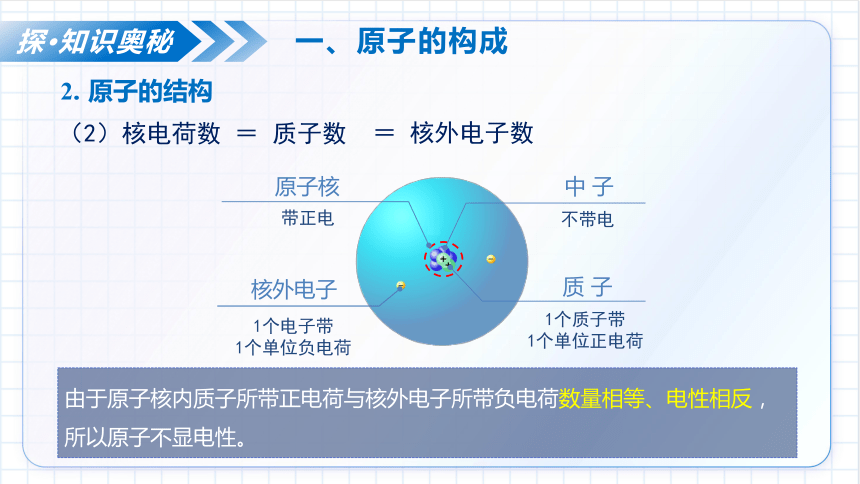
(2)核电荷数 = 质子数
一、原子的构成
探·知识奥秘
2. 原子的结构
不带电
中 子
1个质子带
1个单位正电荷
质 子
原子核
带正电
1个电子带
1个单位负电荷
核外电子
由于原子核内质子所带正电荷与核外电子所带负电荷数量相等、电性相反,所以原子不显电性。
= 核外电子数
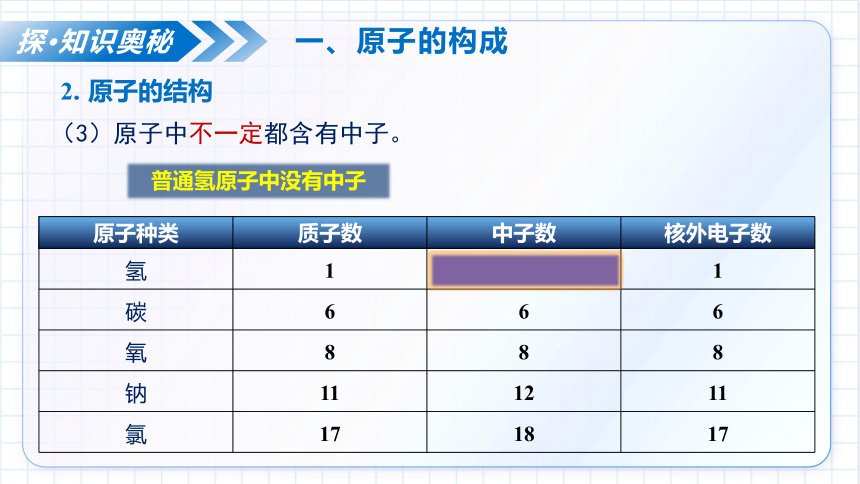
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
(3)原子中不一定都含有中子。
普通氢原子中没有中子
探·知识奥秘
一、原子的构成
2. 原子的结构
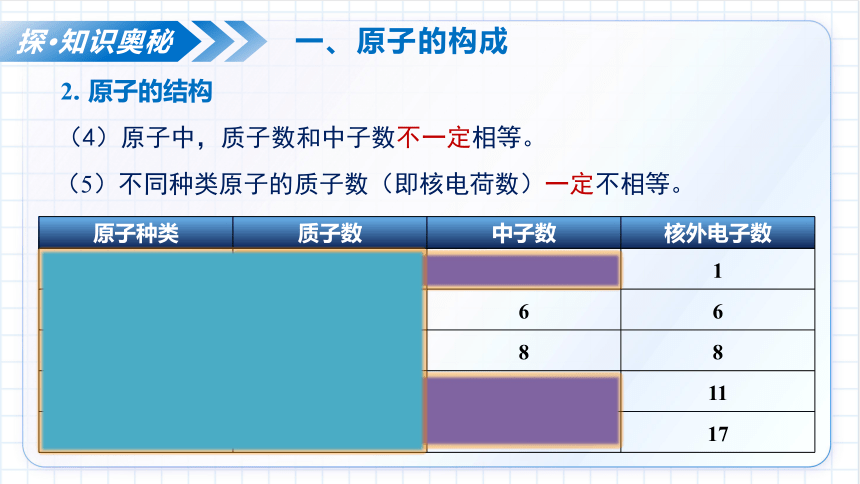
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
(4)原子中,质子数和中子数不一定相等。
探·知识奥秘
一、原子的构成
2. 原子的结构
(5)不同种类原子的质子数(即核电荷数)一定不相等。
【典例】人类认识原子不同阶段的模型示意图如下,结合你所学的知识判断下列有关说法不正确的是( )
A. 道尔顿的观点是错误的,他的模型也没有任何价值
B.汤姆孙发现了电子,推翻了道尔顿原子不可再分的认识
C.科学的发展道路是漫长而曲折的,探索永无止境
D.化学家通过构建模型有力地促进了化学理论的发展
A
析·典型范例
【变式】下列关于原子结构的说法错误的是( )
A.原子核都由质子和中子构成的
B.原子可以直接构成物质
C.在原子中,核电荷数一定等于质子数或核外电子数
D.原子核带正电
析·典型范例
A
相对原子质量
02
二、相对原子质量
探·知识奥秘
1个氢原子的质量是:
0.000 000 000 000 000 000 000 000 001 67 千克
即 1.67×10-27 千克
1个氧原子的质量是:
0.000 000 000 000 000 000 000 000 0266千克
即 2.66×10-26 千克
原子的质量太小了,书写、使用很不方便。
原子的质量很小:
二、相对原子质量
探·知识奥秘
1. 相对原子质量的概念
以一种碳原子质量的 为标准,其他原子的质量与它相比,得到相对原子质量(符号为 Ar)。
1
—
12
碳原子
碳原子的1/12
这种碳原子叫作碳-12(含有 6 个质子和 6 个中子),其质量的1/12约等于1.6605×10-27 kg。
二、相对原子质量
探·知识奥秘
2. 相对原子质量的计算
已知 1 个碳-12原子的质量是1.993×10-26 kg,1个氢原子的质量是1.672×10-27 kg,
1个氧原子的质量是2.657×10-26千克,求氢原子和氧原子的相对原子质量。
解:标准=1.993×10-26 kg× ≈ 1.66×10-27 kg
1.66×10-27 kg
1.672×10-27 kg
≈ 1
相对原子质量是一个比值,单位为“1”,一般不读出也不写出
氢原子的相对原子质量 =
氧原子的相对原子质量 =
1.66×10-27 kg
2.657×10-26 kg
≈ 16
实际质量大的原子,相对原子质量也越大
二、相对原子质量
探·知识奥秘
附录 Ⅱ
相对原子质量表
(按照原子序数排列)
二、相对原子质量
探·知识奥秘
表 3-3 一些常见元素的名称、元素符号和相对原子质量(近似值)
相对原子质量Ar 不是整数,中学计算简化,用近似整数的值,个别如Cl—35.5 等带小数。
二、相对原子质量
探·知识奥秘
3. 原子中各粒子的质量关系
粒子种类 质量
质子 1.672 6×10-27 kg
中子 1.674 9×10-27 kg
电子 质子质量的
(1)质子、中子的相对质量都约等于1。
已知:碳-12 原子质量的 约等于 1.66×10-27 kg。
相对质量
1
1
(2)电子质量很小,整个原子的质量主要集中在原子核上。
探·知识奥秘
二、相对原子质量
4. 相对原子质量与质子数、中子数的关系
原子种类 质子数 中子数 相对原子质量
氢 1 0 1
碳 6 6 12
氧 8 8 16
钠 11 12 23
相对原子质量≈质子数+中子数
探·知识奥秘
二、相对原子质量
中国科学院院士张青莲教授为相对原子质量的测定作出了卓越贡献。他于 1983 年当选为国际纯粹与应用化学联合会原子量与同位素丰度委员会委员。他主持测定的铟、铱、锑、铕、铈、铒、锗、镝、锌的相对原子质量数据被确认为国际标准。
张青莲(1908—2006)
张青莲与相对原子质量的测定
资料卡片
【典例】关于相对原子质量的叙述正确的是( )
A.相对原子质量就是一个原子的质量
B.相对原子质量是一个碳原子质量
C.相对原子质量是原子的相对质量,是一个比值
D.相对原子质量的单位是“千克”
C
析·典型范例
【变式】氮原子的相对原子质量为14,表示的意义是( )
A.氮原子核中有14个质子
B.一个氮原子的质量为14g
C.一个氮原子的质量是一个碳-12原子质量的14倍
D.一个氮原子的质量是一个碳-12原子质量
的 的14倍
析·典型范例
D
1
—
12
原子结构
原子的构成
原子核
理·核心要点
相对原子质量
概念
核外电子
质子
中子
相对原子质量≈质子数+中子数
1.科学家精神是兴国之本,下列哪位科学家为相对原子质量的测定做出了卓越贡献( )
A.拉瓦锡 B.道尔顿
C.张青莲 D.门捷列夫
练·技能实战
C
2.原子模型的演变反映了人类探索物质结构的漫长历程。图示为原子结构模型的演变图,下列排序符合人类认识原子结构历程的是( )
A.①②③ B.②①③
C.①③② D.②③①
练·技能实战
D
3.下列有关粒子的说法中正确的是( )
A.原子的原子核都是由质子和中子构成的
B.分子可分,原子不可分
C.原子的质子数和中子数一定相同
D.相对原子质量与原子的实际质量不相同
练·技能实战
D
4.原子、分子质量很小,为计算和使用方便引入相对原子质量。下列说法正确的是( )
A.相对原子质量是采用以小比小使数值变大的计量原理
B.相对原子质量是一个原子质量与一个碳-12 原子质量的比值
C.两种原子的相对原子质量之比与真实质量之比没有必然联系
D.相对原子质量是一个比值,单位是g
练·技能实战
A
5.相同质量的钠、镁、铜三种金属,含原子数目最多的是( )
A.钠 B.镁 C.铜 D.一样多
练·技能实战
A
THANKS!
谢谢观看
九年级化学 上册·人教版2024
第三单元 物质构成的奥秘
课题2
原子结构
(第1课时)
九年级化学 上册·人教版2024
学习内容导览
相对原子质量
2
原子的构成
1
1.了解原子结构模型的发展历程,能利用科学家的研究成果认识原子的构成。
2.了解原子的构成及构成粒子之间的关系。
3.认识相对原子质量的含义和使用方法。
明·教学目标
引·新课导入
原子是化学变化中的最小粒子,单个原子是不是就是一个简单的实心球体?是否由一些更小的微粒构成?
原子的构成
01
一、原子的构成
探·知识奥秘
1. 原子模型的演变
(1)道尔顿原子模型
1808年,道尔顿提出了原子论。认为原子是坚实的、不可再分的实心球体。
道尔顿(1766—1844)
一、原子的构成
探·知识奥秘
1. 原子模型的演变
(2)汤姆孙原子模型
1897年,汤姆孙发现了电子。认为原子是均匀分布着正电荷的微小球体,带负电荷的电子镶嵌其中。
汤姆孙(1856—1940)
一、原子的构成
探·知识奥秘
1. 原子模型的演变
(3)卢瑟福原子模型
1911年,卢瑟福提出了原子的“核式结构模型”。认为原子中带正电荷部分的体积很小,但几乎占有全部质量,电子在原子核外运动。
卢瑟福(1871-1937)
一、原子的构成
探·知识奥秘
2. 原子的结构
(1)原子是由居其中心的的原子核与核外电子构成的。
中子
质子
原子
原子核
核外电子
质子
中子
(2)核电荷数 = 质子数
一、原子的构成
探·知识奥秘
2. 原子的结构
不带电
中 子
1个质子带
1个单位正电荷
质 子
原子核
带正电
1个电子带
1个单位负电荷
核外电子
由于原子核内质子所带正电荷与核外电子所带负电荷数量相等、电性相反,所以原子不显电性。
= 核外电子数
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
(3)原子中不一定都含有中子。
普通氢原子中没有中子
探·知识奥秘
一、原子的构成
2. 原子的结构
原子种类 质子数 中子数 核外电子数
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
(4)原子中,质子数和中子数不一定相等。
探·知识奥秘
一、原子的构成
2. 原子的结构
(5)不同种类原子的质子数(即核电荷数)一定不相等。
【典例】人类认识原子不同阶段的模型示意图如下,结合你所学的知识判断下列有关说法不正确的是( )
A. 道尔顿的观点是错误的,他的模型也没有任何价值
B.汤姆孙发现了电子,推翻了道尔顿原子不可再分的认识
C.科学的发展道路是漫长而曲折的,探索永无止境
D.化学家通过构建模型有力地促进了化学理论的发展
A
析·典型范例
【变式】下列关于原子结构的说法错误的是( )
A.原子核都由质子和中子构成的
B.原子可以直接构成物质
C.在原子中,核电荷数一定等于质子数或核外电子数
D.原子核带正电
析·典型范例
A
相对原子质量
02
二、相对原子质量
探·知识奥秘
1个氢原子的质量是:
0.000 000 000 000 000 000 000 000 001 67 千克
即 1.67×10-27 千克
1个氧原子的质量是:
0.000 000 000 000 000 000 000 000 0266千克
即 2.66×10-26 千克
原子的质量太小了,书写、使用很不方便。
原子的质量很小:
二、相对原子质量
探·知识奥秘
1. 相对原子质量的概念
以一种碳原子质量的 为标准,其他原子的质量与它相比,得到相对原子质量(符号为 Ar)。
1
—
12
碳原子
碳原子的1/12
这种碳原子叫作碳-12(含有 6 个质子和 6 个中子),其质量的1/12约等于1.6605×10-27 kg。
二、相对原子质量
探·知识奥秘
2. 相对原子质量的计算
已知 1 个碳-12原子的质量是1.993×10-26 kg,1个氢原子的质量是1.672×10-27 kg,
1个氧原子的质量是2.657×10-26千克,求氢原子和氧原子的相对原子质量。
解:标准=1.993×10-26 kg× ≈ 1.66×10-27 kg
1.66×10-27 kg
1.672×10-27 kg
≈ 1
相对原子质量是一个比值,单位为“1”,一般不读出也不写出
氢原子的相对原子质量 =
氧原子的相对原子质量 =
1.66×10-27 kg
2.657×10-26 kg
≈ 16
实际质量大的原子,相对原子质量也越大
二、相对原子质量
探·知识奥秘
附录 Ⅱ
相对原子质量表
(按照原子序数排列)
二、相对原子质量
探·知识奥秘
表 3-3 一些常见元素的名称、元素符号和相对原子质量(近似值)
相对原子质量Ar 不是整数,中学计算简化,用近似整数的值,个别如Cl—35.5 等带小数。
二、相对原子质量
探·知识奥秘
3. 原子中各粒子的质量关系
粒子种类 质量
质子 1.672 6×10-27 kg
中子 1.674 9×10-27 kg
电子 质子质量的
(1)质子、中子的相对质量都约等于1。
已知:碳-12 原子质量的 约等于 1.66×10-27 kg。
相对质量
1
1
(2)电子质量很小,整个原子的质量主要集中在原子核上。
探·知识奥秘
二、相对原子质量
4. 相对原子质量与质子数、中子数的关系
原子种类 质子数 中子数 相对原子质量
氢 1 0 1
碳 6 6 12
氧 8 8 16
钠 11 12 23
相对原子质量≈质子数+中子数
探·知识奥秘
二、相对原子质量
中国科学院院士张青莲教授为相对原子质量的测定作出了卓越贡献。他于 1983 年当选为国际纯粹与应用化学联合会原子量与同位素丰度委员会委员。他主持测定的铟、铱、锑、铕、铈、铒、锗、镝、锌的相对原子质量数据被确认为国际标准。
张青莲(1908—2006)
张青莲与相对原子质量的测定
资料卡片
【典例】关于相对原子质量的叙述正确的是( )
A.相对原子质量就是一个原子的质量
B.相对原子质量是一个碳原子质量
C.相对原子质量是原子的相对质量,是一个比值
D.相对原子质量的单位是“千克”
C
析·典型范例
【变式】氮原子的相对原子质量为14,表示的意义是( )
A.氮原子核中有14个质子
B.一个氮原子的质量为14g
C.一个氮原子的质量是一个碳-12原子质量的14倍
D.一个氮原子的质量是一个碳-12原子质量
的 的14倍
析·典型范例
D
1
—
12
原子结构
原子的构成
原子核
理·核心要点
相对原子质量
概念
核外电子
质子
中子
相对原子质量≈质子数+中子数
1.科学家精神是兴国之本,下列哪位科学家为相对原子质量的测定做出了卓越贡献( )
A.拉瓦锡 B.道尔顿
C.张青莲 D.门捷列夫
练·技能实战
C
2.原子模型的演变反映了人类探索物质结构的漫长历程。图示为原子结构模型的演变图,下列排序符合人类认识原子结构历程的是( )
A.①②③ B.②①③
C.①③② D.②③①
练·技能实战
D
3.下列有关粒子的说法中正确的是( )
A.原子的原子核都是由质子和中子构成的
B.分子可分,原子不可分
C.原子的质子数和中子数一定相同
D.相对原子质量与原子的实际质量不相同
练·技能实战
D
4.原子、分子质量很小,为计算和使用方便引入相对原子质量。下列说法正确的是( )
A.相对原子质量是采用以小比小使数值变大的计量原理
B.相对原子质量是一个原子质量与一个碳-12 原子质量的比值
C.两种原子的相对原子质量之比与真实质量之比没有必然联系
D.相对原子质量是一个比值,单位是g
练·技能实战
A
5.相同质量的钠、镁、铜三种金属,含原子数目最多的是( )
A.钠 B.镁 C.铜 D.一样多
练·技能实战
A
THANKS!
谢谢观看
九年级化学 上册·人教版2024
同课章节目录
