课题2 原子结构 第2课时 原子核外电子排布、离子 课件(共29张PPT)2025-2026学年人教版九年级化学上册
文档属性
| 名称 | 课题2 原子结构 第2课时 原子核外电子排布、离子 课件(共29张PPT)2025-2026学年人教版九年级化学上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-27 00:00:00 | ||
图片预览





文档简介
(共29张PPT)
第三单元 物质构成的奥秘
课题2
原子结构
(第2课时)
九年级化学 上册·人教版2024
学习内容导览
离子
2
原子核外电子的排布
1
1.知道原子核外电子是分层排布的;了解原子结构示意图的含义。
2.以氯化钠为例,了解离子的形成过程。
3.知道离子是构成物质的一种粒子,知道离子与原子的区别与联系。
明·教学目标
引·新课导入
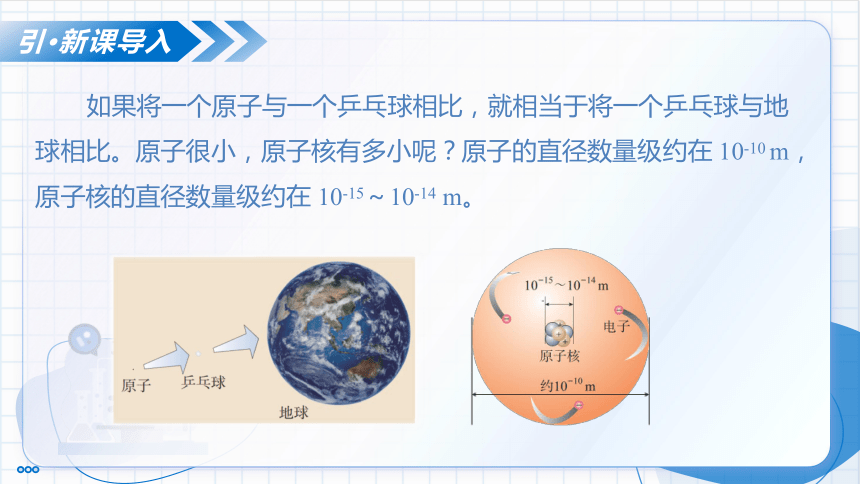
如果将一个原子与一个乒乓球相比,就相当于将一个乒乓球与地球相比。原子很小,原子核有多小呢?原子的直径数量级约在 10-10 m,原子核的直径数量级约在 10-15~10-14 m。
引·新课导入
如果把原子比作一个庞大的体育场,那么原子核就相当于一只蚂蚁。原子核外的电子如何在广阔的空间里高速运动?
原子核
原子核外电子的排布
01
一、原子核外电子的排布
探·知识奥秘
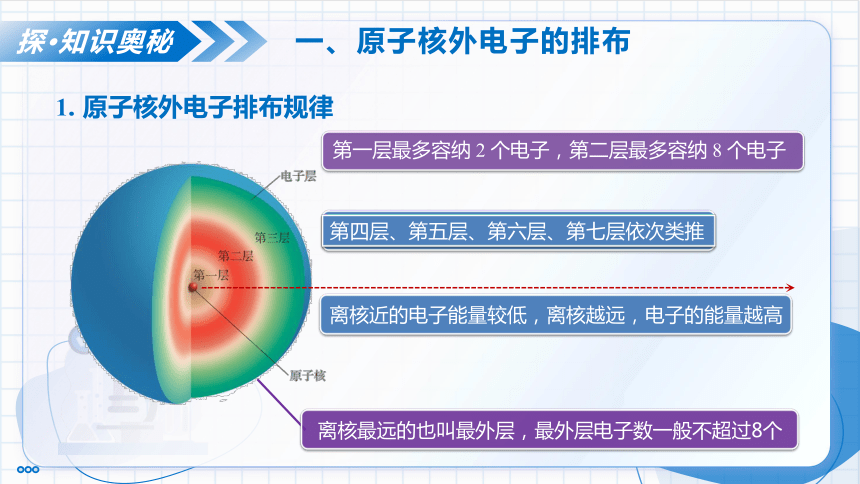
1. 原子核外电子排布规律
玻尔(1885—1962)
1913年,玻尔(卢瑟福的学生)提出原子轨道模型,认为当原子只有一个电子时,电子沿特定球形轨道运行;当原子有多个电子时,电子将分层排布,在不同的轨道上运行,按能量高低而距核远近不同。
一、原子核外电子的排布
探·知识奥秘
1. 原子核外电子排布规律
离核近的电子能量较低,离核越远,电子的能量越高
第四层、第五层、第六层、第七层依次类推
第一层最多容纳 2 个电子,第二层最多容纳 8 个电子
离核最远的也叫最外层,最外层电子数一般不超过8个
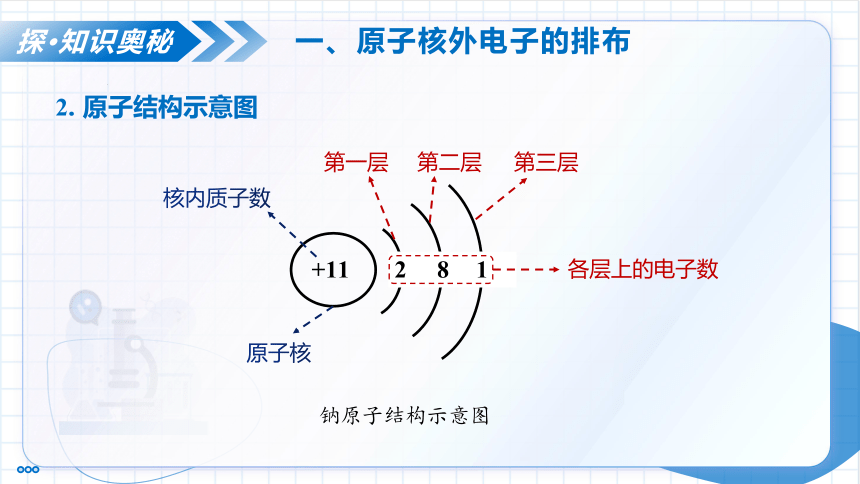
+11
2 8 1
原子核
核内质子数
第一层
第二层
第三层
各层上的电子数
钠原子结构示意图
2. 原子结构示意图
探·知识奥秘
一、原子核外电子的排布
探·知识奥秘
1. 标出下列氯原子结构示意图中横线所指部分的含义。
思考与讨论:
一、原子核外电子的排布
表示原子核及 ___________________________________
原子的核电荷数为17,质子数为17
弧线表示 __________
电子层
弧线上的数字表示该层上的 __________
电子数
+17
2 8 7
氯原子的结构示意图
一、原子核外电子的排布
探·知识奥秘
金属原子
非金属原子
稀有气体原子
2. 原子结构示意图
最外层电子
一般少于4个
最外层电子
一般多于4个
最外层一般都有8个电子(氦有2个电子)
相对稳定结构
原子种类 实例 最外层电子数 化学性质
稀有气体 He、Ne、Ar
金 属 Na、Mg、Al
非金属 O、S、Cl
8个(He为2)
< 4
> 4
最外层电子数决定原子的化学性质
探·知识奥秘
一、原子核外电子的排布
3. 原子的化学性质与核外电子的关系
相对稳定
不稳定,易失去电子
不稳定,易得到电子
【典例】电车锂电池的创新发展为我国国内经济大循环贡献力量。锂原子的结构示意图如下,相关说法正确的是( )
A.锂原子的质子数为3
B.原子核外有3个电子层
C.“+3”表示锂原子带正电
D.最外层有3个电子
析·典型范例
A
【变式】如图为氪原子的结构示意图,有关该原子的说法错误的是( )
A.核内质子数为36
B.核外有4个电子层
C.第一层电子数为8
D.在化学反应中不易得失电子
C
析·典型范例
离子
02
二、离子
探·知识奥秘
1. 离子的形成
钠原子和氯原子是如何形成氯化钠的?
+11
2 8 1
+17
2 8 7
Na
Cl
二、离子
探·知识奥秘
1. 离子的形成
钠原子与氯原子在化学反应中通过得失电子形成离子的过程 原子 原子结构示意图 反应时得失电子情况 离子结构示意图
钠原子 (Na)
氯原子 (Cl)
最外层的1个电子转移到氯原子的最外层,形成相对稳定结构
最外层的7个电子得到1个电子后,形成相对稳定结构
探·知识奥秘
2. 离子的定义与分类
定 义
带电荷的原子或原子团
分 类
阳离子:带正电荷
阴离子:带负电荷
氯化钠的形成
Na
Cl
钠离子带正电荷
氯离子带负电荷
静电作用
氯化钠
氯化钠由钠离子和氯离子构成
离子也是构成物质的微观粒子
二、离子
二、离子
探·知识奥秘
3. 离子的表示方法
举 例
位置:在元素符号右上角标明电性和电荷数。
先后:电荷数在前(电荷数为1时,1省略不写),电性在后(“+”表示带正电荷,“-”表示带负电荷)。
钠离子 镁离子 氯离子 氧离子
Na
+
Mg
2+
Cl
-
O
2-
探·知识奥秘
二、离子
4. 离子符号的意义
2Mg2+
表示 1 个镁离子带 2 个单位的正电荷
表示 2 个镁离子
R
表示每个R离子带n个单位的正(负)电荷
n+
m
表示m个R离子
【典例】下列粒子结构示意图,表示阴离子的是( )
A. B. C. D.
析·典型范例
C
【变式】当氢原子变成氢离子后,下列各项发生改变的是( )
A.质子数 B.相对原子质量
C.电子数 D.中子数
C
析·典型范例
原子结构
原子核外电子的排布
原子核外电子排布规律
理·核心要点
离子
离子的定义与分类
原子结构示意图
原子的化学性质与核外电子的关系
离子的表示方法
离子符号的意义
离子的形成
1. 下图为硫原子的结构示意图,下列说法不正确的是( )
A.硫原子的质子数为 16
B.硫原子在化学变化中易失电子
C.硫原子的第二层电子数为 8
D.硫原子核外有 3 个电子层
练·技能实战
B
+16
2 8 6
2. 钠与氯气反应生成氯化钠的示意图如下。下列有关说法正确的是( )
A.氯化钠固体由氯化钠分子构成
B.反应中一个钠原子失去一个电子,形成相对稳定结构
C.氯原子核外有两个电子层
D.反应中Cl变成Cl-,化学性质未改变
练·技能实战
B
3. 大多数手机中使用的电池是锂离子电池。已知锂离子(Li+)的核内质子数为 3,中子数为 4。下列说法错误的是( )
A.锂离子核外只有 1 个电子层
B.1 个锂离子带 1 个单位正电荷
C.锂离子得到 1 个电子可以变成锂原子
D.锂原子的中子数为 3
练·技能实战
D
4. 下图是几种微粒的结构示意图,请用相应微粒的代号填空。
(1)属于金属原子的是 _______;
(2)具有相对稳定结构的是 _______;
(3)易得电子的是 _______。
练·技能实战
BD
A
C
5. 某粒子的结构示意图如图所示:
(1)当 b=8,且该粒子不显电性时,a=____。
(2)当 b=8,且该粒子带有 2 个单位负电荷时,该粒子的化学符号是______。
(3)当 b=8,且该粒子带有 3 个单位正电荷时,该粒子的化学符号是______。
练·技能实战
10
O2-
Al3+
THANKS!
谢谢观看
九年级化学 上册·人教版2024
第三单元 物质构成的奥秘
课题2
原子结构
(第2课时)
九年级化学 上册·人教版2024
学习内容导览
离子
2
原子核外电子的排布
1
1.知道原子核外电子是分层排布的;了解原子结构示意图的含义。
2.以氯化钠为例,了解离子的形成过程。
3.知道离子是构成物质的一种粒子,知道离子与原子的区别与联系。
明·教学目标
引·新课导入
如果将一个原子与一个乒乓球相比,就相当于将一个乒乓球与地球相比。原子很小,原子核有多小呢?原子的直径数量级约在 10-10 m,原子核的直径数量级约在 10-15~10-14 m。
引·新课导入
如果把原子比作一个庞大的体育场,那么原子核就相当于一只蚂蚁。原子核外的电子如何在广阔的空间里高速运动?
原子核
原子核外电子的排布
01
一、原子核外电子的排布
探·知识奥秘
1. 原子核外电子排布规律
玻尔(1885—1962)
1913年,玻尔(卢瑟福的学生)提出原子轨道模型,认为当原子只有一个电子时,电子沿特定球形轨道运行;当原子有多个电子时,电子将分层排布,在不同的轨道上运行,按能量高低而距核远近不同。
一、原子核外电子的排布
探·知识奥秘
1. 原子核外电子排布规律
离核近的电子能量较低,离核越远,电子的能量越高
第四层、第五层、第六层、第七层依次类推
第一层最多容纳 2 个电子,第二层最多容纳 8 个电子
离核最远的也叫最外层,最外层电子数一般不超过8个
+11
2 8 1
原子核
核内质子数
第一层
第二层
第三层
各层上的电子数
钠原子结构示意图
2. 原子结构示意图
探·知识奥秘
一、原子核外电子的排布
探·知识奥秘
1. 标出下列氯原子结构示意图中横线所指部分的含义。
思考与讨论:
一、原子核外电子的排布
表示原子核及 ___________________________________
原子的核电荷数为17,质子数为17
弧线表示 __________
电子层
弧线上的数字表示该层上的 __________
电子数
+17
2 8 7
氯原子的结构示意图
一、原子核外电子的排布
探·知识奥秘
金属原子
非金属原子
稀有气体原子
2. 原子结构示意图
最外层电子
一般少于4个
最外层电子
一般多于4个
最外层一般都有8个电子(氦有2个电子)
相对稳定结构
原子种类 实例 最外层电子数 化学性质
稀有气体 He、Ne、Ar
金 属 Na、Mg、Al
非金属 O、S、Cl
8个(He为2)
< 4
> 4
最外层电子数决定原子的化学性质
探·知识奥秘
一、原子核外电子的排布
3. 原子的化学性质与核外电子的关系
相对稳定
不稳定,易失去电子
不稳定,易得到电子
【典例】电车锂电池的创新发展为我国国内经济大循环贡献力量。锂原子的结构示意图如下,相关说法正确的是( )
A.锂原子的质子数为3
B.原子核外有3个电子层
C.“+3”表示锂原子带正电
D.最外层有3个电子
析·典型范例
A
【变式】如图为氪原子的结构示意图,有关该原子的说法错误的是( )
A.核内质子数为36
B.核外有4个电子层
C.第一层电子数为8
D.在化学反应中不易得失电子
C
析·典型范例
离子
02
二、离子
探·知识奥秘
1. 离子的形成
钠原子和氯原子是如何形成氯化钠的?
+11
2 8 1
+17
2 8 7
Na
Cl
二、离子
探·知识奥秘
1. 离子的形成
钠原子与氯原子在化学反应中通过得失电子形成离子的过程 原子 原子结构示意图 反应时得失电子情况 离子结构示意图
钠原子 (Na)
氯原子 (Cl)
最外层的1个电子转移到氯原子的最外层,形成相对稳定结构
最外层的7个电子得到1个电子后,形成相对稳定结构
探·知识奥秘
2. 离子的定义与分类
定 义
带电荷的原子或原子团
分 类
阳离子:带正电荷
阴离子:带负电荷
氯化钠的形成
Na
Cl
钠离子带正电荷
氯离子带负电荷
静电作用
氯化钠
氯化钠由钠离子和氯离子构成
离子也是构成物质的微观粒子
二、离子
二、离子
探·知识奥秘
3. 离子的表示方法
举 例
位置:在元素符号右上角标明电性和电荷数。
先后:电荷数在前(电荷数为1时,1省略不写),电性在后(“+”表示带正电荷,“-”表示带负电荷)。
钠离子 镁离子 氯离子 氧离子
Na
+
Mg
2+
Cl
-
O
2-
探·知识奥秘
二、离子
4. 离子符号的意义
2Mg2+
表示 1 个镁离子带 2 个单位的正电荷
表示 2 个镁离子
R
表示每个R离子带n个单位的正(负)电荷
n+
m
表示m个R离子
【典例】下列粒子结构示意图,表示阴离子的是( )
A. B. C. D.
析·典型范例
C
【变式】当氢原子变成氢离子后,下列各项发生改变的是( )
A.质子数 B.相对原子质量
C.电子数 D.中子数
C
析·典型范例
原子结构
原子核外电子的排布
原子核外电子排布规律
理·核心要点
离子
离子的定义与分类
原子结构示意图
原子的化学性质与核外电子的关系
离子的表示方法
离子符号的意义
离子的形成
1. 下图为硫原子的结构示意图,下列说法不正确的是( )
A.硫原子的质子数为 16
B.硫原子在化学变化中易失电子
C.硫原子的第二层电子数为 8
D.硫原子核外有 3 个电子层
练·技能实战
B
+16
2 8 6
2. 钠与氯气反应生成氯化钠的示意图如下。下列有关说法正确的是( )
A.氯化钠固体由氯化钠分子构成
B.反应中一个钠原子失去一个电子,形成相对稳定结构
C.氯原子核外有两个电子层
D.反应中Cl变成Cl-,化学性质未改变
练·技能实战
B
3. 大多数手机中使用的电池是锂离子电池。已知锂离子(Li+)的核内质子数为 3,中子数为 4。下列说法错误的是( )
A.锂离子核外只有 1 个电子层
B.1 个锂离子带 1 个单位正电荷
C.锂离子得到 1 个电子可以变成锂原子
D.锂原子的中子数为 3
练·技能实战
D
4. 下图是几种微粒的结构示意图,请用相应微粒的代号填空。
(1)属于金属原子的是 _______;
(2)具有相对稳定结构的是 _______;
(3)易得电子的是 _______。
练·技能实战
BD
A
C
5. 某粒子的结构示意图如图所示:
(1)当 b=8,且该粒子不显电性时,a=____。
(2)当 b=8,且该粒子带有 2 个单位负电荷时,该粒子的化学符号是______。
(3)当 b=8,且该粒子带有 3 个单位正电荷时,该粒子的化学符号是______。
练·技能实战
10
O2-
Al3+
THANKS!
谢谢观看
九年级化学 上册·人教版2024
同课章节目录
