2.1 空气的组成 课件(共28张PPT内嵌视频) 2025-2026学年化学沪教版(2024)九年级上册
文档属性
| 名称 | 2.1 空气的组成 课件(共28张PPT内嵌视频) 2025-2026学年化学沪教版(2024)九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 108.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-28 00:00:00 | ||
图片预览








文档简介
(共28张PPT)
2.1 空气的组成
1.能依据观察的实验现象初步推断空气的主要成分;
2.能从组成上对物质进行分类,识别纯净物和混合物;
3.能体会科学家在探索空气成分过程中的智慧和方法。
我们每时每刻都离不开空气
一个敞口的集气瓶,经常被认为里面是“空的”,意指瓶中“没有东西”。其实不然,用简单的实验即可证明这个集气瓶中充满了空气。
空气看不见摸不着,怎么证明它的存在 空气中含有哪些物质 要回答这些问题,最好的方法就是通过实验来探究。
一、空气的组成
实验探究
利用下图所示的实验仪器,组装成图中所示的实验装置,请你利用该实验装置把一个集气瓶中的部分空气“捕获”到另一个集气瓶中。简要说明其原理。
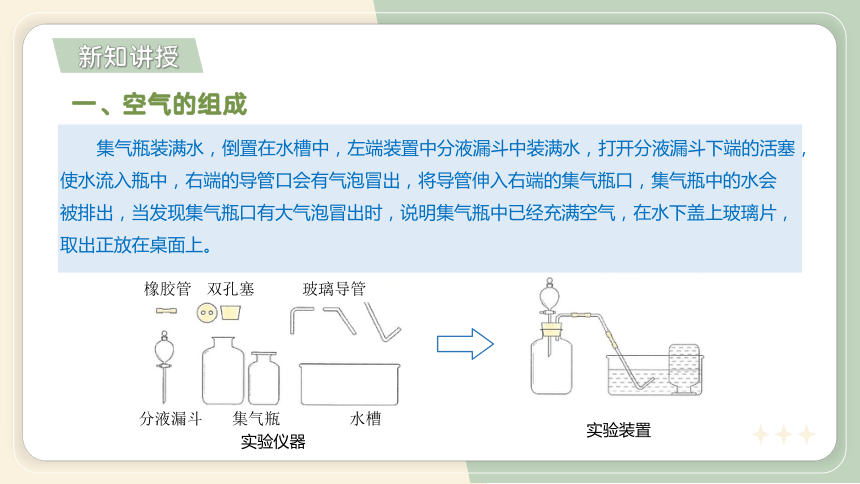
实验仪器
橡胶管 双孔塞 玻璃导管
分液漏斗 集气瓶 水槽
实验装置
集气瓶装满水,倒置在水槽中,左端装置中分液漏斗中装满水,打开分液漏斗下端的活塞,使水流入瓶中,右端的导管口会有气泡冒出,将导管伸入右端的集气瓶口,集气瓶中的水会被排出,当发现集气瓶口有大气泡冒出时,说明集气瓶中已经充满空气,在水下盖上玻璃片,取出正放在桌面上。
方法引导
用手握住试管时,导管口有气泡冒出;松开手后过一段时间,导管中会形成一段水柱,则说明装置的气密性良好。
注意:如果环境温度偏高,也可采用酒精灯微热或热毛巾捂热等其他方法。
吸气
吐气
吸气
呼气
呼吸作用
空气中含有氧气,那空气中氧气的体积分数是多少呢?
1.测定空气中氧气的体积分数
原理:设计实验,让某种物质在一定条件下把盛有空气的容器中的氧气完全消耗掉,测量反应后容器中剩余气体的体积,即可以推断出氧气在空气中所占的体积分数。
观察思考
仔细观察下列实验,并思考相关的问题。
1.将集气瓶的容积划分为5等份并加以标记。
2.将橡胶管上的止水夹夹紧 ,在燃烧匙内装入足量的红磷,在酒精灯火焰上点燃红磷后,将燃烧匙迅速伸入集气瓶内,塞紧橡皮塞。观察到什么现象?红磷在集气瓶中燃烧,消耗了什么气体?
3.待火焰熄灭后,观察红磷是否有剩余。待集气瓶
冷却到室温后,把导管插入盛水的烧杯中,打开止水夹,
观察到什么现象?
4.依据实验现象推断空气中氧气所占的体积分数。
红磷
水
燃烧匙
止水夹
进入的水的体积约占集气瓶容积的五分之一,说明空气中的氧气约占空气总体积的五分之一。剩余气体约占空气总体积的五分之四,不支持红磷燃烧,主要是氮气。
实验结论
红磷燃烧消耗了氧气,生成了五氧化二磷固体,使得集气瓶中的压强减小。在大气压的作用下,烧杯中的水被压入集气瓶中。
实验分析
磷 + 氧气 五氧化二磷
点燃
P O2 P2O5
实验原理
1.测定空气中氧气的体积分数
5.思考讨论。
(1)已知空气中氧气的体积分数约为五分之一。观察到的实验结果是否接近这个数值?若相差较大,分析产生误差的原因。
(2)蜡烛在空气中燃烧生成二氧化碳和水。能否用蜡烛代替红磷进行相同实验,为什么
从测定原理分析,所得实验数据的大小取决于瓶内压强减小的程度,产生误差的原因主要有以下几个方面:
①药品的量不足;②装置漏气; ③没有冷却到室温就打开了止水夹等。
蜡烛在空气中燃烧生成二氧化碳和水等气体,虽消耗了氧气,但增加了新的气体,不能用来测定空气中氧气的体积分数。
1772年
浊气(氮气)
卢瑟福
普利斯特里
1774年
脱燃素空气(氧气)
舍勒
火气(氧气)
1773年
拉瓦锡
氧气、氮气
1777年
空气成分的发现
空气成分的发现
拉瓦锡(法国)
钟罩实验
拓展视野
2.空气的成分
1%
0.94%
0.03%
0.03%
稀有气体
(氦氖氩氪氙氡)
二氧化碳
其他气体和杂质
氮气
78%
氧气
21%
3.物质分类
由一种物质组成
纯净物
由两种或两种以上物质组成
混合物
如:空气 、食盐水、蔗糖水
如:氧气、氮气、二氧化碳、水
混合物中的各成分保持原有的性质。
物 质
在实际应用中,绝对纯净的物质并不存在,当其中杂质成分的含量极少时,即可认为是纯净物。
洁净的空气、 清新的空气、 澄清的石灰水
混合物
冰水混合物
五氧化二磷
纯净物
看组成物质种类的多少
判断方法
不能根据表面字眼,更不能看字的多少。
氮气
(1)制造硝酸和氮肥的重要原料
(2)常用作保护气
硝酸
氮肥
灯泡充氮气延长寿命
食品包装中充氮气防腐
二、氮气和稀有气体
(3)制造低温环境
医疗上用液氮做麻醉
超导材料在液氮低温环境下显示超导性能
物理性质:无色、无味的气体,在标准状况下密度比空气略小,难溶于水。
化学性质: 不活泼,一般情况下,它不支持燃烧也不供给呼吸。
用作保护气: 灯泡、食品、焊接金属
化学性质不活泼
制造低温环境: 医疗、超导材料
液氮汽化吸热(物理性质)
决定
体现
稀有气体
过去人们曾把稀有气体称为惰性气体,是因为他们的化学性质很不活泼,几乎不与任何物质发生反应。
它们都没有颜色,没有气味,且难溶于水,但是在生产和科学研究中,却有着很广泛的用途。
用途:
(1)作保护气 (2)制成多种电光源
(3)用氦气填充气球,不会爆炸(4)氦可以用于制造低温环境
思考:以上稀有气体的用途体现的都是它们的哪些性质?
电光源:霓虹灯、航标灯、闪光灯等
①化学性质不活泼
②氦气的密度比空气的小
用作保护气:灯泡、金属焊接等
氦气:飞艇、热气球
通电发光(物理性质)
化学性质不活泼
决定
体现
化学性质:很不活泼,但在一定条件下也能与某些物质发生化学反应。
物理性质:无色、无味的气体,难溶于水。
1.“空气炸锅”的工作原理是将锅内空气加热后循环吹向食物,则循环气体中含量最高的是( )
A.氧气
B.氮气
C.稀有气体
D.二氧化碳
B
.
2.用如图装置验证空气中O2的含量。下列说法不正确的是( )
A.实验前需检查装置气密性
B.红磷的作用是消耗集气瓶中的氧气
C.红磷燃烧时产生大量白烟
D.集气瓶中水面最终上升至3处
D
3.医学上常用“冷冻法”治疗咽喉炎,其冷冻剂是下列物质中的( )
A.液态氮
B.液态氧
C.液态空气
D.液态二氧化碳
A
4.下列物质中,前者是纯净物,后者是混合物的是( )
A.净化后的空气、氧气
B.氮气、硫
C.澄清的石灰水、二氧化碳
D.冰水混合物、稀有气体
D
2.1 空气的组成
混合物和纯净物
空气的组成
氮气和稀有气体
探究空气中氧气的体积分数
空气的成分(N2占78%、O2占21%)
氮气的性质和用途
稀有气体的性质和用途
2.1 空气的组成
1.能依据观察的实验现象初步推断空气的主要成分;
2.能从组成上对物质进行分类,识别纯净物和混合物;
3.能体会科学家在探索空气成分过程中的智慧和方法。
我们每时每刻都离不开空气
一个敞口的集气瓶,经常被认为里面是“空的”,意指瓶中“没有东西”。其实不然,用简单的实验即可证明这个集气瓶中充满了空气。
空气看不见摸不着,怎么证明它的存在 空气中含有哪些物质 要回答这些问题,最好的方法就是通过实验来探究。
一、空气的组成
实验探究
利用下图所示的实验仪器,组装成图中所示的实验装置,请你利用该实验装置把一个集气瓶中的部分空气“捕获”到另一个集气瓶中。简要说明其原理。
实验仪器
橡胶管 双孔塞 玻璃导管
分液漏斗 集气瓶 水槽
实验装置
集气瓶装满水,倒置在水槽中,左端装置中分液漏斗中装满水,打开分液漏斗下端的活塞,使水流入瓶中,右端的导管口会有气泡冒出,将导管伸入右端的集气瓶口,集气瓶中的水会被排出,当发现集气瓶口有大气泡冒出时,说明集气瓶中已经充满空气,在水下盖上玻璃片,取出正放在桌面上。
方法引导
用手握住试管时,导管口有气泡冒出;松开手后过一段时间,导管中会形成一段水柱,则说明装置的气密性良好。
注意:如果环境温度偏高,也可采用酒精灯微热或热毛巾捂热等其他方法。
吸气
吐气
吸气
呼气
呼吸作用
空气中含有氧气,那空气中氧气的体积分数是多少呢?
1.测定空气中氧气的体积分数
原理:设计实验,让某种物质在一定条件下把盛有空气的容器中的氧气完全消耗掉,测量反应后容器中剩余气体的体积,即可以推断出氧气在空气中所占的体积分数。
观察思考
仔细观察下列实验,并思考相关的问题。
1.将集气瓶的容积划分为5等份并加以标记。
2.将橡胶管上的止水夹夹紧 ,在燃烧匙内装入足量的红磷,在酒精灯火焰上点燃红磷后,将燃烧匙迅速伸入集气瓶内,塞紧橡皮塞。观察到什么现象?红磷在集气瓶中燃烧,消耗了什么气体?
3.待火焰熄灭后,观察红磷是否有剩余。待集气瓶
冷却到室温后,把导管插入盛水的烧杯中,打开止水夹,
观察到什么现象?
4.依据实验现象推断空气中氧气所占的体积分数。
红磷
水
燃烧匙
止水夹
进入的水的体积约占集气瓶容积的五分之一,说明空气中的氧气约占空气总体积的五分之一。剩余气体约占空气总体积的五分之四,不支持红磷燃烧,主要是氮气。
实验结论
红磷燃烧消耗了氧气,生成了五氧化二磷固体,使得集气瓶中的压强减小。在大气压的作用下,烧杯中的水被压入集气瓶中。
实验分析
磷 + 氧气 五氧化二磷
点燃
P O2 P2O5
实验原理
1.测定空气中氧气的体积分数
5.思考讨论。
(1)已知空气中氧气的体积分数约为五分之一。观察到的实验结果是否接近这个数值?若相差较大,分析产生误差的原因。
(2)蜡烛在空气中燃烧生成二氧化碳和水。能否用蜡烛代替红磷进行相同实验,为什么
从测定原理分析,所得实验数据的大小取决于瓶内压强减小的程度,产生误差的原因主要有以下几个方面:
①药品的量不足;②装置漏气; ③没有冷却到室温就打开了止水夹等。
蜡烛在空气中燃烧生成二氧化碳和水等气体,虽消耗了氧气,但增加了新的气体,不能用来测定空气中氧气的体积分数。
1772年
浊气(氮气)
卢瑟福
普利斯特里
1774年
脱燃素空气(氧气)
舍勒
火气(氧气)
1773年
拉瓦锡
氧气、氮气
1777年
空气成分的发现
空气成分的发现
拉瓦锡(法国)
钟罩实验
拓展视野
2.空气的成分
1%
0.94%
0.03%
0.03%
稀有气体
(氦氖氩氪氙氡)
二氧化碳
其他气体和杂质
氮气
78%
氧气
21%
3.物质分类
由一种物质组成
纯净物
由两种或两种以上物质组成
混合物
如:空气 、食盐水、蔗糖水
如:氧气、氮气、二氧化碳、水
混合物中的各成分保持原有的性质。
物 质
在实际应用中,绝对纯净的物质并不存在,当其中杂质成分的含量极少时,即可认为是纯净物。
洁净的空气、 清新的空气、 澄清的石灰水
混合物
冰水混合物
五氧化二磷
纯净物
看组成物质种类的多少
判断方法
不能根据表面字眼,更不能看字的多少。
氮气
(1)制造硝酸和氮肥的重要原料
(2)常用作保护气
硝酸
氮肥
灯泡充氮气延长寿命
食品包装中充氮气防腐
二、氮气和稀有气体
(3)制造低温环境
医疗上用液氮做麻醉
超导材料在液氮低温环境下显示超导性能
物理性质:无色、无味的气体,在标准状况下密度比空气略小,难溶于水。
化学性质: 不活泼,一般情况下,它不支持燃烧也不供给呼吸。
用作保护气: 灯泡、食品、焊接金属
化学性质不活泼
制造低温环境: 医疗、超导材料
液氮汽化吸热(物理性质)
决定
体现
稀有气体
过去人们曾把稀有气体称为惰性气体,是因为他们的化学性质很不活泼,几乎不与任何物质发生反应。
它们都没有颜色,没有气味,且难溶于水,但是在生产和科学研究中,却有着很广泛的用途。
用途:
(1)作保护气 (2)制成多种电光源
(3)用氦气填充气球,不会爆炸(4)氦可以用于制造低温环境
思考:以上稀有气体的用途体现的都是它们的哪些性质?
电光源:霓虹灯、航标灯、闪光灯等
①化学性质不活泼
②氦气的密度比空气的小
用作保护气:灯泡、金属焊接等
氦气:飞艇、热气球
通电发光(物理性质)
化学性质不活泼
决定
体现
化学性质:很不活泼,但在一定条件下也能与某些物质发生化学反应。
物理性质:无色、无味的气体,难溶于水。
1.“空气炸锅”的工作原理是将锅内空气加热后循环吹向食物,则循环气体中含量最高的是( )
A.氧气
B.氮气
C.稀有气体
D.二氧化碳
B
.
2.用如图装置验证空气中O2的含量。下列说法不正确的是( )
A.实验前需检查装置气密性
B.红磷的作用是消耗集气瓶中的氧气
C.红磷燃烧时产生大量白烟
D.集气瓶中水面最终上升至3处
D
3.医学上常用“冷冻法”治疗咽喉炎,其冷冻剂是下列物质中的( )
A.液态氮
B.液态氧
C.液态空气
D.液态二氧化碳
A
4.下列物质中,前者是纯净物,后者是混合物的是( )
A.净化后的空气、氧气
B.氮气、硫
C.澄清的石灰水、二氧化碳
D.冰水混合物、稀有气体
D
2.1 空气的组成
混合物和纯净物
空气的组成
氮气和稀有气体
探究空气中氧气的体积分数
空气的成分(N2占78%、O2占21%)
氮气的性质和用途
稀有气体的性质和用途
同课章节目录
