2.3 课时1 从空气中分离出氧气 利用过氧化氢制氧气课件(共29张PPT内嵌视频) 2025-2026学年化学沪教版(2024)九年级上册
文档属性
| 名称 | 2.3 课时1 从空气中分离出氧气 利用过氧化氢制氧气课件(共29张PPT内嵌视频) 2025-2026学年化学沪教版(2024)九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 59.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-28 00:00:00 | ||
图片预览








文档简介
(共29张PPT)
2.3 氧气的制备
课时1 从空气中分离出氧气
利用过氧化氢制取氧气
沪教版 九年级上册
1.了解工业制取氧气的思路和方法。
2.学习实验室用过氧化氢溶液和二氧化锰制取氧气的实验装置和实验步骤。
3.认识催化剂和催化作用,知道催化剂对化学反应的重要作用。
4.认识分解反应,并会判断分解反应。
工业生产、医疗卫生、科学研究等行业往往需要比较纯净的氧气 ,因此需要将空气中的氧气分离出来,或通过化学反应来制备氧气。到底如何来制备氧气呢?
医用氧气袋
潜水氧气瓶
交流讨论
在分离液态空气制取氧气时,一般先将空气除尘,再除去二氧化碳和水蒸气等,获得净化后的气体混合物。已知在1.01×105Pa时,氧气的沸点为-183℃,氮气的沸点为-196℃。请和同学讨论并设计从上述气体混合物中获取氧气的方案。
分离液态空气法
一、工业制法——
原理:利用液氮和液氧的沸点不同
(-196℃)(-183℃)
低温加压
升温
气态氮气
液氧
-196℃
-183℃
液态空气
为了便于贮存、运输和使用,通常把氧气加压贮存在淡蓝色的钢瓶中。
分离液态空气法
空气是工业上制取氧气价廉易得的原料,但上述过程需消耗大量的能量,制得的氧气的储存和运输也不方便。随着科学技术的进步,工业制氧气的方法也有了新的发展。请你查阅资料并与同学交流,提出一种制取氧
气的新思路、新工艺。
技术设计
随着科学技术的发展,出现了许多新的工业制氧气的方法。例如,在一定压力下,让空气通过特殊薄膜或多孔性材料 (如分子筛 ),将氧气和氮气分离,可以得到高纯度的氧气,据此原理生产的制氧设备在危重病人的救护过程中发挥了重要作用。
制氧新方法
史料记载 ,早在春秋 中期 ,我 国劳动
(主要成分为硝酸钾 )三种物质按一定比
囱淦
^0
旷
圊
· △
△
·
·
3△
·
翩
∷ˉ ·△ ∷ 一
一
一 ·
.汪
一
一
·
一尹 一一
蜿
·
ˉ 一 么
肛
〓默■勰黥的发明奠定了基础。到宋代时,曾 公亮和丁度所著的
《武经总要》中已明确记载了三种不同性能、不同用途
的火药配方(图 1-10),被 公认是世界上最早的成熟
的火药配方。
气体膜分离技术是利用不同种类的气体分子在通过特定薄膜时渗透速率不同的性质,从而达到分离的目的。渗透速率大的气体穿透薄膜而得到富集,渗透速率小的气体则被截留。使用膜分离制氧机时,空气透过特定薄膜,氧气和氮气在膜的两侧分别富集。
拓展视野
制氧新方法
史料记载 ,早在春秋 中期 ,我 国劳动
(主要成分为硝酸钾 )三种物质按一定比
囱淦
^0
旷
圊
· △
△
·
·
3△
·
翩
∷ˉ ·△ ∷ 一
一
一 ·
.汪
一
一
·
一尹 一一
蜿
·
ˉ 一 么
肛
〓默■勰黥的发明奠定了基础。到宋代时,曾 公亮和丁度所著的
《武经总要》中已明确记载了三种不同性能、不同用途
的火药配方(图 1-10),被 公认是世界上最早的成熟
的火药配方。
分子筛是一种具有均匀微孔结构的材料,有很强的吸附能力,能把不同的分子分离开,起到“筛分”分子的作用,故称为分子筛。分子筛制氧机是利用分子筛特殊的吸附能力和解吸技术,加压时吸附空气中的氮气、二氧化碳气体,将未被吸收的氧气收集起来,经过净化处理后即成为高纯度的氧气;在减压条件下,分子筛将所吸附的氮气、二氧化碳气体排放回空气中,再加压又可继续吸附空气中的氮气、二氧化碳气体以获得氧气。
拓展视野
分子筛是制氧机的核心部件,其性能直接影响制氧的效果。在制氧机工作过程中,分子筛并不会被消耗,但它有一定的使用寿命,一段时间后需要更换。
制氧新方法
史料记载 ,早在春秋 中期 ,我 国劳动
(主要成分为硝酸钾 )三种物质按一定比
囱淦
^0
旷
圊
· △
△
·
·
3△
·
翩
∷ˉ ·△ ∷ 一
一
一 ·
.汪
一
一
·
一尹 一一
蜿
·
ˉ 一 么
肛
〓默■勰黥的发明奠定了基础。到宋代时,曾 公亮和丁度所著的
《武经总要》中已明确记载了三种不同性能、不同用途
的火药配方(图 1-10),被 公认是世界上最早的成熟
的火药配方。
新开发的制氧设备能耗低,无污染,装置简单,占用空间小,具有广泛的用途。
拓展视野
【主要成分】过氧化氢
【含量规格】15%
【作用与用途】
本品在分解过程中释放出活泼的新生态氧,可用于养殖池塘的增氧,药性温和,使用方便,无残留且绿色环保。
【用法与用量】
用法:将本品以1000倍水稀释后直接泼洒于养殖池塘中。
用量:每亩水深1米用本品100~150mL,病情严重可加量使用。
过氧化氢分解只产生氧气、水
二、利用化学反应制取氧气
1.分解过氧化氢制氧气
(1)试剂
过氧化氢:无色液体
H2O2 H2O + O2
过氧化氢 水+氧气
二氧化锰
(2)原理:
MnO2
二氧化锰:黑色粉末
固液常温型
(3)发生装置:
反应物状态:固体液体
反 应 条 件:不加热
装置
优点 操作简单 便于随时添加液体 便于随时添加液体,可以控制反应
注意事项 \ 长颈漏斗下端伸到液面以下 \
①查—连接仪器,检查装置气密性;
②装—装入药品(二氧化锰);
③定—固定装置;
④倒—倒入过氧化氢溶液;
⑤收—排水法或向上排空气法收集
(4)实验步骤:
排水法
气体不易溶于水
气体不与水反应
排空气法
密度比空气大
向上排空气法
(5)收集装置
观察思考
过氧化氢分解制氧气
观察思考
过氧化氢分解制氧气
现象 分析
产生大量气泡;
带火星的木条复燃;
产生大量气泡
过氧化氢在二氧化锰的作用下迅速分解产生氧气
氧气具有助燃性,能使带火星木条复燃
二氧化锰能继续加快过氧化氢分解的速率
将带火星的木条伸入集气瓶内,若木条复燃,则为氧气
(6)检验方法:
(7)验满方法:
排水法收集时:当有较大气泡从集气瓶口冒出时,说明已集满
向上排空气法收集时:将带火星的木条放在集气瓶口,若木条复燃,说明已集满
便于控制液体的滴加速率从而控制反应速率
(1)该实验中采取了什么方法加快反应速率 。
加二氧化锰催化剂
(2)采取了什么方法减慢反应速率:
;
.
调节活塞,减慢液体滴加的速率
加水减小反应物过氧化氢的浓度
本套装置的优点(分液漏斗的优点):
三、催化剂
在化学反应中能增大化学反应速率,但本身的质量和化学性质在化学反应前后都没有发生变化的物质称为该反应的催化剂。
2. 作用
催化剂在化学反应中所起的作用叫
催化作用。
1. 定义
反应中,二氧化锰既不是反应物也不是生成物,只是一种催化剂,应算作一个反应条件,所以二氧化锰写在箭头的上方。
MnO2只起加速H2O2分解的作用
①“一变”:增大其他物质的化学反应速率。
②“二不变”:本身的质量和化学性质在反应前后都不变。
催化剂的特点
a.催化剂只是一个反应条件;
b.催化剂不改变生成物的量;
c.催化剂是针对具体的化学反应而言,不能单独的说某种物质是催化剂;
d.同一个反应可以有多种催化剂。
硫酸铜溶液,氧化铁等都可以作过氧化氢制取氧气的催化剂
下列反应有什么相同点:
实验室制取氧气的原理可以表示为:
加热
高锰酸钾
锰酸钾
氧气
+
+
二氧化锰
过氧化氢 水 + 氧气
二氧化锰
两种或两种以上生成物
一种反应物
特点:
表示:
由一种反应物生成两种或两种以上其他物质的反应,叫作分解反应。它是化学反应的基本类型。
X A + B + …
定义:
一变多
四、分解反应
1. 工业制取氧气主要有以下步骤,下列有关说法不正确的是( )
A.液态空气是混合物
B.氮气先被蒸发出来,说明氮气沸点比氧气低
C.步骤②属于化学变化
D.得到的剩余液体大部分为液氧,颜色为淡蓝色
C
2.下列是有关氧气的收集和验满的实验操作,其中正确的是( )
D
3.下列反应中属于分解反应的是( )
A.氧化钙+水→氢氧化钙
B.碳酸钙→氧化钙+二氧化碳
C.氢氧化钠+盐酸→氯化钠+水
D.铁+硫酸铜→硫酸亚铁+铜
B
4.我国石油化工专家闵恩泽院士,研发了多种用于石油化工生产的催化剂,为我国炼油催化剂制造技术奠定了基础。下列有关催化剂的说法正确的是( )
A.催化剂能增加生成物的质量
B.在化学反应中催化剂只能加快反应速率
C.催化剂在反应前后化学性质不变
D.过氧化氢溶液必须加入二氧化锰才能分解出氧气
C
制取氧气
催化剂与催化作用
过氧化氢制氧气
发生装置:固液常温型
收集装置:排水法 ,向上排空气法
分解反应
一变多
改变化学反应速率
反应前后催化剂的质量和化学性质不变
从空气中分离氧气
2.3 氧气的制备
课时1 从空气中分离出氧气
利用过氧化氢制取氧气
沪教版 九年级上册
1.了解工业制取氧气的思路和方法。
2.学习实验室用过氧化氢溶液和二氧化锰制取氧气的实验装置和实验步骤。
3.认识催化剂和催化作用,知道催化剂对化学反应的重要作用。
4.认识分解反应,并会判断分解反应。
工业生产、医疗卫生、科学研究等行业往往需要比较纯净的氧气 ,因此需要将空气中的氧气分离出来,或通过化学反应来制备氧气。到底如何来制备氧气呢?
医用氧气袋
潜水氧气瓶
交流讨论
在分离液态空气制取氧气时,一般先将空气除尘,再除去二氧化碳和水蒸气等,获得净化后的气体混合物。已知在1.01×105Pa时,氧气的沸点为-183℃,氮气的沸点为-196℃。请和同学讨论并设计从上述气体混合物中获取氧气的方案。
分离液态空气法
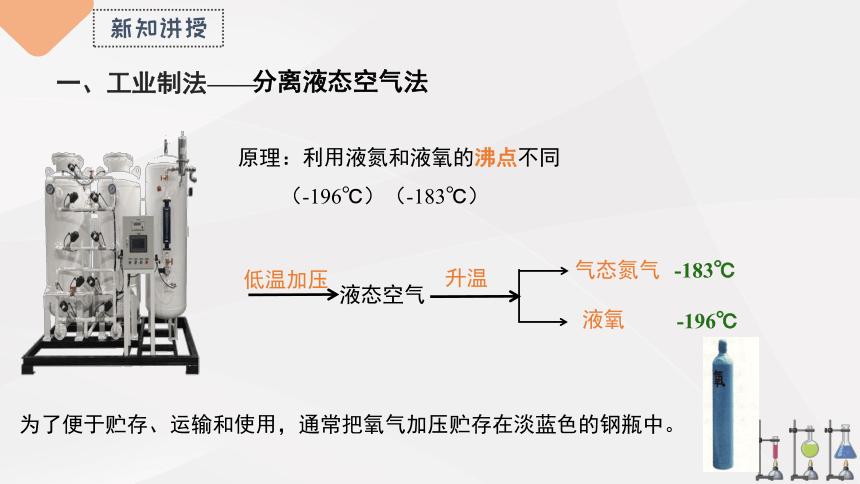
一、工业制法——
原理:利用液氮和液氧的沸点不同
(-196℃)(-183℃)
低温加压
升温
气态氮气
液氧
-196℃
-183℃
液态空气
为了便于贮存、运输和使用,通常把氧气加压贮存在淡蓝色的钢瓶中。
分离液态空气法
空气是工业上制取氧气价廉易得的原料,但上述过程需消耗大量的能量,制得的氧气的储存和运输也不方便。随着科学技术的进步,工业制氧气的方法也有了新的发展。请你查阅资料并与同学交流,提出一种制取氧
气的新思路、新工艺。
技术设计
随着科学技术的发展,出现了许多新的工业制氧气的方法。例如,在一定压力下,让空气通过特殊薄膜或多孔性材料 (如分子筛 ),将氧气和氮气分离,可以得到高纯度的氧气,据此原理生产的制氧设备在危重病人的救护过程中发挥了重要作用。
制氧新方法
史料记载 ,早在春秋 中期 ,我 国劳动
(主要成分为硝酸钾 )三种物质按一定比
囱淦
^0
旷
圊
· △
△
·
·
3△
·
翩
∷ˉ ·△ ∷ 一
一
一 ·
.汪
一
一
·
一尹 一一
蜿
·
ˉ 一 么
肛
〓默■勰黥的发明奠定了基础。到宋代时,曾 公亮和丁度所著的
《武经总要》中已明确记载了三种不同性能、不同用途
的火药配方(图 1-10),被 公认是世界上最早的成熟
的火药配方。
气体膜分离技术是利用不同种类的气体分子在通过特定薄膜时渗透速率不同的性质,从而达到分离的目的。渗透速率大的气体穿透薄膜而得到富集,渗透速率小的气体则被截留。使用膜分离制氧机时,空气透过特定薄膜,氧气和氮气在膜的两侧分别富集。
拓展视野
制氧新方法
史料记载 ,早在春秋 中期 ,我 国劳动
(主要成分为硝酸钾 )三种物质按一定比
囱淦
^0
旷
圊
· △
△
·
·
3△
·
翩
∷ˉ ·△ ∷ 一
一
一 ·
.汪
一
一
·
一尹 一一
蜿
·
ˉ 一 么
肛
〓默■勰黥的发明奠定了基础。到宋代时,曾 公亮和丁度所著的
《武经总要》中已明确记载了三种不同性能、不同用途
的火药配方(图 1-10),被 公认是世界上最早的成熟
的火药配方。
分子筛是一种具有均匀微孔结构的材料,有很强的吸附能力,能把不同的分子分离开,起到“筛分”分子的作用,故称为分子筛。分子筛制氧机是利用分子筛特殊的吸附能力和解吸技术,加压时吸附空气中的氮气、二氧化碳气体,将未被吸收的氧气收集起来,经过净化处理后即成为高纯度的氧气;在减压条件下,分子筛将所吸附的氮气、二氧化碳气体排放回空气中,再加压又可继续吸附空气中的氮气、二氧化碳气体以获得氧气。
拓展视野
分子筛是制氧机的核心部件,其性能直接影响制氧的效果。在制氧机工作过程中,分子筛并不会被消耗,但它有一定的使用寿命,一段时间后需要更换。
制氧新方法
史料记载 ,早在春秋 中期 ,我 国劳动
(主要成分为硝酸钾 )三种物质按一定比
囱淦
^0
旷
圊
· △
△
·
·
3△
·
翩
∷ˉ ·△ ∷ 一
一
一 ·
.汪
一
一
·
一尹 一一
蜿
·
ˉ 一 么
肛
〓默■勰黥的发明奠定了基础。到宋代时,曾 公亮和丁度所著的
《武经总要》中已明确记载了三种不同性能、不同用途
的火药配方(图 1-10),被 公认是世界上最早的成熟
的火药配方。
新开发的制氧设备能耗低,无污染,装置简单,占用空间小,具有广泛的用途。
拓展视野
【主要成分】过氧化氢
【含量规格】15%
【作用与用途】
本品在分解过程中释放出活泼的新生态氧,可用于养殖池塘的增氧,药性温和,使用方便,无残留且绿色环保。
【用法与用量】
用法:将本品以1000倍水稀释后直接泼洒于养殖池塘中。
用量:每亩水深1米用本品100~150mL,病情严重可加量使用。
过氧化氢分解只产生氧气、水
二、利用化学反应制取氧气
1.分解过氧化氢制氧气
(1)试剂
过氧化氢:无色液体
H2O2 H2O + O2
过氧化氢 水+氧气
二氧化锰
(2)原理:
MnO2
二氧化锰:黑色粉末
固液常温型
(3)发生装置:
反应物状态:固体液体
反 应 条 件:不加热
装置
优点 操作简单 便于随时添加液体 便于随时添加液体,可以控制反应
注意事项 \ 长颈漏斗下端伸到液面以下 \
①查—连接仪器,检查装置气密性;
②装—装入药品(二氧化锰);
③定—固定装置;
④倒—倒入过氧化氢溶液;
⑤收—排水法或向上排空气法收集
(4)实验步骤:
排水法
气体不易溶于水
气体不与水反应
排空气法
密度比空气大
向上排空气法
(5)收集装置
观察思考
过氧化氢分解制氧气
观察思考
过氧化氢分解制氧气
现象 分析
产生大量气泡;
带火星的木条复燃;
产生大量气泡
过氧化氢在二氧化锰的作用下迅速分解产生氧气
氧气具有助燃性,能使带火星木条复燃
二氧化锰能继续加快过氧化氢分解的速率
将带火星的木条伸入集气瓶内,若木条复燃,则为氧气
(6)检验方法:
(7)验满方法:
排水法收集时:当有较大气泡从集气瓶口冒出时,说明已集满
向上排空气法收集时:将带火星的木条放在集气瓶口,若木条复燃,说明已集满
便于控制液体的滴加速率从而控制反应速率
(1)该实验中采取了什么方法加快反应速率 。
加二氧化锰催化剂
(2)采取了什么方法减慢反应速率:
;
.
调节活塞,减慢液体滴加的速率
加水减小反应物过氧化氢的浓度
本套装置的优点(分液漏斗的优点):
三、催化剂
在化学反应中能增大化学反应速率,但本身的质量和化学性质在化学反应前后都没有发生变化的物质称为该反应的催化剂。
2. 作用
催化剂在化学反应中所起的作用叫
催化作用。
1. 定义
反应中,二氧化锰既不是反应物也不是生成物,只是一种催化剂,应算作一个反应条件,所以二氧化锰写在箭头的上方。
MnO2只起加速H2O2分解的作用
①“一变”:增大其他物质的化学反应速率。
②“二不变”:本身的质量和化学性质在反应前后都不变。
催化剂的特点
a.催化剂只是一个反应条件;
b.催化剂不改变生成物的量;
c.催化剂是针对具体的化学反应而言,不能单独的说某种物质是催化剂;
d.同一个反应可以有多种催化剂。
硫酸铜溶液,氧化铁等都可以作过氧化氢制取氧气的催化剂
下列反应有什么相同点:
实验室制取氧气的原理可以表示为:
加热
高锰酸钾
锰酸钾
氧气
+
+
二氧化锰
过氧化氢 水 + 氧气
二氧化锰
两种或两种以上生成物
一种反应物
特点:
表示:
由一种反应物生成两种或两种以上其他物质的反应,叫作分解反应。它是化学反应的基本类型。
X A + B + …
定义:
一变多
四、分解反应
1. 工业制取氧气主要有以下步骤,下列有关说法不正确的是( )
A.液态空气是混合物
B.氮气先被蒸发出来,说明氮气沸点比氧气低
C.步骤②属于化学变化
D.得到的剩余液体大部分为液氧,颜色为淡蓝色
C
2.下列是有关氧气的收集和验满的实验操作,其中正确的是( )
D
3.下列反应中属于分解反应的是( )
A.氧化钙+水→氢氧化钙
B.碳酸钙→氧化钙+二氧化碳
C.氢氧化钠+盐酸→氯化钠+水
D.铁+硫酸铜→硫酸亚铁+铜
B
4.我国石油化工专家闵恩泽院士,研发了多种用于石油化工生产的催化剂,为我国炼油催化剂制造技术奠定了基础。下列有关催化剂的说法正确的是( )
A.催化剂能增加生成物的质量
B.在化学反应中催化剂只能加快反应速率
C.催化剂在反应前后化学性质不变
D.过氧化氢溶液必须加入二氧化锰才能分解出氧气
C
制取氧气
催化剂与催化作用
过氧化氢制氧气
发生装置:固液常温型
收集装置:排水法 ,向上排空气法
分解反应
一变多
改变化学反应速率
反应前后催化剂的质量和化学性质不变
从空气中分离氧气
同课章节目录
