2.2 性质活泼的氧气课件(共29张PPT内嵌视频) 2025-2026学年化学沪教版(2024)九年级上册
文档属性
| 名称 | 2.2 性质活泼的氧气课件(共29张PPT内嵌视频) 2025-2026学年化学沪教版(2024)九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 64.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-28 00:00:00 | ||
图片预览







文档简介
(共29张PPT)
2.2 性质活泼的氧气
沪教版 九年级上册
1.能通过实验探究活动认识氧气的化学性质,比较不同实验条件下实验现象的差异,根据观察到的实验事实归纳出反应的本质;
2.能列举氧气在日常生活、工业生产和科学研究中的应用,从辩证的角度初步认识物质的化学变化。
大气中的O2
呼吸作用
支持燃烧
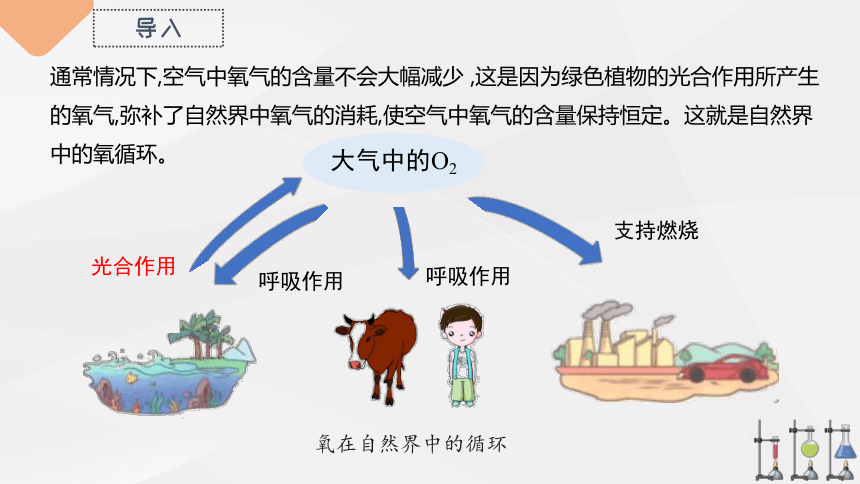
通常情况下,空气中氧气的含量不会大幅减少 ,这是因为绿色植物的光合作用所产生的氧气,弥补了自然界中氧气的消耗,使空气中氧气的含量保持恒定。这就是自然界中的氧循环。
光合作用
呼吸作用
氧在自然界中的循环
O2
空气的密度为1.293 g/L
氧气的密度为1.429 g/L
一、氧气的物理性质
在通常状况下,氧气 (oxygen)是一种无色、无气味的气体,密度稍大于空气。
注:常温下,1 L水中大约
能溶解30 mL氧气。
氧气不易溶于水 ,常温、常压下1体积水中约能溶解 0.03体积氧气。水中的生物就是依靠溶解在水中的氧气生存的。
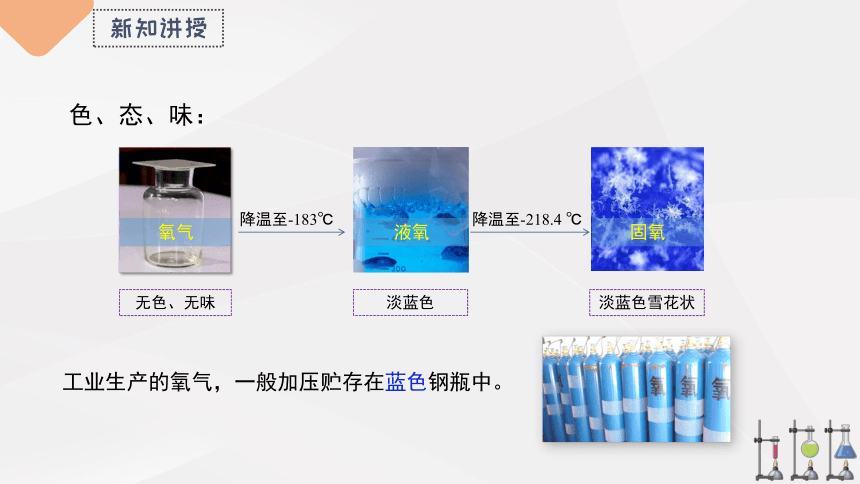
色、态、味:
无色、无味
淡蓝色
淡蓝色雪花状
工业生产的氧气,一般加压贮存在蓝色钢瓶中。
降温至-183℃
降温至-218.4 ℃
氧气
液氧
固氧
实验探究
物质在氧气中的燃烧
1.木炭的燃烧:用坩埚钳夹住木炭,在空气中点燃,再将点燃的木炭放入燃烧匙,由上而下缓慢伸入集满氧气的集气瓶中。反应结束后,向集气瓶中加入少量澄清石灰水并振荡。
实验探究
物质的燃烧
1.木炭的燃烧:用坩埚钳夹住木炭,在空气中点燃,再将点燃的木炭放入燃烧匙,由上而下缓慢伸入集满氧气的集气瓶中。反应结束后,向集气瓶中加入少量澄清石灰水并振荡。
实验名称 实验现象 实验结论 反应表达式
木炭在空气中 燃烧
木炭在氧气中 燃烧
持续发红,
放出热量
剧烈燃烧,发出白光,放出热量,生成无色的能使澄清石灰水变浑浊的气体
木炭在氧气中比在空气中燃烧更剧烈
碳 + 氧气 二氧化碳
点燃
C O2 CO2
1.为了使木炭与氧气完全反应,其操作的方法 ?
由瓶口向下缓慢插入,目的是防止因木炭在氧气中燃烧放出大量热并产生二氧化碳,使集气瓶中的氧气逸出损失,迅速使瓶中氧气含量降低,影响实验现象。
实验探究
物质在氧气中的燃烧
2.蜡烛的燃烧:将蜡烛固定在燃烧匙内,在空气中点燃。将燃着的蜡烛由上而下缓慢伸入集满氧气的集气瓶中。反应结束后,向集气瓶中加入少量澄清石灰水并振荡。
实验探究
物质在氧气中的燃烧
2.蜡烛的燃烧:将蜡烛固定在燃烧匙内,在空气中点燃。将燃着的蜡烛由上而下缓慢伸入集满氧气的集气瓶中。反应结束后,向集气瓶中加入少量澄清石灰水并振荡。
实验名称 实验现象 实验结论 反应表达式
蜡烛在空气中 燃烧
蜡烛在氧气中 燃烧
发出黄色火焰,
放出热量
剧烈燃烧,发出白光,放出热量,集气瓶内壁有小水珠,产生使澄清石灰水变浑的气体
蜡烛在氧气中比在空气中燃烧更剧烈
石蜡+ 氧气 二氧化碳+ 水
点燃
C O2 CO2
实验探究
物质在氧气中的燃烧
3.铁丝在氧气中燃烧:在螺旋状的细铁丝末端系上火柴梗,用坩埚钳夹住铁丝并点燃火柴梗,待火柴梗即将燃尽时,将它们由上而下缓慢伸入集满氧气的集气瓶中。提示:预先在集气瓶底加少量水(或铺少量沙子),防 止反应产生的高温固体溅落瓶底,避免集气瓶炸裂。
实验探究
物质在氧气中的燃烧
实验名称 实验现象 实验结论 反应表达式
铁丝在空气中加热
铁丝在氧气中燃烧
持续红热,不能燃烧
剧烈燃烧,火星四射,放出大量的热,有黑色固体产生
在空气中不能燃烧的铁丝在纯氧中能迅速燃烧
铁 + 氧气 四氧化三铁
点燃
Fe O2 Fe3O4
注意事项:
(1)集气瓶底部要有一薄层细沙或少量水,
防止溅落的高温物质使集气瓶炸裂。
(2) 要在火柴快燃尽时把铁丝插入集气瓶中, 防止火柴梗燃烧过多消耗瓶里的氧气,导致氧气浓度降低,影响实验效果。
(3)铁丝插入时,要保持在集气瓶的中央,不要靠近或碰到瓶壁,以免集气瓶受高温而炸裂。
(4) 实验用的铁丝可从铁纱窗或陶土网上抽取,用砂纸磨去表面的氧化物后使用。
通过上面的实验可以发现,可燃物在氧气中燃烧通常比在空气中燃烧更剧烈。
氧气的化学性质比较活泼,许多物质会与氧气发生化学反应。
思考与讨论:分析下列四个化学反应,有什么共同特点?
红磷 + 氧气 五氧化二磷
硫 + 氧气 二氧化硫
碳 + 氧气 二氧化碳
铁 + 氧气 四氧化三铁
点燃
点燃
点燃
点燃
产物只有一种
化合反应:由两种或两种以上的物质生成另一种物质的化学反应。
多变一
特点
化合反应属于化学反应的四种基本反应类型之一
注意
思考与讨论:分析下列四个化学反应,有什么共同特点?
红磷 + 氧气 五氧化二磷
硫 + 氧气 二氧化硫
碳 + 氧气 二氧化碳
铁 + 氧气 四氧化三铁
点燃
点燃
点燃
点燃
都有氧气参加
氧化反应:物质与氧气发生的反应。
方法引导
归纳是化学科学研究中一种常用的方法。化学研究物质的性质和它们的变化,各种各样的物质在化学变化中遵循一些共同的规律。为了寻找这些规律,归纳是科学家通常使用的一种方法。归纳需要以大量的实验事实作为基础。例如,通过观察、研究物质与氧气反应的大量实验现象,可以归纳出反应规律:一定条件下,氧气能与许多物质发生化学反应。
归纳
燃烧和缓慢氧化
1.燃烧是可燃物与空气中的氧气发生的 剧烈的氧化反应。
发光、放热的
燃烧是剧烈氧化反应,通常伴随着发光, 放热等现象。
2.缓慢氧化:反应进行的很慢,不容易被察觉。
食物腐烂
钢铁锈蚀
酿醋
如 细胞的呼吸
食物的腐烂
钢铁生锈
醋的酿造
农家肥料的腐熟
认识氧气的化学性质,可以指导我们更好地利用氧气。
氧气具有支持物质燃烧的性质,可用作助燃剂。煤、木柴、液化气和天然气等燃料在空气中燃烧,产生的热量可以烹饪食物。工业生产和科学研究中,用纯氧代替空气,可以获得更高的温度。
供给生物体呼吸是氧气的另一重要用途。生物体吸人空气中的氧气,与体内许多物质发生反应,生成新的物质,并放出能量,提供生物体必需的养分和能量以保证生命活动的需要。对由于疾病而不同程度缺氧的患者和在低氧或缺氧条件下工作的人员,需要向他们直接提供氧气 ,以维持生命正常的新陈代谢。
在一些情况下,人们也需要防止物质与氧气发生化学反应。如将食品袋抽成真空或充人氮气,避免食品因氧化而变质;为防止金属发生缓慢氧化而被锈蚀,常常采用表面喷漆、涂油等多种措施以隔绝氧气。
辩证认识与合理利用物质
事物往往具有两面性,自 然界中的物质及其变化在一定条件下也常常表现出两面性,某些性质与变化在一些情况下表现出对人类有利的一面,在另一些情况下也可能表现出有害的一面。我们要充分认识物质性质与变化的两面性,合理地利用物质及其变化,采用科学的手段避免对人类产生危害。
观念构建
1. 下列关于氧气物理性质的说法错误的是( )
A. 通常状况下氧气是无色、无味的气体
B. 鱼类能在水中生活,证明氧气易溶于水
C. 通常状况下,氧气的密度略大于空气
D. 通过低温加压,可使氧气液化成淡蓝色的液体
B
2. 下列有关氧气性质的描述,正确的是( )
A.氧气易溶于水,使得一些生物能在水中生存
B.氧气化学性质活泼,能与所有物质发生剧烈的化学反应
C.氧气在低温高压时能变成液体或固体
D.氧气密度比空气小,能填充探空气球
C
3. 下列说法中正确的是( )
A. 铁丝在空气中加热能剧烈燃烧,火星四射
B. 物质发生氧化反应时总会发光、放热
C. 红磷可以在空气中燃烧,产生大量白雾
D. 食物的腐败与动植物的呼吸都是常见的氧化反应
D
4. 下列变化过程中,均包含缓慢氧化的是( )
①金属锈蚀 ②“铜绿”分解 ③食物腐烂 ④动植物呼吸
A.①②③ B.①②④ C.①③④ D.①②③④
C
氧气的性质
氧在自然界中的循环
2.1 性质活泼的氧气
氧气的用途
2.2 性质活泼的氧气
沪教版 九年级上册
1.能通过实验探究活动认识氧气的化学性质,比较不同实验条件下实验现象的差异,根据观察到的实验事实归纳出反应的本质;
2.能列举氧气在日常生活、工业生产和科学研究中的应用,从辩证的角度初步认识物质的化学变化。
大气中的O2
呼吸作用
支持燃烧
通常情况下,空气中氧气的含量不会大幅减少 ,这是因为绿色植物的光合作用所产生的氧气,弥补了自然界中氧气的消耗,使空气中氧气的含量保持恒定。这就是自然界中的氧循环。
光合作用
呼吸作用
氧在自然界中的循环
O2
空气的密度为1.293 g/L
氧气的密度为1.429 g/L
一、氧气的物理性质
在通常状况下,氧气 (oxygen)是一种无色、无气味的气体,密度稍大于空气。
注:常温下,1 L水中大约
能溶解30 mL氧气。
氧气不易溶于水 ,常温、常压下1体积水中约能溶解 0.03体积氧气。水中的生物就是依靠溶解在水中的氧气生存的。
色、态、味:
无色、无味
淡蓝色
淡蓝色雪花状
工业生产的氧气,一般加压贮存在蓝色钢瓶中。
降温至-183℃
降温至-218.4 ℃
氧气
液氧
固氧
实验探究
物质在氧气中的燃烧
1.木炭的燃烧:用坩埚钳夹住木炭,在空气中点燃,再将点燃的木炭放入燃烧匙,由上而下缓慢伸入集满氧气的集气瓶中。反应结束后,向集气瓶中加入少量澄清石灰水并振荡。
实验探究
物质的燃烧
1.木炭的燃烧:用坩埚钳夹住木炭,在空气中点燃,再将点燃的木炭放入燃烧匙,由上而下缓慢伸入集满氧气的集气瓶中。反应结束后,向集气瓶中加入少量澄清石灰水并振荡。
实验名称 实验现象 实验结论 反应表达式
木炭在空气中 燃烧
木炭在氧气中 燃烧
持续发红,
放出热量
剧烈燃烧,发出白光,放出热量,生成无色的能使澄清石灰水变浑浊的气体
木炭在氧气中比在空气中燃烧更剧烈
碳 + 氧气 二氧化碳
点燃
C O2 CO2
1.为了使木炭与氧气完全反应,其操作的方法 ?
由瓶口向下缓慢插入,目的是防止因木炭在氧气中燃烧放出大量热并产生二氧化碳,使集气瓶中的氧气逸出损失,迅速使瓶中氧气含量降低,影响实验现象。
实验探究
物质在氧气中的燃烧
2.蜡烛的燃烧:将蜡烛固定在燃烧匙内,在空气中点燃。将燃着的蜡烛由上而下缓慢伸入集满氧气的集气瓶中。反应结束后,向集气瓶中加入少量澄清石灰水并振荡。
实验探究
物质在氧气中的燃烧
2.蜡烛的燃烧:将蜡烛固定在燃烧匙内,在空气中点燃。将燃着的蜡烛由上而下缓慢伸入集满氧气的集气瓶中。反应结束后,向集气瓶中加入少量澄清石灰水并振荡。
实验名称 实验现象 实验结论 反应表达式
蜡烛在空气中 燃烧
蜡烛在氧气中 燃烧
发出黄色火焰,
放出热量
剧烈燃烧,发出白光,放出热量,集气瓶内壁有小水珠,产生使澄清石灰水变浑的气体
蜡烛在氧气中比在空气中燃烧更剧烈
石蜡+ 氧气 二氧化碳+ 水
点燃
C O2 CO2
实验探究
物质在氧气中的燃烧
3.铁丝在氧气中燃烧:在螺旋状的细铁丝末端系上火柴梗,用坩埚钳夹住铁丝并点燃火柴梗,待火柴梗即将燃尽时,将它们由上而下缓慢伸入集满氧气的集气瓶中。提示:预先在集气瓶底加少量水(或铺少量沙子),防 止反应产生的高温固体溅落瓶底,避免集气瓶炸裂。
实验探究
物质在氧气中的燃烧
实验名称 实验现象 实验结论 反应表达式
铁丝在空气中加热
铁丝在氧气中燃烧
持续红热,不能燃烧
剧烈燃烧,火星四射,放出大量的热,有黑色固体产生
在空气中不能燃烧的铁丝在纯氧中能迅速燃烧
铁 + 氧气 四氧化三铁
点燃
Fe O2 Fe3O4
注意事项:
(1)集气瓶底部要有一薄层细沙或少量水,
防止溅落的高温物质使集气瓶炸裂。
(2) 要在火柴快燃尽时把铁丝插入集气瓶中, 防止火柴梗燃烧过多消耗瓶里的氧气,导致氧气浓度降低,影响实验效果。
(3)铁丝插入时,要保持在集气瓶的中央,不要靠近或碰到瓶壁,以免集气瓶受高温而炸裂。
(4) 实验用的铁丝可从铁纱窗或陶土网上抽取,用砂纸磨去表面的氧化物后使用。
通过上面的实验可以发现,可燃物在氧气中燃烧通常比在空气中燃烧更剧烈。
氧气的化学性质比较活泼,许多物质会与氧气发生化学反应。
思考与讨论:分析下列四个化学反应,有什么共同特点?
红磷 + 氧气 五氧化二磷
硫 + 氧气 二氧化硫
碳 + 氧气 二氧化碳
铁 + 氧气 四氧化三铁
点燃
点燃
点燃
点燃
产物只有一种
化合反应:由两种或两种以上的物质生成另一种物质的化学反应。
多变一
特点
化合反应属于化学反应的四种基本反应类型之一
注意
思考与讨论:分析下列四个化学反应,有什么共同特点?
红磷 + 氧气 五氧化二磷
硫 + 氧气 二氧化硫
碳 + 氧气 二氧化碳
铁 + 氧气 四氧化三铁
点燃
点燃
点燃
点燃
都有氧气参加
氧化反应:物质与氧气发生的反应。
方法引导
归纳是化学科学研究中一种常用的方法。化学研究物质的性质和它们的变化,各种各样的物质在化学变化中遵循一些共同的规律。为了寻找这些规律,归纳是科学家通常使用的一种方法。归纳需要以大量的实验事实作为基础。例如,通过观察、研究物质与氧气反应的大量实验现象,可以归纳出反应规律:一定条件下,氧气能与许多物质发生化学反应。
归纳
燃烧和缓慢氧化
1.燃烧是可燃物与空气中的氧气发生的 剧烈的氧化反应。
发光、放热的
燃烧是剧烈氧化反应,通常伴随着发光, 放热等现象。
2.缓慢氧化:反应进行的很慢,不容易被察觉。
食物腐烂
钢铁锈蚀
酿醋
如 细胞的呼吸
食物的腐烂
钢铁生锈
醋的酿造
农家肥料的腐熟
认识氧气的化学性质,可以指导我们更好地利用氧气。
氧气具有支持物质燃烧的性质,可用作助燃剂。煤、木柴、液化气和天然气等燃料在空气中燃烧,产生的热量可以烹饪食物。工业生产和科学研究中,用纯氧代替空气,可以获得更高的温度。
供给生物体呼吸是氧气的另一重要用途。生物体吸人空气中的氧气,与体内许多物质发生反应,生成新的物质,并放出能量,提供生物体必需的养分和能量以保证生命活动的需要。对由于疾病而不同程度缺氧的患者和在低氧或缺氧条件下工作的人员,需要向他们直接提供氧气 ,以维持生命正常的新陈代谢。
在一些情况下,人们也需要防止物质与氧气发生化学反应。如将食品袋抽成真空或充人氮气,避免食品因氧化而变质;为防止金属发生缓慢氧化而被锈蚀,常常采用表面喷漆、涂油等多种措施以隔绝氧气。
辩证认识与合理利用物质
事物往往具有两面性,自 然界中的物质及其变化在一定条件下也常常表现出两面性,某些性质与变化在一些情况下表现出对人类有利的一面,在另一些情况下也可能表现出有害的一面。我们要充分认识物质性质与变化的两面性,合理地利用物质及其变化,采用科学的手段避免对人类产生危害。
观念构建
1. 下列关于氧气物理性质的说法错误的是( )
A. 通常状况下氧气是无色、无味的气体
B. 鱼类能在水中生活,证明氧气易溶于水
C. 通常状况下,氧气的密度略大于空气
D. 通过低温加压,可使氧气液化成淡蓝色的液体
B
2. 下列有关氧气性质的描述,正确的是( )
A.氧气易溶于水,使得一些生物能在水中生存
B.氧气化学性质活泼,能与所有物质发生剧烈的化学反应
C.氧气在低温高压时能变成液体或固体
D.氧气密度比空气小,能填充探空气球
C
3. 下列说法中正确的是( )
A. 铁丝在空气中加热能剧烈燃烧,火星四射
B. 物质发生氧化反应时总会发光、放热
C. 红磷可以在空气中燃烧,产生大量白雾
D. 食物的腐败与动植物的呼吸都是常见的氧化反应
D
4. 下列变化过程中,均包含缓慢氧化的是( )
①金属锈蚀 ②“铜绿”分解 ③食物腐烂 ④动植物呼吸
A.①②③ B.①②④ C.①③④ D.①②③④
C
氧气的性质
氧在自然界中的循环
2.1 性质活泼的氧气
氧气的用途
同课章节目录
