2.3 课时2 高锰酸钾制氧气课件(共19张PPT内嵌视频) 2025-2026学年化学沪教版(2024)九年级上册
文档属性
| 名称 | 2.3 课时2 高锰酸钾制氧气课件(共19张PPT内嵌视频) 2025-2026学年化学沪教版(2024)九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 109.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-28 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
2.3 氧气的制备
课时2 高锰酸钾制氧气
1.掌握实验室用高锰酸钾制氧气的原理、装置、操作步骤及注意事项;
2.初步形成实验室制备气体的一般思路。
获取氧气还有哪些方法?
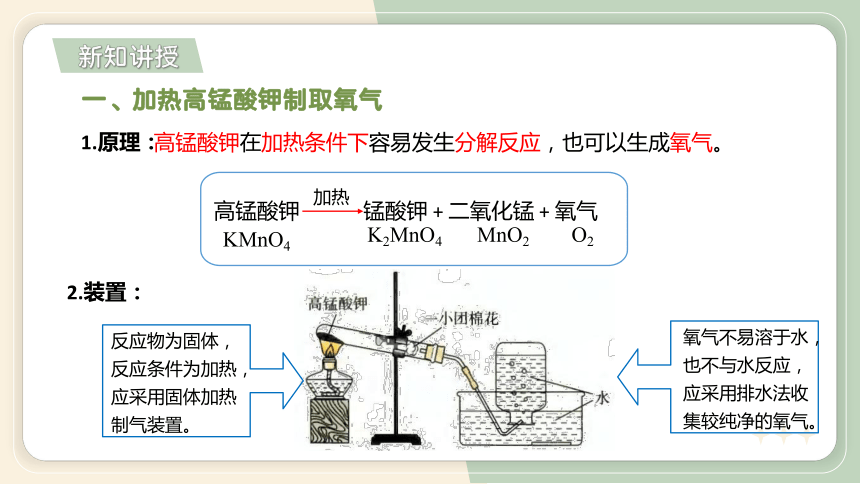
一、加热高锰酸钾制取氧气
高锰酸钾在加热条件下容易发生分解反应,也可以生成氧气。
1.原理:
高锰酸钾 锰酸钾 + 二氧化锰 + 氧气
加热
KMnO4
K2MnO4 MnO2 O2
2.装置:
反应物为固体,反应条件为加热,应采用固体加热制气装置。
氧气不易溶于水,也不与水反应,
应采用排水法收集较纯净的氧气。
实验步骤:
(1)组装并检查气密性
(2)装药品放棉花团
试管口放一团棉花
热捂法:
将导管一端放入水中,手紧握试管,若导管口有气泡冒出,则不漏气
目的:防止高锰酸钾粉末进入导管
(3)固定试管
试管口略向下倾斜。
(4)点灯加热
目的:防止冷凝水倒流使试管炸裂
先预热,再用外焰对药品部位加热
目的:防止受热不均使试管炸裂
(5)收集氧气
止:集气瓶口有较大气泡冒出
始:导管口有气泡连续均匀冒出时开始收集
否则氧气不纯,刚出气体是空气
水下盖好玻璃片取出正放
(6)移出导管
(7)熄灯
不能颠倒,防止水槽中的水被倒吸入试管,使试管炸裂
(1)查 检查装置气密性
(2)装 装药品(在试管口放一团棉)
(3)定 将装置固定在铁架台上
(4)点 点燃酒精灯(先预热、后集中加热)
(5)收 收集气体(排水法:气泡连续均匀冒出时收集)
(6)离 实验结束后先将导管撤离出水槽
(7)熄 最后熄灭酒精灯。
【步骤总结】
茶 庄 定 点 收 利 息
学以致用
实验室中,还可加热氯酸钾(KClO3)和二氧化锰的固体混合物来制取氧气。该反应中二氧化锰是催化剂。
氯酸钾 氯化钾+ 氧气
二氧化锰
加热
KClO3
KCl O2
根据氯酸钾(KClO3)分解制氧气的化学原理,设计实验装置,并说明实验操作的具体要求。
实验室制取气体,需要依据实验目的、反应原理和气体收集方法,选择反应试剂,设计实验装置(包括气体的发生装置和气体的收集装置两部分),控制反应条件,关注环境保护等。
友情提示
(氯酸钾:白色固体)
(二氧化锰:黑色固体)
1. 药品:
2. 原理:
二、加热氯酸钾和二氧化锰制取氧气
氯酸钾 氯化钾+ 氧气
二氧化锰
加热
KClO3
KCl O2
二氧化锰作催化剂
氯酸钾和
二氧化锰
高锰酸钾
没有棉花团
有棉花团
4. 步骤:
查、装、定、点、收、离、熄
(同高锰酸钾)
3. 装置:
固体加热型
观念构建
物质制备的要求
利用化学反应制备物质,应选择价廉易得的物质为原料;物质制备的装置要安全可靠,物质制备反应的条件要便于控制,生成物要易于分离和收集;物质制备过程中能源的消耗要尽可能少,要尽量避免对环境造成不利的影响。
1.高锰酸钾(KMnO4)是一种受热或见光易分解的晶体,可用于实验室制取氧气,反应原理为KMnO4 K2MnO4+MnO2+O2。下列关于高锰酸钾的说法正确的是( )
A. 高锰酸钾应保存于棕色细口瓶中
B. 高锰酸钾为紫黑色固体
C. 高锰酸钾受热不易发生分解
D. 制氧气时,高锰酸钾中的氧元素全部转化为氧气
B
加热
2.实验室用高锰酸钾制取氧气的实验中,不需要使用的一组仪器是( )
A.大试管、集气瓶
B.烧杯、玻璃棒
C.酒精灯、铁架台
D.导气管、单孔塞
B
3.常温下是一种难溶于水的气体,密度比空气略大,它能跟氧气迅速反应生成NO2,现在要收集NO气体,可采用的方法是( )
A.只有① B.只有② C.①和② D.①和③
A
4.做实验一定要注意先后顺序,如果先后顺序错误,可能会导致实验失败,甚至产生严重后果。下列有关用高锰酸钾制取氧气的实验中,先后顺序正确的是( )
A. 检查装置气密性时,先用手紧握试管的外壁,再将导管伸入水中;
B. 实验完毕,先熄灭酒精灯,再把导管移出水面;
C. 先将高锰酸钾装入试管, 再检查装置的气密性;
D. 加热时先对试管进行预热,再对准药品部位进行加热。
D
操作步骤
反应原理
查、装、定、点、收、移、熄
2.3氧气的制备
(第2课时)
加热
实验装置
固体加热制气装置
排水法或向上排空气法
高锰酸钾 锰酸钾+二氧化锰+氧气
二氧化锰
加热
氯酸钾 氯化钾+氧气
2.3 氧气的制备
课时2 高锰酸钾制氧气
1.掌握实验室用高锰酸钾制氧气的原理、装置、操作步骤及注意事项;
2.初步形成实验室制备气体的一般思路。
获取氧气还有哪些方法?
一、加热高锰酸钾制取氧气
高锰酸钾在加热条件下容易发生分解反应,也可以生成氧气。
1.原理:
高锰酸钾 锰酸钾 + 二氧化锰 + 氧气
加热
KMnO4
K2MnO4 MnO2 O2
2.装置:
反应物为固体,反应条件为加热,应采用固体加热制气装置。
氧气不易溶于水,也不与水反应,
应采用排水法收集较纯净的氧气。
实验步骤:
(1)组装并检查气密性
(2)装药品放棉花团
试管口放一团棉花
热捂法:
将导管一端放入水中,手紧握试管,若导管口有气泡冒出,则不漏气
目的:防止高锰酸钾粉末进入导管
(3)固定试管
试管口略向下倾斜。
(4)点灯加热
目的:防止冷凝水倒流使试管炸裂
先预热,再用外焰对药品部位加热
目的:防止受热不均使试管炸裂
(5)收集氧气
止:集气瓶口有较大气泡冒出
始:导管口有气泡连续均匀冒出时开始收集
否则氧气不纯,刚出气体是空气
水下盖好玻璃片取出正放
(6)移出导管
(7)熄灯
不能颠倒,防止水槽中的水被倒吸入试管,使试管炸裂
(1)查 检查装置气密性
(2)装 装药品(在试管口放一团棉)
(3)定 将装置固定在铁架台上
(4)点 点燃酒精灯(先预热、后集中加热)
(5)收 收集气体(排水法:气泡连续均匀冒出时收集)
(6)离 实验结束后先将导管撤离出水槽
(7)熄 最后熄灭酒精灯。
【步骤总结】
茶 庄 定 点 收 利 息
学以致用
实验室中,还可加热氯酸钾(KClO3)和二氧化锰的固体混合物来制取氧气。该反应中二氧化锰是催化剂。
氯酸钾 氯化钾+ 氧气
二氧化锰
加热
KClO3
KCl O2
根据氯酸钾(KClO3)分解制氧气的化学原理,设计实验装置,并说明实验操作的具体要求。
实验室制取气体,需要依据实验目的、反应原理和气体收集方法,选择反应试剂,设计实验装置(包括气体的发生装置和气体的收集装置两部分),控制反应条件,关注环境保护等。
友情提示
(氯酸钾:白色固体)
(二氧化锰:黑色固体)
1. 药品:
2. 原理:
二、加热氯酸钾和二氧化锰制取氧气
氯酸钾 氯化钾+ 氧气
二氧化锰
加热
KClO3
KCl O2
二氧化锰作催化剂
氯酸钾和
二氧化锰
高锰酸钾
没有棉花团
有棉花团
4. 步骤:
查、装、定、点、收、离、熄
(同高锰酸钾)
3. 装置:
固体加热型
观念构建
物质制备的要求
利用化学反应制备物质,应选择价廉易得的物质为原料;物质制备的装置要安全可靠,物质制备反应的条件要便于控制,生成物要易于分离和收集;物质制备过程中能源的消耗要尽可能少,要尽量避免对环境造成不利的影响。
1.高锰酸钾(KMnO4)是一种受热或见光易分解的晶体,可用于实验室制取氧气,反应原理为KMnO4 K2MnO4+MnO2+O2。下列关于高锰酸钾的说法正确的是( )
A. 高锰酸钾应保存于棕色细口瓶中
B. 高锰酸钾为紫黑色固体
C. 高锰酸钾受热不易发生分解
D. 制氧气时,高锰酸钾中的氧元素全部转化为氧气
B
加热
2.实验室用高锰酸钾制取氧气的实验中,不需要使用的一组仪器是( )
A.大试管、集气瓶
B.烧杯、玻璃棒
C.酒精灯、铁架台
D.导气管、单孔塞
B
3.常温下是一种难溶于水的气体,密度比空气略大,它能跟氧气迅速反应生成NO2,现在要收集NO气体,可采用的方法是( )
A.只有① B.只有② C.①和② D.①和③
A
4.做实验一定要注意先后顺序,如果先后顺序错误,可能会导致实验失败,甚至产生严重后果。下列有关用高锰酸钾制取氧气的实验中,先后顺序正确的是( )
A. 检查装置气密性时,先用手紧握试管的外壁,再将导管伸入水中;
B. 实验完毕,先熄灭酒精灯,再把导管移出水面;
C. 先将高锰酸钾装入试管, 再检查装置的气密性;
D. 加热时先对试管进行预热,再对准药品部位进行加热。
D
操作步骤
反应原理
查、装、定、点、收、移、熄
2.3氧气的制备
(第2课时)
加热
实验装置
固体加热制气装置
排水法或向上排空气法
高锰酸钾 锰酸钾+二氧化锰+氧气
二氧化锰
加热
氯酸钾 氯化钾+氧气
同课章节目录
