3.1 课时4 离子课件(共18张PPT内嵌视频) 2025-2026学年化学沪教版(2024)九年级上册
文档属性
| 名称 | 3.1 课时4 离子课件(共18张PPT内嵌视频) 2025-2026学年化学沪教版(2024)九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 37.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-08-28 00:00:00 | ||
图片预览



文档简介
(共18张PPT)
3.1 构成物质的微观粒子
课时4 离子
1.知道离子的形成过程及表示方法;
2.能用比较等方法说明分子、原子、离子的区别与联系。
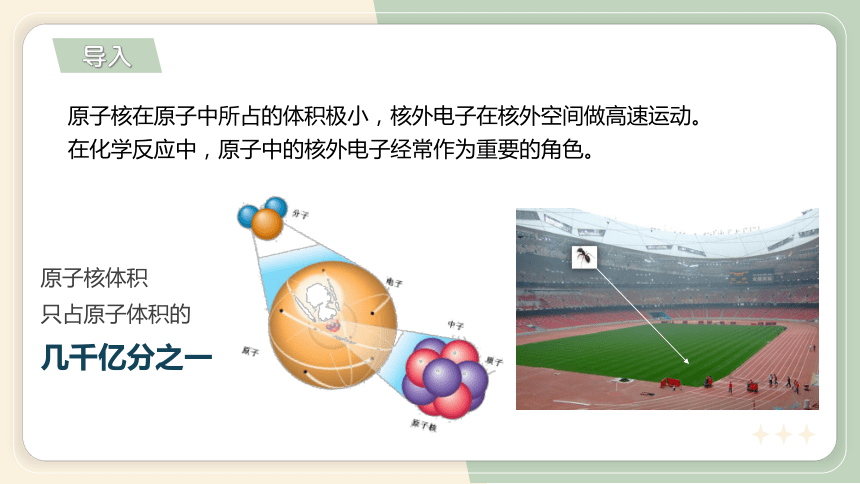
原子核体积
只占原子体积的
几千亿分之一
原子核在原子中所占的体积极小,核外电子在核外空间做高速运动。
在化学反应中,原子中的核外电子经常作为重要的角色。
实验探究
以下实验是金属钠与氯气的反应,观察实验,说说有哪些现象?你能得出什么结论?
钠在氯气中剧烈反应,产生黄色火焰,生成白色固体。
钠 + 氯气 氯化钠
点燃
Na Cl2 NaCl
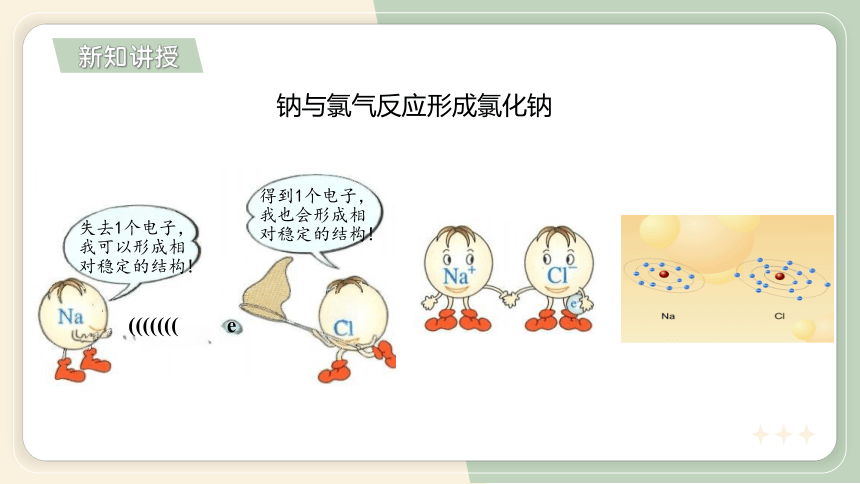
失去1个电子,
我可以形成相
对稳定的结构!
得到1个电子, 我也会形成相对稳定的结构!
((((((( e
钠与氯气反应形成氯化钠
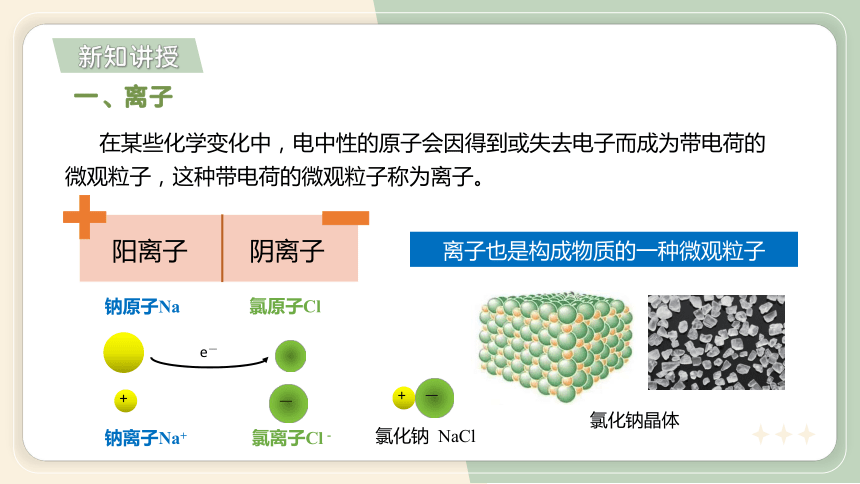
一、离子
在某些化学变化中,电中性的原子会因得到或失去电子而成为带电荷的微观粒子,这种带电荷的微观粒子称为离子。
钠原子Na
阳离子
阴离子
氯原子Cl
e-
钠离子Na+
+
-
氯离子Cl-
+
-
氯化钠 NaCl
氯化钠晶体
离子也是构成物质的一种微观粒子
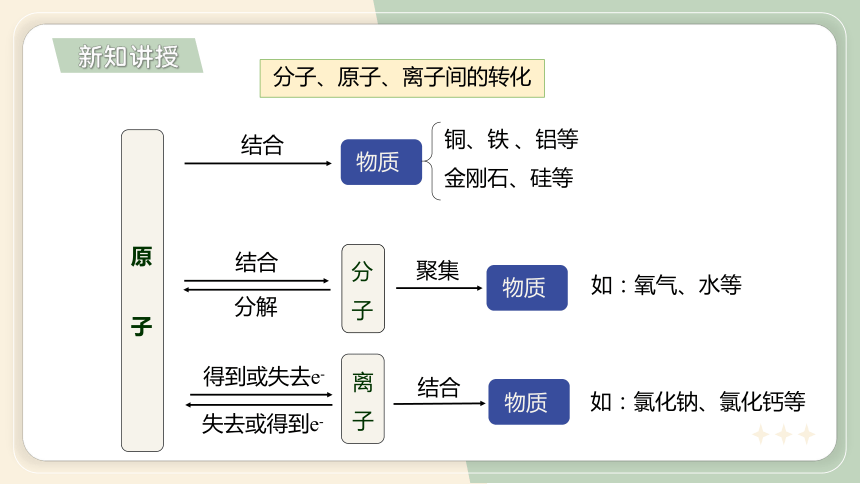
原 子
铜、铁 、铝等
金刚石、硅等
如:氧气、水等
如:氯化钠、氯化钙等
结合
结合
分解
聚集
结合
离
子
得到或失去e-
物质
分
子
失去或得到e-
物质
物质
分子、原子、离子间的转化
拓展视野
电子层
原子核
原子并不是一个实心的球体,原子核位于原子的中心,体积很小,原子核外有很大的空间,电子围绕原子核在这个空间里作高速运动。
原子核外电子的排布
氢原子的结构
(1个电子)
电子在原子核外一定区域内出现,这些区域叫做“电子层”,核外电子是在不同的电子层内运动的,此现象叫做核外电子的分层排布。
1.电子层的定义
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
+
+
+
+
+
原子核
第一层
第二层
第三层
2. 核外电子的能量规律
电子层数 一、二、三、四、五、六、七
离核远近
能量高低
近 远
低 高
氯 原 子
由内到外分层排布
第一层最多只容纳2个电子
第二层最多只容纳8个电子
最外层电子数不超过8个(只有一层的,电子数不超过2个)
氧
镁
氯
钠
2、8、8规律
3.核外电子的排布规律
第n层最多只容纳2n2个电子
4.原子结构示意图
+11
2 8 1
原子核
核内质子数
第一层
第二层
第三层
各层的电子数
钠原子结构示意图
5.氯化钠的形成
+11
2 8 1
+17
7 8 2
钠 Na
氯 Cl
e-
+11
2 8
钠离子 Na+
+17
8 8 2
氯离子 Cl-
Na+
Cl-
钠原子的最外层有1个电子,氯原子的最外层有7个电子,当钠与氯气反应时,钠原子最外层的 1 个电子转移到氯原子的最外层上,这样两者都形成相对稳定的结构
钠原子因失去 1 个电子而带上 1 个单位的正电荷
氯原子因得到 1 个电子而带上 1 个单位的负电荷
带相反电荷的Na+ 与Cl- 相互作用就形成了NaCl(氯化钠)
1.物质由微观粒子构成。下列由离子构成的物质是( )
A.干冰
B.金刚石
C.氯化钠
D.氨气
C
2.如图为金属钠与氯气反应生成氯化钠的示意图,下列说法错误的是( )
A .每个氯离子带一个单位负电荷
B .钠原子在该反应中形成了阴离子
C .氯化钠是由钠离子和氯离子构成的
D .钠离子和氯离子的结构都相对稳定
B
.
3.下列有关原子、分子、离子的说法正确的是( )
A. 分子可以再分,原子不能再分
B. 原子通过得失电子变成离子,但离子不能变成原子
C. 原子、离子、分子都是构成物质的微粒
D. 原子的质量主要集中在质子和电子上
C
4.早晨,在公园里可以看到人们运动的身影。公园里含有丰富的负氧离子(O2﹣),负氧离子是氧分子得到电子形成的。一个负氧离子与一个氧分子相比较,不相同的是( )
A.含氧原子个数 B.质子总数
C.电子总数 D .相对分子质量之和
C
3.1 构成物质的微观粒子
(第4课时)
离子
分子、原子、离子间的转化
原子失去电子变为阳离子
原子得到电子变为阴离子
3.1 构成物质的微观粒子
课时4 离子
1.知道离子的形成过程及表示方法;
2.能用比较等方法说明分子、原子、离子的区别与联系。
原子核体积
只占原子体积的
几千亿分之一
原子核在原子中所占的体积极小,核外电子在核外空间做高速运动。
在化学反应中,原子中的核外电子经常作为重要的角色。
实验探究
以下实验是金属钠与氯气的反应,观察实验,说说有哪些现象?你能得出什么结论?
钠在氯气中剧烈反应,产生黄色火焰,生成白色固体。
钠 + 氯气 氯化钠
点燃
Na Cl2 NaCl
失去1个电子,
我可以形成相
对稳定的结构!
得到1个电子, 我也会形成相对稳定的结构!
((((((( e
钠与氯气反应形成氯化钠
一、离子
在某些化学变化中,电中性的原子会因得到或失去电子而成为带电荷的微观粒子,这种带电荷的微观粒子称为离子。
钠原子Na
阳离子
阴离子
氯原子Cl
e-
钠离子Na+
+
-
氯离子Cl-
+
-
氯化钠 NaCl
氯化钠晶体
离子也是构成物质的一种微观粒子
原 子
铜、铁 、铝等
金刚石、硅等
如:氧气、水等
如:氯化钠、氯化钙等
结合
结合
分解
聚集
结合
离
子
得到或失去e-
物质
分
子
失去或得到e-
物质
物质
分子、原子、离子间的转化
拓展视野
电子层
原子核
原子并不是一个实心的球体,原子核位于原子的中心,体积很小,原子核外有很大的空间,电子围绕原子核在这个空间里作高速运动。
原子核外电子的排布
氢原子的结构
(1个电子)
电子在原子核外一定区域内出现,这些区域叫做“电子层”,核外电子是在不同的电子层内运动的,此现象叫做核外电子的分层排布。
1.电子层的定义
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
﹣
+
+
+
+
+
原子核
第一层
第二层
第三层
2. 核外电子的能量规律
电子层数 一、二、三、四、五、六、七
离核远近
能量高低
近 远
低 高
氯 原 子
由内到外分层排布
第一层最多只容纳2个电子
第二层最多只容纳8个电子
最外层电子数不超过8个(只有一层的,电子数不超过2个)
氧
镁
氯
钠
2、8、8规律
3.核外电子的排布规律
第n层最多只容纳2n2个电子
4.原子结构示意图
+11
2 8 1
原子核
核内质子数
第一层
第二层
第三层
各层的电子数
钠原子结构示意图
5.氯化钠的形成
+11
2 8 1
+17
7 8 2
钠 Na
氯 Cl
e-
+11
2 8
钠离子 Na+
+17
8 8 2
氯离子 Cl-
Na+
Cl-
钠原子的最外层有1个电子,氯原子的最外层有7个电子,当钠与氯气反应时,钠原子最外层的 1 个电子转移到氯原子的最外层上,这样两者都形成相对稳定的结构
钠原子因失去 1 个电子而带上 1 个单位的正电荷
氯原子因得到 1 个电子而带上 1 个单位的负电荷
带相反电荷的Na+ 与Cl- 相互作用就形成了NaCl(氯化钠)
1.物质由微观粒子构成。下列由离子构成的物质是( )
A.干冰
B.金刚石
C.氯化钠
D.氨气
C
2.如图为金属钠与氯气反应生成氯化钠的示意图,下列说法错误的是( )
A .每个氯离子带一个单位负电荷
B .钠原子在该反应中形成了阴离子
C .氯化钠是由钠离子和氯离子构成的
D .钠离子和氯离子的结构都相对稳定
B
.
3.下列有关原子、分子、离子的说法正确的是( )
A. 分子可以再分,原子不能再分
B. 原子通过得失电子变成离子,但离子不能变成原子
C. 原子、离子、分子都是构成物质的微粒
D. 原子的质量主要集中在质子和电子上
C
4.早晨,在公园里可以看到人们运动的身影。公园里含有丰富的负氧离子(O2﹣),负氧离子是氧分子得到电子形成的。一个负氧离子与一个氧分子相比较,不相同的是( )
A.含氧原子个数 B.质子总数
C.电子总数 D .相对分子质量之和
C
3.1 构成物质的微观粒子
(第4课时)
离子
分子、原子、离子间的转化
原子失去电子变为阳离子
原子得到电子变为阴离子
同课章节目录
