苏教版化学选修二2.4《镁和铝的冶炼》课件 (共30张PPT)
文档属性
| 名称 | 苏教版化学选修二2.4《镁和铝的冶炼》课件 (共30张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 403.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-08-18 00:00:00 | ||
图片预览










文档简介
课件30张PPT。第四单元 镁和铝的冶炼 1.为什么不用电解AlCl3(熔融)制备Al?
提示 AlCl3是共价化合物,熔融态不导电,无法电解得到
Al。
2.Al3+、Mg2+均易发生水解,其离子方程式?
1.了解如何根据元素在自然界的存在状态和性质来开发、利用自然资源。
2.了解从海水中提取氯化镁、从铝土矿中提取氧化铝的方法,以及获得金属镁、铝的基本原理。
3.通过学习活动提高学习能力、交流合作能力和分析、解决实际问题的能力。石灰 石灰乳 氢氧化镁
1. 制备纯度较高的氧化铝
(1)铝元素的含量占地壳中元素总量的7.45%,是地壳中含量最 的金属元素。铝在地壳中主要以 的形式存在。要从铝土矿中提取铝,首先必须制备纯度较高的 。多铝土矿氧化铝(2)原料: 。
(3)制备过程:先要除去铝土矿中的 、 等杂质。在工业上可以使用 来处理铝土矿得到偏铝酸钠溶液,在得到的偏铝酸钠溶液中通入 ,析出 ,加热分解 ,就得到纯度较高的 。主要方程式有:
氧化铁二氧化硅二氧化碳氢氧化铝沉淀氢氧化铝氧化铝浓氢氧化钠溶液铝土矿较强 电解熔融氧化铝 熔点 冰晶石 将MgCl2·6H2O中的结晶水失去,在加热时需注意什么?
提示 由于Mg2+水解得到Mg(OH)2故加热MgCl2·6H2O时需在HCl(g)气氛中防止Mg2+水解。
电解熔融态的Al2O3制备Al时,将Al2O3熔化需较高能量,为了使Al2O3在相对较低的温度下熔化需加什么物质?作用是什么?
提示 冰晶石(Na3AlF6)、降低Al2O3的熔化温度。
电解MgCl2和Al2O3时,阳极材料能否为活泼电极?为什么?
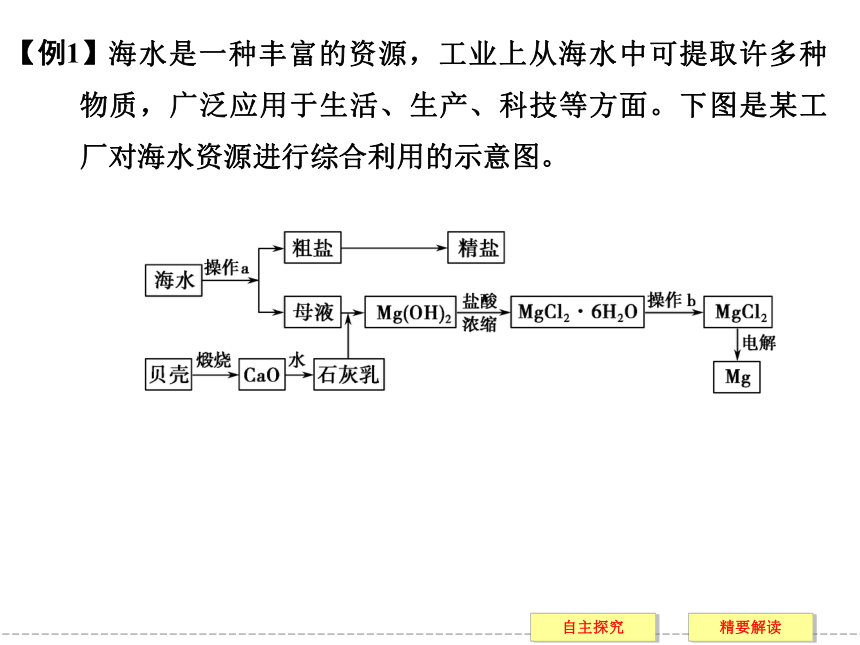
提示 需用惰性电极,否则阳极本身发生氧化反应。【慎思1】【慎思2】【慎思3】 海水是一种丰富的资源,工业上从海水中可提取许多种物质,广泛应用于生活、生产、科技等方面。下图是某工厂对海水资源进行综合利用的示意图。【例1】回答下列问题:
(1)流程图中操作a的名称为________。
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱。
①气体A、B是CO2或NH3,则气体A应是________(填化学式)。
②滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却析出不含有NaHCO3的副产品NH4Cl晶体,则通入NH3的作用是________。(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是_________________________________________________。
②操作b是在________氛围中进行,若在空气中加热,则会生成Mg(OH)Cl,写出有关反应的化学方程式:___________。答案 C
阴极(和电源负极相连):4Al3++12e-===4Al
阳极(和电源正极相连):6O2--12e-===3O2↑
在高温下,阳极产生的氧气会跟碳电极发生反应,生成二氧化碳,所以在电解中要定时补充碳块。铝的熔点是660 ℃,电冶铝反应的温度是1 000 ℃左右。所以电解生成的铝呈液态,从电解装置的底部流出。2.电解过程: 铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业上冶炼铝的化学方程式是________________。
(2)铝与氢氧化钾溶液反应的离子方程式是___________。
(3)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。【例2】①该电解槽的阳极反应式是_______________。
②通电开始后,阴极附近溶液pH会增大,请简述原因
________________________________________________。
③除去杂质后的氢氧化钾溶液从液体出口________(填写“A”或“B”)导出。
解析 (1)金属铝的冶炼是电解熔融Al2O3。(2)铝与强碱反应放出氢气生成偏铝酸盐。(3)结合题中给出的信息提示进行解题。①溶液中存在阴离子为OH-和含氧酸根,应是OH-先放电。②溶液中存在的阳离子为K+和H+,应是H+先放电。在阴极由于H+放电,H+不断减少,水的电离平衡向正反应方向移动,OH-浓度增大,pH增大。③K+可通过阳离子交换膜流向B口,B口的OH-不断增多,但无法通过阳离子交换膜,故氢氧化钾溶液从B口导出。 从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为________。
_________。
【体验2】(3)验证滤液B含Fe3+,可取少量滤液并加入________(填试剂名称)。
(4)滤液E、K中溶质的主要成分是________(填化学式),写出该溶质的一种用途_______________________。
(5)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12。取适量的滤液B,加入一定量的烧碱至达到沉淀溶液平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=________。
解析 本题考查的基本原理:利用氧化铝的两性进行氧化铝的分离与提纯。(4)由于CO2过量与碱反应时均产生碳酸氢盐;(5)根据溶度积Ksp=c(Mg2+)·c2(OH-),又根据pH=13.00,即c(OH-)=0.1 mol·L-1代入易得。
提示 AlCl3是共价化合物,熔融态不导电,无法电解得到
Al。
2.Al3+、Mg2+均易发生水解,其离子方程式?
1.了解如何根据元素在自然界的存在状态和性质来开发、利用自然资源。
2.了解从海水中提取氯化镁、从铝土矿中提取氧化铝的方法,以及获得金属镁、铝的基本原理。
3.通过学习活动提高学习能力、交流合作能力和分析、解决实际问题的能力。石灰 石灰乳 氢氧化镁
1. 制备纯度较高的氧化铝
(1)铝元素的含量占地壳中元素总量的7.45%,是地壳中含量最 的金属元素。铝在地壳中主要以 的形式存在。要从铝土矿中提取铝,首先必须制备纯度较高的 。多铝土矿氧化铝(2)原料: 。
(3)制备过程:先要除去铝土矿中的 、 等杂质。在工业上可以使用 来处理铝土矿得到偏铝酸钠溶液,在得到的偏铝酸钠溶液中通入 ,析出 ,加热分解 ,就得到纯度较高的 。主要方程式有:
氧化铁二氧化硅二氧化碳氢氧化铝沉淀氢氧化铝氧化铝浓氢氧化钠溶液铝土矿较强 电解熔融氧化铝 熔点 冰晶石 将MgCl2·6H2O中的结晶水失去,在加热时需注意什么?
提示 由于Mg2+水解得到Mg(OH)2故加热MgCl2·6H2O时需在HCl(g)气氛中防止Mg2+水解。
电解熔融态的Al2O3制备Al时,将Al2O3熔化需较高能量,为了使Al2O3在相对较低的温度下熔化需加什么物质?作用是什么?
提示 冰晶石(Na3AlF6)、降低Al2O3的熔化温度。
电解MgCl2和Al2O3时,阳极材料能否为活泼电极?为什么?
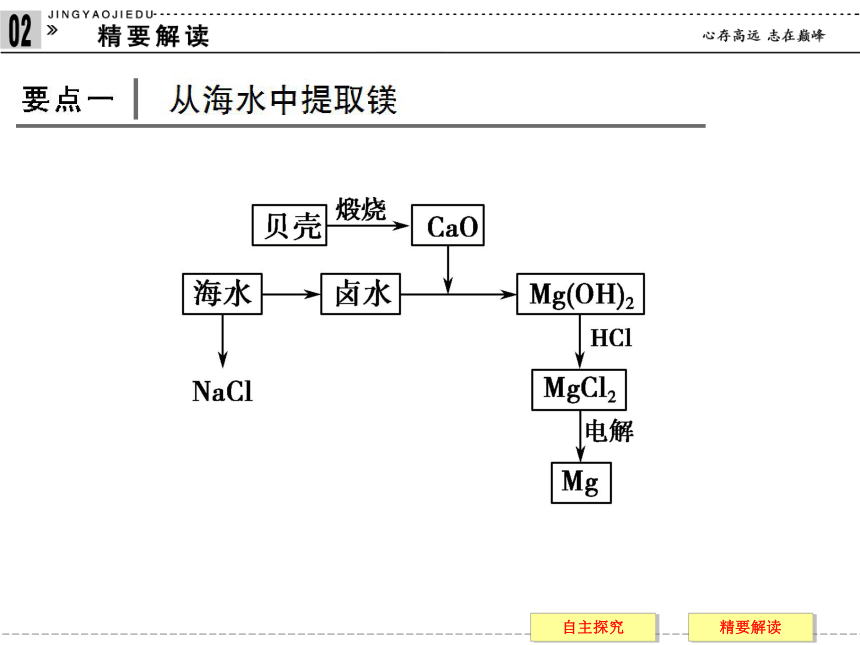
提示 需用惰性电极,否则阳极本身发生氧化反应。【慎思1】【慎思2】【慎思3】 海水是一种丰富的资源,工业上从海水中可提取许多种物质,广泛应用于生活、生产、科技等方面。下图是某工厂对海水资源进行综合利用的示意图。【例1】回答下列问题:
(1)流程图中操作a的名称为________。
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱。
①气体A、B是CO2或NH3,则气体A应是________(填化学式)。
②滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却析出不含有NaHCO3的副产品NH4Cl晶体,则通入NH3的作用是________。(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是_________________________________________________。
②操作b是在________氛围中进行,若在空气中加热,则会生成Mg(OH)Cl,写出有关反应的化学方程式:___________。答案 C
阴极(和电源负极相连):4Al3++12e-===4Al
阳极(和电源正极相连):6O2--12e-===3O2↑
在高温下,阳极产生的氧气会跟碳电极发生反应,生成二氧化碳,所以在电解中要定时补充碳块。铝的熔点是660 ℃,电冶铝反应的温度是1 000 ℃左右。所以电解生成的铝呈液态,从电解装置的底部流出。2.电解过程: 铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业上冶炼铝的化学方程式是________________。
(2)铝与氢氧化钾溶液反应的离子方程式是___________。
(3)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。【例2】①该电解槽的阳极反应式是_______________。
②通电开始后,阴极附近溶液pH会增大,请简述原因
________________________________________________。
③除去杂质后的氢氧化钾溶液从液体出口________(填写“A”或“B”)导出。
解析 (1)金属铝的冶炼是电解熔融Al2O3。(2)铝与强碱反应放出氢气生成偏铝酸盐。(3)结合题中给出的信息提示进行解题。①溶液中存在阴离子为OH-和含氧酸根,应是OH-先放电。②溶液中存在的阳离子为K+和H+,应是H+先放电。在阴极由于H+放电,H+不断减少,水的电离平衡向正反应方向移动,OH-浓度增大,pH增大。③K+可通过阳离子交换膜流向B口,B口的OH-不断增多,但无法通过阳离子交换膜,故氢氧化钾溶液从B口导出。 从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为________。
_________。
【体验2】(3)验证滤液B含Fe3+,可取少量滤液并加入________(填试剂名称)。
(4)滤液E、K中溶质的主要成分是________(填化学式),写出该溶质的一种用途_______________________。
(5)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12。取适量的滤液B,加入一定量的烧碱至达到沉淀溶液平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=________。
解析 本题考查的基本原理:利用氧化铝的两性进行氧化铝的分离与提纯。(4)由于CO2过量与碱反应时均产生碳酸氢盐;(5)根据溶度积Ksp=c(Mg2+)·c2(OH-),又根据pH=13.00,即c(OH-)=0.1 mol·L-1代入易得。
同课章节目录
- 专题一 多样化的水处理技术
- 第一单元 水的净化与污水处理
- 第二单元 硬水软化
- 第三单元 海水淡化
- 专题二 从自然资源到化学品
- 第一单元 氨的合成
- 第二单元 氯碱生产
- 第三单元 硫酸工业
- 第四单元 镁和铝的冶炼
- 专题三 让有机反应为人类造福
- 第一单元 有机药物制备
- 第二单元 合成洗涤济的生产
- 第三单元 纤维素的化学加工
- 第四单元 有机高分子合成
- 专题四 材料加工与性能优化
- 第一单元 材料的加工处理
- 第二单元 材料组成的优化
- 第三单元 复合材料的制造
- 专题五 为现代农业技术添翼
- 第一单元 土壤酸碱性的改良
- 第二单元 化肥的生产与合理使用
- 第三单元 无土栽培技术
- 第四单元 化学农药的发展
- 专题六 从污染防治到绿色化学
- 第一单元 环境污染的化学防治
- 第二单元 绿色化学与可持续发展
