高中化学人教必修一 4.1 无机非金属材料的主角---硅 课件 (共31张PPT)
文档属性
| 名称 | 高中化学人教必修一 4.1 无机非金属材料的主角---硅 课件 (共31张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-08-21 00:00:00 | ||
图片预览










文档简介
课件31张PPT。第四章 非金属及其化合物 第一节
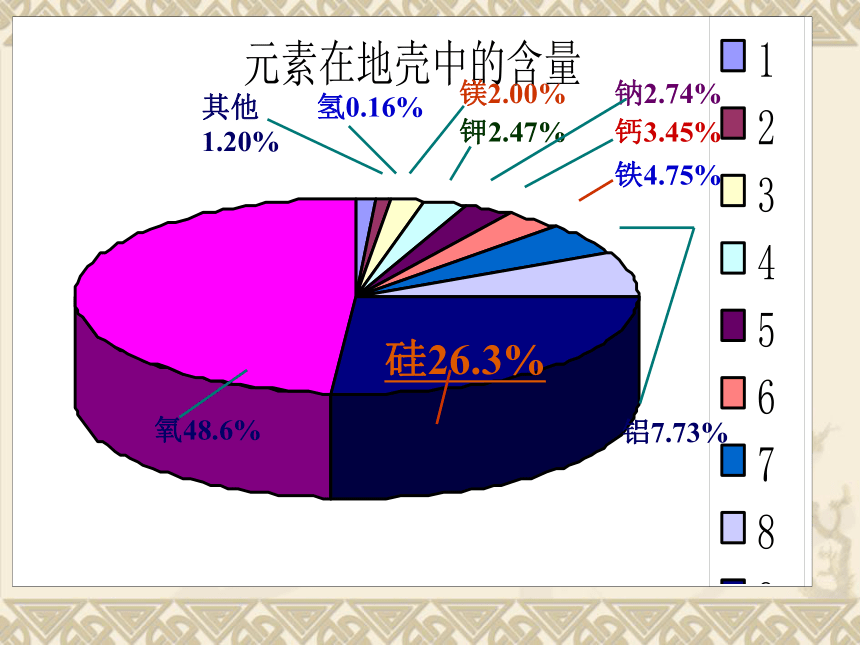
无机非金属材料的主角——硅氧48.6%硅26.3%铝7.73%铁4.75%钙3.45%钠2.74%钾2.47%镁2.00%氢0.16%其他1.20%硅的存在与分布:硅在地壳中含量第二,硅的氧化物及
硅酸盐约占地壳质量的90%以上。没有游离态,只有化合态(因为它是亲氧元素);自然界中分布广泛,是构成矿物和岩石的基本元素。天然水晶天然玛瑙天
然
的
SiO2
硅
石一、二氧化硅( SiO2 )1、存在 2、二氧化硅的用途:石英制品现代通信用光缆光学纤维胃镜用光导纤维做
无开刀手术光导纤维手术头灯二氧化硅的重要用途:光导纤维材料P76思考与交流物理性质:熔点高,硬度大,不溶于水。根据SiO2的存在和应用。分析:①SiO2有哪些物理性质?②化学稳定性如何?化学稳定性良好,不活泼。想一想: SiO2属于酸性氧化物,推测它的化学性质。酸性氧化物 + 水 = 酸
酸性氧化物 + 碱 = 盐 + 水
酸性氧化物 + 碱性氧化物 = 盐 3、二氧化硅的化学性质(1)酸性氧化物的性质(如同CO2)①与强碱反应生成盐和水 SiO2 + 2NaOH =Na2SiO3 +H2O②与碱性氧化物反应生成盐(有粘性)(1)酸性氧化物的性质(如同CO2)硅酸钠实验室盛装NaOH溶液的试剂瓶为什么用橡胶塞而不用玻璃塞? NaOH溶液能与玻璃中的SiO2反应生成Na2SiO3,使瓶塞部分粘结而无法打开。因此盛装NaOH溶液的试剂瓶不能用玻璃塞而要用橡胶塞。想一想2、特性:只能与酸中的氢氟酸HF反应SiO2 + 4HF = SiF4↑+2H2O此反应常用于雕刻玻璃1、SiO2既可与碱反应,也能与氢氟酸反应, SiO2是不是两性氧化物 ? 想一想2、实验室为什么不用玻璃瓶盛装氢氟酸?HF能腐蚀玻璃,因此,盛装氢氟酸不能用玻璃试剂瓶而要用塑料瓶。我们知道:CO2+H2O=H2CO3
但是SiO2不能与水直接化合成H2SiO3 ,那怎样制备H2SiO3呢? 二、 硅酸(H2SiO3)想一想【实验4-1】在试管中加入3-5ml Na2SiO3液,
滴入1-2酚酞,再逐滴加入稀盐酸,边滴
边振荡,直至溶液红色消失,静置,观察现象。滴入酚酞后溶液变为红色;再滴入稀盐酸,溶液红色变浅至无色,同时有白色胶状沉淀产生。 Na2SiO3溶液呈碱性;硅酸不溶于水;
形成硅酸凝胶。Na2SiO3 + 2HCl == 2NaCl + H2SiO3SiO32- + 2H+ == H2SiO3离子方程式:动手写:P77表格。练一练已知酸性强弱: H2SiO3 ﹤ H2CO3依据“强酸可以制取弱酸”,写出
少量CO2的通入Na2SiO3溶液的反应
的化学方程式。CO2 + H2O + Na2SiO3 = H2SiO3 + Na2CO3比较强的酸盐比较弱的新酸新盐三、硅酸盐结构复杂,一般不溶于水。2.硅酸钠(Na2SiO3), 其水溶液俗称水玻璃,是制备硅胶和木材防火剂等的原料。1.是由硅、氧和金属组成的化合物的总称。3.硅酸盐的化学性质
(1)有很强的热稳定性,能耐高温。
(2)硅酸盐易于酸反应
Na2SiO3 + H2O + CO2 == Na2CO3 + H2SiO3↓ Na2SiO3 + 2HCl == 2NaCl + H2SiO3 ↓当水分蒸发后燃烧当水分蒸发后不易燃烧用水玻璃浸泡过的木材或织物可防火制备木材防火剂的原料【实验4-2 】硅酸钠的耐热性实验。取两张滤纸,分别
放入蒸馏水和Na2SiO3的饱和溶液,使之充分吸湿、
浸透,取出沥干后,同时放在酒精灯外焰。放入蒸馏水放入Na2SiO3饱和溶液结论现象4、硅酸盐组成表示顺序:
活泼金属氧化物·较活泼金属氧化物· SiO2 · H2O方法:保持原有各元素化合价不变,按下列顺序写出各种元素的氧化物,用分隔号隔开。如:硅酸钠(Na2SiO3)Na2O ·SiO2 镁橄榄石(Mg2SiO4)2MgO ·SiO2钙沸石 Ca(Al2Si3O10) ·3H2OCaO ·Al2O3 ·3SiO2·3H2O陶瓷:原料——黏土
玻璃:原料——纯碱、石灰石和石英;
水泥:原料——黏土和石灰石;
加适量石膏;5.用途:重要的无机非金属材料陶瓷日用器皿、建筑饰材、卫生洁具玻璃普通玻璃: 以纯碱 、石灰石和石英 为原料,经混合、粉碎,在玻璃窑中熔融制得。 (Na2CO3)(SiO2 )以黏土和石灰石为主要原料具有特殊功能的含硅物质1.碳化硅(SiC俗称金刚砂),具有金刚石的结构。硬度很大,用作砂纸、砂轮的磨料。2. 硅 钢
高导磁性
用作变压器铁芯
4.分子筛 吸附剂、催化剂 具有均匀微孔结构的铝硅酸盐3.硅橡胶
良好的弹性
新型无机非金属材料:新型陶瓷高温结构陶瓷、压电陶瓷透明陶瓷、超导陶瓷等科学视野生物陶瓷人造骨
1.物理性质:
(1)存在:硅有晶体硅和无定形硅两种
(自然界中没有游离态的硅)。
(2)有金属光泽的灰黑色固体,结构类似
于金刚石,熔点(1410℃)和沸点都很高,
硬度大。
(3)导电性介于导体和绝缘体之间,可以
做半导体材料。
四、硅单质2、化学性质------不活泼
(1)常温下,不能与强酸、强氧化性酸反应,只能与
氟气、氢氟酸和烧碱等物质反应。Si+2F2==SiF4 Si+4HF==SiF4 +2H2Si+2NaOH+H2O==Na2SiO3+2H2(2)加热条件下,能跟一些非金属单质起反应Si+O2==SiO2 Si+2H2==SiH4高温3、制法SiO2 + 2C === Si + 2CO↑(制取粗硅)高温5.用途晶体硅的导电性介于导体和半导体之间,是良好的半导体材料,硅是信息技术的关键材料硅太阳能电池电脑的中央处理器(CPU)
无机非金属材料的主角——硅氧48.6%硅26.3%铝7.73%铁4.75%钙3.45%钠2.74%钾2.47%镁2.00%氢0.16%其他1.20%硅的存在与分布:硅在地壳中含量第二,硅的氧化物及
硅酸盐约占地壳质量的90%以上。没有游离态,只有化合态(因为它是亲氧元素);自然界中分布广泛,是构成矿物和岩石的基本元素。天然水晶天然玛瑙天
然
的
SiO2
硅
石一、二氧化硅( SiO2 )1、存在 2、二氧化硅的用途:石英制品现代通信用光缆光学纤维胃镜用光导纤维做
无开刀手术光导纤维手术头灯二氧化硅的重要用途:光导纤维材料P76思考与交流物理性质:熔点高,硬度大,不溶于水。根据SiO2的存在和应用。分析:①SiO2有哪些物理性质?②化学稳定性如何?化学稳定性良好,不活泼。想一想: SiO2属于酸性氧化物,推测它的化学性质。酸性氧化物 + 水 = 酸
酸性氧化物 + 碱 = 盐 + 水
酸性氧化物 + 碱性氧化物 = 盐 3、二氧化硅的化学性质(1)酸性氧化物的性质(如同CO2)①与强碱反应生成盐和水 SiO2 + 2NaOH =Na2SiO3 +H2O②与碱性氧化物反应生成盐(有粘性)(1)酸性氧化物的性质(如同CO2)硅酸钠实验室盛装NaOH溶液的试剂瓶为什么用橡胶塞而不用玻璃塞? NaOH溶液能与玻璃中的SiO2反应生成Na2SiO3,使瓶塞部分粘结而无法打开。因此盛装NaOH溶液的试剂瓶不能用玻璃塞而要用橡胶塞。想一想2、特性:只能与酸中的氢氟酸HF反应SiO2 + 4HF = SiF4↑+2H2O此反应常用于雕刻玻璃1、SiO2既可与碱反应,也能与氢氟酸反应, SiO2是不是两性氧化物 ? 想一想2、实验室为什么不用玻璃瓶盛装氢氟酸?HF能腐蚀玻璃,因此,盛装氢氟酸不能用玻璃试剂瓶而要用塑料瓶。我们知道:CO2+H2O=H2CO3
但是SiO2不能与水直接化合成H2SiO3 ,那怎样制备H2SiO3呢? 二、 硅酸(H2SiO3)想一想【实验4-1】在试管中加入3-5ml Na2SiO3液,
滴入1-2酚酞,再逐滴加入稀盐酸,边滴
边振荡,直至溶液红色消失,静置,观察现象。滴入酚酞后溶液变为红色;再滴入稀盐酸,溶液红色变浅至无色,同时有白色胶状沉淀产生。 Na2SiO3溶液呈碱性;硅酸不溶于水;
形成硅酸凝胶。Na2SiO3 + 2HCl == 2NaCl + H2SiO3SiO32- + 2H+ == H2SiO3离子方程式:动手写:P77表格。练一练已知酸性强弱: H2SiO3 ﹤ H2CO3依据“强酸可以制取弱酸”,写出
少量CO2的通入Na2SiO3溶液的反应
的化学方程式。CO2 + H2O + Na2SiO3 = H2SiO3 + Na2CO3比较强的酸盐比较弱的新酸新盐三、硅酸盐结构复杂,一般不溶于水。2.硅酸钠(Na2SiO3), 其水溶液俗称水玻璃,是制备硅胶和木材防火剂等的原料。1.是由硅、氧和金属组成的化合物的总称。3.硅酸盐的化学性质
(1)有很强的热稳定性,能耐高温。
(2)硅酸盐易于酸反应
Na2SiO3 + H2O + CO2 == Na2CO3 + H2SiO3↓ Na2SiO3 + 2HCl == 2NaCl + H2SiO3 ↓当水分蒸发后燃烧当水分蒸发后不易燃烧用水玻璃浸泡过的木材或织物可防火制备木材防火剂的原料【实验4-2 】硅酸钠的耐热性实验。取两张滤纸,分别
放入蒸馏水和Na2SiO3的饱和溶液,使之充分吸湿、
浸透,取出沥干后,同时放在酒精灯外焰。放入蒸馏水放入Na2SiO3饱和溶液结论现象4、硅酸盐组成表示顺序:
活泼金属氧化物·较活泼金属氧化物· SiO2 · H2O方法:保持原有各元素化合价不变,按下列顺序写出各种元素的氧化物,用分隔号隔开。如:硅酸钠(Na2SiO3)Na2O ·SiO2 镁橄榄石(Mg2SiO4)2MgO ·SiO2钙沸石 Ca(Al2Si3O10) ·3H2OCaO ·Al2O3 ·3SiO2·3H2O陶瓷:原料——黏土
玻璃:原料——纯碱、石灰石和石英;
水泥:原料——黏土和石灰石;
加适量石膏;5.用途:重要的无机非金属材料陶瓷日用器皿、建筑饰材、卫生洁具玻璃普通玻璃: 以纯碱 、石灰石和石英 为原料,经混合、粉碎,在玻璃窑中熔融制得。 (Na2CO3)(SiO2 )以黏土和石灰石为主要原料具有特殊功能的含硅物质1.碳化硅(SiC俗称金刚砂),具有金刚石的结构。硬度很大,用作砂纸、砂轮的磨料。2. 硅 钢
高导磁性
用作变压器铁芯
4.分子筛 吸附剂、催化剂 具有均匀微孔结构的铝硅酸盐3.硅橡胶
良好的弹性
新型无机非金属材料:新型陶瓷高温结构陶瓷、压电陶瓷透明陶瓷、超导陶瓷等科学视野生物陶瓷人造骨
1.物理性质:
(1)存在:硅有晶体硅和无定形硅两种
(自然界中没有游离态的硅)。
(2)有金属光泽的灰黑色固体,结构类似
于金刚石,熔点(1410℃)和沸点都很高,
硬度大。
(3)导电性介于导体和绝缘体之间,可以
做半导体材料。
四、硅单质2、化学性质------不活泼
(1)常温下,不能与强酸、强氧化性酸反应,只能与
氟气、氢氟酸和烧碱等物质反应。Si+2F2==SiF4 Si+4HF==SiF4 +2H2Si+2NaOH+H2O==Na2SiO3+2H2(2)加热条件下,能跟一些非金属单质起反应Si+O2==SiO2 Si+2H2==SiH4高温3、制法SiO2 + 2C === Si + 2CO↑(制取粗硅)高温5.用途晶体硅的导电性介于导体和半导体之间,是良好的半导体材料,硅是信息技术的关键材料硅太阳能电池电脑的中央处理器(CPU)
