人教版化学九下第十单元10.2-酸和碱的中和反应-习题和答案
文档属性
| 名称 | 人教版化学九下第十单元10.2-酸和碱的中和反应-习题和答案 |
|
|
| 格式 | zip | ||
| 文件大小 | 90.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-08-21 00:00:00 | ||
图片预览

文档简介
第十单元
课题2
酸和碱的中和反应
测试题
一、选择
1.
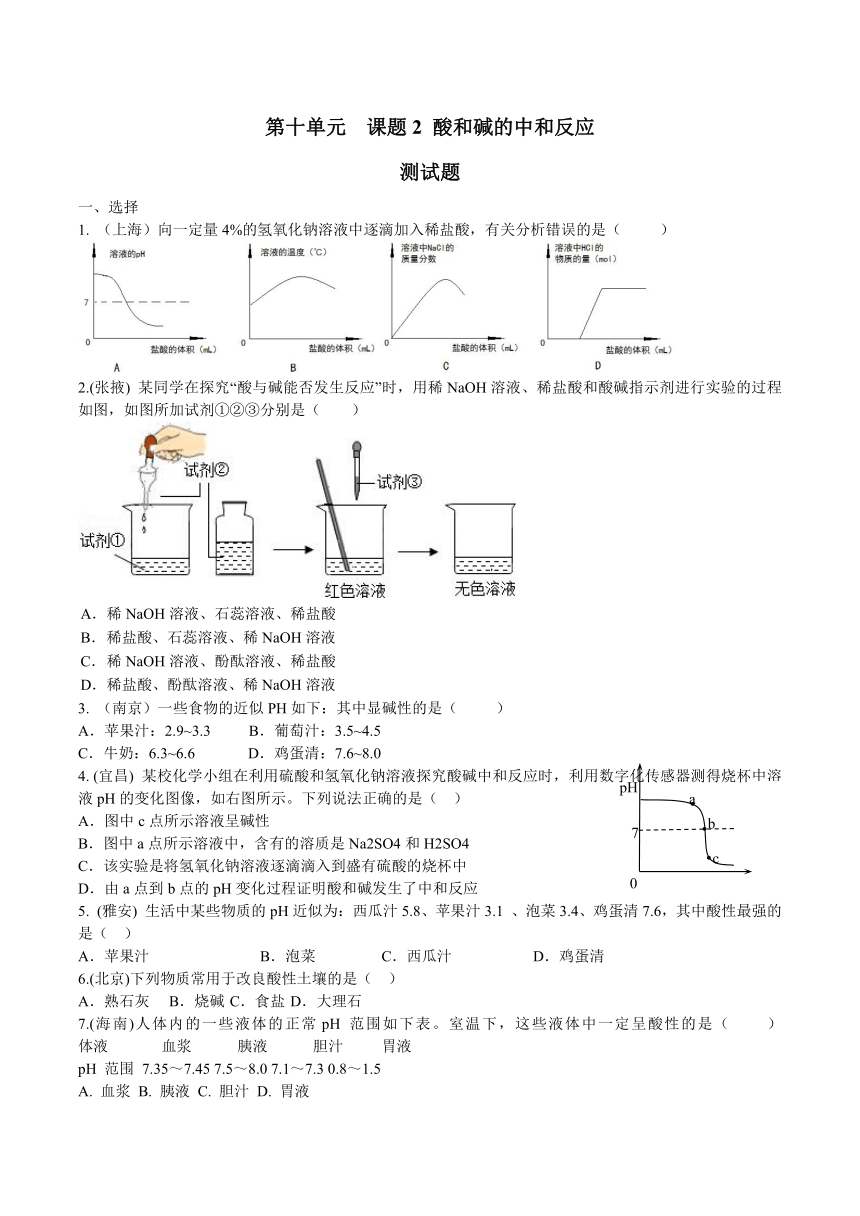
(上海)向一定量4%的氢氧化钠溶液中逐滴加入稀盐酸,有关分析错误的是(
)
2.(张掖)
某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和酸碱指示剂进行实验的过程如图,如图所加试剂①②③分别是( )
A.
稀NaOH溶液、石蕊溶液、稀盐酸
B.
稀盐酸、石蕊溶液、稀NaOH溶液
C.
稀NaOH溶液、酚酞溶液、稀盐酸
D.
稀盐酸、酚酞溶液、稀NaOH溶液
3.
(南京)一些食物的近似PH如下:其中显碱性的是(
)
A.苹果汁:2.9~3.3
B.葡萄汁:3.5~4.5
C.牛奶:6.3~6.6
D.鸡蛋清:7.6~8.0
4.
(宜昌)
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像,如右图所示。下列说法正确的是(
)
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是Na2SO4和H2SO4
C.该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中
D.由a点到b点的pH变化过程证明酸和碱发生了中和反应
(雅安)
生活中某些物质的pH近似为:西瓜汁5.8、苹果汁3.1
、泡菜3.4、鸡蛋清7.6,其中酸性最强的是(
)
A.苹果汁
B.泡菜
C.西瓜汁
D.鸡蛋清
6.(北京)下列物质常用于改良酸性土壤的是(
)
A.熟石灰
B.烧碱
C.食盐
D.大理石
7.(海南)人体内的一些液体的正常pH
范围如下表。室温下,这些液体中一定呈酸性的是(
)
体液
血浆
胰液
胆汁
胃液
pH
范围
7.35~7.45
7.5~8.0
7.1~7.3
0.8~1.5
A.
血浆
B.
胰液
C.
胆汁
D.
胃液
8.(郴州)下列没有运用中和反应原理的是(
)
A.服用含氢氧化镁的药物,可以治疗胃酸过多症B.用熟石灰改良酸性土壤
C.蚊虫叮咬处涂上肥皂水,可减轻痛痒D.用生石灰作干燥剂
9.小烧杯中盛有含石蕊的氢氧化钠溶液.逐滴加入稀盐酸至过量,烧杯中溶液颜色变化的顺序是
(
)
A.紫色——红色——蓝色
B.蓝色——紫色——红色
C.蓝色——红色——紫色
D.紫色——蓝色——红色
10.右图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是
(
)
A.
反应后溶液的pH大于7
B.
反应前的溶液均可导电,反应后的溶液不导电
C.
反应后溶液中存在的粒子只有Na+和Cl―
D.
反应前后所有元素的化合价均无变化
二、填空
11、.硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料。它们既有相似之处,又有不同之处。
(1)它们水溶液的PH都7(填“大于”、“小于”或“等于”)。
(2)它们都能除铁锈,写出盐酸与铁锈主要成分反应的化学方程式
(3)它们都能与碱反应生成盐和水,该类反应叫反应。
(4)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是。
(5)请写出把硫酸转变为盐酸的化学方程式。
12.是常用物质的主要成分及其溶液的pH:
编号
①
②
③
④
常用物质
食醋
白酒
石灰水
纯碱
主要成分
CH3COOH
C2H5OH
Ca(OH)2
Na2CO3
pH
3
7
11
10
请按下列要求将表中对应物质的编号填入空格处:
(1)属于酸的是_____________,属于碱的是___________。
(2)黄蜂毒刺呈碱性,若某人被黄蜂蜇了,可用上述____________物质涂在皮肤上。
13.胃酸的主要成分是盐酸,胃酸过多会引起胃痛。下图是一种治疗胃病药物的标签。
请回答:
(1)该药物的主要作用是_________________,这种药物在胃中发生反应的化学方程式是______________________________________。
(2)胃痛时吃几块苏打饼干(含纯碱)可减轻胃痛,该反应的化学方程式是:_________。
14.(1)用pH试纸测定溶液的pH时,正确的操作是:。
(2)小华同学用pH试纸,按正确操作测定洗发剂和护发剂的pH。测得洗发剂的pH略大于7,则洗发剂显性;测得护发剂的pH略小于7,则护发剂显性。
(3)弱酸性有益于头发的健康。想一想,洗发时应先用剂,后用剂。
15.用下图装置测定因存放不当而部分变质的烧碱中氢氧化钠的质量分数。所取试样质量8.00
g、锥形瓶质量140.00
g,加入足量稀硫酸(质量为50.00
g)每隔相同时间读数一次,数据如下表:
(1)不必进行第七次读数的原因是____________________________。
(2)计算氢氧化钠的质量分数。
(3)所用稀硫酸中H2SO4的质量分数不低于多少?
【参考答案】
一、选择
1
2
3
4
5
6
7
8
9
10
D
C
D
D
A
A
D
D
B
D
二、填空
11.(1)小于
(2)6HCl
+
Fe2O3 =2FeCl3
+
3
H2O
(3)中和反应
(4)浓盐酸
(5)H2SO4+
BaCl2=
BaSO4↓+
2HCI
12.(1)①,
③
(2)①
13.中和胃液中过多的盐酸
Al(OH)3+3HCl=AlCl3+3H2O(2)Na2CO3+2HCl=2NaCl+H2O+CO2↑
14.(1)将pH试纸放在白瓷板(或玻璃片或表面皿)上,用干净的玻璃棒蘸取(或胶头滴管吸取)待测液滴于pH试纸上,然后将试纸颜色与标准比色卡对照读数。(2)碱,酸
(3)洗发,护发
15.⑴第5次和第6次读数相同,说明已充分反应
(2)73.5%
(3)18.3%
pH
7
c
0
t/s
a
b
课题2
酸和碱的中和反应
测试题
一、选择
1.
(上海)向一定量4%的氢氧化钠溶液中逐滴加入稀盐酸,有关分析错误的是(
)
2.(张掖)
某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和酸碱指示剂进行实验的过程如图,如图所加试剂①②③分别是( )
A.
稀NaOH溶液、石蕊溶液、稀盐酸
B.
稀盐酸、石蕊溶液、稀NaOH溶液
C.
稀NaOH溶液、酚酞溶液、稀盐酸
D.
稀盐酸、酚酞溶液、稀NaOH溶液
3.
(南京)一些食物的近似PH如下:其中显碱性的是(
)
A.苹果汁:2.9~3.3
B.葡萄汁:3.5~4.5
C.牛奶:6.3~6.6
D.鸡蛋清:7.6~8.0
4.
(宜昌)
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像,如右图所示。下列说法正确的是(
)
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是Na2SO4和H2SO4
C.该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中
D.由a点到b点的pH变化过程证明酸和碱发生了中和反应
(雅安)
生活中某些物质的pH近似为:西瓜汁5.8、苹果汁3.1
、泡菜3.4、鸡蛋清7.6,其中酸性最强的是(
)
A.苹果汁
B.泡菜
C.西瓜汁
D.鸡蛋清
6.(北京)下列物质常用于改良酸性土壤的是(
)
A.熟石灰
B.烧碱
C.食盐
D.大理石
7.(海南)人体内的一些液体的正常pH
范围如下表。室温下,这些液体中一定呈酸性的是(
)
体液
血浆
胰液
胆汁
胃液
pH
范围
7.35~7.45
7.5~8.0
7.1~7.3
0.8~1.5
A.
血浆
B.
胰液
C.
胆汁
D.
胃液
8.(郴州)下列没有运用中和反应原理的是(
)
A.服用含氢氧化镁的药物,可以治疗胃酸过多症B.用熟石灰改良酸性土壤
C.蚊虫叮咬处涂上肥皂水,可减轻痛痒D.用生石灰作干燥剂
9.小烧杯中盛有含石蕊的氢氧化钠溶液.逐滴加入稀盐酸至过量,烧杯中溶液颜色变化的顺序是
(
)
A.紫色——红色——蓝色
B.蓝色——紫色——红色
C.蓝色——红色——紫色
D.紫色——蓝色——红色
10.右图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论正确的是
(
)
A.
反应后溶液的pH大于7
B.
反应前的溶液均可导电,反应后的溶液不导电
C.
反应后溶液中存在的粒子只有Na+和Cl―
D.
反应前后所有元素的化合价均无变化
二、填空
11、.硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料。它们既有相似之处,又有不同之处。
(1)它们水溶液的PH都7(填“大于”、“小于”或“等于”)。
(2)它们都能除铁锈,写出盐酸与铁锈主要成分反应的化学方程式
(3)它们都能与碱反应生成盐和水,该类反应叫反应。
(4)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是。
(5)请写出把硫酸转变为盐酸的化学方程式。
12.是常用物质的主要成分及其溶液的pH:
编号
①
②
③
④
常用物质
食醋
白酒
石灰水
纯碱
主要成分
CH3COOH
C2H5OH
Ca(OH)2
Na2CO3
pH
3
7
11
10
请按下列要求将表中对应物质的编号填入空格处:
(1)属于酸的是_____________,属于碱的是___________。
(2)黄蜂毒刺呈碱性,若某人被黄蜂蜇了,可用上述____________物质涂在皮肤上。
13.胃酸的主要成分是盐酸,胃酸过多会引起胃痛。下图是一种治疗胃病药物的标签。
请回答:
(1)该药物的主要作用是_________________,这种药物在胃中发生反应的化学方程式是______________________________________。
(2)胃痛时吃几块苏打饼干(含纯碱)可减轻胃痛,该反应的化学方程式是:_________。
14.(1)用pH试纸测定溶液的pH时,正确的操作是:。
(2)小华同学用pH试纸,按正确操作测定洗发剂和护发剂的pH。测得洗发剂的pH略大于7,则洗发剂显性;测得护发剂的pH略小于7,则护发剂显性。
(3)弱酸性有益于头发的健康。想一想,洗发时应先用剂,后用剂。
15.用下图装置测定因存放不当而部分变质的烧碱中氢氧化钠的质量分数。所取试样质量8.00
g、锥形瓶质量140.00
g,加入足量稀硫酸(质量为50.00
g)每隔相同时间读数一次,数据如下表:
(1)不必进行第七次读数的原因是____________________________。
(2)计算氢氧化钠的质量分数。
(3)所用稀硫酸中H2SO4的质量分数不低于多少?
【参考答案】
一、选择
1
2
3
4
5
6
7
8
9
10
D
C
D
D
A
A
D
D
B
D
二、填空
11.(1)小于
(2)6HCl
+
Fe2O3 =2FeCl3
+
3
H2O
(3)中和反应
(4)浓盐酸
(5)H2SO4+
BaCl2=
BaSO4↓+
2HCI
12.(1)①,
③
(2)①
13.中和胃液中过多的盐酸
Al(OH)3+3HCl=AlCl3+3H2O(2)Na2CO3+2HCl=2NaCl+H2O+CO2↑
14.(1)将pH试纸放在白瓷板(或玻璃片或表面皿)上,用干净的玻璃棒蘸取(或胶头滴管吸取)待测液滴于pH试纸上,然后将试纸颜色与标准比色卡对照读数。(2)碱,酸
(3)洗发,护发
15.⑴第5次和第6次读数相同,说明已充分反应
(2)73.5%
(3)18.3%
pH
7
c
0
t/s
a
b
同课章节目录
