【全国百强校】海南省国兴中学高中化学必修一课件:1-2-1-2 摩尔质量 (共22张PPT)
文档属性
| 名称 | 【全国百强校】海南省国兴中学高中化学必修一课件:1-2-1-2 摩尔质量 (共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 194.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-08-27 00:00:00 | ||
图片预览








文档简介
课件22张PPT。1-2-1-2 摩尔质量海南省国兴中学
曾垂云团队合作学习 自主管理 先学后教
第一章《从实验学化学》
第二节《化学计量在实验中的应用》【学习目标】
1、掌握摩尔质量的概念;
2、了解物质的量、微观粒子数、物质的质量、摩尔质量
间的联系,能根据它们之间的关系进行简单计算。 摩尔质量 M 1-2-1-2 摩尔质量9、概念:单位物质的量(n)的物质所具有的质量(m)
叫做摩尔质量,符号为M,单位g·mol-1。(1) 单位物质的量:即1 mol,所以顾名思义,摩尔质量
可以理解为1 mol物质所具有的质量。
如下面两种说法,正确的是:____
① 2 mol H2O的质量是1 mol H2O的2倍
② 2 mol H2O的摩尔质量是1 mol H2O的2倍摩尔质量 M 1-2-1-2 摩尔质量9、摩尔质量(M): 1 mol物质所具有的质量。
当质量以克(g)为单位时,其数值等于该
粒子的相对原子质量或相对分子质量。摩尔质量 M 1-2-1-2 摩尔质量(2) 摩尔质量与相对原子/分子质量关系:只是数值相等
所以物质的摩尔质量通常默认为是已知条件
① Mg的相对原子质量是____,摩尔质量是________;
② KCl的相对原子质量是____,摩尔质量是________;
③ SO2的相对原子质量是____,摩尔质量是________;
④ CO32-的相对原子质量是___,摩尔质量是________;
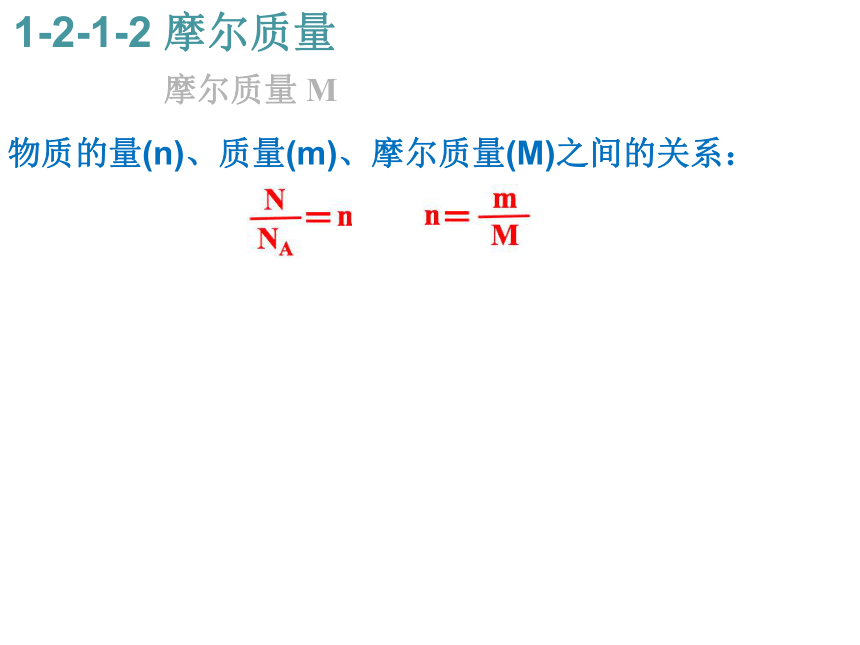
24 24 g/mol 74.5 74.5 g/mol 64 64 g/mol 60 60 g/mol 物质的量(n)、质量(m)、摩尔质量(M)之间的关系:
11、【学与问】 课本13页
24.5 g H2SO4的摩尔质量是______,物质的量是____。
1.50 mol Na2CO3的摩尔质量是_______,质量是____。摩尔质量 M 1-2-1-2 摩尔质量98 g/mol 0.25 mol 106 g/mol 159 g 物质的量(n)、质量(m)、摩尔质量(M)之间的关系:
摩尔质量 M 1-2-1-2 摩尔质量物质的量(n)、质量(m)、摩尔质量(M) 、物质的粒子数(N)之间的关系:
10、填报表练习
摩尔质量 M 1-2-1-2 摩尔质量1 mol 18 g/mol 18 18 g 3.01×1023 18 g/mol 18 9 g 18 g/mol 27 18 g/mol 18 1 mol 6.02×1023 2 mol 54 g 物质的量(n)、质量(m)、摩尔质量(M) 、物质的粒子数(N)之间的关系:
11、【学与问】 课本13页
24.5 g H2SO4的摩尔质量是_________ ,物质的量
是_____,含有___mol H原子,_______个 O原子。
(2) 1.50 mol Na2CO3的摩尔质量是________,质量
是_____,含有___ mol Na+,_________个CO32-。 摩尔质量 M 1-2-1-2 摩尔质量98 g/mol 0.25 mol 106 g/mol 159 g 0.5 6.02×1023 3 9.03×1023 【学习目标】
1、掌握摩尔质量的概念;
2、了解物质的量、微观粒子数、物质的质量、摩尔质量
间的联系,能根据它们之间的关系进行简单计算。 摩尔质量 M 1-2-1-2 摩尔质量 2 1 2
2×6.02×1023 6.02×1023 2×6.02×1023
2NA NA 2NA
2 mol 1 mol 2 mol
补充:物质的量与化学方程式的计算 8、(6)
6.02×1023
NA
mol
补充:物质的量与化学方程式的计算 8、(6)
6.02×1023 3.01×1023 6.02×1023
NA 0.5NA NA
1 mol 0.5 mol 1 mol
补充:物质的量与化学方程式的计算【合作运用】
11.(1分) 下列说法中正确的是
A.1 mol氧 B.1 mol H2SO4
C.1 mol米 D.1 mol面粉
12.(1分) 相同物质的量的SO2和SO3它们之间的关系
不正确的是
A.所含硫原子的物质的量之比为1:1
B.所含氧原子的物质的量之比为1:1
C.氧元素的质量比为2:3
D.硫元素的质量比为1:1 B B 摩尔质量 M 1-2-1-2 摩尔质量【合作运用】
13.(1分) 下列说法中正确的是
(NA代表阿伏加德罗常数的值)
A.1 mol N2和1 mol CO所含的原子数都是NA
B.1 mol H2和1 mol CO2所含的原子数都是2NA
C.1 mol CO和1 mol CO2所含的氧原子数都是NA
D.1 mol H2 SO4和1 mol H3PO4所含的氧原子数
都是4NA
D 摩尔质量 M 1-2-1-2 摩尔质量【合作运用】
4.下列说法中正确的是(NA代表阿伏加德罗常数的值)
A.1 mol N2和1 mol CO所含的原子数都是NA
B.1 mol H2和1 mol CO2所含的原子数都是2NA
C.1 mol CO和1 mol CO2所含的氧原子数都是NA
D.1 mol H2 SO4和1 mol H3PO4所含的氧原子数
都是4NA
D 摩尔质量 M 1-2-1-2 摩尔质量【合作运用】
14.(2分) 某混有水蒸气的CO2 45.8 g,依次通过如下
装置,最后测得浓硫酸重量增加了1.8 g.
则碱石灰增加的质量是多少?
请计算混合气体中H2O和CO2的物质的量之比。
摩尔质量 M 1-2-1-2 摩尔质量【合作运用】
14.(2分) 某混有水蒸气的CO2 45.8 g,依次通过如下
装置,最后测得浓硫酸重量增加了1.8 g.
则碱石灰增加的质量是多少?
请计算混合气体中H2O和CO2的物质的量之比。
H2O CO2
质量m 1.8g 45.8g - 1.8g = 44g
物质的量n 1.8g/18g·mol-1 44g/44g·mol-1
= 0.1 mol = 1 mol摩尔质量 M 1-2-1-2 摩尔质量【当堂作业】
15.(1分) 0.5 mol Na2SO4中所含的Na+离子数为
A.3.01×1023 B.6.02×1023
C.0.5 D.1
16.(1分) 1 g O2和1 g O3之间的关系,正确的是
A.所含分子数相同
B.摩尔质量相同
C.所含原子数相同
D.1 g O3中所含分子数较多
B C 摩尔质量 M 1-2-1-2 摩尔质量【当堂作业】
17.(1分) 下列叙述中错误的是
A.H2SO4的摩尔质量是98 g
B.2 mol NO和2 mol NO2含原子数不相同
C.等质量的O2和O3中所含氧原子个数相同
D.等物质的量的CO和CO2中所含碳原子数相等
A 摩尔质量 M 1-2-1-2 摩尔质量【当堂作业】
18.(2分) 有一块锌片插入Fe2(SO4)3溶液中,
完全反应后,算得锌片反应了6.5 g,求:
参加反应的Zn的物质的量
(2) 析出Fe的物质的量
摩尔质量 M 1-2-1-2 摩尔质量【当堂作业】
18.(2分) 有一块锌片插入Fe2(SO4)3溶液中,
完全反应后,算得锌片反应了6.5 g,求:
(1) 参加反应的Zn的物质的量
n(Zn) = m/M = 6.5g/65g·mol-1 = 0.1 mol
(2) 析出Fe的物质的量
3Zn + Fe2(SO4)3 = 3ZnSO4 + 2Fe
3 mol 2 mol
0.1 mol x
算得x ≈ 0.07 mol摩尔质量 M 1-2-1-2 摩尔质量谢谢诸位!让我们一起努力将化学变得更美好!
曾垂云团队合作学习 自主管理 先学后教
第一章《从实验学化学》
第二节《化学计量在实验中的应用》【学习目标】
1、掌握摩尔质量的概念;
2、了解物质的量、微观粒子数、物质的质量、摩尔质量
间的联系,能根据它们之间的关系进行简单计算。 摩尔质量 M 1-2-1-2 摩尔质量9、概念:单位物质的量(n)的物质所具有的质量(m)
叫做摩尔质量,符号为M,单位g·mol-1。(1) 单位物质的量:即1 mol,所以顾名思义,摩尔质量
可以理解为1 mol物质所具有的质量。
如下面两种说法,正确的是:____
① 2 mol H2O的质量是1 mol H2O的2倍
② 2 mol H2O的摩尔质量是1 mol H2O的2倍摩尔质量 M 1-2-1-2 摩尔质量9、摩尔质量(M): 1 mol物质所具有的质量。
当质量以克(g)为单位时,其数值等于该
粒子的相对原子质量或相对分子质量。摩尔质量 M 1-2-1-2 摩尔质量(2) 摩尔质量与相对原子/分子质量关系:只是数值相等
所以物质的摩尔质量通常默认为是已知条件
① Mg的相对原子质量是____,摩尔质量是________;
② KCl的相对原子质量是____,摩尔质量是________;
③ SO2的相对原子质量是____,摩尔质量是________;
④ CO32-的相对原子质量是___,摩尔质量是________;
24 24 g/mol 74.5 74.5 g/mol 64 64 g/mol 60 60 g/mol 物质的量(n)、质量(m)、摩尔质量(M)之间的关系:
11、【学与问】 课本13页
24.5 g H2SO4的摩尔质量是______,物质的量是____。
1.50 mol Na2CO3的摩尔质量是_______,质量是____。摩尔质量 M 1-2-1-2 摩尔质量98 g/mol 0.25 mol 106 g/mol 159 g 物质的量(n)、质量(m)、摩尔质量(M)之间的关系:
摩尔质量 M 1-2-1-2 摩尔质量物质的量(n)、质量(m)、摩尔质量(M) 、物质的粒子数(N)之间的关系:
10、填报表练习
摩尔质量 M 1-2-1-2 摩尔质量1 mol 18 g/mol 18 18 g 3.01×1023 18 g/mol 18 9 g 18 g/mol 27 18 g/mol 18 1 mol 6.02×1023 2 mol 54 g 物质的量(n)、质量(m)、摩尔质量(M) 、物质的粒子数(N)之间的关系:
11、【学与问】 课本13页
24.5 g H2SO4的摩尔质量是_________ ,物质的量
是_____,含有___mol H原子,_______个 O原子。
(2) 1.50 mol Na2CO3的摩尔质量是________,质量
是_____,含有___ mol Na+,_________个CO32-。 摩尔质量 M 1-2-1-2 摩尔质量98 g/mol 0.25 mol 106 g/mol 159 g 0.5 6.02×1023 3 9.03×1023 【学习目标】
1、掌握摩尔质量的概念;
2、了解物质的量、微观粒子数、物质的质量、摩尔质量
间的联系,能根据它们之间的关系进行简单计算。 摩尔质量 M 1-2-1-2 摩尔质量 2 1 2
2×6.02×1023 6.02×1023 2×6.02×1023
2NA NA 2NA
2 mol 1 mol 2 mol
补充:物质的量与化学方程式的计算 8、(6)
6.02×1023
NA
mol
补充:物质的量与化学方程式的计算 8、(6)
6.02×1023 3.01×1023 6.02×1023
NA 0.5NA NA
1 mol 0.5 mol 1 mol
补充:物质的量与化学方程式的计算【合作运用】
11.(1分) 下列说法中正确的是
A.1 mol氧 B.1 mol H2SO4
C.1 mol米 D.1 mol面粉
12.(1分) 相同物质的量的SO2和SO3它们之间的关系
不正确的是
A.所含硫原子的物质的量之比为1:1
B.所含氧原子的物质的量之比为1:1
C.氧元素的质量比为2:3
D.硫元素的质量比为1:1 B B 摩尔质量 M 1-2-1-2 摩尔质量【合作运用】
13.(1分) 下列说法中正确的是
(NA代表阿伏加德罗常数的值)
A.1 mol N2和1 mol CO所含的原子数都是NA
B.1 mol H2和1 mol CO2所含的原子数都是2NA
C.1 mol CO和1 mol CO2所含的氧原子数都是NA
D.1 mol H2 SO4和1 mol H3PO4所含的氧原子数
都是4NA
D 摩尔质量 M 1-2-1-2 摩尔质量【合作运用】
4.下列说法中正确的是(NA代表阿伏加德罗常数的值)
A.1 mol N2和1 mol CO所含的原子数都是NA
B.1 mol H2和1 mol CO2所含的原子数都是2NA
C.1 mol CO和1 mol CO2所含的氧原子数都是NA
D.1 mol H2 SO4和1 mol H3PO4所含的氧原子数
都是4NA
D 摩尔质量 M 1-2-1-2 摩尔质量【合作运用】
14.(2分) 某混有水蒸气的CO2 45.8 g,依次通过如下
装置,最后测得浓硫酸重量增加了1.8 g.
则碱石灰增加的质量是多少?
请计算混合气体中H2O和CO2的物质的量之比。
摩尔质量 M 1-2-1-2 摩尔质量【合作运用】
14.(2分) 某混有水蒸气的CO2 45.8 g,依次通过如下
装置,最后测得浓硫酸重量增加了1.8 g.
则碱石灰增加的质量是多少?
请计算混合气体中H2O和CO2的物质的量之比。
H2O CO2
质量m 1.8g 45.8g - 1.8g = 44g
物质的量n 1.8g/18g·mol-1 44g/44g·mol-1
= 0.1 mol = 1 mol摩尔质量 M 1-2-1-2 摩尔质量【当堂作业】
15.(1分) 0.5 mol Na2SO4中所含的Na+离子数为
A.3.01×1023 B.6.02×1023
C.0.5 D.1
16.(1分) 1 g O2和1 g O3之间的关系,正确的是
A.所含分子数相同
B.摩尔质量相同
C.所含原子数相同
D.1 g O3中所含分子数较多
B C 摩尔质量 M 1-2-1-2 摩尔质量【当堂作业】
17.(1分) 下列叙述中错误的是
A.H2SO4的摩尔质量是98 g
B.2 mol NO和2 mol NO2含原子数不相同
C.等质量的O2和O3中所含氧原子个数相同
D.等物质的量的CO和CO2中所含碳原子数相等
A 摩尔质量 M 1-2-1-2 摩尔质量【当堂作业】
18.(2分) 有一块锌片插入Fe2(SO4)3溶液中,
完全反应后,算得锌片反应了6.5 g,求:
参加反应的Zn的物质的量
(2) 析出Fe的物质的量
摩尔质量 M 1-2-1-2 摩尔质量【当堂作业】
18.(2分) 有一块锌片插入Fe2(SO4)3溶液中,
完全反应后,算得锌片反应了6.5 g,求:
(1) 参加反应的Zn的物质的量
n(Zn) = m/M = 6.5g/65g·mol-1 = 0.1 mol
(2) 析出Fe的物质的量
3Zn + Fe2(SO4)3 = 3ZnSO4 + 2Fe
3 mol 2 mol
0.1 mol x
算得x ≈ 0.07 mol摩尔质量 M 1-2-1-2 摩尔质量谢谢诸位!让我们一起努力将化学变得更美好!
