1.6几种重要的盐(共计2课时)
图片预览









文档简介
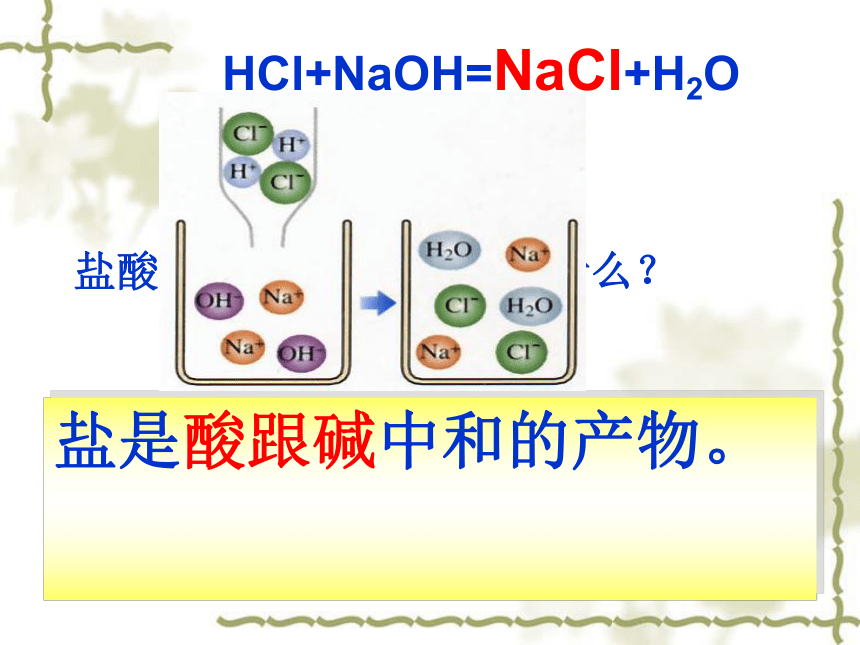
课件51张PPT。食盐晶体明矾晶体碳酸钠 晶体1.6 几种重要的盐 锆 石第1课时 盐酸和氢氧化钠反应生成什么?生成水的同时,溶液里剩下酸根Cl-离子和金属Na+离子,通过蒸发溶液,这两种离子就会结晶析出晶体,也就是食盐晶体。HCl+NaOH=NaCl+H2O盐是酸跟碱中和的产物。
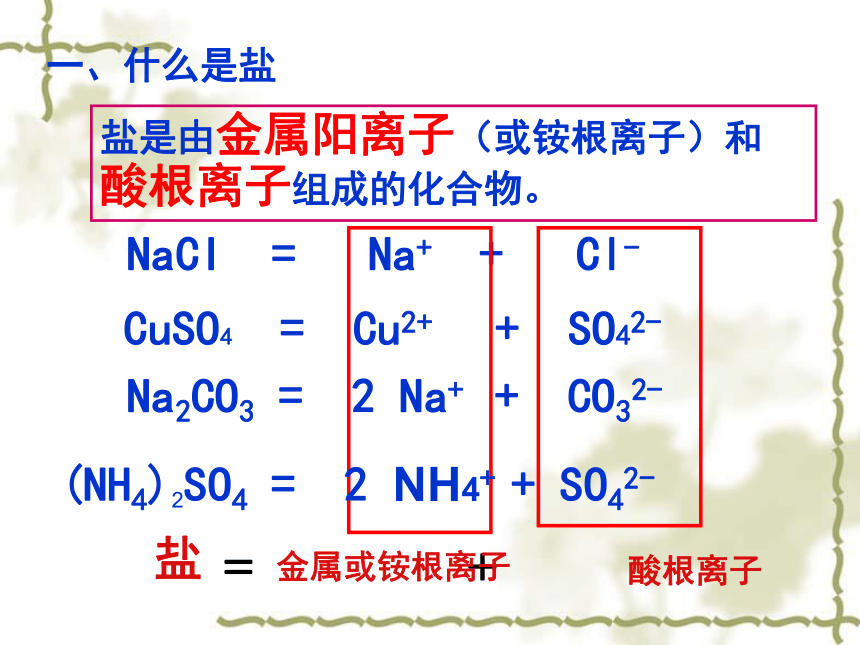
NaCI = Na+ + Cl-CuSO4 = Cu2+ + SO42-盐= +一、什么是盐盐是由金属阳离子(或铵根离子)和酸根离子组成的化合物。金属或铵根离子酸根离子Na2CO3 = 2 Na+ + CO32-(NH4)2SO4 = 2 NH4+ + SO42-思考:我们现在所说的盐是不是就是我们平时吃的食盐呢?盐不仅仅是食盐,食盐只是盐中的一种物质,而盐是一类物质 我国某地曾发生白色的工业用盐误作食盐食用引起的中毒事件,这种工业用盐是亚硝酸钠(化学式为 NaNO2 )悲剧自然界中有些盐晶体非常美丽你还见过其他盐的晶体?盐有什么性质?用途?二、几种盐的性质(一)碳酸钠(纯碱或苏打Na2CO3) ①晶体:Na2CO3·10H2O结晶水合物:含结晶水的化合物
说明:结晶水合物是具有一定组成的纯净物,化学式中的“.’表示结合,算相对分子量时,表示加。
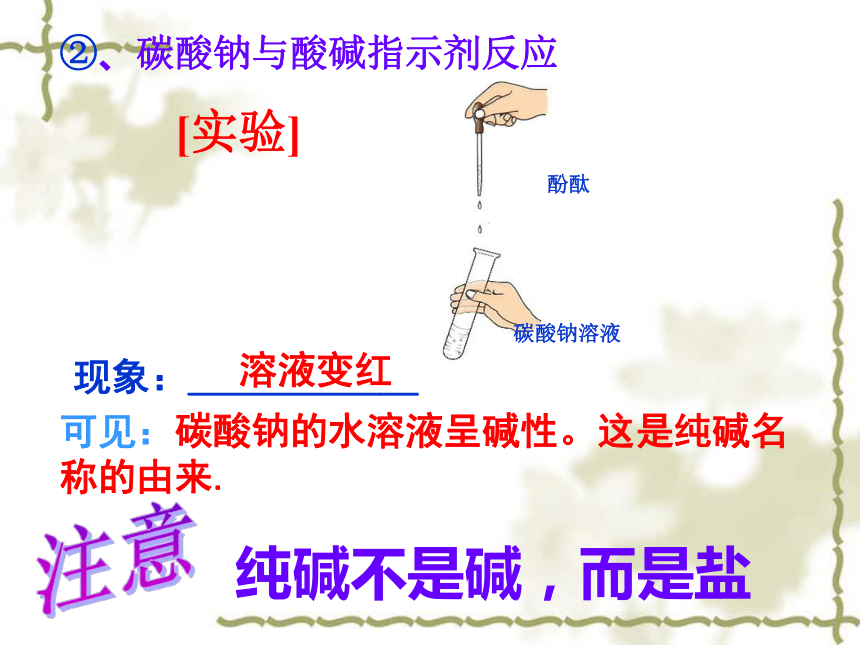
结晶水:晶体从溶液中析出时结合的水分子。Na2CO3? 10H2O= Na2CO3+ 10H2O易风化(自然条件失去结晶水)风化是化学变化干燥环境里,碳酸钠晶体会逐渐失去结晶水而成为碳酸钠粉末 溶液变红可见:碳酸钠的水溶液呈碱性。这是纯碱名称的由来.②、碳酸钠与酸碱指示剂反应现象:______ 纯碱不是碱,而是盐注意碳酸钠溶液酚酞[实验]二、几种盐的性质及用途(一)碳酸钠(纯碱或苏打Na2CO3) ②水溶液显碱性①晶体:Na2CO3·10H2O易失去结晶水纯碱不是碱,而是盐(5)在常温下,放在干燥的空气里, Na2CO3·10H2O会逐渐失去结晶水而成为碳酸钠粉末。——风化(3)碳酸钠晶体的化学式:Na2CO3·10H2O;
相对分子质量为286(23×2+12+16×3+10×18),晶体中Na2CO3和H2O的质量比为106︰180,属纯净物。(4)结晶水合物:晶体里含有一定数目水分子的物质称为结晶水合物,所含的水称为结晶水。(2)碳酸钠从溶液中结晶析出时,晶体结合了一定数目的水分子,化学式是Na2CO3·10H2O。【例1】28.6克碳酸钠晶体(Na2CO3·10H2O)完全溶于71.4克水中,所得溶液的溶质质量分数为28.6%吗?【做一做】把3.1克氧化钠(Na2O)完全溶于46.9克水中,所得溶液的溶质质量分数为多少?答:不是28.6%,是10.6%。8%答:天安门汉白玉华表大理石贝壳珍珠 石灰石、大理石、白垩、汉白玉,贝壳虽外表不同,但主要成分都是CaCO3,化学性质相同(二)碳酸钙(CaCO3)
(大理石、石灰石的主要成分) 1、难溶于水,固体,白色2、工艺品、建筑材料、水泥3、高温分解:工业制取CO2H2CO3+Ca(OH)2==CaCO3↓+2H2O制取:思考:怎样证明一块岩石是碳酸盐?*用稀盐酸和澄清的石灰水,
(即检验CO32-)先加盐酸,再将产生气体通入澄清石灰水中,看是否有浑浊出现。大家叫我钟乳石、石柱、石笋,我的主要成分是碳酸钙,成长了n年,个子还不高,可我已经顶天立地了.不可否认我长得很丑,可是遇到酸,我也会很温柔石灰岩的主要成分是碳酸钙,碳酸钙遇到溶有二氧化碳的水时,会慢慢变成可溶于水的碳酸氢钙Ca(HCO3)2
CaCO3 + H2O + CO2 = Ca(HCO3)2
当受热或其他原因,水中碳酸氢钙会分解,重新变成碳酸钙沉积下来。
Ca(HCO3)2 = CaCO3↓ + CO2↑+ H2O
在自然界里不断发生上述反应,石灰岩逐渐变成碳酸氢钙而溶解掉,形成溶洞;碳酸氢钙不断分解,生成的碳酸钙逐渐沉积,形成千姿百态的钟乳石.石笋和石柱。 (3)溶洞的形成:(三) 氯化钠(NaCl) 俗称食盐1、食盐主要来自于海水、井水、盐湖水等(三)氯化钠(NaCl)俗称:食盐 2.物理性质:白色晶体,能溶于水3.用途:食用,防腐剂,重要化工原料,
制生理盐水( 0.9%的氯化钠溶液),杀菌等。 粗盐含MgCl2,CaCl2等杂质易潮解,精盐不易潮解。 日常生活中常用食盐水清洗伤口,你知道这是为什么吗? 思考与讨论: 为何用食盐腌过的肉类和蔬菜不易腐败?腊肉咸菜实验:收集一些汗液盛放在试管中,滴入几滴硝酸银溶液,有什么现象产生?
有白色沉淀生成NaCl+AgNO3==AgCl↓+NaNO3氯离子的鉴别方法:用硝酸银溶液和稀硝酸4、化学性质思考与讨论: 百度一下食盐在工业生产中的应用侯氏联合制碱法侯德榜,著名科学家,杰出的化工专家,我国重工业化学的开拓者。他于
20年代突破氨碱法制碱技术的奥秘,主持建成亚洲第一座纯碱厂;30年代领导建成了我国第一座兼产合成氨、硝酸、硫酸和硫酸铵的联合企业;四五十年代又发明了连续生产纯碱与氯化铵的联合制碱新工艺。
这个新工艺是把氨厂和碱厂建在一起,联合生产。由氨厂提供碱厂需要的氨和二氧化碳。母液里的氯化铵用加入食盐的办法使它结晶出来,作为化工产品或化肥。食盐溶液又可以循环使用。命名为“侯氏联合制碱法”。
侯德榜 鉴别氢氧化钠是否变质:
甲的做法:取样品加入蒸馏水,配成溶液,滴入酚酞试液,试液变红则说明没变质,试液不变色证明已变质.
乙的做法:加入盐酸,产生气泡证明变质,不产生气泡证明没变质.
思考:你还有什么方法证明它变质呢?若有变质如何除去杂质?碱溶钾钠钡钙铵大多酸溶水中间钾钠铵盐均易溶硝酸盐遇水影无踪氯化物不溶氯化银硫酸盐不溶硫酸钡碳酸盐只溶钾钠铵硫酸盐微溶是银钙课内练习1.证明生石灰( CaO)中是否含有未煅烧的石灰石(CaCO3)的方法,是滴加( ),若有( )产生,就证明生石灰中含有未煅烧的石灰石,有关化学方程式是( ).稀盐酸气泡CaCO3 + 2HCl === CaCl2 + H2O +CO2↑2.对人的生理活动关系最大的盐是( )A.Na2CO3 B.CaCO3 C.NaCl D.MgCl2C3.下列物质中不属于盐的是( )A.CuSO4 B.Na2S C.CaCl2 D.Ba(OH)2D1.6 几种重要的盐 第2课时 1.下列物质的名称、俗称、化学式三者都相符的是
A氢氧化钠、火碱、NaCl
B氧化钙、消石灰、CaO
C碳酸钠、纯碱、Na2CO3
D硫酸铜、胆矾、CuSO4·5H2O2、用做鉴别碳酸根离子的试剂是
(A)稀硫酸 (B)食盐水
(C)石灰水 (D)稀盐酸和澄清石灰水3、如何鉴别氯化钠、碳酸钠、硫酸钠三种无色溶液?复习三、盐的制取1.盐的溶解性(1) 盐分为_________盐和_______盐。(2)常见盐的溶解性表:钾、钠、硝、铵盐皆可溶,
氯化物不溶氯化银,硫酸盐不溶钡和银,
碳酸盐只溶钾钠铵。溶解性口诀可溶性不溶性碱只溶钾、钠、 钡、钙酸都可溶(除硅酸外)口诀二:钾钠硝铵皆可溶,硫酸铅钡两不溶;
盐酸不溶银亚汞,弱酸盐大多沉水中。常见碱盐的溶解性表根据溶解性口诀,判断下列物质的溶解性。1.Zn(OH)2:______ 2.AgCl:________
3.NaNO3:________ 4.K2CO3:________
5.BaSO4:________ 6.BaCl2:________
7.CaCO3:________ 8.Na2CO3:_______
9.CuCl2:________ 10.AgNO3:_______
11.BaCO3:_______ 12.Ma(OH)2:______
13.H2SO4:_______ 14.H3PO4:________不溶不溶不溶不溶不溶不溶溶溶溶溶溶溶溶溶2.复分解反应(1).[实验]在盛有Na2CO3溶液的试管里加入CaCl2溶液,可发现:________白色沉淀 Na2CO3+CaCl2 = CaCO3↓ +2NaCl这个反应的原理是怎样的? 盐 + 盐 = 新盐 + 新盐思考:除了酸与碱中和反应能生成盐外,还有其他什么方法能生成盐呢?Na2CO3溶液和CaCl2溶液反应原理 Na2CO3 溶液中
含有的离子 CaCl2溶液中
含有的离子 2Na+CO32— Ca2+2CI—Na2CO3+CaCl2 = CaCO3↓+ 2NaCl你能找出这个反应类型有什么特点?两种化合物互相交换成分生成新的化合物 Na2CO3+CaCl2 = CaCO3↓+ 2NaCl复分解反应。AB+CD==AD+CB2NaOH + H2SO4 = Na2SO4 + 2H2O Na2CO3+Ca(OH)2 = CaCO3↓ +2NaOH2HCl + CaCO3 = CaCl2 + H2O + CO2↑酸、碱、盐等物质之间是不是都能发生复分解反应?NaOH+BaCl2= Ba(OH)2+NaCl这个反应是不能进行。×Cu(OH)2+BaCl2= Ba(OH)2+CuCl2×复分解反应的条件: 2、反应物均可溶(酸参与除外)1、生成物有水或气体或沉淀复分解反应的实质: 阴、阳离子结合生成难电离的物质(水、气体、沉淀)H+ + OH- = H2O(中和反应)2H+ + CO32- = H2O+CO2↑
Ag+ + Cl- = AgCl↓ 酸碱反应是否是复分解反应?酸碱盐之间的反应一般是复分解反应。 复分解反应不一定是酸碱反应,而酸碱反应一定是复分解反应,即酸碱反应是复分解反应中的一种。下列方程式属酸碱反应的有______;属复分解的有_________; 1、BaCl2 + H2SO4 = BaSO4 ↓ + 2HCl
2、Na2CO3 + H2SO4 =Na2SO4 + CO2 ↑+ H2O
3、 Ca(OH)2 + H2SO4 == CaSO4 + 2H2O
4、 BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2
5、 (NH4)2SO4+Ca(OH)2==CaSO4+2NH3 ↑ +H2O
6、Na2CO3+ Ca(OH)2= CaCO3↓+H2O
3123456讨论:参照酸和碱性质的推断方法,你能否说说盐有哪些性质. 1、盐 + 酸 —— 新盐 + 新酸2、盐 + 碱 —— 新盐 + 新碱3、盐 + 盐 —— 新盐 + 新盐 盐的性质:CaCO3+2HCl=CaCl2+H2O+CO2↑Na2CO3+Ca(OH)2=CaCO3↓+2NaOHNaCl+AgNO3=AgCl↓+NaNO3 注意:2、3中的反应物(盐和碱)都必须溶于水。4、某些盐加热能分解 根据酸的共性和碱的共性,以及盐的有关性质,你知道可以用哪些方法制取盐?3.盐的制取有些盐是天然存在的。如:食盐、纯碱等,但有些是用化学方法制取。1、物理方法:结晶法(天然碱)2、化学方法:常用复分解反应盐的制取:1、物理方法:结晶法(天然碱) 酸 + 碱 —— 盐+水
盐 + 酸 —— 新盐 + 新酸
可溶性盐+可溶性碱 — 新盐+新碱
可溶性盐+可溶性盐 —新盐+新盐阅读:侯德榜“庄稼一枝花,全靠肥当家”1.什么是化肥? 化学肥料是用矿物质、空气、水等作原料,经过化学加工精制而成的肥料。2.化肥有哪些类型?氮肥:化肥主要含有氮元素的称氮肥。磷肥:化肥主要含有磷元素的称磷肥。钾肥:化肥主要含有氮元素的称钾肥。复合肥:化肥中含有两种或两种以上
主要营养元素的称复合肥。四、盐与化肥读图,连线3.化肥的作用与制取能促使农作物的茎叶生长茂盛,含有组成叶绿素的重要元素氮 肥(1)作用:(2)氮肥(铵盐)的制取:常用酸与氨气反应制取NH3+H2O+CO2=NH4HCO3(碳铵)2NH3+H2SO4=(NH4)2SO4(硫铵)因此:盐的组成中,所含的阳离子不一定都是金属阳离子,也可以是复杂阳离子(带电原子团)(3) 氮肥的种类:除铵盐外还有最常用的氮肥:是含氮有机物即人的尿液化 肥:尿素 CO(NH2)2尿素在微生物中作用下会转变为铵盐或氨气磷 肥促进农作物要根系发达,增强吸收养份和抗寒抗旱能力,促进作物穗数增多,籽粒饱满等。过磷酸钙:
CaSO4和Ca (H2PO4)2的混合物3.化肥的作用与制取(1)作用:(2)种类:3.化肥的作用与制取钾 肥(1)作用:促进农作物生长旺盛,茎杆粗壮,增强抗病虫害能力,促进糖和淀粉的生成。(2)种类:硫酸钾(K2SO4)、氯化钾(KCI)、 草木灰(成份K2CO3)4. 使用化肥时注意: 长期使用会造成土壤板结,破坏土壤结构。 1.小明家是种植蔬菜的专业户,他学习了初三科学后告诉父母:施用适量的氮肥可以使种植的蔬菜叶色浓绿。因此,
(1)他建议其父母去买的氮肥的是 。
A、碳酸氢铵[NH4HCO3] B、硫酸钾[K2SO4]
C、磷矿粉 [Ca3(PO4)2]
(2)他还告戒父母在施用氮肥的同时 (填“能”或“不能”)施用草木灰(呈碱性) 。
理由是
。
(3)他还建议父母经常向大棚中补充气体肥料CO2,目的是促进绿色植物 作用。A不能草木灰和他们买的氮肥混合使用会放出氨气,降低氮肥肥效光合课内练习2.已知可溶性钡盐有毒,而在医院里做胃镜透视时,要用BaSO4造影,俗称“钡餐”,吃下BaSO4无毒是因为( )。但如果无意中误服了BaCO3则会引起中毒,这是因为(用化学方程式表示,下同)( ),误服后, 应立即用泻盐MgSO4解毒,这是因为( )。BaSO4不溶于水,也不与酸反应式BaCO3+ 2HCl ==== BaCl2 + H2O +CO2↑BaCl2 + MgSO4 ==== BaSO4 ↓ + MgCl2课内练习下列物质能发生化学反应吗?为什么?1、CuO+Ba(OH)2= Cu(OH)2 ↓ +BaO
2、SO2+HNO3=NO2 + H2SO3
3、2Fe(OH)3+3MgCl2=2FeCl3+3Mg (OH)2 ↓
4、Na2CO3+CaCl2 = CaCO3 ↓ +2NaCl上述物质能发生化学反应的是: ___________________________4因为---1:碱不能与金属氧化物反应。2:酸不能与非金属氧化物反应。3:Fe(OH)3难溶课内拓展下列物质能发生化学反应吗?为什么?5、Na2CO3+2HCl= 2Na Cl +H2O+ CO2↑
6、 Ba(OH)2+H2SO4= BaSO4 ↓ +2H2 O
7、NaOH+BaCl2= Ba(OH)2+NaCl
8、2NaCl+Cu(NO 3) 2= 2Na NO3+CuCl2上述物质能发生化学反应的是: ____________________________5、6、因为---7和8:不符合复分解反应的条件。课内拓展
NaCI = Na+ + Cl-CuSO4 = Cu2+ + SO42-盐= +一、什么是盐盐是由金属阳离子(或铵根离子)和酸根离子组成的化合物。金属或铵根离子酸根离子Na2CO3 = 2 Na+ + CO32-(NH4)2SO4 = 2 NH4+ + SO42-思考:我们现在所说的盐是不是就是我们平时吃的食盐呢?盐不仅仅是食盐,食盐只是盐中的一种物质,而盐是一类物质 我国某地曾发生白色的工业用盐误作食盐食用引起的中毒事件,这种工业用盐是亚硝酸钠(化学式为 NaNO2 )悲剧自然界中有些盐晶体非常美丽你还见过其他盐的晶体?盐有什么性质?用途?二、几种盐的性质(一)碳酸钠(纯碱或苏打Na2CO3) ①晶体:Na2CO3·10H2O结晶水合物:含结晶水的化合物
说明:结晶水合物是具有一定组成的纯净物,化学式中的“.’表示结合,算相对分子量时,表示加。
结晶水:晶体从溶液中析出时结合的水分子。Na2CO3? 10H2O= Na2CO3+ 10H2O易风化(自然条件失去结晶水)风化是化学变化干燥环境里,碳酸钠晶体会逐渐失去结晶水而成为碳酸钠粉末 溶液变红可见:碳酸钠的水溶液呈碱性。这是纯碱名称的由来.②、碳酸钠与酸碱指示剂反应现象:______ 纯碱不是碱,而是盐注意碳酸钠溶液酚酞[实验]二、几种盐的性质及用途(一)碳酸钠(纯碱或苏打Na2CO3) ②水溶液显碱性①晶体:Na2CO3·10H2O易失去结晶水纯碱不是碱,而是盐(5)在常温下,放在干燥的空气里, Na2CO3·10H2O会逐渐失去结晶水而成为碳酸钠粉末。——风化(3)碳酸钠晶体的化学式:Na2CO3·10H2O;
相对分子质量为286(23×2+12+16×3+10×18),晶体中Na2CO3和H2O的质量比为106︰180,属纯净物。(4)结晶水合物:晶体里含有一定数目水分子的物质称为结晶水合物,所含的水称为结晶水。(2)碳酸钠从溶液中结晶析出时,晶体结合了一定数目的水分子,化学式是Na2CO3·10H2O。【例1】28.6克碳酸钠晶体(Na2CO3·10H2O)完全溶于71.4克水中,所得溶液的溶质质量分数为28.6%吗?【做一做】把3.1克氧化钠(Na2O)完全溶于46.9克水中,所得溶液的溶质质量分数为多少?答:不是28.6%,是10.6%。8%答:天安门汉白玉华表大理石贝壳珍珠 石灰石、大理石、白垩、汉白玉,贝壳虽外表不同,但主要成分都是CaCO3,化学性质相同(二)碳酸钙(CaCO3)
(大理石、石灰石的主要成分) 1、难溶于水,固体,白色2、工艺品、建筑材料、水泥3、高温分解:工业制取CO2H2CO3+Ca(OH)2==CaCO3↓+2H2O制取:思考:怎样证明一块岩石是碳酸盐?*用稀盐酸和澄清的石灰水,
(即检验CO32-)先加盐酸,再将产生气体通入澄清石灰水中,看是否有浑浊出现。大家叫我钟乳石、石柱、石笋,我的主要成分是碳酸钙,成长了n年,个子还不高,可我已经顶天立地了.不可否认我长得很丑,可是遇到酸,我也会很温柔石灰岩的主要成分是碳酸钙,碳酸钙遇到溶有二氧化碳的水时,会慢慢变成可溶于水的碳酸氢钙Ca(HCO3)2
CaCO3 + H2O + CO2 = Ca(HCO3)2
当受热或其他原因,水中碳酸氢钙会分解,重新变成碳酸钙沉积下来。
Ca(HCO3)2 = CaCO3↓ + CO2↑+ H2O
在自然界里不断发生上述反应,石灰岩逐渐变成碳酸氢钙而溶解掉,形成溶洞;碳酸氢钙不断分解,生成的碳酸钙逐渐沉积,形成千姿百态的钟乳石.石笋和石柱。 (3)溶洞的形成:(三) 氯化钠(NaCl) 俗称食盐1、食盐主要来自于海水、井水、盐湖水等(三)氯化钠(NaCl)俗称:食盐 2.物理性质:白色晶体,能溶于水3.用途:食用,防腐剂,重要化工原料,
制生理盐水( 0.9%的氯化钠溶液),杀菌等。 粗盐含MgCl2,CaCl2等杂质易潮解,精盐不易潮解。 日常生活中常用食盐水清洗伤口,你知道这是为什么吗? 思考与讨论: 为何用食盐腌过的肉类和蔬菜不易腐败?腊肉咸菜实验:收集一些汗液盛放在试管中,滴入几滴硝酸银溶液,有什么现象产生?
有白色沉淀生成NaCl+AgNO3==AgCl↓+NaNO3氯离子的鉴别方法:用硝酸银溶液和稀硝酸4、化学性质思考与讨论: 百度一下食盐在工业生产中的应用侯氏联合制碱法侯德榜,著名科学家,杰出的化工专家,我国重工业化学的开拓者。他于
20年代突破氨碱法制碱技术的奥秘,主持建成亚洲第一座纯碱厂;30年代领导建成了我国第一座兼产合成氨、硝酸、硫酸和硫酸铵的联合企业;四五十年代又发明了连续生产纯碱与氯化铵的联合制碱新工艺。
这个新工艺是把氨厂和碱厂建在一起,联合生产。由氨厂提供碱厂需要的氨和二氧化碳。母液里的氯化铵用加入食盐的办法使它结晶出来,作为化工产品或化肥。食盐溶液又可以循环使用。命名为“侯氏联合制碱法”。
侯德榜 鉴别氢氧化钠是否变质:
甲的做法:取样品加入蒸馏水,配成溶液,滴入酚酞试液,试液变红则说明没变质,试液不变色证明已变质.
乙的做法:加入盐酸,产生气泡证明变质,不产生气泡证明没变质.
思考:你还有什么方法证明它变质呢?若有变质如何除去杂质?碱溶钾钠钡钙铵大多酸溶水中间钾钠铵盐均易溶硝酸盐遇水影无踪氯化物不溶氯化银硫酸盐不溶硫酸钡碳酸盐只溶钾钠铵硫酸盐微溶是银钙课内练习1.证明生石灰( CaO)中是否含有未煅烧的石灰石(CaCO3)的方法,是滴加( ),若有( )产生,就证明生石灰中含有未煅烧的石灰石,有关化学方程式是( ).稀盐酸气泡CaCO3 + 2HCl === CaCl2 + H2O +CO2↑2.对人的生理活动关系最大的盐是( )A.Na2CO3 B.CaCO3 C.NaCl D.MgCl2C3.下列物质中不属于盐的是( )A.CuSO4 B.Na2S C.CaCl2 D.Ba(OH)2D1.6 几种重要的盐 第2课时 1.下列物质的名称、俗称、化学式三者都相符的是
A氢氧化钠、火碱、NaCl
B氧化钙、消石灰、CaO
C碳酸钠、纯碱、Na2CO3
D硫酸铜、胆矾、CuSO4·5H2O2、用做鉴别碳酸根离子的试剂是
(A)稀硫酸 (B)食盐水
(C)石灰水 (D)稀盐酸和澄清石灰水3、如何鉴别氯化钠、碳酸钠、硫酸钠三种无色溶液?复习三、盐的制取1.盐的溶解性(1) 盐分为_________盐和_______盐。(2)常见盐的溶解性表:钾、钠、硝、铵盐皆可溶,
氯化物不溶氯化银,硫酸盐不溶钡和银,
碳酸盐只溶钾钠铵。溶解性口诀可溶性不溶性碱只溶钾、钠、 钡、钙酸都可溶(除硅酸外)口诀二:钾钠硝铵皆可溶,硫酸铅钡两不溶;
盐酸不溶银亚汞,弱酸盐大多沉水中。常见碱盐的溶解性表根据溶解性口诀,判断下列物质的溶解性。1.Zn(OH)2:______ 2.AgCl:________
3.NaNO3:________ 4.K2CO3:________
5.BaSO4:________ 6.BaCl2:________
7.CaCO3:________ 8.Na2CO3:_______
9.CuCl2:________ 10.AgNO3:_______
11.BaCO3:_______ 12.Ma(OH)2:______
13.H2SO4:_______ 14.H3PO4:________不溶不溶不溶不溶不溶不溶溶溶溶溶溶溶溶溶2.复分解反应(1).[实验]在盛有Na2CO3溶液的试管里加入CaCl2溶液,可发现:________白色沉淀 Na2CO3+CaCl2 = CaCO3↓ +2NaCl这个反应的原理是怎样的? 盐 + 盐 = 新盐 + 新盐思考:除了酸与碱中和反应能生成盐外,还有其他什么方法能生成盐呢?Na2CO3溶液和CaCl2溶液反应原理 Na2CO3 溶液中
含有的离子 CaCl2溶液中
含有的离子 2Na+CO32— Ca2+2CI—Na2CO3+CaCl2 = CaCO3↓+ 2NaCl你能找出这个反应类型有什么特点?两种化合物互相交换成分生成新的化合物 Na2CO3+CaCl2 = CaCO3↓+ 2NaCl复分解反应。AB+CD==AD+CB2NaOH + H2SO4 = Na2SO4 + 2H2O Na2CO3+Ca(OH)2 = CaCO3↓ +2NaOH2HCl + CaCO3 = CaCl2 + H2O + CO2↑酸、碱、盐等物质之间是不是都能发生复分解反应?NaOH+BaCl2= Ba(OH)2+NaCl这个反应是不能进行。×Cu(OH)2+BaCl2= Ba(OH)2+CuCl2×复分解反应的条件: 2、反应物均可溶(酸参与除外)1、生成物有水或气体或沉淀复分解反应的实质: 阴、阳离子结合生成难电离的物质(水、气体、沉淀)H+ + OH- = H2O(中和反应)2H+ + CO32- = H2O+CO2↑
Ag+ + Cl- = AgCl↓ 酸碱反应是否是复分解反应?酸碱盐之间的反应一般是复分解反应。 复分解反应不一定是酸碱反应,而酸碱反应一定是复分解反应,即酸碱反应是复分解反应中的一种。下列方程式属酸碱反应的有______;属复分解的有_________; 1、BaCl2 + H2SO4 = BaSO4 ↓ + 2HCl
2、Na2CO3 + H2SO4 =Na2SO4 + CO2 ↑+ H2O
3、 Ca(OH)2 + H2SO4 == CaSO4 + 2H2O
4、 BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2
5、 (NH4)2SO4+Ca(OH)2==CaSO4+2NH3 ↑ +H2O
6、Na2CO3+ Ca(OH)2= CaCO3↓+H2O
3123456讨论:参照酸和碱性质的推断方法,你能否说说盐有哪些性质. 1、盐 + 酸 —— 新盐 + 新酸2、盐 + 碱 —— 新盐 + 新碱3、盐 + 盐 —— 新盐 + 新盐 盐的性质:CaCO3+2HCl=CaCl2+H2O+CO2↑Na2CO3+Ca(OH)2=CaCO3↓+2NaOHNaCl+AgNO3=AgCl↓+NaNO3 注意:2、3中的反应物(盐和碱)都必须溶于水。4、某些盐加热能分解 根据酸的共性和碱的共性,以及盐的有关性质,你知道可以用哪些方法制取盐?3.盐的制取有些盐是天然存在的。如:食盐、纯碱等,但有些是用化学方法制取。1、物理方法:结晶法(天然碱)2、化学方法:常用复分解反应盐的制取:1、物理方法:结晶法(天然碱) 酸 + 碱 —— 盐+水
盐 + 酸 —— 新盐 + 新酸
可溶性盐+可溶性碱 — 新盐+新碱
可溶性盐+可溶性盐 —新盐+新盐阅读:侯德榜“庄稼一枝花,全靠肥当家”1.什么是化肥? 化学肥料是用矿物质、空气、水等作原料,经过化学加工精制而成的肥料。2.化肥有哪些类型?氮肥:化肥主要含有氮元素的称氮肥。磷肥:化肥主要含有磷元素的称磷肥。钾肥:化肥主要含有氮元素的称钾肥。复合肥:化肥中含有两种或两种以上
主要营养元素的称复合肥。四、盐与化肥读图,连线3.化肥的作用与制取能促使农作物的茎叶生长茂盛,含有组成叶绿素的重要元素氮 肥(1)作用:(2)氮肥(铵盐)的制取:常用酸与氨气反应制取NH3+H2O+CO2=NH4HCO3(碳铵)2NH3+H2SO4=(NH4)2SO4(硫铵)因此:盐的组成中,所含的阳离子不一定都是金属阳离子,也可以是复杂阳离子(带电原子团)(3) 氮肥的种类:除铵盐外还有最常用的氮肥:是含氮有机物即人的尿液化 肥:尿素 CO(NH2)2尿素在微生物中作用下会转变为铵盐或氨气磷 肥促进农作物要根系发达,增强吸收养份和抗寒抗旱能力,促进作物穗数增多,籽粒饱满等。过磷酸钙:
CaSO4和Ca (H2PO4)2的混合物3.化肥的作用与制取(1)作用:(2)种类:3.化肥的作用与制取钾 肥(1)作用:促进农作物生长旺盛,茎杆粗壮,增强抗病虫害能力,促进糖和淀粉的生成。(2)种类:硫酸钾(K2SO4)、氯化钾(KCI)、 草木灰(成份K2CO3)4. 使用化肥时注意: 长期使用会造成土壤板结,破坏土壤结构。 1.小明家是种植蔬菜的专业户,他学习了初三科学后告诉父母:施用适量的氮肥可以使种植的蔬菜叶色浓绿。因此,
(1)他建议其父母去买的氮肥的是 。
A、碳酸氢铵[NH4HCO3] B、硫酸钾[K2SO4]
C、磷矿粉 [Ca3(PO4)2]
(2)他还告戒父母在施用氮肥的同时 (填“能”或“不能”)施用草木灰(呈碱性) 。
理由是
。
(3)他还建议父母经常向大棚中补充气体肥料CO2,目的是促进绿色植物 作用。A不能草木灰和他们买的氮肥混合使用会放出氨气,降低氮肥肥效光合课内练习2.已知可溶性钡盐有毒,而在医院里做胃镜透视时,要用BaSO4造影,俗称“钡餐”,吃下BaSO4无毒是因为( )。但如果无意中误服了BaCO3则会引起中毒,这是因为(用化学方程式表示,下同)( ),误服后, 应立即用泻盐MgSO4解毒,这是因为( )。BaSO4不溶于水,也不与酸反应式BaCO3+ 2HCl ==== BaCl2 + H2O +CO2↑BaCl2 + MgSO4 ==== BaSO4 ↓ + MgCl2课内练习下列物质能发生化学反应吗?为什么?1、CuO+Ba(OH)2= Cu(OH)2 ↓ +BaO
2、SO2+HNO3=NO2 + H2SO3
3、2Fe(OH)3+3MgCl2=2FeCl3+3Mg (OH)2 ↓
4、Na2CO3+CaCl2 = CaCO3 ↓ +2NaCl上述物质能发生化学反应的是: ___________________________4因为---1:碱不能与金属氧化物反应。2:酸不能与非金属氧化物反应。3:Fe(OH)3难溶课内拓展下列物质能发生化学反应吗?为什么?5、Na2CO3+2HCl= 2Na Cl +H2O+ CO2↑
6、 Ba(OH)2+H2SO4= BaSO4 ↓ +2H2 O
7、NaOH+BaCl2= Ba(OH)2+NaCl
8、2NaCl+Cu(NO 3) 2= 2Na NO3+CuCl2上述物质能发生化学反应的是: ____________________________5、6、因为---7和8:不符合复分解反应的条件。课内拓展
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
