必修1 3.3 硫的转化 同步练习 (含答案解析) (2)
文档属性
| 名称 | 必修1 3.3 硫的转化 同步练习 (含答案解析) (2) |

|
|
| 格式 | zip | ||
| 文件大小 | 132.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-09-09 00:00:00 | ||
图片预览

文档简介
第三节
硫的转化
同步练习
1.SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02
mg/L。下列措施中能够减少SO2
排放量的是( )
①用天然气代替煤炭做民用燃料 ②提高热能利用率 ③硫酸厂采用更好的催化剂使SO2氧化成SO3 ④使用CS2萃取煤炭中的硫 ⑤燃煤中加入石灰后再使用
A.①②⑤
B.①③⑤
C.①③④
D.③④⑤
2.下列关于浓硫酸的叙述正确的是( )
A.浓硫酸具有吸水性,因而能使蔗糖碳化
B.浓硫酸在常温时可以与木炭反应
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
3.将浓硫酸和2
mol/L的硫酸在实验室中敞口放置。它们的质量和放置天数的关系如下图所示。分析a、b曲线变化的原因是( )
A.a升华、b冷凝
B.a挥发、b吸水
C.a蒸发、b潮解
D.a冷凝、b吸水
4.(富阳高一质检)将过量的金属锌投入到含0.200
mol
H2SO4的热浓硫酸中,下列判断正确的是(双选)( )
A.因发生“钝化”而不反应
B.产生的SO2为0.100
mol
C.产生的SO2少于0.100
mol
D.除SO2外还会有H2产生
5.m
g铜与足量的浓H2SO4共热时完全反应,在标准状况下生成n
L气体,则被还原的H2SO4的量是(双选)( )
A.
mol
B.
mol
C.
g
D.
g
6.(常德高一质检)三位学生设计了下述三个方案,并都认为,如果观察到的现象和自己设计的方案一致,即可确定试液中有SO。
方案甲:试液白色沉淀沉淀不溶解
方案乙:试液无沉淀白色沉淀
方案丙:试液无沉淀白色沉淀
试评价上述各种方案是否严密,并分别说明理由。
方案甲:
______________________________________________________
________________________________________________________________。
方案乙:
_____________________
_______________________________
________________________________________________________________。
方案丙:
________________________________
_________________
________________________________________________________________。
7.(长沙高一质检)(1)浓硫酸与木炭粉在加热条件下反应的化学方程式为__________________________________________________________________。
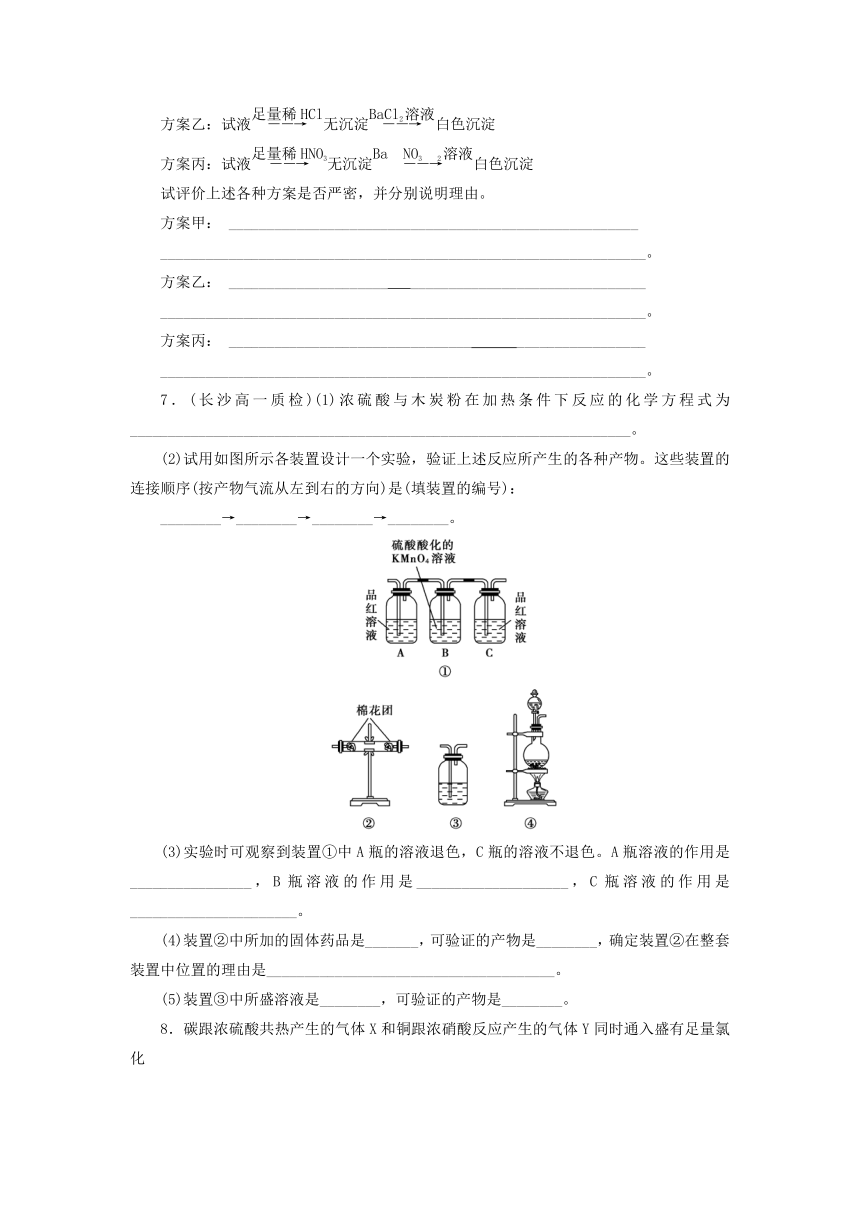
(2)试用如图所示各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):
________→________→________→________。
(3)实验时可观察到装置①中A瓶的溶液退色,C瓶的溶液不退色。A瓶溶液的作用是________________,B瓶溶液的作用是____________________,C瓶溶液的作用是______________________。
(4)装置②中所加的固体药品是_______,可验证的产物是________,确定装置②在整套装置中位置的理由是______________________________________。
(5)装置③中所盛溶液是________,可验证的产物是________。
8.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化
钡溶液的洗气瓶中(如图装置),下列有关说法正确的是(双选)( )
A.洗气瓶中产生的沉淀是碳酸钡
B.在Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是硫酸钡
D.在Z导管口有红棕色气体出现
9.A~H等8种物质存在如下图所示转化关系(反应条件、部分产物未标出)。已知:A是正盐,B是能使品红溶液退色的气体,G是红棕色气体。按要求回答问题:
(1)写出下列物质的化学式:
A________,B________,C________。
(2)写出下列反应的化学方程式:
E―→F__________________________________________________________;
G―→H_________________________________________________________;
D的浓溶液与木炭反应的方程式:
________________________________________________________________。
(3)检验某溶液中是否含D中阴离子的方法是
________________________________________________________________。
参考答案
1.答案: A
2.解析: 使蔗糖碳化这是浓硫酸显示了脱水性。浓硫酸与木炭的反应需要加热,在常温下不反应。浓硫酸是一种干燥剂,但它是具有强氧化性和酸性的干燥剂,因其有酸性,所以不能干燥具有碱性的氨气。
答案: D
3.解析: 图中a曲线为稀硫酸,其质量减小,原因是溶液中的水蒸发了,b曲线为浓硫酸,其质量增加,原因是其吸收了空气中的水。
答案: B
4.解析: 锌与浓硫酸不会“钝化”,故A选项不正确;开始发生:Zn+2H2SO4ZnSO4+SO2↑+2H2O,随反应进行,H2SO4浓度变稀,又发生反应:Zn+H2SO4===ZnSO4+H2↑,因生成SO2的反应中消耗H2SO4的物质的量不到0.200
mol,故生成的SO2少于0.100
mol,因此本题C、D选项正确。
答案: CD
5.解析: Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O
mol
mol
参加反应的Cu、生成的SO2与被还原的H2SO4的物质的量相等。
答案: BC
6.答案: 方案甲:不严密。因为含有Ag+而不含SO的无色透明溶液,也会出现此方案的现象
方案乙:严密。因为只有含有SO的无色透明溶液才会出现此方案的现象
方案丙:不严密。因为含有SO而不含SO的无色透明溶液,也会出现此方案的现象
7.解析: 由题中所给的各种装置可知:④是反应发生器;①中有品红溶液,是用来验证SO2的装置;③中装有某种水溶液,显然③可用来验证CO2;②可验证水蒸气。由于①、③中装的都是水溶液,气流经过后一定会带出水蒸气,所以必须先用②验证产物中的水蒸气,然后再验证SO2和CO2,不然就不能确定水蒸气一定是反应产物;由于SO2和CO2都能与石灰水反应,使澄清的石灰水变浑浊,因此从②出来的气体必须先经过①验证和除去SO2后,再进入③,验证CO2,由此可以得出正确的连接顺序应当是④②①③。
答案: (1)C+2H2SO4(浓)2SO2↑+CO2↑+2H2O
(2)④ ② ① ③ (3)验证产物中有SO2 将SO2全部氧化吸收 确定产物中SO2已被B瓶溶液全部吸收 (4)无水CuSO4 水蒸气 气流通过①、③时会带出水蒸气,所以②必须放在①、③之前 (5)澄清石灰水 CO2
8.解析: Cu与浓HNO3反应后生成NO2,通入BaCl2溶液后生成硝酸,同时生成NO,C与浓H2SO4反应后生成了CO2、SO2。混合气体通入BaCl2溶液后SO2被氧化成H2SO4,故有BaSO4沉淀生成,但在酸性条件下不会生成BaCO3沉淀。所以选项A、B不正确,选项C正确,选项D正确,NO遇O2生成红棕色NO2气体。
答案: CD
9.解析: 本题有两个较为明显的突破口。根据“B是能使品红溶液退色的气体”可知B是SO2气体,则C是SO3,D是硫酸。根据“G是红棕色气体”可知G是NO2气体,逆推,F是NO气体,E是NH3。A能与硫酸反应放出SO2,其阴离子必然是亚硫酸根离子或亚硫酸氢根离子,但已知A是正盐,可以确定其阴离子是亚硫酸根离子;同时A又能与NaOH溶液反应放出氨气,A中必然含有铵根离子。由此判断A为(NH4)2SO3。
答案: (1)(NH4)2SO3 SO2 SO3 (2)4NH3+5O24NO+6H2O 3NO2+H2O===2HNO3+NO C+2H2SO4(浓)CO2↑+2SO2↑+2H2O (3)取少量该溶液于试管中,加足量稀盐酸酸化,未见白色沉淀产生。再加入少量BaCl2溶液,如果出现白色沉淀,则证明含有SO
硫的转化
同步练习
1.SO2是常见的大气污染物之一,我国规定空气中SO2含量不得超过0.02
mg/L。下列措施中能够减少SO2
排放量的是( )
①用天然气代替煤炭做民用燃料 ②提高热能利用率 ③硫酸厂采用更好的催化剂使SO2氧化成SO3 ④使用CS2萃取煤炭中的硫 ⑤燃煤中加入石灰后再使用
A.①②⑤
B.①③⑤
C.①③④
D.③④⑤
2.下列关于浓硫酸的叙述正确的是( )
A.浓硫酸具有吸水性,因而能使蔗糖碳化
B.浓硫酸在常温时可以与木炭反应
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
3.将浓硫酸和2
mol/L的硫酸在实验室中敞口放置。它们的质量和放置天数的关系如下图所示。分析a、b曲线变化的原因是( )
A.a升华、b冷凝
B.a挥发、b吸水
C.a蒸发、b潮解
D.a冷凝、b吸水
4.(富阳高一质检)将过量的金属锌投入到含0.200
mol
H2SO4的热浓硫酸中,下列判断正确的是(双选)( )
A.因发生“钝化”而不反应
B.产生的SO2为0.100
mol
C.产生的SO2少于0.100
mol
D.除SO2外还会有H2产生
5.m
g铜与足量的浓H2SO4共热时完全反应,在标准状况下生成n
L气体,则被还原的H2SO4的量是(双选)( )
A.
mol
B.
mol
C.
g
D.
g
6.(常德高一质检)三位学生设计了下述三个方案,并都认为,如果观察到的现象和自己设计的方案一致,即可确定试液中有SO。
方案甲:试液白色沉淀沉淀不溶解
方案乙:试液无沉淀白色沉淀
方案丙:试液无沉淀白色沉淀
试评价上述各种方案是否严密,并分别说明理由。
方案甲:
______________________________________________________
________________________________________________________________。
方案乙:
_____________________
_______________________________
________________________________________________________________。
方案丙:
________________________________
_________________
________________________________________________________________。
7.(长沙高一质检)(1)浓硫酸与木炭粉在加热条件下反应的化学方程式为__________________________________________________________________。
(2)试用如图所示各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):
________→________→________→________。
(3)实验时可观察到装置①中A瓶的溶液退色,C瓶的溶液不退色。A瓶溶液的作用是________________,B瓶溶液的作用是____________________,C瓶溶液的作用是______________________。
(4)装置②中所加的固体药品是_______,可验证的产物是________,确定装置②在整套装置中位置的理由是______________________________________。
(5)装置③中所盛溶液是________,可验证的产物是________。
8.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化
钡溶液的洗气瓶中(如图装置),下列有关说法正确的是(双选)( )
A.洗气瓶中产生的沉淀是碳酸钡
B.在Z导管出来的气体中无二氧化碳
C.洗气瓶中产生的沉淀是硫酸钡
D.在Z导管口有红棕色气体出现
9.A~H等8种物质存在如下图所示转化关系(反应条件、部分产物未标出)。已知:A是正盐,B是能使品红溶液退色的气体,G是红棕色气体。按要求回答问题:
(1)写出下列物质的化学式:
A________,B________,C________。
(2)写出下列反应的化学方程式:
E―→F__________________________________________________________;
G―→H_________________________________________________________;
D的浓溶液与木炭反应的方程式:
________________________________________________________________。
(3)检验某溶液中是否含D中阴离子的方法是
________________________________________________________________。
参考答案
1.答案: A
2.解析: 使蔗糖碳化这是浓硫酸显示了脱水性。浓硫酸与木炭的反应需要加热,在常温下不反应。浓硫酸是一种干燥剂,但它是具有强氧化性和酸性的干燥剂,因其有酸性,所以不能干燥具有碱性的氨气。
答案: D
3.解析: 图中a曲线为稀硫酸,其质量减小,原因是溶液中的水蒸发了,b曲线为浓硫酸,其质量增加,原因是其吸收了空气中的水。
答案: B
4.解析: 锌与浓硫酸不会“钝化”,故A选项不正确;开始发生:Zn+2H2SO4ZnSO4+SO2↑+2H2O,随反应进行,H2SO4浓度变稀,又发生反应:Zn+H2SO4===ZnSO4+H2↑,因生成SO2的反应中消耗H2SO4的物质的量不到0.200
mol,故生成的SO2少于0.100
mol,因此本题C、D选项正确。
答案: CD
5.解析: Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O
mol
mol
参加反应的Cu、生成的SO2与被还原的H2SO4的物质的量相等。
答案: BC
6.答案: 方案甲:不严密。因为含有Ag+而不含SO的无色透明溶液,也会出现此方案的现象
方案乙:严密。因为只有含有SO的无色透明溶液才会出现此方案的现象
方案丙:不严密。因为含有SO而不含SO的无色透明溶液,也会出现此方案的现象
7.解析: 由题中所给的各种装置可知:④是反应发生器;①中有品红溶液,是用来验证SO2的装置;③中装有某种水溶液,显然③可用来验证CO2;②可验证水蒸气。由于①、③中装的都是水溶液,气流经过后一定会带出水蒸气,所以必须先用②验证产物中的水蒸气,然后再验证SO2和CO2,不然就不能确定水蒸气一定是反应产物;由于SO2和CO2都能与石灰水反应,使澄清的石灰水变浑浊,因此从②出来的气体必须先经过①验证和除去SO2后,再进入③,验证CO2,由此可以得出正确的连接顺序应当是④②①③。
答案: (1)C+2H2SO4(浓)2SO2↑+CO2↑+2H2O
(2)④ ② ① ③ (3)验证产物中有SO2 将SO2全部氧化吸收 确定产物中SO2已被B瓶溶液全部吸收 (4)无水CuSO4 水蒸气 气流通过①、③时会带出水蒸气,所以②必须放在①、③之前 (5)澄清石灰水 CO2
8.解析: Cu与浓HNO3反应后生成NO2,通入BaCl2溶液后生成硝酸,同时生成NO,C与浓H2SO4反应后生成了CO2、SO2。混合气体通入BaCl2溶液后SO2被氧化成H2SO4,故有BaSO4沉淀生成,但在酸性条件下不会生成BaCO3沉淀。所以选项A、B不正确,选项C正确,选项D正确,NO遇O2生成红棕色NO2气体。
答案: CD
9.解析: 本题有两个较为明显的突破口。根据“B是能使品红溶液退色的气体”可知B是SO2气体,则C是SO3,D是硫酸。根据“G是红棕色气体”可知G是NO2气体,逆推,F是NO气体,E是NH3。A能与硫酸反应放出SO2,其阴离子必然是亚硫酸根离子或亚硫酸氢根离子,但已知A是正盐,可以确定其阴离子是亚硫酸根离子;同时A又能与NaOH溶液反应放出氨气,A中必然含有铵根离子。由此判断A为(NH4)2SO3。
答案: (1)(NH4)2SO3 SO2 SO3 (2)4NH3+5O24NO+6H2O 3NO2+H2O===2HNO3+NO C+2H2SO4(浓)CO2↑+2SO2↑+2H2O (3)取少量该溶液于试管中,加足量稀盐酸酸化,未见白色沉淀产生。再加入少量BaCl2溶液,如果出现白色沉淀,则证明含有SO
