浙教版九年级(上)课堂同步练习:第一章 第3节 常见的酸(第2课时)
文档属性
| 名称 | 浙教版九年级(上)课堂同步练习:第一章 第3节 常见的酸(第2课时) |

|
|
| 格式 | zip | ||
| 文件大小 | 315.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2016-09-11 00:00:00 | ||
图片预览


文档简介
第3节 常见的酸(第2课时)
一、稀硫酸的化学性质
1.跟指示剂的反应:使紫色石蕊试液变________;遇无色酚酞试液________。
2.跟金属的反应:H2SO4+Zn===______________。
3.跟金属氧化物的反应:Fe2O3+3H2SO4===________________。
二、浓硫酸
1.浓硫酸(通常浓度为98%)为无色黏稠油状液体,无________性,无气味。
2.浓硫酸具有________,故可作干
( http: / / www.21cnjy.com )燥剂,可以干燥H2、O2、CO2、CO等气体,但不可以干燥NH3、H2S等气体,因为硫酸可以与它们发生反应。
3.浓硫酸具有________________。
4.因浓硫酸具有强烈的________(从脱水导致的效果而言),如果不慎将浓硫酸沾在皮肤或衣服上,应________________,用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液。
5.浓硫酸的稀释。由于浓硫酸溶于水时会放出
( http: / / www.21cnjy.com )大量的热,因而在稀释浓硫酸时,一定要将浓硫酸________________________,使产生的热量迅速扩散,____________________。
6.H2SO4+Ba(NO3)2===________________。
常用Ba(NO3)2溶液和稀硝酸检验SO。
A组 基础训练
1.(苏州中考模拟)下列有关酸的性质说法正确的是(
)
A.浓盐酸、浓硫酸都能使纸张炭化
B.稀盐酸和稀硫酸都可用于除铁锈
C.浓盐酸、浓硫酸都可用来干燥氧气
D.打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
2.有三种液体:①盐酸;②氢氧化钠溶液;③水。它们的pH值由大到小的排列顺序是(
)
A.①③②
B.①②③
C.②③①
D.③②①
3.下列氧化物中,不能跟稀硫酸反应的是(
)
A.氧化钙
B.二氧化碳
C.氧化铜
D.氧化铁
4.有关浓硫酸的说法,错误的是(
)
A.浓硫酸具有吸水性,在实验室中常用作干燥剂
B.浓硫酸具有强腐蚀性,它能使纸张、布料、皮肤等脱水炭化
C.浓硫酸溶于水时会吸收大量的热,可作制冷剂
D.如果不慎将浓硫酸沾到皮肤或衣服上,应迅速用抹布擦拭,然后用大量水冲洗,再涂3%~5%的碳酸氢钠溶液
5.(上海中考)用稀硫酸除铁锈的原理是(
)
A.FeO+H2SO4→FeSO4+H2O
B.Fe2O3+3H2SO4→Fe2(SO4)3+3H2↑
C.Fe2O3+2H2SO4→2FeSO4+2H2O
D.Fe2O3+3H2SO4→Fe2(SO4)3+3H2O
6.(金华中考)为区别稀盐
( http: / / www.21cnjy.com )酸和稀硫酸,小强同学设计如图所示的实验方案:在每组的两支试管中分别盛放稀盐酸和稀硫酸;向同组的两支试管各滴加同种试剂。其中能达到实验目的的是(
)
7.(株洲市天元区中考模拟)把一根洁净的铁钉放入稀硫酸中,下列叙述正确的是( )
①在铁钉表面产生气泡 ②溶液由无色逐渐变为浅绿色 ③铁钉的质量增加 ④溶液的质量减轻
A.②③
B.①②③
C.①②④
D.①②
第8题图
8.要使如图装置中的小气球明显鼓起来,则使用的固体和液体可以是(
)
①锌和稀硫酸;②石灰石和稀盐酸;③氧化铁和硫酸;④食盐和水。
A.①②
B.①②③
C.①②④
D.①②③④
9.某化工厂发生硫酸泄漏事件,为了减少硫酸对环境的污染,可以在泄漏的硫酸上喷洒一种化学试剂,这种试剂可以是(
)
A.硫酸铜
B.食盐
C.熟石灰
D.水
10.有甲、乙、丙三种溶液,它们是H2
( http: / / www.21cnjy.com )SO4、NaCl、NaOH中的任一种。将无色酚酞试液滴入乙溶液中,溶液呈红色;取此红色溶液少量,滴加到甲溶液中仍显红色,则甲、乙、丙三种溶液依次是( )
A.H2SO4、NaOH、NaCl
B.NaCl、NaOH、H2SO4
C.NaOH、NaCl、H2SO4
D.NaCl、H2SO4、NaOH
11.盐酸、稀硫酸在水溶液中都能产生H+,故有许多共同的性质。下列有关叙述正确的是(
)
A.打开盛有浓硫酸和浓盐酸的试剂瓶瓶塞,在瓶口都有白雾
B.稀盐酸和稀硫酸都可用于除铁锈
C.浓盐酸、浓硫酸都可用来干燥氧气
D.在稀盐酸、稀硫酸中滴加氢氧化钡溶液,都有白色沉淀
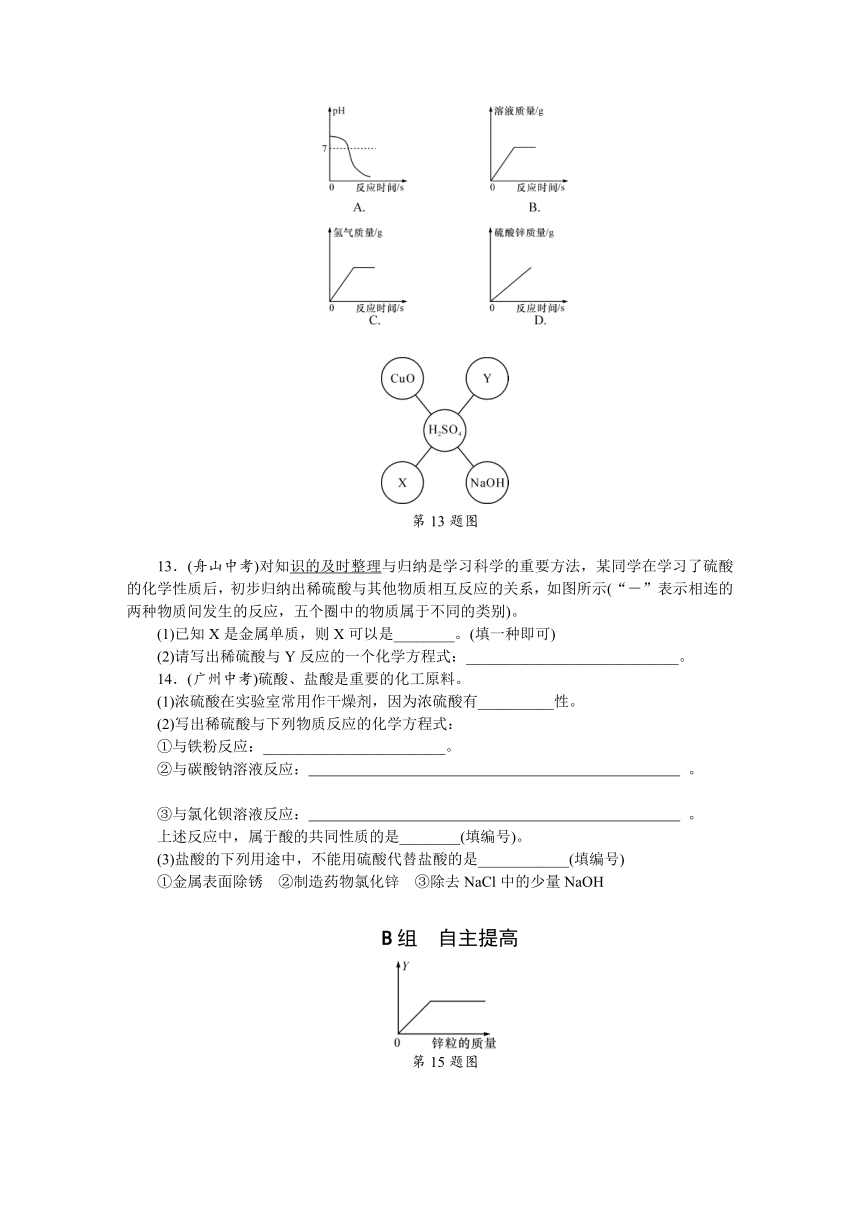
12.向一定质量的稀硫酸中加入锌粉至过量,下列图像合理的是(
)
第13题图
13.(舟山中考)对知识的及时整理
( http: / / www.21cnjy.com )与归纳是学习科学的重要方法,某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“-”表示相连的两种物质间发生的反应,五个圈中的物质属于不同的类别)。
(1)已知X是金属单质,则X可以是________。(填一种即可)
(2)请写出稀硫酸与Y反应的一个化学方程式:____________________________。
14.(广州中考)硫酸、盐酸是重要的化工原料。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有__________性。
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应:________________________。
②与碳酸钠溶液反应:
。
③与氯化钡溶液反应:
。
上述反应中,属于酸的共同性质的是________(填编号)。
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是____________(填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
B组 自主提高
第15题图
15.(舟山中考)往一定量的稀硫酸中加入过量的锌粒,如图是反应过程中某种量Y随加入锌粒的质量变化的关系,则Y不可能表示(
)
A.硫酸的质量分数
B.生成硫酸锌的质量
C.溶液的Ph
D.生成氢气的质量
第16题图
16.如图是两种稀酸与铁铬合金反应随铬(Cr)的质量分数变化的实验结果(铬与稀酸反应)。下列有关说法错误的是( )
A.稀硫酸、稀盐酸中的阳离子都是H+
B.图中的“5%”表示酸溶液中溶质的质量分数
C.同一种酸与铁铬合金的反应速度随着Cr质量分数的增加一直加快
D.与相同铁铬合金反应,5%硫酸比5%盐酸反应快
第17题图
17.实验室中有一瓶标签受损的无色
( http: / / www.21cnjy.com )液体,如图所示。这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸和蒸馏水中的一种。
(1)大家讨论后一致认为不可能是蒸馏水,理由是
___________________________________________________________________
_____。
(2)为确定该液体成分,同学们继续进行了如下实验探究:
实验操作
实验现象
实验结论
步骤一:取该液体适量于试管中,向其中加入少量________粉末。
没有气泡产生
该液体不是过氧化氢溶液。
步骤二:取该液体适量于试管中,向其中滴加少量氯化钡溶液。
____________
该液体是稀硫酸。
【反思交流】
(1)大家认为标签受损的原因可能是
;
(2)如果该液体是过氧化氢溶液,则步骤一中产生的变化用化学方程式表示为
__________
__________。
18.(温州中考)小明为了测定某钙片中碳酸钙的质量分数,用如图装置进行如下实验:
①取研碎后的钙片4克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量。
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量。
③整理相关数据如表所示,计算出钙片中碳酸钙的质量分数。
反应前总质量(克)
275.58
反应后总质量(克)
274.92
反应前后总质量差(克)
0.66
容器内气体质量差(克)
m
(1)该实验中,对装置中的固态干燥剂的性质有何要求?
________________________________________________________________________。
(2)反应前容器内是空气(密度为ρ1)
( http: / / www.21cnjy.com ),反应后全部是二氧化碳(密度为ρ2),则反应前后容器(容积为V)内的气体质量差m为____________。(用字母表示,反应物的体积忽略不计)
(3)小明查阅有关数据后,计算出反应前
( http: / / www.21cnjy.com )后容器内的气体质量差m为0.22克,结合表中数据,计算该钙片中碳酸钙的质量分数。(CaCO3+2HCl===CaCl2+H2O+CO2↑)。钙片中的其他成分不与盐酸反应。
第18题图
第3节 常见的酸(第2课时)
【课堂笔记】
一、1.红色 不变色 2.ZnSO4+H2↑
3.Fe2(SO4)3+3H2O
二、1.挥发 2.吸水性 3.脱水性 4.腐蚀性 迅速用抹布擦拭 5.沿着器壁慢慢地注入水里,并不断搅动 切不可将水倒进浓硫酸里
6.BaSO4↓+2HNO3
【课时训练】
1-5.BCBCD 6-10.DDACB 11-12.BC
13.(1)锌等 (2)BaCl2+H2SO4===BaSO4↓+2HCl(合理即可)
14.(1)吸水 (2)①Fe+H2SO4===FeSO4+H2↑
②Na2CO3+H2SO4===Na2SO4+H2O+CO2↑ ③H2SO4+BaCl2===BaSO4↓+2HCl ①②
(3)②③
15.A 16.C
17.(1)由标签知该液体是混合物
( http: / / www.21cnjy.com ),而蒸馏水为纯净物(答案合理即可) (2)二氧化锰(或MnO2) 产生白色沉淀 【反思交流】(1)倾倒液体时标签未朝向手心(答案合理均可) (2)2H2O22H2O+O2↑
18.(1)能吸收水但不吸收二氧化碳 (2)(ρ2-ρ1)V
(3)设钙片中碳酸钙的质量为x
反应后生成的二氧化碳的质量为:0.66g+0.22g=0.88g
CaCO3+2HCl===CaCl2+H2O+CO2↑
100
44
x
0.88g
= 解得:x=2g
该钙片中碳酸钙的质量分数为:×100%=50%
一、稀硫酸的化学性质
1.跟指示剂的反应:使紫色石蕊试液变________;遇无色酚酞试液________。
2.跟金属的反应:H2SO4+Zn===______________。
3.跟金属氧化物的反应:Fe2O3+3H2SO4===________________。
二、浓硫酸
1.浓硫酸(通常浓度为98%)为无色黏稠油状液体,无________性,无气味。
2.浓硫酸具有________,故可作干
( http: / / www.21cnjy.com )燥剂,可以干燥H2、O2、CO2、CO等气体,但不可以干燥NH3、H2S等气体,因为硫酸可以与它们发生反应。
3.浓硫酸具有________________。
4.因浓硫酸具有强烈的________(从脱水导致的效果而言),如果不慎将浓硫酸沾在皮肤或衣服上,应________________,用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液。
5.浓硫酸的稀释。由于浓硫酸溶于水时会放出
( http: / / www.21cnjy.com )大量的热,因而在稀释浓硫酸时,一定要将浓硫酸________________________,使产生的热量迅速扩散,____________________。
6.H2SO4+Ba(NO3)2===________________。
常用Ba(NO3)2溶液和稀硝酸检验SO。
A组 基础训练
1.(苏州中考模拟)下列有关酸的性质说法正确的是(
)
A.浓盐酸、浓硫酸都能使纸张炭化
B.稀盐酸和稀硫酸都可用于除铁锈
C.浓盐酸、浓硫酸都可用来干燥氧气
D.打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
2.有三种液体:①盐酸;②氢氧化钠溶液;③水。它们的pH值由大到小的排列顺序是(
)
A.①③②
B.①②③
C.②③①
D.③②①
3.下列氧化物中,不能跟稀硫酸反应的是(
)
A.氧化钙
B.二氧化碳
C.氧化铜
D.氧化铁
4.有关浓硫酸的说法,错误的是(
)
A.浓硫酸具有吸水性,在实验室中常用作干燥剂
B.浓硫酸具有强腐蚀性,它能使纸张、布料、皮肤等脱水炭化
C.浓硫酸溶于水时会吸收大量的热,可作制冷剂
D.如果不慎将浓硫酸沾到皮肤或衣服上,应迅速用抹布擦拭,然后用大量水冲洗,再涂3%~5%的碳酸氢钠溶液
5.(上海中考)用稀硫酸除铁锈的原理是(
)
A.FeO+H2SO4→FeSO4+H2O
B.Fe2O3+3H2SO4→Fe2(SO4)3+3H2↑
C.Fe2O3+2H2SO4→2FeSO4+2H2O
D.Fe2O3+3H2SO4→Fe2(SO4)3+3H2O
6.(金华中考)为区别稀盐
( http: / / www.21cnjy.com )酸和稀硫酸,小强同学设计如图所示的实验方案:在每组的两支试管中分别盛放稀盐酸和稀硫酸;向同组的两支试管各滴加同种试剂。其中能达到实验目的的是(
)
7.(株洲市天元区中考模拟)把一根洁净的铁钉放入稀硫酸中,下列叙述正确的是( )
①在铁钉表面产生气泡 ②溶液由无色逐渐变为浅绿色 ③铁钉的质量增加 ④溶液的质量减轻
A.②③
B.①②③
C.①②④
D.①②
第8题图
8.要使如图装置中的小气球明显鼓起来,则使用的固体和液体可以是(
)
①锌和稀硫酸;②石灰石和稀盐酸;③氧化铁和硫酸;④食盐和水。
A.①②
B.①②③
C.①②④
D.①②③④
9.某化工厂发生硫酸泄漏事件,为了减少硫酸对环境的污染,可以在泄漏的硫酸上喷洒一种化学试剂,这种试剂可以是(
)
A.硫酸铜
B.食盐
C.熟石灰
D.水
10.有甲、乙、丙三种溶液,它们是H2
( http: / / www.21cnjy.com )SO4、NaCl、NaOH中的任一种。将无色酚酞试液滴入乙溶液中,溶液呈红色;取此红色溶液少量,滴加到甲溶液中仍显红色,则甲、乙、丙三种溶液依次是( )
A.H2SO4、NaOH、NaCl
B.NaCl、NaOH、H2SO4
C.NaOH、NaCl、H2SO4
D.NaCl、H2SO4、NaOH
11.盐酸、稀硫酸在水溶液中都能产生H+,故有许多共同的性质。下列有关叙述正确的是(
)
A.打开盛有浓硫酸和浓盐酸的试剂瓶瓶塞,在瓶口都有白雾
B.稀盐酸和稀硫酸都可用于除铁锈
C.浓盐酸、浓硫酸都可用来干燥氧气
D.在稀盐酸、稀硫酸中滴加氢氧化钡溶液,都有白色沉淀
12.向一定质量的稀硫酸中加入锌粉至过量,下列图像合理的是(
)
第13题图
13.(舟山中考)对知识的及时整理
( http: / / www.21cnjy.com )与归纳是学习科学的重要方法,某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“-”表示相连的两种物质间发生的反应,五个圈中的物质属于不同的类别)。
(1)已知X是金属单质,则X可以是________。(填一种即可)
(2)请写出稀硫酸与Y反应的一个化学方程式:____________________________。
14.(广州中考)硫酸、盐酸是重要的化工原料。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有__________性。
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应:________________________。
②与碳酸钠溶液反应:
。
③与氯化钡溶液反应:
。
上述反应中,属于酸的共同性质的是________(填编号)。
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是____________(填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
B组 自主提高
第15题图
15.(舟山中考)往一定量的稀硫酸中加入过量的锌粒,如图是反应过程中某种量Y随加入锌粒的质量变化的关系,则Y不可能表示(
)
A.硫酸的质量分数
B.生成硫酸锌的质量
C.溶液的Ph
D.生成氢气的质量
第16题图
16.如图是两种稀酸与铁铬合金反应随铬(Cr)的质量分数变化的实验结果(铬与稀酸反应)。下列有关说法错误的是( )
A.稀硫酸、稀盐酸中的阳离子都是H+
B.图中的“5%”表示酸溶液中溶质的质量分数
C.同一种酸与铁铬合金的反应速度随着Cr质量分数的增加一直加快
D.与相同铁铬合金反应,5%硫酸比5%盐酸反应快
第17题图
17.实验室中有一瓶标签受损的无色
( http: / / www.21cnjy.com )液体,如图所示。这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸和蒸馏水中的一种。
(1)大家讨论后一致认为不可能是蒸馏水,理由是
___________________________________________________________________
_____。
(2)为确定该液体成分,同学们继续进行了如下实验探究:
实验操作
实验现象
实验结论
步骤一:取该液体适量于试管中,向其中加入少量________粉末。
没有气泡产生
该液体不是过氧化氢溶液。
步骤二:取该液体适量于试管中,向其中滴加少量氯化钡溶液。
____________
该液体是稀硫酸。
【反思交流】
(1)大家认为标签受损的原因可能是
;
(2)如果该液体是过氧化氢溶液,则步骤一中产生的变化用化学方程式表示为
__________
__________。
18.(温州中考)小明为了测定某钙片中碳酸钙的质量分数,用如图装置进行如下实验:
①取研碎后的钙片4克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量。
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量。
③整理相关数据如表所示,计算出钙片中碳酸钙的质量分数。
反应前总质量(克)
275.58
反应后总质量(克)
274.92
反应前后总质量差(克)
0.66
容器内气体质量差(克)
m
(1)该实验中,对装置中的固态干燥剂的性质有何要求?
________________________________________________________________________。
(2)反应前容器内是空气(密度为ρ1)
( http: / / www.21cnjy.com ),反应后全部是二氧化碳(密度为ρ2),则反应前后容器(容积为V)内的气体质量差m为____________。(用字母表示,反应物的体积忽略不计)
(3)小明查阅有关数据后,计算出反应前
( http: / / www.21cnjy.com )后容器内的气体质量差m为0.22克,结合表中数据,计算该钙片中碳酸钙的质量分数。(CaCO3+2HCl===CaCl2+H2O+CO2↑)。钙片中的其他成分不与盐酸反应。
第18题图
第3节 常见的酸(第2课时)
【课堂笔记】
一、1.红色 不变色 2.ZnSO4+H2↑
3.Fe2(SO4)3+3H2O
二、1.挥发 2.吸水性 3.脱水性 4.腐蚀性 迅速用抹布擦拭 5.沿着器壁慢慢地注入水里,并不断搅动 切不可将水倒进浓硫酸里
6.BaSO4↓+2HNO3
【课时训练】
1-5.BCBCD 6-10.DDACB 11-12.BC
13.(1)锌等 (2)BaCl2+H2SO4===BaSO4↓+2HCl(合理即可)
14.(1)吸水 (2)①Fe+H2SO4===FeSO4+H2↑
②Na2CO3+H2SO4===Na2SO4+H2O+CO2↑ ③H2SO4+BaCl2===BaSO4↓+2HCl ①②
(3)②③
15.A 16.C
17.(1)由标签知该液体是混合物
( http: / / www.21cnjy.com ),而蒸馏水为纯净物(答案合理即可) (2)二氧化锰(或MnO2) 产生白色沉淀 【反思交流】(1)倾倒液体时标签未朝向手心(答案合理均可) (2)2H2O22H2O+O2↑
18.(1)能吸收水但不吸收二氧化碳 (2)(ρ2-ρ1)V
(3)设钙片中碳酸钙的质量为x
反应后生成的二氧化碳的质量为:0.66g+0.22g=0.88g
CaCO3+2HCl===CaCl2+H2O+CO2↑
100
44
x
0.88g
= 解得:x=2g
该钙片中碳酸钙的质量分数为:×100%=50%
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
