鲁科版高中化学必修一 3.1《碳的多样性》 (共15张PPT)
文档属性
| 名称 | 鲁科版高中化学必修一 3.1《碳的多样性》 (共15张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 314.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-09-11 00:00:00 | ||
图片预览




文档简介
课件15张PPT。第一节 碳的多样性碳及其化合物之间的转化 1、了解同素异形体的概念,知道碳有三种常见的同素异形体,
它们的物理性质差异主要是由于碳原子的排列方式不同引起
2、知道含碳化合物种类繁多,一般为无机化合物和有机化合物。
3、认识Na2CO3和NaHCO3的主要性质,初步体会其性质差异。
4、了解碳及其化合物之间的转化和性质,并利用所学知识解释
社会生活和自然现象。体会化学在人类生产生活中的应用。学习目标Na2CO3 + CO2 + H2O === 2 NaHCO3复习回顾4、CO2分别通入饱和NaHCO3 、Na2CO3溶液中2、 NaOH溶液分别和NaHCO3 、Na2CO3溶液3、 CaCl 2溶液分别和NaHCO3 、Na2CO3溶液1、盐酸分别和NaHCO3 、 Na2CO3溶液写化学方程式或离子方程式Na2CO3与NaHCO3的化学性质比较产生气泡CO32-+2H+= CO2↑ + H2O
HCO3-+H+= CO2↑ +H2O无明显现象Na2CO3不反应
HCO3-+OH-= CO32- +H2O产生白色沉淀CO32-+Ca2+= Ca CO3↓
Ca2+ +HCO3-+OH- =
Ca CO3 ↓ +H2ONa2CO3产生白色沉淀
NaHCO3无现象CO32-+Ca2+= Ca CO3↓
NaHCO3不反应Na2CO3 无现象
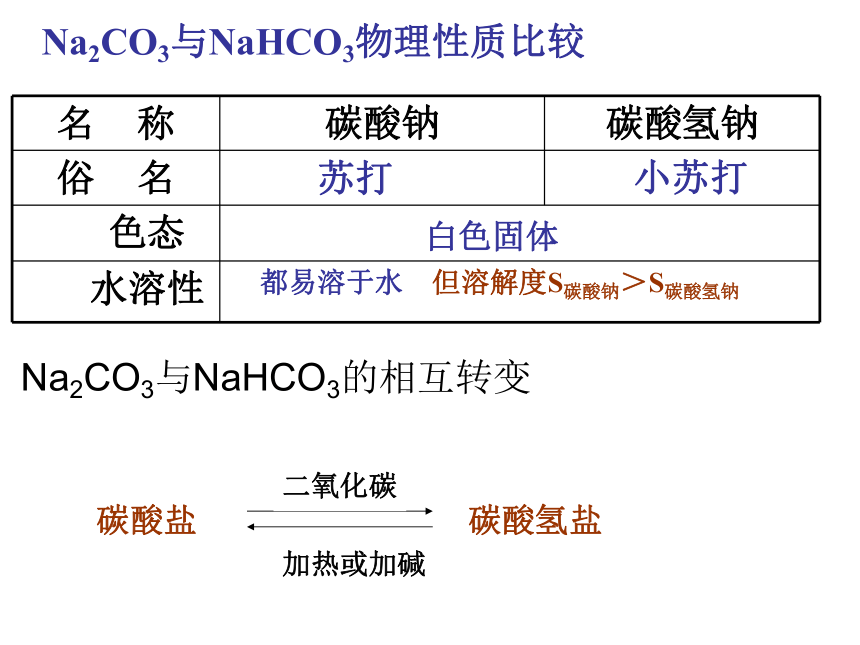
NaHCO3分解产生CO2Na2CO3与NaHCO3物理性质比较白色固体苏打小苏打都易溶于水 但溶解度S碳酸钠>S碳酸氢钠Na2CO3与NaHCO3的相互转变Na2CO3与NaHCO3的相互转变
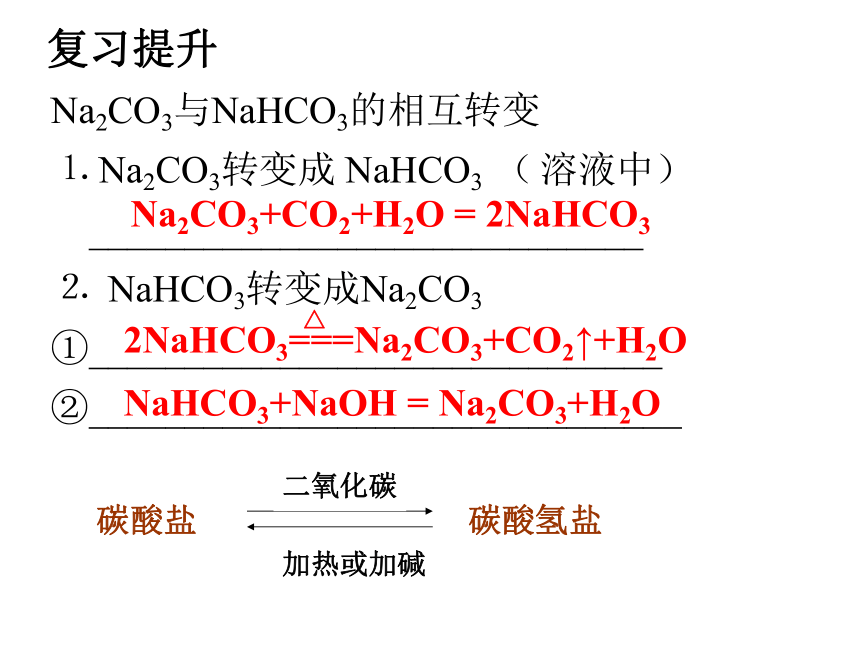
⒈ Na2CO3转变成 NaHCO3 ( 溶液中)
_____________________________
⒉ NaHCO3转变成Na2CO3
①______________________________
②_______________________________复习提升〖应用〗1、如何鉴别Na2CO3与NaHCO3 ?
2、如何除去Na2CO3中少量的NaHCO3?
3、如何除去NaHCO3中少量的Na2CO3?
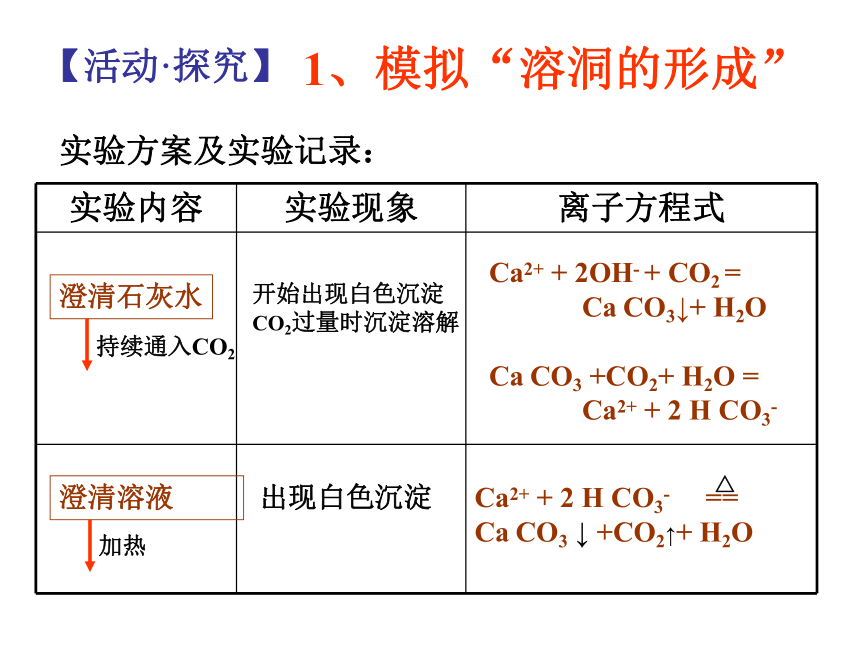
① 滴 加CaCl2溶液;② 加热 ③滴加盐酸① 加适量NaOH溶液;② 加热通入CO2CDCDCD 0.05mol 0.1mol 2 mol/L【活动·探究】1、模拟“溶洞的形成”实验方案及实验记录:开始出现白色沉淀
CO2过量时沉淀溶解出现白色沉淀Ca2+ + 2OH- + CO2 =
Ca CO3↓+ H2O
Ca CO3 +CO2+ H2O =
Ca2+ + 2 H CO3-2、生产和生活中碳及其化合物间的转化①写出高炉炼铁过程中碳元素所发生化学反应方程式
高炉炼铁主要的反应原理
C+O2==CO2 C+CO2==2CO
Fe2O3+3CO==2Fe+3CO2
②碳“三角”
C+O2==CO2 2C+O2==2CO
C+CO2==2CO 2CO+O2==2CO2
③水垢的主要成分是什么?它是怎样形成的?如何除去水壶中的水垢?
Ca(HCO3)2==CaCO3↓+CO2↑+H2O
CaCO3+2CH3COOH= Ca2+ + 2CH3COO- +CO2↑+H2O高温高温点燃点燃点燃高温点燃△概括·整合作业:写出下列反应的化学方程式探究实验Ⅱ:先用两支试管分别取相同体积相同浓度的碳酸钠溶液和碳酸氢钠溶液,然后向试管中分别逐滴加入相同浓度的稀盐酸,边滴边振荡。观察其现象。现象:碳酸钠溶液中刚开始滴加稀盐酸时没有气泡产生,随稀盐酸滴入量的增加才产生气泡。
碳酸氢钠溶液中滴入稀盐酸立即产生大量气泡。问题:碳酸氢钠与稀盐酸反应为什么比碳酸钠与稀盐酸反应剧烈得多?演示微观机理:反应原理(化学方程式):Na2CO3+HCl=NaCl+Na HCO3二、化学性质 4、热稳定性探究实验Ⅲ:把少量NaHCO3固体放在试管里,往烧杯里倒入澄清的石灰水,然后加热,如图。观察澄清的石灰水是否起变化。现象:加热,导管口有气泡产生,烧杯中澄清石灰水变浑浊。最后又变为澄清溶液。试管口有水珠产生。结论:NaHCO3受热易分解,即具有不稳定性。七、关于Na2CO3与NaHCO3混合物中各成份质量分数的计算。
〖例题〗将某碳酸钠和碳酸氢钠的混合物 2.74g 加热到质量不再变化时,剩余物质量为 2.12g 。求:
⑴混合物中碳酸氢钠与碳酸钠的物质的量;
⑵将这种混合物与足量的稀盐酸反应可以
生成标准状况下的气体体积。解:用差量法计算:
2NaHCO3==Na2CO3+CO2↑+H2O 固体质量减少
2mol 62.0g
n (NaHCO3) 0.620g
n (NaHCO3)=0.02mol
n (Na2CO3) =(2.74g-0.02mol×84g/mol)/106g·mol-1
=0.01mol
CO32-+2H+= CO2↑ + H2O HCO3-+H+= CO2↑ +H2O
∴ n (CO2)=n (NaHCO3) + n (Na2CO3)=0.03mol
V (CO2)= 0.03mol ×22.4L ·mol-1=0.672L
它们的物理性质差异主要是由于碳原子的排列方式不同引起
2、知道含碳化合物种类繁多,一般为无机化合物和有机化合物。
3、认识Na2CO3和NaHCO3的主要性质,初步体会其性质差异。
4、了解碳及其化合物之间的转化和性质,并利用所学知识解释
社会生活和自然现象。体会化学在人类生产生活中的应用。学习目标Na2CO3 + CO2 + H2O === 2 NaHCO3复习回顾4、CO2分别通入饱和NaHCO3 、Na2CO3溶液中2、 NaOH溶液分别和NaHCO3 、Na2CO3溶液3、 CaCl 2溶液分别和NaHCO3 、Na2CO3溶液1、盐酸分别和NaHCO3 、 Na2CO3溶液写化学方程式或离子方程式Na2CO3与NaHCO3的化学性质比较产生气泡CO32-+2H+= CO2↑ + H2O
HCO3-+H+= CO2↑ +H2O无明显现象Na2CO3不反应
HCO3-+OH-= CO32- +H2O产生白色沉淀CO32-+Ca2+= Ca CO3↓
Ca2+ +HCO3-+OH- =
Ca CO3 ↓ +H2ONa2CO3产生白色沉淀
NaHCO3无现象CO32-+Ca2+= Ca CO3↓
NaHCO3不反应Na2CO3 无现象
NaHCO3分解产生CO2Na2CO3与NaHCO3物理性质比较白色固体苏打小苏打都易溶于水 但溶解度S碳酸钠>S碳酸氢钠Na2CO3与NaHCO3的相互转变Na2CO3与NaHCO3的相互转变
⒈ Na2CO3转变成 NaHCO3 ( 溶液中)
_____________________________
⒉ NaHCO3转变成Na2CO3
①______________________________
②_______________________________复习提升〖应用〗1、如何鉴别Na2CO3与NaHCO3 ?
2、如何除去Na2CO3中少量的NaHCO3?
3、如何除去NaHCO3中少量的Na2CO3?
① 滴 加CaCl2溶液;② 加热 ③滴加盐酸① 加适量NaOH溶液;② 加热通入CO2CDCDCD 0.05mol 0.1mol 2 mol/L【活动·探究】1、模拟“溶洞的形成”实验方案及实验记录:开始出现白色沉淀
CO2过量时沉淀溶解出现白色沉淀Ca2+ + 2OH- + CO2 =
Ca CO3↓+ H2O
Ca CO3 +CO2+ H2O =
Ca2+ + 2 H CO3-2、生产和生活中碳及其化合物间的转化①写出高炉炼铁过程中碳元素所发生化学反应方程式
高炉炼铁主要的反应原理
C+O2==CO2 C+CO2==2CO
Fe2O3+3CO==2Fe+3CO2
②碳“三角”
C+O2==CO2 2C+O2==2CO
C+CO2==2CO 2CO+O2==2CO2
③水垢的主要成分是什么?它是怎样形成的?如何除去水壶中的水垢?
Ca(HCO3)2==CaCO3↓+CO2↑+H2O
CaCO3+2CH3COOH= Ca2+ + 2CH3COO- +CO2↑+H2O高温高温点燃点燃点燃高温点燃△概括·整合作业:写出下列反应的化学方程式探究实验Ⅱ:先用两支试管分别取相同体积相同浓度的碳酸钠溶液和碳酸氢钠溶液,然后向试管中分别逐滴加入相同浓度的稀盐酸,边滴边振荡。观察其现象。现象:碳酸钠溶液中刚开始滴加稀盐酸时没有气泡产生,随稀盐酸滴入量的增加才产生气泡。
碳酸氢钠溶液中滴入稀盐酸立即产生大量气泡。问题:碳酸氢钠与稀盐酸反应为什么比碳酸钠与稀盐酸反应剧烈得多?演示微观机理:反应原理(化学方程式):Na2CO3+HCl=NaCl+Na HCO3二、化学性质 4、热稳定性探究实验Ⅲ:把少量NaHCO3固体放在试管里,往烧杯里倒入澄清的石灰水,然后加热,如图。观察澄清的石灰水是否起变化。现象:加热,导管口有气泡产生,烧杯中澄清石灰水变浑浊。最后又变为澄清溶液。试管口有水珠产生。结论:NaHCO3受热易分解,即具有不稳定性。七、关于Na2CO3与NaHCO3混合物中各成份质量分数的计算。
〖例题〗将某碳酸钠和碳酸氢钠的混合物 2.74g 加热到质量不再变化时,剩余物质量为 2.12g 。求:
⑴混合物中碳酸氢钠与碳酸钠的物质的量;
⑵将这种混合物与足量的稀盐酸反应可以
生成标准状况下的气体体积。解:用差量法计算:
2NaHCO3==Na2CO3+CO2↑+H2O 固体质量减少
2mol 62.0g
n (NaHCO3) 0.620g
n (NaHCO3)=0.02mol
n (Na2CO3) =(2.74g-0.02mol×84g/mol)/106g·mol-1
=0.01mol
CO32-+2H+= CO2↑ + H2O HCO3-+H+= CO2↑ +H2O
∴ n (CO2)=n (NaHCO3) + n (Na2CO3)=0.03mol
V (CO2)= 0.03mol ×22.4L ·mol-1=0.672L
