浙教版九年级(上)课堂同步练习:第二章 第2节 金属的化学性质(第2课时)
文档属性
| 名称 | 浙教版九年级(上)课堂同步练习:第二章 第2节 金属的化学性质(第2课时) |

|
|
| 格式 | zip | ||
| 文件大小 | 245.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2016-09-11 00:00:00 | ||
图片预览


文档简介
第2节 金属的化学性质(第2课时)
一、金属的化学性质
金属跟某些盐溶液的反应
Fe+CuSO4===________________(铁丝表面有一层红色物质生成)
Cu+2AgNO3===________________(铜丝表面有一层银白色物质生成)
Cu+FeSO4——没有变化
Cu+ZnSO4——没有变化
金属活动性应用:在金属活动性顺序中,只有
( http: / / www.21cnjy.com )一种活动性________的金属才能把另一种活动性________的金属从它的盐________中置换出来。
思考:如何设计实验比较Mg、Zn、Cu三种金属活动性的强弱?
二、金属的锈蚀
1.铁锈蚀条件:铁与________和________等物质相互作用。
2.防止铁生锈的方法:
(1)使铁制品隔绝________或隔绝_
( http: / / www.21cnjy.com )_______,保持铁制品表面干燥和洁净或在铁制品表面涂一层保护膜。如刷油漆、涂油、电镀、烤蓝等。
(2)改变铁的________、________,制成合金钢,如不锈钢等。
A组 基础训练
1.往相同质量的10%稀盐酸中加入下列金属,反应最剧烈的是( )
A.Cu
B.Zn
C.Fe
D.Mg
2.(巴中中考)向氯化铜和氯化镁的混合溶液中,加入过量锌粉,充分反应后过滤,滤纸上得到的固体物质是( )
A.锌和铜
B.铜
C.镁和铜
D.锌
3.(潍坊中考)金属腐蚀的快慢与外界条件密切相关,下列条件下,铁钉的腐蚀速度最快的是( )
4.钢铁是使用最多的金属材料,但每年因锈蚀
( http: / / www.21cnjy.com )而损失的数量巨大,防止金属腐蚀已成为科学研究中的重大问题。以下有关金属腐蚀的叙述不正确的是( )
A.钢铁在潮湿的空气中比在干燥的空气中更易锈蚀
B.钢铁锈蚀的实质是铁与空气中的氧气、水蒸气等发生了化学反应
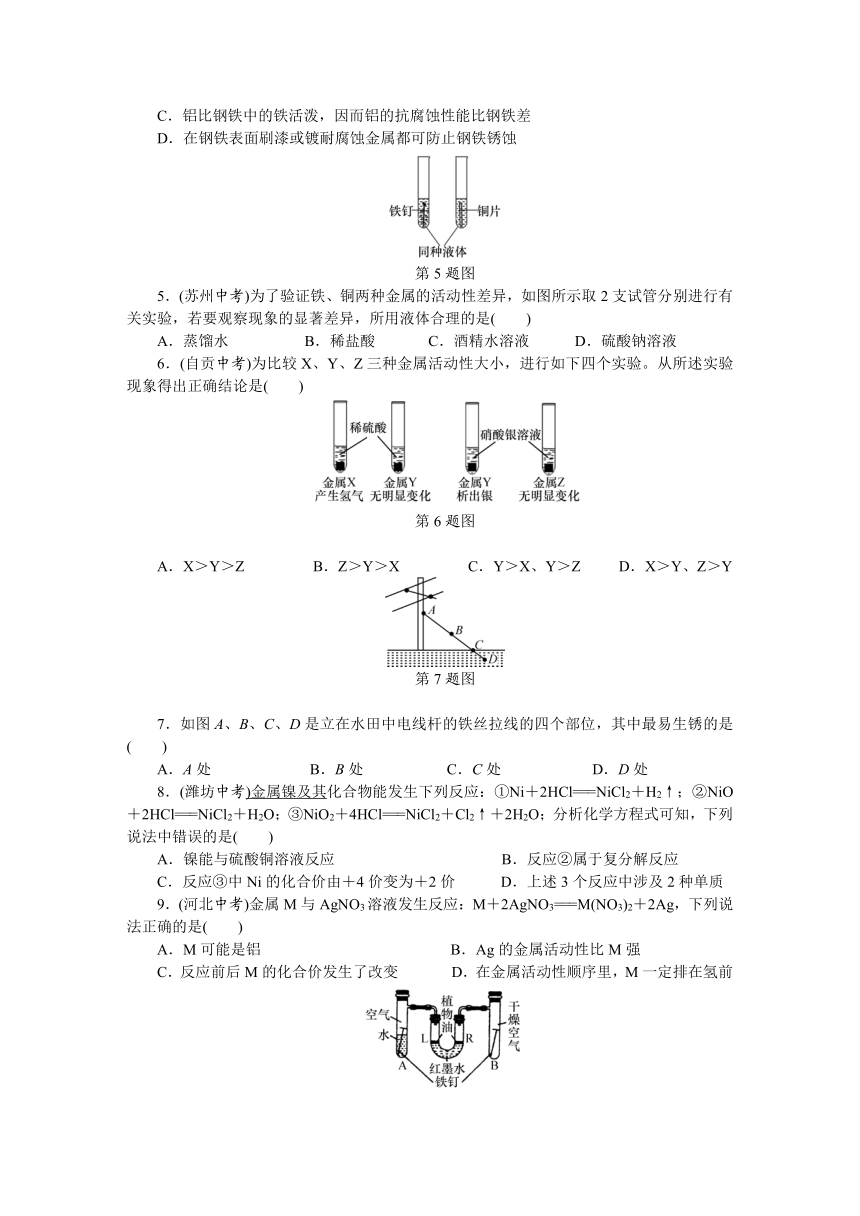
C.铝比钢铁中的铁活泼,因而铝的抗腐蚀性能比钢铁差
D.在钢铁表面刷漆或镀耐腐蚀金属都可防止钢铁锈蚀
第5题图
5.(苏州中考)为了验证铁、铜两种金属的活动性差异,如图所示取2支试管分别进行有关实验,若要观察现象的显著差异,所用液体合理的是( )
A.蒸馏水
B.稀盐酸
C.酒精水溶液
D.硫酸钠溶液
6.(自贡中考)为比较X、Y、Z三种金属活动性大小,进行如下四个实验。从所述实验现象得出正确结论是( )
第6题图
A.X>Y>Z
B.Z>Y>X
C.Y>X、Y>Z
D.X>Y、Z>Y
第7题图
7.如图A、B、C、D是立在水田中电线杆的铁丝拉线的四个部位,其中最易生锈的是( )
A.A处
B.B处
C.C处
D.D处
8.(潍坊中考)金属镍及其
( http: / / www.21cnjy.com )化合物能发生下列反应:①Ni+2HCl===NiCl2+H2↑;②NiO+2HCl===NiCl2+H2O;③NiO2+4HCl===NiCl2+Cl2↑+2H2O;分析化学方程式可知,下列说法中错误的是( )
A.镍能与硫酸铜溶液反应
B.反应②属于复分解反应
C.反应③中Ni的化合价由+4价变为+2价
D.上述3个反应中涉及2种单质
9.(河北中考)金属M与AgNO3溶液发生反应:M+2AgNO3===M(NO3)2+2Ag,下列说法正确的是( )
A.M可能是铝
B.Ag的金属活动性比M强
C.反应前后M的化合价发生了改变
D.在金属活动性顺序里,M一定排在氢前
第10题图
10.如图所示是探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧木塞,一周后观察。下列推断错误的是( )
A.B管中铁钉不会锈蚀
B.L端与R端液面高度仍然保持一致
C.该实验说明铁锈蚀与水有关
D.若将A管中的水改为食盐水能加快铁的锈蚀
11.向CuSO4溶液中加入一定量的铁粉充分反应,下列情况可能出现的是:( )
①溶液中有Fe2+,不溶物为Fe、Cu
( http: / / www.21cnjy.com ) ②溶液中有Fe2+、Cu2+,不溶物为Fe ③溶液中有Fe2+、Cu2+,不溶物为Cu ④溶液中有Cu2+,不溶物为Fe。
A.②③
B.①④
C.①③
D.③④
12.(广西中考)根据金属活动性顺序的相关知识回答。
(1)从左到右,金属的活动性逐渐__________(填“增强”或“减弱”)。
(2)不能用铁制容器盛装硫酸铜溶液
( http: / / www.21cnjy.com )的原因(用化学方程式表示):________________________________________________________________________。
(3)金属的活动性顺序还可以给你以
( http: / / www.21cnjy.com )下判断的依据:位于氢前面的金属能________________________________________________________________________。
13.(泰安中考)某兴趣小组的同学从实验室收
( http: / / www.21cnjy.com )集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题:
第13题图
(1)步骤①中,金属X是________,该反应的化学方程式为__________
____________;
(2)步骤②中,加入过量稀硫酸的目的是_________________
_____________
____
________________________________________________________________________;
(3)从滤液中获得硫酸亚铁晶体采用的方法是
________________________________________________________________________。
B组 自主提高
14.(岳阳中考)向AgNO3溶液中加入一定质量Fe和Al,充分反应后过滤,得到滤渣和浅绿色滤液。下列说法正确的是( )
A.滤液中一定含有Al3+、Ag+
B.滤液中一定含有Fe2+、Ag+
C.滤渣中一定含有Fe
D.滤渣中一定含有Ag
第15题图
15.往盛有稀硫酸的烧杯中加入足量的氧
( http: / / www.21cnjy.com )化铜粉末,充分反应后,再向烧杯中继续加入某种金属。实验过程中,烧杯中硫酸铜的质量随时间变化如图所示(不考虑其他因素对烧杯中物质的影响)。下列判断错误的是( )
A.从0到t3,烧杯中水的质量不断增加
B.t1时与t2时烧杯中物质总质量相等
C.加入的金属一定是银
D.从t3到t4,硫酸铜质量变化可通过置换反应实现
第16题图
16.(泰安中考)向一定质量AgNO3
( http: / / www.21cnjy.com )和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示。下列说法正确的是( )
A.取a点溶液,滴加稀盐酸,无白色沉淀
B.图标上b-c段质量增加的原因是Zn与Cu(NO3)2溶液反应
C.b点时溶液中金属离子有Zn2+、Cu2+,金属单质有Zn、Cu、Ag
D.c点和d点溶质种类不同,金属单质种类也不同
17.(新疆中考)某工厂欲从含有CuSO4的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图:
第17题图
(1)操作Ⅰ的名称是________,需用到的玻璃仪器除烧杯之外还有____________________。
(2)加入过量A物质的化学式是________。
(3)加入适量B物质时反应的化学方程式是________________________。
18.(泸州中考)黄铜是一种重要的
( http: / / www.21cnjy.com )金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品。为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
样品
第1份
第2份
第3份
第4份
第5份
取样品质量(g)
40.0
40.0
40.0
40.0
40.0
取稀硫酸质量(g)
30.0
60.0
90.0
120.0
150.0
产生气体质量(g)
0.3
0.6
0.9
1.0
1.0
按要求回答下列问题:
(1)根据实验数据分析,从第________份开始,金属已经反应完全了。
(2)列式计算该黄铜样品中金属锌的质量分数。(要求写出计算过程)
第2节 金属的化学性质(第2课时)
【课堂笔记】
一、FeSO4+Cu Cu(NO3)2+2Ag 较强 较弱 溶液
二、1.空气 水 2.(1)空气 水 (2)组成 结构
【课时训练】
1-5.DAACB 6-10.ACDCB 11.C
12.(1)减弱 (2)Fe+CuSO4===FeSO4+Cu (3)置换出盐酸、稀硫酸中的氢
13.(1)铁 Fe+CuSO4===FeSO4+Cu (2)除去铜中的铁 (3)蒸发结晶
14-16.DCB
17.(1)过滤 漏斗、玻璃棒 (2)Fe (3)Fe+H2SO4===FeSO4+H2↑
18.(1)4 (2)81.25%
一、金属的化学性质
金属跟某些盐溶液的反应
Fe+CuSO4===________________(铁丝表面有一层红色物质生成)
Cu+2AgNO3===________________(铜丝表面有一层银白色物质生成)
Cu+FeSO4——没有变化
Cu+ZnSO4——没有变化
金属活动性应用:在金属活动性顺序中,只有
( http: / / www.21cnjy.com )一种活动性________的金属才能把另一种活动性________的金属从它的盐________中置换出来。
思考:如何设计实验比较Mg、Zn、Cu三种金属活动性的强弱?
二、金属的锈蚀
1.铁锈蚀条件:铁与________和________等物质相互作用。
2.防止铁生锈的方法:
(1)使铁制品隔绝________或隔绝_
( http: / / www.21cnjy.com )_______,保持铁制品表面干燥和洁净或在铁制品表面涂一层保护膜。如刷油漆、涂油、电镀、烤蓝等。
(2)改变铁的________、________,制成合金钢,如不锈钢等。
A组 基础训练
1.往相同质量的10%稀盐酸中加入下列金属,反应最剧烈的是( )
A.Cu
B.Zn
C.Fe
D.Mg
2.(巴中中考)向氯化铜和氯化镁的混合溶液中,加入过量锌粉,充分反应后过滤,滤纸上得到的固体物质是( )
A.锌和铜
B.铜
C.镁和铜
D.锌
3.(潍坊中考)金属腐蚀的快慢与外界条件密切相关,下列条件下,铁钉的腐蚀速度最快的是( )
4.钢铁是使用最多的金属材料,但每年因锈蚀
( http: / / www.21cnjy.com )而损失的数量巨大,防止金属腐蚀已成为科学研究中的重大问题。以下有关金属腐蚀的叙述不正确的是( )
A.钢铁在潮湿的空气中比在干燥的空气中更易锈蚀
B.钢铁锈蚀的实质是铁与空气中的氧气、水蒸气等发生了化学反应
C.铝比钢铁中的铁活泼,因而铝的抗腐蚀性能比钢铁差
D.在钢铁表面刷漆或镀耐腐蚀金属都可防止钢铁锈蚀
第5题图
5.(苏州中考)为了验证铁、铜两种金属的活动性差异,如图所示取2支试管分别进行有关实验,若要观察现象的显著差异,所用液体合理的是( )
A.蒸馏水
B.稀盐酸
C.酒精水溶液
D.硫酸钠溶液
6.(自贡中考)为比较X、Y、Z三种金属活动性大小,进行如下四个实验。从所述实验现象得出正确结论是( )
第6题图
A.X>Y>Z
B.Z>Y>X
C.Y>X、Y>Z
D.X>Y、Z>Y
第7题图
7.如图A、B、C、D是立在水田中电线杆的铁丝拉线的四个部位,其中最易生锈的是( )
A.A处
B.B处
C.C处
D.D处
8.(潍坊中考)金属镍及其
( http: / / www.21cnjy.com )化合物能发生下列反应:①Ni+2HCl===NiCl2+H2↑;②NiO+2HCl===NiCl2+H2O;③NiO2+4HCl===NiCl2+Cl2↑+2H2O;分析化学方程式可知,下列说法中错误的是( )
A.镍能与硫酸铜溶液反应
B.反应②属于复分解反应
C.反应③中Ni的化合价由+4价变为+2价
D.上述3个反应中涉及2种单质
9.(河北中考)金属M与AgNO3溶液发生反应:M+2AgNO3===M(NO3)2+2Ag,下列说法正确的是( )
A.M可能是铝
B.Ag的金属活动性比M强
C.反应前后M的化合价发生了改变
D.在金属活动性顺序里,M一定排在氢前
第10题图
10.如图所示是探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧木塞,一周后观察。下列推断错误的是( )
A.B管中铁钉不会锈蚀
B.L端与R端液面高度仍然保持一致
C.该实验说明铁锈蚀与水有关
D.若将A管中的水改为食盐水能加快铁的锈蚀
11.向CuSO4溶液中加入一定量的铁粉充分反应,下列情况可能出现的是:( )
①溶液中有Fe2+,不溶物为Fe、Cu
( http: / / www.21cnjy.com ) ②溶液中有Fe2+、Cu2+,不溶物为Fe ③溶液中有Fe2+、Cu2+,不溶物为Cu ④溶液中有Cu2+,不溶物为Fe。
A.②③
B.①④
C.①③
D.③④
12.(广西中考)根据金属活动性顺序的相关知识回答。
(1)从左到右,金属的活动性逐渐__________(填“增强”或“减弱”)。
(2)不能用铁制容器盛装硫酸铜溶液
( http: / / www.21cnjy.com )的原因(用化学方程式表示):________________________________________________________________________。
(3)金属的活动性顺序还可以给你以
( http: / / www.21cnjy.com )下判断的依据:位于氢前面的金属能________________________________________________________________________。
13.(泰安中考)某兴趣小组的同学从实验室收
( http: / / www.21cnjy.com )集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题:
第13题图
(1)步骤①中,金属X是________,该反应的化学方程式为__________
____________;
(2)步骤②中,加入过量稀硫酸的目的是_________________
_____________
____
________________________________________________________________________;
(3)从滤液中获得硫酸亚铁晶体采用的方法是
________________________________________________________________________。
B组 自主提高
14.(岳阳中考)向AgNO3溶液中加入一定质量Fe和Al,充分反应后过滤,得到滤渣和浅绿色滤液。下列说法正确的是( )
A.滤液中一定含有Al3+、Ag+
B.滤液中一定含有Fe2+、Ag+
C.滤渣中一定含有Fe
D.滤渣中一定含有Ag
第15题图
15.往盛有稀硫酸的烧杯中加入足量的氧
( http: / / www.21cnjy.com )化铜粉末,充分反应后,再向烧杯中继续加入某种金属。实验过程中,烧杯中硫酸铜的质量随时间变化如图所示(不考虑其他因素对烧杯中物质的影响)。下列判断错误的是( )
A.从0到t3,烧杯中水的质量不断增加
B.t1时与t2时烧杯中物质总质量相等
C.加入的金属一定是银
D.从t3到t4,硫酸铜质量变化可通过置换反应实现
第16题图
16.(泰安中考)向一定质量AgNO3
( http: / / www.21cnjy.com )和Cu(NO3)2的混合溶液中加入过量的Zn粉,溶液质量随反应时间变化的情况如图所示。下列说法正确的是( )
A.取a点溶液,滴加稀盐酸,无白色沉淀
B.图标上b-c段质量增加的原因是Zn与Cu(NO3)2溶液反应
C.b点时溶液中金属离子有Zn2+、Cu2+,金属单质有Zn、Cu、Ag
D.c点和d点溶质种类不同,金属单质种类也不同
17.(新疆中考)某工厂欲从含有CuSO4的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图:
第17题图
(1)操作Ⅰ的名称是________,需用到的玻璃仪器除烧杯之外还有____________________。
(2)加入过量A物质的化学式是________。
(3)加入适量B物质时反应的化学方程式是________________________。
18.(泸州中考)黄铜是一种重要的
( http: / / www.21cnjy.com )金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品。为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
样品
第1份
第2份
第3份
第4份
第5份
取样品质量(g)
40.0
40.0
40.0
40.0
40.0
取稀硫酸质量(g)
30.0
60.0
90.0
120.0
150.0
产生气体质量(g)
0.3
0.6
0.9
1.0
1.0
按要求回答下列问题:
(1)根据实验数据分析,从第________份开始,金属已经反应完全了。
(2)列式计算该黄铜样品中金属锌的质量分数。(要求写出计算过程)
第2节 金属的化学性质(第2课时)
【课堂笔记】
一、FeSO4+Cu Cu(NO3)2+2Ag 较强 较弱 溶液
二、1.空气 水 2.(1)空气 水 (2)组成 结构
【课时训练】
1-5.DAACB 6-10.ACDCB 11.C
12.(1)减弱 (2)Fe+CuSO4===FeSO4+Cu (3)置换出盐酸、稀硫酸中的氢
13.(1)铁 Fe+CuSO4===FeSO4+Cu (2)除去铜中的铁 (3)蒸发结晶
14-16.DCB
17.(1)过滤 漏斗、玻璃棒 (2)Fe (3)Fe+H2SO4===FeSO4+H2↑
18.(1)4 (2)81.25%
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
