1.5 酸和碱之间发生的反应
图片预览







文档简介
课件20张PPT。第5节 酸和碱之间发生的反应酸(H+ + 酸根离子)3.在酸中加入锌粒,会看到 ,
这说明了酸能跟 反应。4.往生锈的铁钉中加入酸,看到铁锈会 ,
这说明了酸能跟 反应。有大量的气泡冒出金属溶解 金属氧化物2.酸加入紫色石蕊试液,溶液变 色,加入无色酚酞,溶液 ,这说明了酸能跟
反应。 红不变色酸碱指示剂1.常见的酸有: 盐酸(HCl)、硫酸(H2SO4)等复习练习:2.在碱中加入紫色石蕊试液变 色,加入无色
酚酞溶液变 色,这说明了碱能
跟反应。 碱(金属离子 + OH-)3.澄清的石灰水中通入二氧化碳,石灰水变 说明碱能跟 反应。蓝红酸碱指示剂浑浊非金属氧化物1.常见的碱有 ;
其中比较便宜的是 ,它可以用 与水反应直接制得。氢氧化钠、氢氧化钙等氢氧化钙生石灰在2支试管中加入少量NaOH溶液,滴入几滴酚酞溶液,再用滴管慢慢滴入稀盐酸和稀硫酸,并不断振荡,至溶液颜色恰好变成无色为止。用滴管吸取反应后的溶液滴在蒸发皿中,用酒精灯烘干,观察现象?演示实验化学方程式:NaOH + HCl = NaCl + H2O
2NaOH + H2SO4 = Na2SO4 + 2H2O上述活动中,滴入一定量的稀盐酸或稀硫酸以后,溶液从红色变为无色,这说明溶液的酸碱性发生了什么变化?思考与讨论:3.酸碱反应:思考:请你找出下列两个化学方程式的共同点:
NaOH + HCl = NaCl + H2O
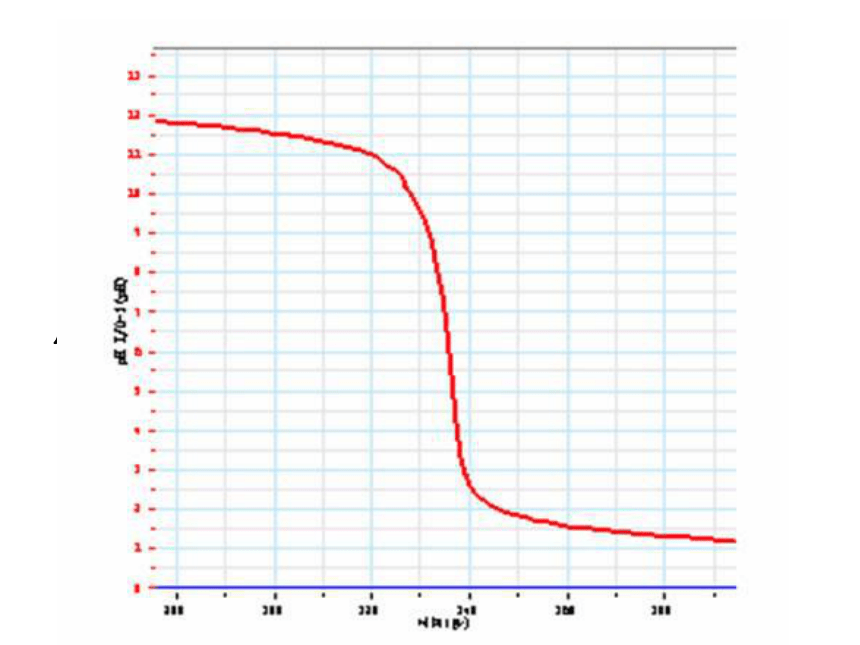
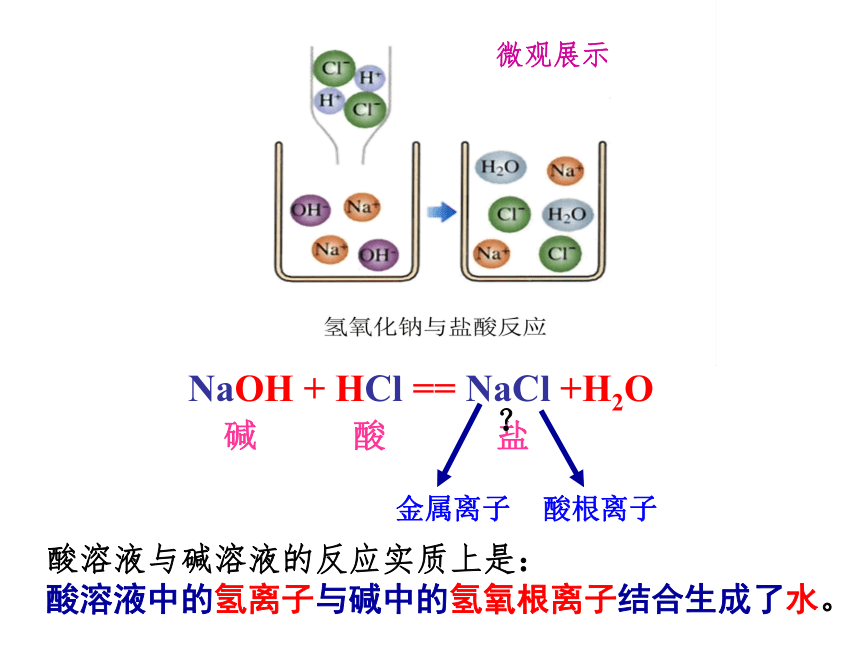
2NaOH + H2SO4 = Na2SO4 + 2H2O NaOH是碱, HCl、 H2SO4都属酸, NaCl、 Na2SO4都是盐,它们都是酸与碱反应生成盐和水。1)定义:碱跟酸作用生成盐和水的反应叫酸碱反应。思考:用什么办法能够知道在稀盐酸和氢氧化钠溶液的反应过程中,酸和碱没有剩余,恰好完全反应?答:可用酸碱指示剂来检验,如再滴入紫色石蕊试液变红色说明是酸过量,变蓝色,说明是碱过量.也可以用pH试纸来检验,反应完后,若pH>7时,说明是碱过量,若pH<7时,说明是酸过量.请你读图,能说出酸碱反应的实质吗?NaOH + HCl == NaCl +H2O碱酸盐?酸溶液与碱溶液的反应实质上是:
酸溶液中的氢离子与碱中的氢氧根离子结合生成了水。 3)酸碱反应的实质:
实质是酸电离的H+与碱电离的OH-结合成中性的水。
H+ + OH- = H2O判定:MgO和H2SO4反应,生成了MgSO4和H2O(生成盐和水),这个反应是酸碱反应吗?答:这不是酸碱反应,因为酸碱反应应该是酸和碱作用生成盐和水的反应,不能单看生成物是盐和水,所以这个反应不是酸碱反应。阅读教材P20,回答酸碱反应工农业生产上有何用途?二、酸碱反应的应用1.改变土壤的酸碱性:
用熟石灰Ca(OH)2中和,降低土壤的酸性2.处理工厂的废水:
硫酸厂的污水用Ca(OH)2中和处理Ca(OH)2 + H2SO4 == CaSO4 +2H2O3.用于医药:
胃酸过多 Al(OH)3 + 3HCl == AlCl3 + 3H2O Mg(OH)2 + 2HCl ==MgCl2 + 2H2O 蚊虫叮咬:涂肥皂水或NH3?H2O等碱性药水可用生石灰代替熟石灰,因为CaO+H2O== Ca(OH)2在酸性土壤中加入熟石灰熟石灰(说明:该地区的酸雨为硫酸型酸雨)胃乐说明书
[药品名称] 胃乐胶囊
[性状] 本品为胶囊剂,内容物为灰黄棕色,气味香,味微苦
[主要成分] 氢氧化铝[Al(OH)3]、甘草提取物、白芨、木香等
[药理作用] 中和胃酸过多、抗溃疡、镇痛、抗炎
[功能与主治] 用于慢性胃炎胃酸和多酸胃痛。行气止痛,收敛生肌,促进溃疡愈合。用于胃胀闷疼痛,嗳气泛酸,恶心呕吐,气滞引起的胃腕疼痛。
[用法与用量] 口服,一次2~3粒,一日3次,空腹服用
[规格] 0.4g/粒
[贮藏] 密封,置干燥阴凉处
[包装] 20粒/盒
[有效期] 两年胃 乐胶囊好药用心制造3.用于医药你知道它的作用吗?盐酸氢氧化铝Al(OH)3 + 3HCl === AlCl3+3H2O氢氧化铝能中和胃酸你能写出化学方程式吗?思考:为什么被蚊虫叮咬过之后会觉得痛痒?有什么办法会消除肿痛?蚊虫叮咬能在人的皮肤内分泌出蚁酸,从而使皮肤肿痛,应涂一些弱碱性的药水,可减轻痛痒。1.在氢氧化钠溶液里加入1~2滴酚酞试液,然后逐渐滴入稀盐酸,直到反应完成.在整个过程中溶液的颜色变化为( )A.红色→无色→红色B.红色→无色→无色C.无色→红色→无色D.无色→蓝色→无色C2.制革工业中用熟石灰[Ca(OH)2]给毛皮脱毛,剩余的熟石灰用盐酸中和,该反应的化学方程式是Ca(OH)2 + 2HCl = CaCl2 + 2H2O3.下列反应,属于酸碱反应的是( )
A Zn +2HCl == ZnCl2 + H2↑
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D AgNO3 + HCl == AgCl↓ + HNO3
C4.完成下列化学方程式:
① Cu(OH)2 + H2SO4 == +
② KOH + === K2SO4 +
CuSO4 2H2O 2 H2SO4 2H2O5.消化药片所含的物质能中和胃里过多的胃酸。某种消化药品的标记如右图。医生给某胃酸过多的患者开出服用此药的处方为:每日3次,每次2片。试计算,患者按处方服用该药一天,理论上可中和HCl多少毫克?(计算结果取整数)Stomachease
帮助消化
减缓胃痛
每片含250mg
氢氧化镁Mg(OH)2 + 2HCl == MgCl2 + 2H2O
58 73250mg×3×2XX=1888mg
这说明了酸能跟 反应。4.往生锈的铁钉中加入酸,看到铁锈会 ,
这说明了酸能跟 反应。有大量的气泡冒出金属溶解 金属氧化物2.酸加入紫色石蕊试液,溶液变 色,加入无色酚酞,溶液 ,这说明了酸能跟
反应。 红不变色酸碱指示剂1.常见的酸有: 盐酸(HCl)、硫酸(H2SO4)等复习练习:2.在碱中加入紫色石蕊试液变 色,加入无色
酚酞溶液变 色,这说明了碱能
跟反应。 碱(金属离子 + OH-)3.澄清的石灰水中通入二氧化碳,石灰水变 说明碱能跟 反应。蓝红酸碱指示剂浑浊非金属氧化物1.常见的碱有 ;
其中比较便宜的是 ,它可以用 与水反应直接制得。氢氧化钠、氢氧化钙等氢氧化钙生石灰在2支试管中加入少量NaOH溶液,滴入几滴酚酞溶液,再用滴管慢慢滴入稀盐酸和稀硫酸,并不断振荡,至溶液颜色恰好变成无色为止。用滴管吸取反应后的溶液滴在蒸发皿中,用酒精灯烘干,观察现象?演示实验化学方程式:NaOH + HCl = NaCl + H2O
2NaOH + H2SO4 = Na2SO4 + 2H2O上述活动中,滴入一定量的稀盐酸或稀硫酸以后,溶液从红色变为无色,这说明溶液的酸碱性发生了什么变化?思考与讨论:3.酸碱反应:思考:请你找出下列两个化学方程式的共同点:
NaOH + HCl = NaCl + H2O
2NaOH + H2SO4 = Na2SO4 + 2H2O NaOH是碱, HCl、 H2SO4都属酸, NaCl、 Na2SO4都是盐,它们都是酸与碱反应生成盐和水。1)定义:碱跟酸作用生成盐和水的反应叫酸碱反应。思考:用什么办法能够知道在稀盐酸和氢氧化钠溶液的反应过程中,酸和碱没有剩余,恰好完全反应?答:可用酸碱指示剂来检验,如再滴入紫色石蕊试液变红色说明是酸过量,变蓝色,说明是碱过量.也可以用pH试纸来检验,反应完后,若pH>7时,说明是碱过量,若pH<7时,说明是酸过量.请你读图,能说出酸碱反应的实质吗?NaOH + HCl == NaCl +H2O碱酸盐?酸溶液与碱溶液的反应实质上是:
酸溶液中的氢离子与碱中的氢氧根离子结合生成了水。 3)酸碱反应的实质:
实质是酸电离的H+与碱电离的OH-结合成中性的水。
H+ + OH- = H2O判定:MgO和H2SO4反应,生成了MgSO4和H2O(生成盐和水),这个反应是酸碱反应吗?答:这不是酸碱反应,因为酸碱反应应该是酸和碱作用生成盐和水的反应,不能单看生成物是盐和水,所以这个反应不是酸碱反应。阅读教材P20,回答酸碱反应工农业生产上有何用途?二、酸碱反应的应用1.改变土壤的酸碱性:
用熟石灰Ca(OH)2中和,降低土壤的酸性2.处理工厂的废水:
硫酸厂的污水用Ca(OH)2中和处理Ca(OH)2 + H2SO4 == CaSO4 +2H2O3.用于医药:
胃酸过多 Al(OH)3 + 3HCl == AlCl3 + 3H2O Mg(OH)2 + 2HCl ==MgCl2 + 2H2O 蚊虫叮咬:涂肥皂水或NH3?H2O等碱性药水可用生石灰代替熟石灰,因为CaO+H2O== Ca(OH)2在酸性土壤中加入熟石灰熟石灰(说明:该地区的酸雨为硫酸型酸雨)胃乐说明书
[药品名称] 胃乐胶囊
[性状] 本品为胶囊剂,内容物为灰黄棕色,气味香,味微苦
[主要成分] 氢氧化铝[Al(OH)3]、甘草提取物、白芨、木香等
[药理作用] 中和胃酸过多、抗溃疡、镇痛、抗炎
[功能与主治] 用于慢性胃炎胃酸和多酸胃痛。行气止痛,收敛生肌,促进溃疡愈合。用于胃胀闷疼痛,嗳气泛酸,恶心呕吐,气滞引起的胃腕疼痛。
[用法与用量] 口服,一次2~3粒,一日3次,空腹服用
[规格] 0.4g/粒
[贮藏] 密封,置干燥阴凉处
[包装] 20粒/盒
[有效期] 两年胃 乐胶囊好药用心制造3.用于医药你知道它的作用吗?盐酸氢氧化铝Al(OH)3 + 3HCl === AlCl3+3H2O氢氧化铝能中和胃酸你能写出化学方程式吗?思考:为什么被蚊虫叮咬过之后会觉得痛痒?有什么办法会消除肿痛?蚊虫叮咬能在人的皮肤内分泌出蚁酸,从而使皮肤肿痛,应涂一些弱碱性的药水,可减轻痛痒。1.在氢氧化钠溶液里加入1~2滴酚酞试液,然后逐渐滴入稀盐酸,直到反应完成.在整个过程中溶液的颜色变化为( )A.红色→无色→红色B.红色→无色→无色C.无色→红色→无色D.无色→蓝色→无色C2.制革工业中用熟石灰[Ca(OH)2]给毛皮脱毛,剩余的熟石灰用盐酸中和,该反应的化学方程式是Ca(OH)2 + 2HCl = CaCl2 + 2H2O3.下列反应,属于酸碱反应的是( )
A Zn +2HCl == ZnCl2 + H2↑
B CuO + 2HCl == CuCl2 + H2O
C Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
D AgNO3 + HCl == AgCl↓ + HNO3
C4.完成下列化学方程式:
① Cu(OH)2 + H2SO4 == +
② KOH + === K2SO4 +
CuSO4 2H2O 2 H2SO4 2H2O5.消化药片所含的物质能中和胃里过多的胃酸。某种消化药品的标记如右图。医生给某胃酸过多的患者开出服用此药的处方为:每日3次,每次2片。试计算,患者按处方服用该药一天,理论上可中和HCl多少毫克?(计算结果取整数)Stomachease
帮助消化
减缓胃痛
每片含250mg
氢氧化镁Mg(OH)2 + 2HCl == MgCl2 + 2H2O
58 73250mg×3×2XX=1888mg
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
