高中化学必修2课件:1-1 第一节《元素周期表》课时4
文档属性
| 名称 | 高中化学必修2课件:1-1 第一节《元素周期表》课时4 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-09-23 00:00:00 | ||
图片预览





文档简介
课件16张PPT。第4课时 核素第四章 化学与自然资源的开发利用第一节 元素周期表1.了解原子的构成;
2.了解核素、同位素、质量数的概念;
3.掌握质量数与质子数、中子数之间的相互关系。 本课以《如何去鉴定物品的年代》的视频导入,提取与本课有关关键词,进而导入新课,从原子结构入手,确定原子组成;然后讲述原子内微粒间的数量关系,进而拓展到原子离子内微粒间的数量关系;最后系统讲解元素、核素及同位素的关系。
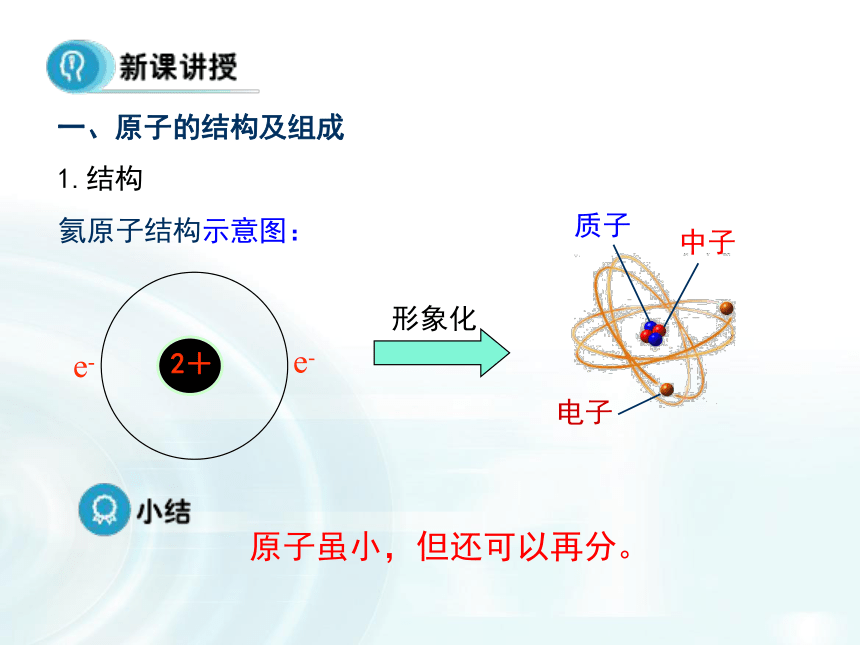
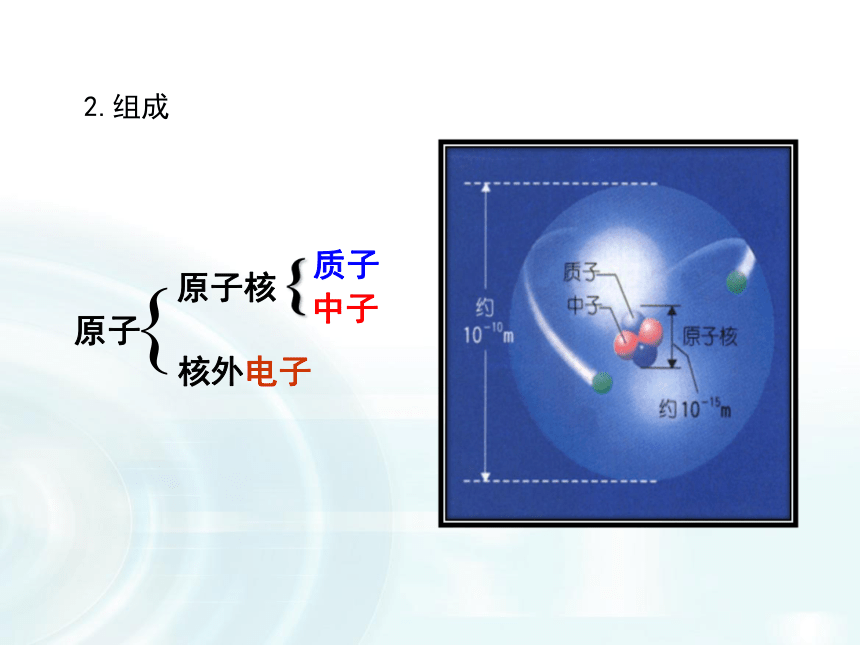
在讲述元素、核素及同位素的关系时,要从原子核本身内部组成入手,同时通过练习巩固解说。如何去鉴定物品的年代(核素导入)视频中涉及如下关键词:C-14 同位素 质子中子。。。一、原子的结构及组成 氦原子结构示意图:原子虽小,但还可以再分。1.结构原子原子核核外电子 质子中子{{2.组成 二、微粒间的数量关系1.原子核内微粒间的数量关系 将原子核内所有的质子和中子的相对质量取近似整数值加起来,所得的数值,叫质量数。质量数(A) = 质子数(Z) + 中子数(N)2.构成原子或离子的微粒间的数量关系原子:没有得失电子,显电中性离子:得到或失去电子,带负电或正电性质子、中子、电子的电性和电量情况?1个质子带一个单位正电荷1个电子带一个单位负电荷中子不带电1.原子核所带的电荷数=质子所带的电荷数核电荷数=质子数2.质子数与核外电子数的关系(2)离子中:核外电子数≠质子数=核电荷数=原子序数(1)原子中:核外电子数=质子数=核电荷数=原子序数阳离子的核外电子数 =质子数 - 离子所带电荷数阴离子的核外电子数 =质子数 + 离子所带电荷数这三种微粒是同一种原子吗?是同一种元素吗?氕 氘 氚
H D T
重氢 超重氢2.核素:具有一定数目质子和一定数目中子的一种原子叫
做核素 1.元素:具有相同核电荷数(质子数)的同一类原子。同种元素:原子的原子核中质子数______。
同种元素:原子的原子核中中子数可以_______。
同种元素:可以有______种不同原子。相同不相同几如:三、元素、核素、同位素元素种类与原子种数一样多吗?1233.同位素
质子数相同而不同中子数的同一元素的不同原子互称为同位素。
即:两同(同质子数、同一元素)
两不同(中子数不同、原子不同) 其特点为:
(1)同位素在周期表里占据同一位置。
(2)同位素的化学性质几乎完全相同,物理性质略有差异。?B同位素的应用:同位素在日常生活、工农业生产和科学研究中有着重要的用途。A——代表质量数;
Z——代表核电荷数;
c——代表离子所带的电荷数;
d——代表化合价;
e——代表一个分子中的原子个数。A、Z、c、d、e各代表什么? 四、微粒的表示方法2.填写下表中空白Z171101340171835101Al3.是不是任何原子核都是由质子和中子构成的? 不是,如上述练习中1H原子,核内无中子,仅有一个质子。
2.了解核素、同位素、质量数的概念;
3.掌握质量数与质子数、中子数之间的相互关系。 本课以《如何去鉴定物品的年代》的视频导入,提取与本课有关关键词,进而导入新课,从原子结构入手,确定原子组成;然后讲述原子内微粒间的数量关系,进而拓展到原子离子内微粒间的数量关系;最后系统讲解元素、核素及同位素的关系。
在讲述元素、核素及同位素的关系时,要从原子核本身内部组成入手,同时通过练习巩固解说。如何去鉴定物品的年代(核素导入)视频中涉及如下关键词:C-14 同位素 质子中子。。。一、原子的结构及组成 氦原子结构示意图:原子虽小,但还可以再分。1.结构原子原子核核外电子 质子中子{{2.组成 二、微粒间的数量关系1.原子核内微粒间的数量关系 将原子核内所有的质子和中子的相对质量取近似整数值加起来,所得的数值,叫质量数。质量数(A) = 质子数(Z) + 中子数(N)2.构成原子或离子的微粒间的数量关系原子:没有得失电子,显电中性离子:得到或失去电子,带负电或正电性质子、中子、电子的电性和电量情况?1个质子带一个单位正电荷1个电子带一个单位负电荷中子不带电1.原子核所带的电荷数=质子所带的电荷数核电荷数=质子数2.质子数与核外电子数的关系(2)离子中:核外电子数≠质子数=核电荷数=原子序数(1)原子中:核外电子数=质子数=核电荷数=原子序数阳离子的核外电子数 =质子数 - 离子所带电荷数阴离子的核外电子数 =质子数 + 离子所带电荷数这三种微粒是同一种原子吗?是同一种元素吗?氕 氘 氚
H D T
重氢 超重氢2.核素:具有一定数目质子和一定数目中子的一种原子叫
做核素 1.元素:具有相同核电荷数(质子数)的同一类原子。同种元素:原子的原子核中质子数______。
同种元素:原子的原子核中中子数可以_______。
同种元素:可以有______种不同原子。相同不相同几如:三、元素、核素、同位素元素种类与原子种数一样多吗?1233.同位素
质子数相同而不同中子数的同一元素的不同原子互称为同位素。
即:两同(同质子数、同一元素)
两不同(中子数不同、原子不同) 其特点为:
(1)同位素在周期表里占据同一位置。
(2)同位素的化学性质几乎完全相同,物理性质略有差异。?B同位素的应用:同位素在日常生活、工农业生产和科学研究中有着重要的用途。A——代表质量数;
Z——代表核电荷数;
c——代表离子所带的电荷数;
d——代表化合价;
e——代表一个分子中的原子个数。A、Z、c、d、e各代表什么? 四、微粒的表示方法2.填写下表中空白Z171101340171835101Al3.是不是任何原子核都是由质子和中子构成的? 不是,如上述练习中1H原子,核内无中子,仅有一个质子。
