【人教版】化学九年级上册课件 5.1质量守恒定律(21张PPT)
文档属性
| 名称 | 【人教版】化学九年级上册课件 5.1质量守恒定律(21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 416.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-10-04 00:00:00 | ||
图片预览





文档简介
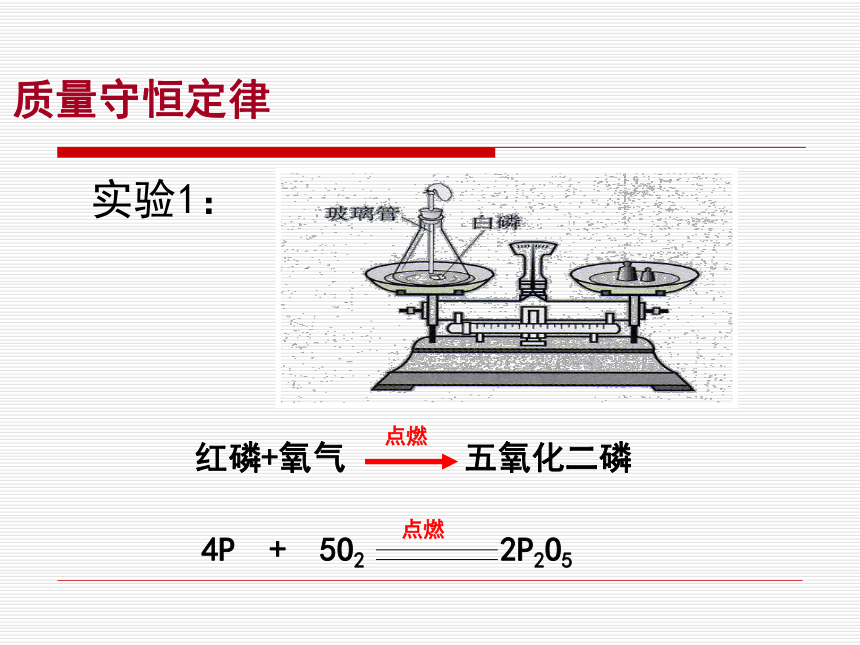
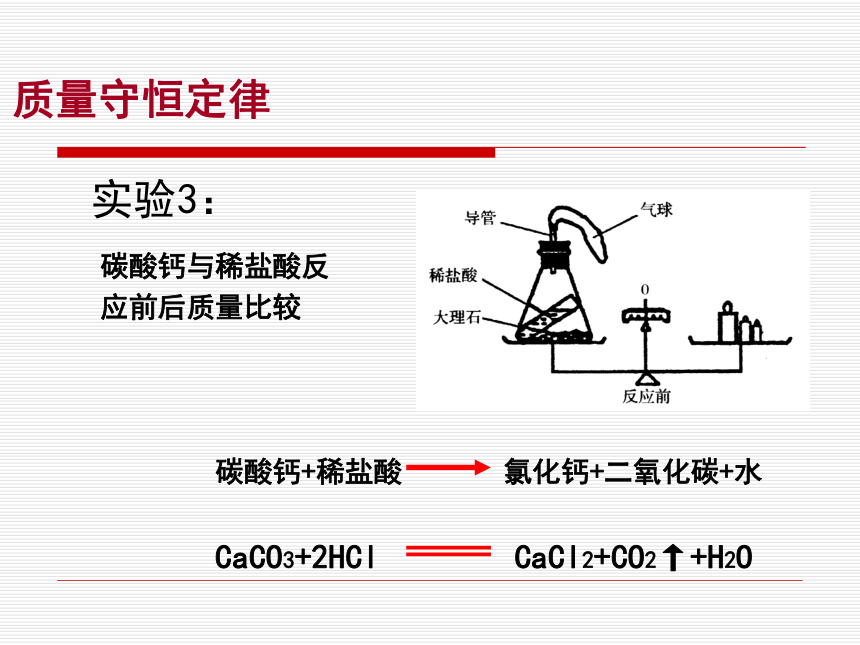
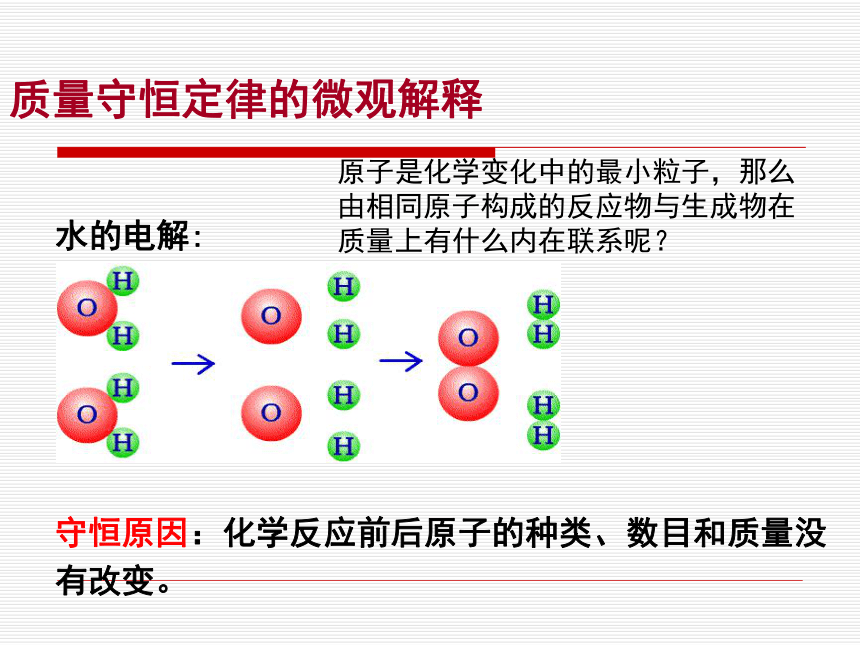
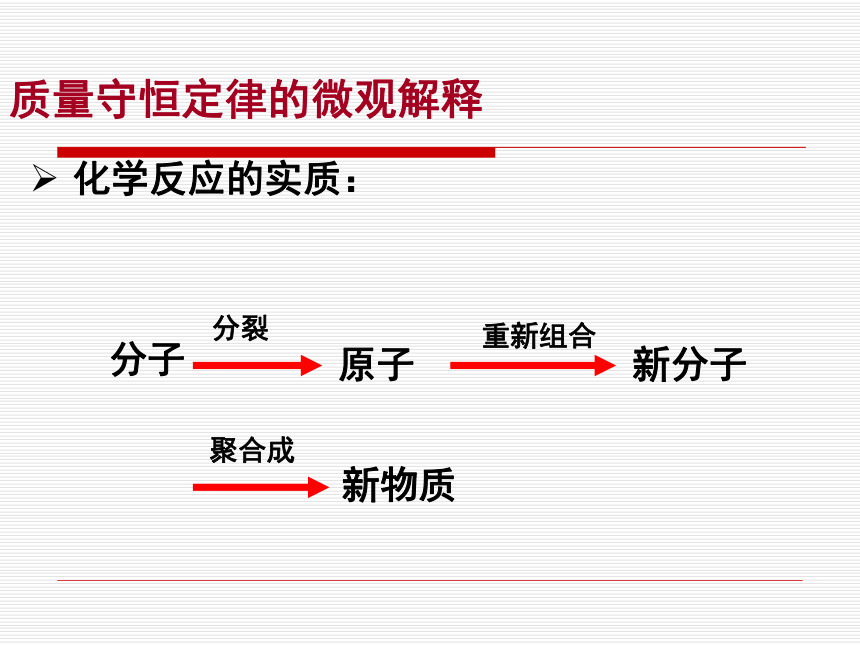
课件21张PPT。第五单元 化学方程式课题1 质量守恒定律实验1:质量守恒定律质量守恒定律实验2:碳酸钙与稀盐酸反应前后质量比较碳酸钙+稀盐酸 氯化钙+二氧化碳+水质量守恒定律实验3:碳酸钠与稀盐酸反应前后质量比较碳酸钠+稀盐酸 氯化钠+二氧化碳+水Na2CO3+2HCl 2NaCl+CO2↑+H2O镁+氧气 氧化镁2Mg+O2 2MgO碳+氧气 二氧化碳点燃C+O2 CO2点燃点燃点燃质量守恒定律实验4:实验5:实验6:概念:在化学反应前后各物质的质量总和相等定义:参加化学反应的各物质的质量总和,等于反应后生成的各物质质量总和。这个规律就是质量守恒定律。 质量守恒定律水的电解:守恒原因:化学反应前后原子的种类、数目和质量没有改变。原子是化学变化中的最小粒子,那么由相同原子构成的反应物与生成物在质量上有什么内在联系呢?质量守恒定律的微观解释分子新分子聚合成原子新物质分裂重新组合质量守恒定律的微观解释化学反应的实质:9在一切化学反应中,反应前后的原子种类没有改变,原子的数目没有增减,原子的质量也没有变化。所以反应前后各物质的质量总和必然相等。
质量守恒定律的微观解释从分子和原子观点来看:5个一定不变,2个一定变,1个可能变化学
反应
过程5个一定不变2个一定变1个可能变:宏观微观宏观:物质的种类原子的质量原子的数目原子的种类元素的种类反应物和生成物的总质量微观:分子的种类分子总数质量守恒定律的微观解释化学反应过程归纳:木炭在氧气中燃烧生成二氧化碳的化学方程式: C + o2 co2点燃C原子个数:O原子个数:原子总个数:该化学方程式等号两边的原子种类和数目都相等121233例如:质量守恒定律的微观解释原子数目原子质量原子种类物质的总质量元素质量元素种类物质的种类分子的种类分子个数可能发生改变质量守恒定律参加化学反应前后质量守恒定律的微观解释讨论:下列事实是否违背质量守恒定律??纸在空气中燃烧后化为灰烬,灰烬的质量比纸的质量小
高锰酸钾受热分解后,固体的质量变小
蜡烛燃烧后消失质量守恒定律的微观解释尝试用质量守恒定律解释下列问题1、 细铁丝在氧气中燃烧后,生成物的质量比细铁丝的质量大。2、加热氯酸钾与二氧化锰的混合物,剩余的固体质量减少了。因为细铁丝与氧气的质量和才等于生成的四氧化三铁的质量,所以生成物比细铁丝的质量大。因为剩余的固体与生成的氧气质量和才等于反应前的质量,而氧气是气体跑掉,所以剩余的固体质量减少了。质量守恒定律的微观解释定义:用化学式表示化学反应的式子。含义:表示反应物,生成物以及反应条件。表示反应物、生成物之间的质量关系(质量比)。表示反应物、生成物之间的粒子个数关系。
(粒子个数比)(化学计量数之比)化学方程式读法碳和氧气在点燃的条件下生成二氧化碳。1个碳原子和1个氧分子在点燃的条件下反应,生成1个二氧化碳分子。例如:C + O2 = CO2每12份质量的碳和32份质量的氧气在点燃的条件下反应生成44份质量的二氧化碳。化学方程式化学方程式书写原则1、以客观事实为基础2、遵循质量守恒定律化学方程式书写原则配平化学方程式常用的方法——观察法H2 + O2 —— H2O以反应式两边最复杂的化学式为“基准”,其他化学
式向“基准”看齐,在看齐的过程中添加适当的计量数。H2 + 1/2O2 —— H2O2H2 + O2 —— 2H2OKCIO3 —— KCI + 2/3O2KCIO3 —— KCI + O2————3KCIO3 —— 3KCI + 2O2化学方程式4P + 502 2P205
化学方程式的书写步骤之一写出反应物
生成物的化学式点燃P + O2 P2O5
配平4P + 502 2P2O5
标明反应发生条件查:检查化学式是否写错,
化学方程式是否配平,
条件和物质状态标注是否标了
标的是否恰当化学方程式
化学方程式的书写步骤之二写出反应物
生成物的化学式△KMnO4 K2MnO4+MnO2+O2配平2KMnO4 K2MnO4+MnO2+O2
标明反应发生条件标出生成物状态 “↑” “↓”KMnO4 K2MnO4+MnO2+O2KMnO4 K2MnO4+MnO2+O2↑(5)查:检查化学式是否写错,化学方程式是否配平,
条件和物质状态标注是否标了标的是否恰当化学方程式
质量守恒定律的微观解释从分子和原子观点来看:5个一定不变,2个一定变,1个可能变化学
反应
过程5个一定不变2个一定变1个可能变:宏观微观宏观:物质的种类原子的质量原子的数目原子的种类元素的种类反应物和生成物的总质量微观:分子的种类分子总数质量守恒定律的微观解释化学反应过程归纳:木炭在氧气中燃烧生成二氧化碳的化学方程式: C + o2 co2点燃C原子个数:O原子个数:原子总个数:该化学方程式等号两边的原子种类和数目都相等121233例如:质量守恒定律的微观解释原子数目原子质量原子种类物质的总质量元素质量元素种类物质的种类分子的种类分子个数可能发生改变质量守恒定律参加化学反应前后质量守恒定律的微观解释讨论:下列事实是否违背质量守恒定律??纸在空气中燃烧后化为灰烬,灰烬的质量比纸的质量小
高锰酸钾受热分解后,固体的质量变小
蜡烛燃烧后消失质量守恒定律的微观解释尝试用质量守恒定律解释下列问题1、 细铁丝在氧气中燃烧后,生成物的质量比细铁丝的质量大。2、加热氯酸钾与二氧化锰的混合物,剩余的固体质量减少了。因为细铁丝与氧气的质量和才等于生成的四氧化三铁的质量,所以生成物比细铁丝的质量大。因为剩余的固体与生成的氧气质量和才等于反应前的质量,而氧气是气体跑掉,所以剩余的固体质量减少了。质量守恒定律的微观解释定义:用化学式表示化学反应的式子。含义:表示反应物,生成物以及反应条件。表示反应物、生成物之间的质量关系(质量比)。表示反应物、生成物之间的粒子个数关系。
(粒子个数比)(化学计量数之比)化学方程式读法碳和氧气在点燃的条件下生成二氧化碳。1个碳原子和1个氧分子在点燃的条件下反应,生成1个二氧化碳分子。例如:C + O2 = CO2每12份质量的碳和32份质量的氧气在点燃的条件下反应生成44份质量的二氧化碳。化学方程式化学方程式书写原则1、以客观事实为基础2、遵循质量守恒定律化学方程式书写原则配平化学方程式常用的方法——观察法H2 + O2 —— H2O以反应式两边最复杂的化学式为“基准”,其他化学
式向“基准”看齐,在看齐的过程中添加适当的计量数。H2 + 1/2O2 —— H2O2H2 + O2 —— 2H2OKCIO3 —— KCI + 2/3O2KCIO3 —— KCI + O2————3KCIO3 —— 3KCI + 2O2化学方程式4P + 502 2P205
化学方程式的书写步骤之一写出反应物
生成物的化学式点燃P + O2 P2O5
配平4P + 502 2P2O5
标明反应发生条件查:检查化学式是否写错,
化学方程式是否配平,
条件和物质状态标注是否标了
标的是否恰当化学方程式
化学方程式的书写步骤之二写出反应物
生成物的化学式△KMnO4 K2MnO4+MnO2+O2配平2KMnO4 K2MnO4+MnO2+O2
标明反应发生条件标出生成物状态 “↑” “↓”KMnO4 K2MnO4+MnO2+O2KMnO4 K2MnO4+MnO2+O2↑(5)查:检查化学式是否写错,化学方程式是否配平,
条件和物质状态标注是否标了标的是否恰当化学方程式
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
