江苏省江阴市山观中学苏教版高一化学必修二专题二第一单元《化学反应速率》教学课件 (共21张PPT)
文档属性
| 名称 | 江苏省江阴市山观中学苏教版高一化学必修二专题二第一单元《化学反应速率》教学课件 (共21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-10-08 00:00:00 | ||
图片预览







文档简介
课件21张PPT。化学反应速率烟花的爆炸是瞬间完成溶洞的形成需要亿万年时间CaCO3+CO2+H2O=Ca(HCO3)2
Ca(HCO3)2=CaCO3+CO2↑+H2O①一次性快餐盒、塑料制品分解需要几百年。
②汽车尾气转化:2NO+2CO = N2+2CO2有的反应我们认为快一点好!有的反应我们认为慢一点好!乐山大佛腐蚀严重钢铁腐蚀一、化学反应速率1、含义:用来衡量化学反应进行快慢程度。
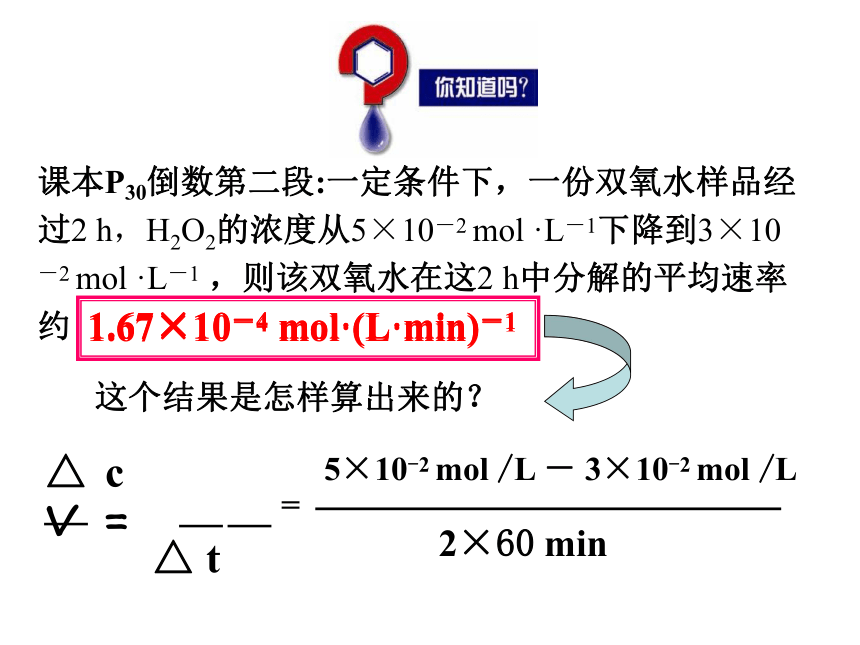
mol·(L· s)-1 或 mol·(L· min)-1 3、数学表达式:2、表示方法: 化学反应速率可以用单位时间内反应物浓度的减少或生成物浓度的增加来表示。4、单位:课本P30倒数第二段:一定条件下,一份双氧水样品经过2 h,H2O2的浓度从5×10-2 mol ·L-1下降到3×10-2 mol ·L-1 ,则该双氧水在这2 h中分解的平均速率约
△ c
V = ———
△ t
=5×10-2 mol /L - 3×10-2 mol /L2×60 min1.67×10-4 mol·(L·min)-11.67×10-4 mol·(L·min)-1同一反应中,用不同物质的浓度
变化来表示的反应速率是否相同?
其大小有什么关系呢? 起始物质的量/mol:
变化的物质的量/mol:
2min后物质的量/mol:例2、在2 L容积不变的容器中,发生 N2+3H2 NH3
的反应。现通3 mol H2 和 1mol N2 ,2 min 后生成了0.4
mol NH3 ,求V (H2)、 V (N2) 、V (NH3)。解: N2 + 3H2 2NH3V (N2) ︰V (H2) ︰ V (NH3) =1 ︰ 3 ︰ 21300.40.60.20.41-0.23-0.6V (H2) = V (N2) =V (NH3) ==0.05 mol·(L· min)-1 0.15mol·(L·min)-1 0.1mol·(L·min)-1 【归纳总结】
(1)定量表示一个化学反应的反应速率时, 必须指明是用哪一种反应物或生成物来表示。
(2)同一化学反应中,各物质的化学反应速率之比等于 .
(3)化学反应速率都取 值,且是某一段时间内的 速率。方程式中的化学计量数之比正平均★化学反应速率可能受到哪些因素的影响呢?外因:反应温度、催化剂、反应物的浓度、接触面积等 内因:反应物本身的性质
如何设计实验方案,探究温度、催化剂、反应物浓度、接触面积对化学反应速率的影响可供选用的试剂如下:
4%H2O2溶液,0.2mol/LFeCl3溶液,热水,MnO2
粉末, 3mol/L的盐酸,0.3mol/L的盐酸,碳酸
钙粉末,块状碳酸钙。【实验探究】实验一:取2只试管,各加入5mL 4%的过氧化氢溶液,分别滴入5滴0.2 mol·L-1氯化铁溶液,用水浴加热其中1支试管。实验二:取2只试管,各加入5 mL 4% H2O2溶液,往其中1支试管中加入少量二氧化锰粉末。实验三:取2只试管各加入3块碳酸钙固体,分别加入3mL3mol/L的盐酸和0.3mol/L的盐酸。实验四:取2只试管分别加入少量粉末状碳酸钙和块状碳酸钙,各加入3mL3mol/L的盐酸。水浴加热的
试管产生气
泡快加热能加快反应速率加入二氧化锰粉末的试管产生气泡快使用催化剂能加快反应速率浓度大的产生气泡快增大反应物的浓度能加快反应速率粉末状碳酸钙产生气泡快增大反应物的接触面积,能加快反应速率 温度催化剂浓度接触面积【归纳总结】增大加快越小越大越快浓度加快减小加快反应速率显著加快请问同学们的100米成绩为多少?如何计算速率?起始物质的量/mol:
变化的物质的量/mol:
2min后物质的量/mol:例2、在2 L容积不变的容器中,发生 N2+3H2 NH3
的反应。现通3 mol H2 和 1mol N2 ,2 min 后生成了0.4
mol NH3 ,求V (H2)、 V (N2) 、V (NH3)。解: N2 + 3H2 2NH3V (N2) ︰V (H2) ︰ V (NH3) =1 ︰ 3 ︰ 21300.40.60.20.41-0.23-0.6V (H2) = V (N2) =V (NH3) ==0.05 mol·(L· min)-1 0.15mol·(L·min)-1 0.1mol·(L·min)-1 溶洞的形成需要亿万年时间
Ca(HCO3)2=CaCO3+CO2↑+H2O①一次性快餐盒、塑料制品分解需要几百年。
②汽车尾气转化:2NO+2CO = N2+2CO2有的反应我们认为快一点好!有的反应我们认为慢一点好!乐山大佛腐蚀严重钢铁腐蚀一、化学反应速率1、含义:用来衡量化学反应进行快慢程度。
mol·(L· s)-1 或 mol·(L· min)-1 3、数学表达式:2、表示方法: 化学反应速率可以用单位时间内反应物浓度的减少或生成物浓度的增加来表示。4、单位:课本P30倒数第二段:一定条件下,一份双氧水样品经过2 h,H2O2的浓度从5×10-2 mol ·L-1下降到3×10-2 mol ·L-1 ,则该双氧水在这2 h中分解的平均速率约
△ c
V = ———
△ t
=5×10-2 mol /L - 3×10-2 mol /L2×60 min1.67×10-4 mol·(L·min)-11.67×10-4 mol·(L·min)-1同一反应中,用不同物质的浓度
变化来表示的反应速率是否相同?
其大小有什么关系呢? 起始物质的量/mol:
变化的物质的量/mol:
2min后物质的量/mol:例2、在2 L容积不变的容器中,发生 N2+3H2 NH3
的反应。现通3 mol H2 和 1mol N2 ,2 min 后生成了0.4
mol NH3 ,求V (H2)、 V (N2) 、V (NH3)。解: N2 + 3H2 2NH3V (N2) ︰V (H2) ︰ V (NH3) =1 ︰ 3 ︰ 21300.40.60.20.41-0.23-0.6V (H2) = V (N2) =V (NH3) ==0.05 mol·(L· min)-1 0.15mol·(L·min)-1 0.1mol·(L·min)-1 【归纳总结】
(1)定量表示一个化学反应的反应速率时, 必须指明是用哪一种反应物或生成物来表示。
(2)同一化学反应中,各物质的化学反应速率之比等于 .
(3)化学反应速率都取 值,且是某一段时间内的 速率。方程式中的化学计量数之比正平均★化学反应速率可能受到哪些因素的影响呢?外因:反应温度、催化剂、反应物的浓度、接触面积等 内因:反应物本身的性质
如何设计实验方案,探究温度、催化剂、反应物浓度、接触面积对化学反应速率的影响可供选用的试剂如下:
4%H2O2溶液,0.2mol/LFeCl3溶液,热水,MnO2
粉末, 3mol/L的盐酸,0.3mol/L的盐酸,碳酸
钙粉末,块状碳酸钙。【实验探究】实验一:取2只试管,各加入5mL 4%的过氧化氢溶液,分别滴入5滴0.2 mol·L-1氯化铁溶液,用水浴加热其中1支试管。实验二:取2只试管,各加入5 mL 4% H2O2溶液,往其中1支试管中加入少量二氧化锰粉末。实验三:取2只试管各加入3块碳酸钙固体,分别加入3mL3mol/L的盐酸和0.3mol/L的盐酸。实验四:取2只试管分别加入少量粉末状碳酸钙和块状碳酸钙,各加入3mL3mol/L的盐酸。水浴加热的
试管产生气
泡快加热能加快反应速率加入二氧化锰粉末的试管产生气泡快使用催化剂能加快反应速率浓度大的产生气泡快增大反应物的浓度能加快反应速率粉末状碳酸钙产生气泡快增大反应物的接触面积,能加快反应速率 温度催化剂浓度接触面积【归纳总结】增大加快越小越大越快浓度加快减小加快反应速率显著加快请问同学们的100米成绩为多少?如何计算速率?起始物质的量/mol:
变化的物质的量/mol:
2min后物质的量/mol:例2、在2 L容积不变的容器中,发生 N2+3H2 NH3
的反应。现通3 mol H2 和 1mol N2 ,2 min 后生成了0.4
mol NH3 ,求V (H2)、 V (N2) 、V (NH3)。解: N2 + 3H2 2NH3V (N2) ︰V (H2) ︰ V (NH3) =1 ︰ 3 ︰ 21300.40.60.20.41-0.23-0.6V (H2) = V (N2) =V (NH3) ==0.05 mol·(L· min)-1 0.15mol·(L·min)-1 0.1mol·(L·min)-1 溶洞的形成需要亿万年时间
