北京市2015年教师培训人教版选修四《化学反应原理的综合应用—再看合成氨》课件 (共22张PPT)
文档属性
| 名称 | 北京市2015年教师培训人教版选修四《化学反应原理的综合应用—再看合成氨》课件 (共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 5.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-10-09 00:00:00 | ||
图片预览








文档简介
课件22张PPT。
反应原理的综合应用
---再看合成氨我们为什么会缺氮?生命元素--氮N植物动物 氮气78%人
类
用
氮
的
历
史“人类向空气要面包成功了,合成氨是历史上最伟大的成就之一。” 哈伯与合成氨合成氨从第一次实验室研制到工业化投产经历了约150年的时间。德国科学家哈伯在10年的时间内进行了无数次的探索,单是寻找高效稳定的催化剂,2年间他们就进行了多达6500次试验,测试了2500种不同的配方,最后选定了一种合适的催化剂,使合成氨的设想在1913年成为工业现实。鉴于合成氨工业的实现,瑞典皇家科学院于1918年向哈伯颁发了诺贝尔化学奖。
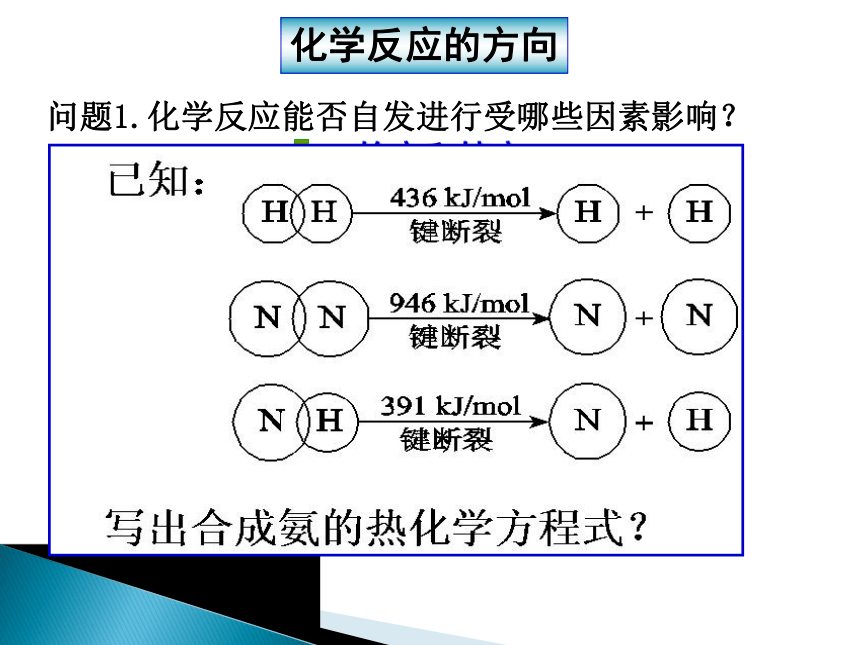
问题1.化学反应能否自发进行受哪些因素影响?化学反应的方向焓变和熵变问题2.分析合成氨反应的焓变和熵变?H<0 ?S<0? 资料卡片--选修4:P38科学视野合成氨反应是一个可逆反应: N2(g)+3H2(g) 2NH3(g)?H-T ?S= -33.1KJ·mol-1<0问题1.化学反应能否自发进行受哪些因素影响?化学反应的方向焓变和熵变问题2.分析合成氨反应的焓变和熵变?H<0 ?S<0?△G <0,反应自发进行问题3:根据你所学的知识,分析合成氨反应难以
发生的原因是什么?(从反应物性质考虑)N≡N 键能很大,N2很不活泼(3)便宜(4)绿色(2)快(1)多【交流】即提高平衡混合物里氨的含量
——化学平衡问题即提高单位时间里氨的产量
——化学反应速率问题成本低,如对耐高温设备
所需材料的要求。即注意环境保护,反应物利用率接近百分之百 假如你是化工厂的厂长,在合成氨的
工业生产过程中,你有什么要求?【交流·研讨】根据此反应特点从理论上分析:
1.什么条件有利于提高合成氨的速率?化学反应的速率和限度 2.用化学平衡移动的知识分析什么条件
有利于提高NH3的含量??H<0 ?S<0理论分析合成氨的适宜条件浓度催化剂温度压强速率分析使NH3生产得快外界条件高压高温使用增大反应物浓度平衡分析使NH3生产得多高压低温无影响增大反应物浓度或减小生成物浓度?原料气氮氢物质的量比与平衡混合气中NH3%的关系图数据分析1---浓度选择 思考:浓度怎么定? N2 和H2的比例怎么定?从平衡的角度,在N2和H2的物质的量比为1:3时,平衡转化率最大。实验测得适当提高N2的浓度,即N2和H2的物质的量比为1:2.8时,更能促进氨的合成。
实际生产中的处理方法:及时将气态氨冷却液化分离出去;及时将氮气和氢气循环利用,使其保持一定的浓度。数据分析2—压强和温度选择反应达到平衡状态时平衡混合气中氨的含量与T、P有什么关系?工业合成氨是否压强越高越好?理论采用: 压强越大越好压强越大,对设备的要求高、压缩H2和N2所需要的动力大,成本高,因此选择压强应符合实际科学技术。实际采用:20MPa~50MPa压强选择理论采用: 高转化率和高速率所用条件矛盾实际采用: 500℃在500℃条件下,催化剂活性最高;
转化率也适当。温度选择 使用催化剂可使合成氨反应
的速率提高上万亿倍。数据分析3—催化剂选择降低活化能归纳高压(20MPa~50MPa) 适宜温度(500℃左右)使用铁触媒作催化剂N2和H2的物质的量比为1:2.8的投料比;及时分离出液态氨新技术1---电化学:
1998年两位希腊化学家提出了电解合成氨的新思路,采用高质子导电性的SCY陶瓷(能传递H+)为介质,实现了高温(570℃)常压下高转化率的电解法合成氨,装置如下图:钯电极A是电解池的 极(填“阳”或“阴”),该极上的电极反应式是 。 阴N2+6e-+6H+=2NH3(78%)新技术2---利用原电池原理:
有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。
电池正极的电极反应式是
A是N2+ 8H+ + 6e- =2NH4+ NH4Cl 科学家用一种含钼的化合物作催化剂,在常温下就能完成氨的合成,从而大大降低了生产成本,使得液氨有望取代液氢成为新一代绿色能源。常温人
类
用
氮
的
未
来氨
经济化学反应条件的优化本 节 内 容氨在解决人类粮食问题中的重要作用 ——化学的伟大贡献人类
发展环境
保护温室效应
水体污染
酸雨固氮引起关注化学与可持续发展
反应原理的综合应用
---再看合成氨我们为什么会缺氮?生命元素--氮N植物动物 氮气78%人
类
用
氮
的
历
史“人类向空气要面包成功了,合成氨是历史上最伟大的成就之一。” 哈伯与合成氨合成氨从第一次实验室研制到工业化投产经历了约150年的时间。德国科学家哈伯在10年的时间内进行了无数次的探索,单是寻找高效稳定的催化剂,2年间他们就进行了多达6500次试验,测试了2500种不同的配方,最后选定了一种合适的催化剂,使合成氨的设想在1913年成为工业现实。鉴于合成氨工业的实现,瑞典皇家科学院于1918年向哈伯颁发了诺贝尔化学奖。
问题1.化学反应能否自发进行受哪些因素影响?化学反应的方向焓变和熵变问题2.分析合成氨反应的焓变和熵变?H<0 ?S<0? 资料卡片--选修4:P38科学视野合成氨反应是一个可逆反应: N2(g)+3H2(g) 2NH3(g)?H-T ?S= -33.1KJ·mol-1<0问题1.化学反应能否自发进行受哪些因素影响?化学反应的方向焓变和熵变问题2.分析合成氨反应的焓变和熵变?H<0 ?S<0?△G <0,反应自发进行问题3:根据你所学的知识,分析合成氨反应难以
发生的原因是什么?(从反应物性质考虑)N≡N 键能很大,N2很不活泼(3)便宜(4)绿色(2)快(1)多【交流】即提高平衡混合物里氨的含量
——化学平衡问题即提高单位时间里氨的产量
——化学反应速率问题成本低,如对耐高温设备
所需材料的要求。即注意环境保护,反应物利用率接近百分之百 假如你是化工厂的厂长,在合成氨的
工业生产过程中,你有什么要求?【交流·研讨】根据此反应特点从理论上分析:
1.什么条件有利于提高合成氨的速率?化学反应的速率和限度 2.用化学平衡移动的知识分析什么条件
有利于提高NH3的含量??H<0 ?S<0理论分析合成氨的适宜条件浓度催化剂温度压强速率分析使NH3生产得快外界条件高压高温使用增大反应物浓度平衡分析使NH3生产得多高压低温无影响增大反应物浓度或减小生成物浓度?原料气氮氢物质的量比与平衡混合气中NH3%的关系图数据分析1---浓度选择 思考:浓度怎么定? N2 和H2的比例怎么定?从平衡的角度,在N2和H2的物质的量比为1:3时,平衡转化率最大。实验测得适当提高N2的浓度,即N2和H2的物质的量比为1:2.8时,更能促进氨的合成。
实际生产中的处理方法:及时将气态氨冷却液化分离出去;及时将氮气和氢气循环利用,使其保持一定的浓度。数据分析2—压强和温度选择反应达到平衡状态时平衡混合气中氨的含量与T、P有什么关系?工业合成氨是否压强越高越好?理论采用: 压强越大越好压强越大,对设备的要求高、压缩H2和N2所需要的动力大,成本高,因此选择压强应符合实际科学技术。实际采用:20MPa~50MPa压强选择理论采用: 高转化率和高速率所用条件矛盾实际采用: 500℃在500℃条件下,催化剂活性最高;
转化率也适当。温度选择 使用催化剂可使合成氨反应
的速率提高上万亿倍。数据分析3—催化剂选择降低活化能归纳高压(20MPa~50MPa) 适宜温度(500℃左右)使用铁触媒作催化剂N2和H2的物质的量比为1:2.8的投料比;及时分离出液态氨新技术1---电化学:
1998年两位希腊化学家提出了电解合成氨的新思路,采用高质子导电性的SCY陶瓷(能传递H+)为介质,实现了高温(570℃)常压下高转化率的电解法合成氨,装置如下图:钯电极A是电解池的 极(填“阳”或“阴”),该极上的电极反应式是 。 阴N2+6e-+6H+=2NH3(78%)新技术2---利用原电池原理:
有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。
电池正极的电极反应式是
A是N2+ 8H+ + 6e- =2NH4+ NH4Cl 科学家用一种含钼的化合物作催化剂,在常温下就能完成氨的合成,从而大大降低了生产成本,使得液氨有望取代液氢成为新一代绿色能源。常温人
类
用
氮
的
未
来氨
经济化学反应条件的优化本 节 内 容氨在解决人类粮食问题中的重要作用 ——化学的伟大贡献人类
发展环境
保护温室效应
水体污染
酸雨固氮引起关注化学与可持续发展
