北京市昌平一中大2015年说课人教版必修一3.2《几种重要的金属化合物—硫酸亚铁》说课课件 (共28张PPT)
文档属性
| 名称 | 北京市昌平一中大2015年说课人教版必修一3.2《几种重要的金属化合物—硫酸亚铁》说课课件 (共28张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-10-09 00:00:00 | ||
图片预览




文档简介
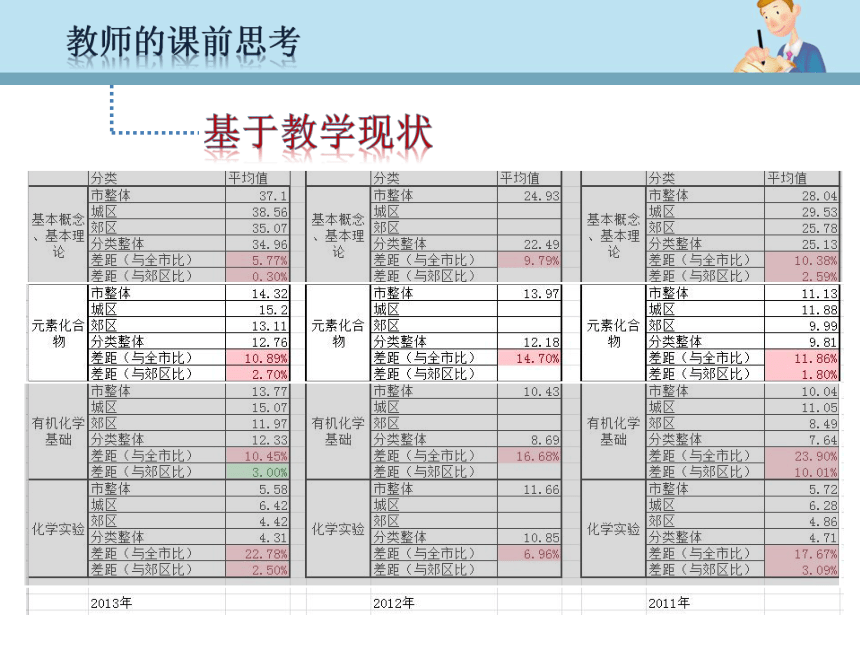
课件28张PPT。基于“分类观”和“价态观”的物质性质教学《硫酸亚铁》 基于“分类观”和“价态观”的教学分析基于“分类观”和“价态观”的教学策略设计教师的课前思考本节课的教学反思《硫酸亚铁》 教师教师的课前思考基于教学现状教师的课前思考第三章:金属及其化合物
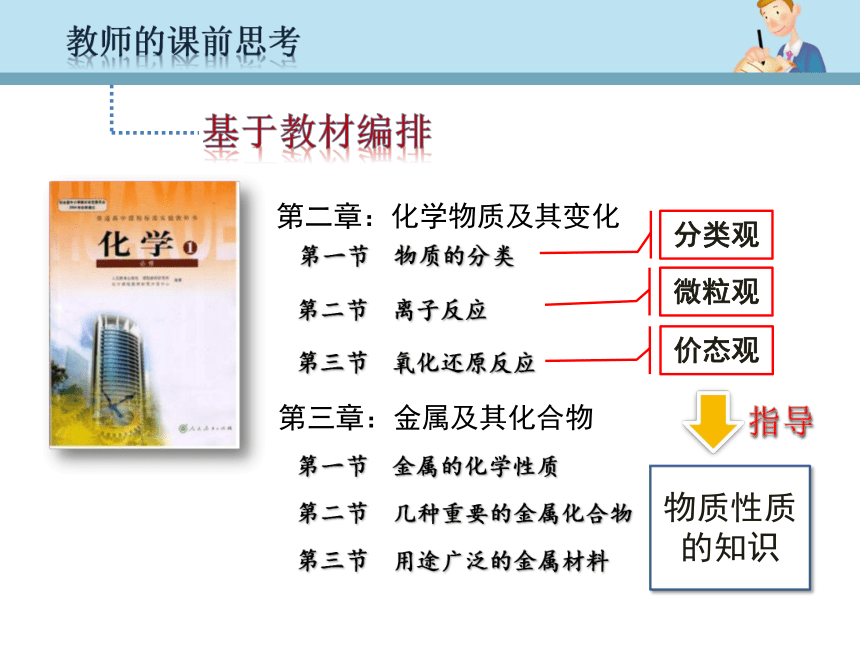
第二章:化学物质及其变化第一节 物质的分类第三节 氧化还原反应第二节 离子反应第一节 金属的化学性质第三节 用途广泛的金属材料第二节 几种重要的金属化合物分类观微粒观价态观物质性质的知识指导基于教材编排教师的课前思考“分类观”
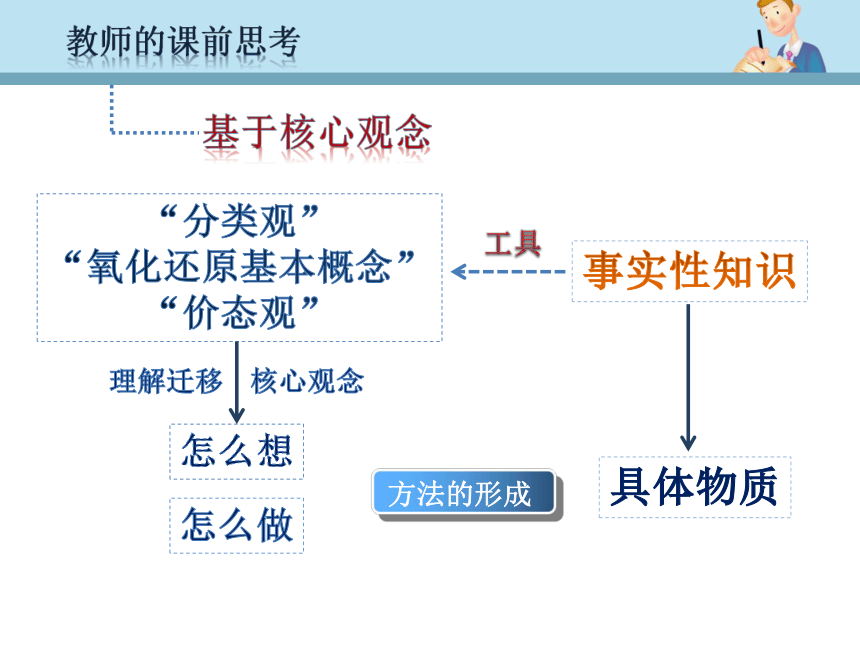
“氧化还原基本概念”
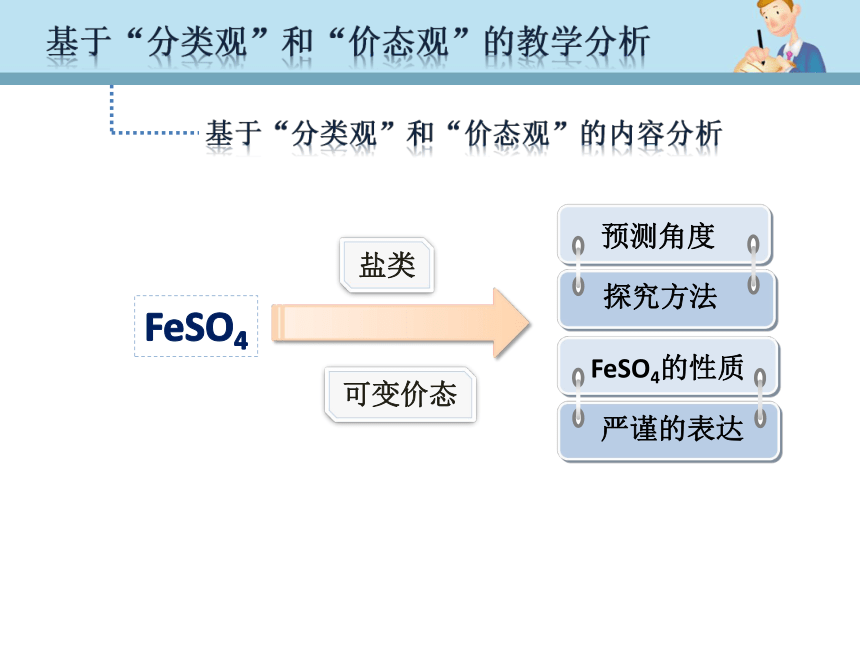
“价态观”事实性知识工具具体物质理解迁移 核心观念怎么想怎么做基于核心观念基于“分类观”和“价态观”的教学分析基于“分类观”和“价态观”的内容分析FeSO4盐类可变价态基于“分类观”和“价态观”的教学分析基于“分类观”和“价态观”的学生特点分析初中元素化合物知识及技能的储备初步学习了物质的分类,离子反应及氧化还原反应在学习过程中善于运用类比的方法在实验过程中仍然以兴趣为主不知道为什么学,
模糊的“类别”意识,不能从核心元素的价态分析物质性质。预测性质无根据实验探究思路混乱,不严谨,表达不清基于“分类观”和“价态观”的教学分析基于核心观念的教学目标1.知识与技能①认识 。
②知道Fe3+的检验方法。能初步预测三价铁盐的
化学性质。
③初步建立起研究物质性质的一般方法和思路。2.过程与方法①经历对硫酸亚铁化学性质的探究过程。
②
③能对自己的化学学习过程进行反思,用完
整的语言表达研究物质性质的一般过程。3.情感态度与
价值观感受化学对于日常生活的重要影响。感受理性的探究过程,体会理论知识在探究物质性质上的具体作用。硫酸亚铁的性质能够从物质“类别”及核心元素的“价态”分
析预测物质的性质重点难点基于“分类观”和“价态观”的教学策略设计教师经验行为
学生的方法是教师“栽”进去的,
还是自己“长”出来的?基于“分类观”和“价态观”的教学策略设计教学环节情境引入分析探究反思小结 从生活常识、保存、及物理性质方面初识硫酸亚铁。 预测性质,暴露学生在学习物质性质的一些问题整理预测思路。从行为上体会研究物质性质的一般过程从语言上提炼研究物质性质的一般过程预测性质 应用研究方法及物质的性质解决实际问题
巩固应用环节一:初识硫酸亚铁核心问题①硫酸亚铁固体是一种什么样的物质呢?它的溶液又是什么样的呢?
?②硫酸亚铁具有怎样的化学性质?在使用和保存方面又应该注意些什么?情境创设学生活动
观察
FeSO4?7H2O晶体
FeSO4溶液
在实验报告单上填写它们的外观、颜色。环节二:预测FeSO4的化学性质核心问题问题序列学生活动环节二:预测FeSO4的化学性质生1 、 NaOH溶液
生2 NaOH溶液、Zn
生3 NaOH溶液、Zn
生4 H2O2溶液暴露学生在学习物质性质的一些问题:
①预测无角度,仅凭借兴趣和好奇心。
②预测反应无理论依据,漫无目的的猜测。酸性KMnO4溶液盐酸教学意图环节三:分析性质总结方法教学策略追问学生回答--分类观的建构“类别”意识模糊环节三:分析性质总结方法教师活动追问学生回答--分类观的建构形成“类别”角度捋清思路,建构思维过程学科思想方法外显环节三:分析性质总结方法--分类观的建构教学策略追问学生回答(4)回忆初中的知识,高锰酸钾可以用来干什么 ?
(5)氧气的氧化能力强不强?生:制氧气
生:强环节三:分析性质总结方法--价态观的建构没有“价态”角度,缺乏对物质氧化性、还原性的基本认识教师活动追问学生回答环节三:分析性质总结方法--分类观的建构教师活动追问学生回答环节三:分析性质总结方法--分类观的建构形成角度,关注物质氧化性、还原性形成分析模型教师活动追问学生回答(15)你预测硫酸亚铁还具有什么
性质?
(16)你是基于什么预测的?生 :预测硫酸亚铁还具备氧化性
因为硫酸亚铁中铁是中间价态,既可以变为+3价也可以变为0价。铁元素的价态还能够降低。
选择具有还原性的金属锌与之反应。(17)如果你没有观察到锌和硫酸亚铁的置换反应,你怎么分析硫酸亚铁可能具有氧化性呢?
(18)你打算选择什么试剂来验证你的预测?环节三:分析性质总结方法--分类观的建构应用分析模型FeSO4分享你的预测 FeSO4+2Fe3++32+还原剂 氧化剂 还原性 0Fe氧化剂 还原剂氧化性 形成方法指导其他元素化合物的学习
环节三:分析性质总结方法教师活动指导实验学生活动进行实验
记录实验现象
描述实验过程汇报实验结果环节四:反思过程、提炼方法物质类别化合价类别通性氧化性
还原性环节五:应用方法,预测新物质环节五:应用方法,预测新物质核心问题板书设计硫酸亚铁
一、外观
FeSO4?7H2O:浅绿色晶体 FeSO4溶液:浅绿色
二、化学性质
1.盐—盐类通性
与碱反应(复分解)
与金属单质反应(置换)
2.氧化还原反应
①氧化性
FeSO4+还原剂(Zn)
②还原性
FeSO4+氧化剂[KMnO4(H+)、氯水、H2O2(H+)溶液]
本节课的教学反思(1)基于“核心观念”建构的问题设计和实施策略(2)基于方法形成的学案设计(3)教学中的问题启示重视并加强核心概念和核心观念的功能性教学谢 谢!
第二章:化学物质及其变化第一节 物质的分类第三节 氧化还原反应第二节 离子反应第一节 金属的化学性质第三节 用途广泛的金属材料第二节 几种重要的金属化合物分类观微粒观价态观物质性质的知识指导基于教材编排教师的课前思考“分类观”
“氧化还原基本概念”
“价态观”事实性知识工具具体物质理解迁移 核心观念怎么想怎么做基于核心观念基于“分类观”和“价态观”的教学分析基于“分类观”和“价态观”的内容分析FeSO4盐类可变价态基于“分类观”和“价态观”的教学分析基于“分类观”和“价态观”的学生特点分析初中元素化合物知识及技能的储备初步学习了物质的分类,离子反应及氧化还原反应在学习过程中善于运用类比的方法在实验过程中仍然以兴趣为主不知道为什么学,
模糊的“类别”意识,不能从核心元素的价态分析物质性质。预测性质无根据实验探究思路混乱,不严谨,表达不清基于“分类观”和“价态观”的教学分析基于核心观念的教学目标1.知识与技能①认识 。
②知道Fe3+的检验方法。能初步预测三价铁盐的
化学性质。
③初步建立起研究物质性质的一般方法和思路。2.过程与方法①经历对硫酸亚铁化学性质的探究过程。
②
③能对自己的化学学习过程进行反思,用完
整的语言表达研究物质性质的一般过程。3.情感态度与
价值观感受化学对于日常生活的重要影响。感受理性的探究过程,体会理论知识在探究物质性质上的具体作用。硫酸亚铁的性质能够从物质“类别”及核心元素的“价态”分
析预测物质的性质重点难点基于“分类观”和“价态观”的教学策略设计教师经验行为
学生的方法是教师“栽”进去的,
还是自己“长”出来的?基于“分类观”和“价态观”的教学策略设计教学环节情境引入分析探究反思小结 从生活常识、保存、及物理性质方面初识硫酸亚铁。 预测性质,暴露学生在学习物质性质的一些问题整理预测思路。从行为上体会研究物质性质的一般过程从语言上提炼研究物质性质的一般过程预测性质 应用研究方法及物质的性质解决实际问题
巩固应用环节一:初识硫酸亚铁核心问题①硫酸亚铁固体是一种什么样的物质呢?它的溶液又是什么样的呢?
?②硫酸亚铁具有怎样的化学性质?在使用和保存方面又应该注意些什么?情境创设学生活动
观察
FeSO4?7H2O晶体
FeSO4溶液
在实验报告单上填写它们的外观、颜色。环节二:预测FeSO4的化学性质核心问题问题序列学生活动环节二:预测FeSO4的化学性质生1 、 NaOH溶液
生2 NaOH溶液、Zn
生3 NaOH溶液、Zn
生4 H2O2溶液暴露学生在学习物质性质的一些问题:
①预测无角度,仅凭借兴趣和好奇心。
②预测反应无理论依据,漫无目的的猜测。酸性KMnO4溶液盐酸教学意图环节三:分析性质总结方法教学策略追问学生回答--分类观的建构“类别”意识模糊环节三:分析性质总结方法教师活动追问学生回答--分类观的建构形成“类别”角度捋清思路,建构思维过程学科思想方法外显环节三:分析性质总结方法--分类观的建构教学策略追问学生回答(4)回忆初中的知识,高锰酸钾可以用来干什么 ?
(5)氧气的氧化能力强不强?生:制氧气
生:强环节三:分析性质总结方法--价态观的建构没有“价态”角度,缺乏对物质氧化性、还原性的基本认识教师活动追问学生回答环节三:分析性质总结方法--分类观的建构教师活动追问学生回答环节三:分析性质总结方法--分类观的建构形成角度,关注物质氧化性、还原性形成分析模型教师活动追问学生回答(15)你预测硫酸亚铁还具有什么
性质?
(16)你是基于什么预测的?生 :预测硫酸亚铁还具备氧化性
因为硫酸亚铁中铁是中间价态,既可以变为+3价也可以变为0价。铁元素的价态还能够降低。
选择具有还原性的金属锌与之反应。(17)如果你没有观察到锌和硫酸亚铁的置换反应,你怎么分析硫酸亚铁可能具有氧化性呢?
(18)你打算选择什么试剂来验证你的预测?环节三:分析性质总结方法--分类观的建构应用分析模型FeSO4分享你的预测 FeSO4+2Fe3++32+还原剂 氧化剂 还原性 0Fe氧化剂 还原剂氧化性 形成方法指导其他元素化合物的学习
环节三:分析性质总结方法教师活动指导实验学生活动进行实验
记录实验现象
描述实验过程汇报实验结果环节四:反思过程、提炼方法物质类别化合价类别通性氧化性
还原性环节五:应用方法,预测新物质环节五:应用方法,预测新物质核心问题板书设计硫酸亚铁
一、外观
FeSO4?7H2O:浅绿色晶体 FeSO4溶液:浅绿色
二、化学性质
1.盐—盐类通性
与碱反应(复分解)
与金属单质反应(置换)
2.氧化还原反应
①氧化性
FeSO4+还原剂(Zn)
②还原性
FeSO4+氧化剂[KMnO4(H+)、氯水、H2O2(H+)溶液]
本节课的教学反思(1)基于“核心观念”建构的问题设计和实施策略(2)基于方法形成的学案设计(3)教学中的问题启示重视并加强核心概念和核心观念的功能性教学谢 谢!
