北京市第十五中学2015年说课人教版必修一3.2《几种重要的金属化合物—三价铁离子的氧化性》说课课件 (共27张PPT)
文档属性
| 名称 | 北京市第十五中学2015年说课人教版必修一3.2《几种重要的金属化合物—三价铁离子的氧化性》说课课件 (共27张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-10-09 00:00:00 | ||
图片预览





文档简介
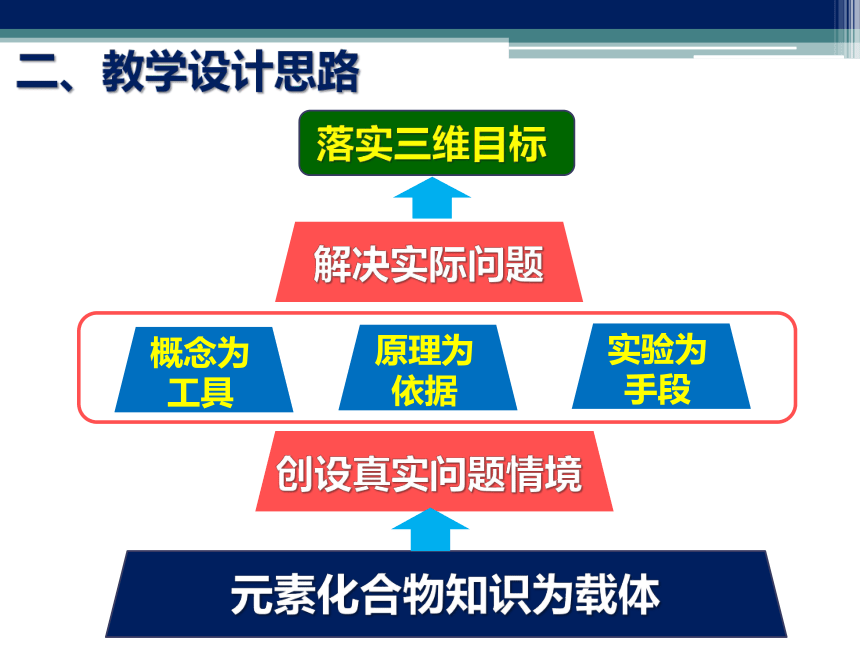
课件27张PPT。——以“Fe3+的氧化性”为例说课建构研究物质性质的方法一、学情分析预测物质性质实验验证得出结论类别氧化还原能够研究简单的化学问题已具备的能力如何研究真实情景中的化学问题?影响因素众多实验现象复杂一、学情分析已有研究方法?如何突破?物质性质化学反应表达已适当拓展二、教学设计思路元素化合物知识为载体概念为
工具原理为
依据实验为
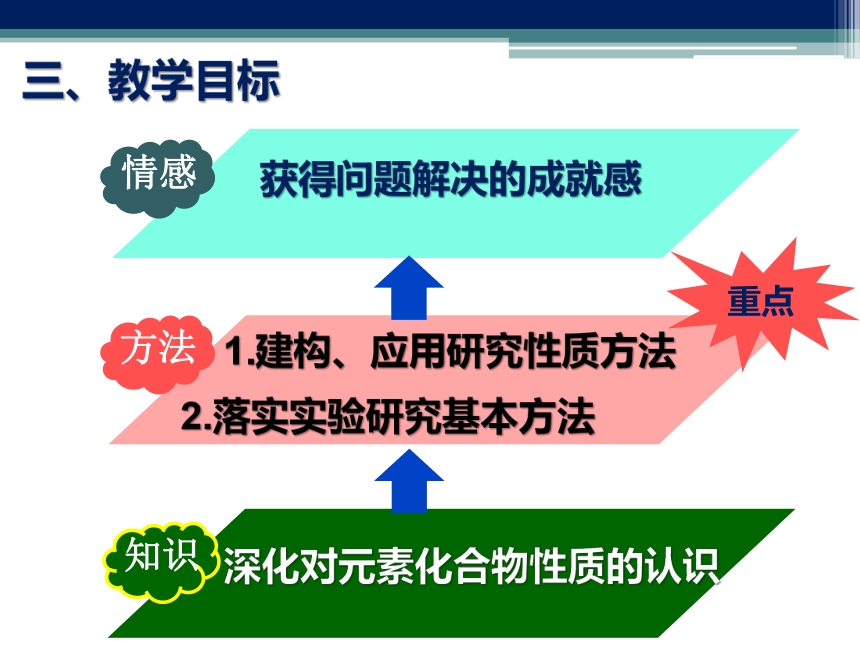
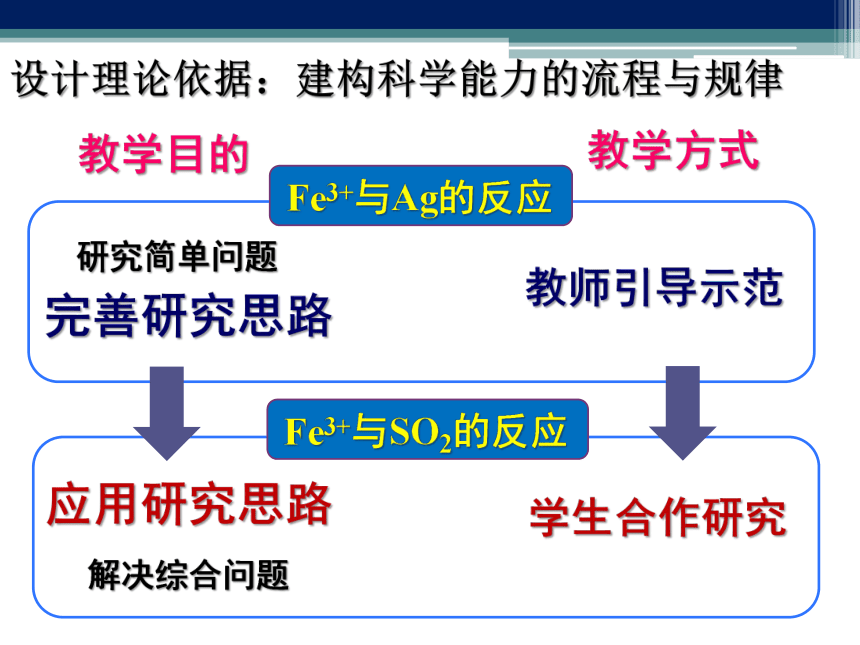
手段创设真实问题情境解决实际问题落实三维目标深化对元素化合物性质的认识1.建构、应用研究性质方法2.落实实验研究基本方法获得问题解决的成就感三、教学目标四、教学框架思路载体:Fe3+的氧化性还原剂按强弱分类强还原剂按组成分类单质化合物AgSO2弱还原剂完善研究思路 应用研究思路教师引导示范 学生合作研究 研究简单问题解决综合问题Fe3+与Ag的反应Fe3+与SO2的反应教学目的教学方式设计理论依据:建构科学能力的流程与规律Fe3+与Ag的反应反应能否发生?如何让实验现象更加明显?Fe3+与SO2的反应研究问题能力发展有哪些反应发生?控制反应的因素是什么?预测、验证调控反应
达到目的研究多影响因素
复杂体系五、具体教学流程1.引入阶段从熟悉入手Fe3++ 还原剂单质化合物Fe、Cu ……H2SO3、SO32-……建立冲突Fe3++ 弱还原剂提问:如何证明Fe3+是一种强氧化剂??还原剂单质CuK、Ca、Na、…H、Cu、Hg、Ag、Pt、Au选择比铜还不活泼的金属2.研究Fe3+与Ag的反应层次1:解决反应能否发生Fe3+ + Ag = Fe2++Ag+预测实验无现象层次2:如何让银镜溶解更明显?Fe3+ + Ag = Fe2++Ag+学生汇报主要方案1.加热4.提高Fe2(SO4)3浓度3.加NaCl固体2.加盐酸5.换FeCl3溶液思维角度混乱学生汇报主要方案思维角度有序化提高速率加热提高c(Fe3+)平衡正移加盐酸加NaCl固体换FeCl3溶液提高c(Fe3+)降低c(Ag+)?实验等量化原则银镜银镜大量
溶解氧化还原预测物质性质Fe3+ + Ag = Fe2++Ag+反应发生得出结论实验验证层次3:课堂小结——建立思路检验Fe2+学生已有的研究思路氧化还原预测物质性质Fe3+ + Ag = Fe2++Ag+层次3:课堂小结——建立思路研究化学反应得出结论实验验证调控反应Fe3+ + Ag = Fe2++Ag+Cl-对反应的影响3.研究Fe3+与SO2的反应2Fe3+ + SO2+2H2O = 2Fe2++SO42-+4H+预测棕黄浅绿实验溶液变红学生主动讨论假设2:反应发生(红色掩盖绿色)能证明吗?假设1:反应不发生层次1:常规预测层次2:反应发生了吗?证明反应发生2Fe3+ + SO2+2H2O = 2Fe2++SO42-+4H+生成物生成反应物消失检验Fe2+检验SO42-检验Fe3+评价方案SO42-Fe3+不严谨有O2干扰无丁达尔效应Fe(OH)3胶体×研究手段补充资料法层次3:研究红色物质究竟是什么?层次4:研究控制反应的因素资料法Fe2+Fe(SO2)63+1秒钟60分钟2.8×10-5 mol/L2.1×10-2 mol/L0.1 mol/L检测不出实验现象Fe3+初始浓度为 0.1 mol/LFe2+Fe(SO2)63+1秒钟60分钟2.8×10-5 mol/L2.1×10-2 mol/L0.1 mol/L检测不出实验现象Fe3++SO2Fe(SO2)63+ Fe2+“竞争关系”4.课堂总结Fe3+的氧化性Fe3++Ag—建立研究思路Fe3++SO2—应用研究思路分类
氧化还原速率
限度实验
证据知识 深化对Fe3+氧化性认识方法 建构研究物质性质的方法研究化学反应5.课后思考——应用与延伸如何研究SO2还原性?如何分析SO2与漂粉精溶液反应出现的复杂现象?六、反思与收获1.必修综合复习课的方式元素化合物、概念、原理、实验解决复杂实际问题基本知识基本方法学生能力在实际应用中得以提升
化学素养在提升中得到发展2.本堂课的推广价值Fe3+的氧化性ClO-的氧化性?+4价 S 的还原性?HNO3的氧化性?……研究对象可以改变,但研究方法不变谢 谢 聆 听
工具原理为
依据实验为
手段创设真实问题情境解决实际问题落实三维目标深化对元素化合物性质的认识1.建构、应用研究性质方法2.落实实验研究基本方法获得问题解决的成就感三、教学目标四、教学框架思路载体:Fe3+的氧化性还原剂按强弱分类强还原剂按组成分类单质化合物AgSO2弱还原剂完善研究思路 应用研究思路教师引导示范 学生合作研究 研究简单问题解决综合问题Fe3+与Ag的反应Fe3+与SO2的反应教学目的教学方式设计理论依据:建构科学能力的流程与规律Fe3+与Ag的反应反应能否发生?如何让实验现象更加明显?Fe3+与SO2的反应研究问题能力发展有哪些反应发生?控制反应的因素是什么?预测、验证调控反应
达到目的研究多影响因素
复杂体系五、具体教学流程1.引入阶段从熟悉入手Fe3++ 还原剂单质化合物Fe、Cu ……H2SO3、SO32-……建立冲突Fe3++ 弱还原剂提问:如何证明Fe3+是一种强氧化剂??还原剂单质CuK、Ca、Na、…H、Cu、Hg、Ag、Pt、Au选择比铜还不活泼的金属2.研究Fe3+与Ag的反应层次1:解决反应能否发生Fe3+ + Ag = Fe2++Ag+预测实验无现象层次2:如何让银镜溶解更明显?Fe3+ + Ag = Fe2++Ag+学生汇报主要方案1.加热4.提高Fe2(SO4)3浓度3.加NaCl固体2.加盐酸5.换FeCl3溶液思维角度混乱学生汇报主要方案思维角度有序化提高速率加热提高c(Fe3+)平衡正移加盐酸加NaCl固体换FeCl3溶液提高c(Fe3+)降低c(Ag+)?实验等量化原则银镜银镜大量
溶解氧化还原预测物质性质Fe3+ + Ag = Fe2++Ag+反应发生得出结论实验验证层次3:课堂小结——建立思路检验Fe2+学生已有的研究思路氧化还原预测物质性质Fe3+ + Ag = Fe2++Ag+层次3:课堂小结——建立思路研究化学反应得出结论实验验证调控反应Fe3+ + Ag = Fe2++Ag+Cl-对反应的影响3.研究Fe3+与SO2的反应2Fe3+ + SO2+2H2O = 2Fe2++SO42-+4H+预测棕黄浅绿实验溶液变红学生主动讨论假设2:反应发生(红色掩盖绿色)能证明吗?假设1:反应不发生层次1:常规预测层次2:反应发生了吗?证明反应发生2Fe3+ + SO2+2H2O = 2Fe2++SO42-+4H+生成物生成反应物消失检验Fe2+检验SO42-检验Fe3+评价方案SO42-Fe3+不严谨有O2干扰无丁达尔效应Fe(OH)3胶体×研究手段补充资料法层次3:研究红色物质究竟是什么?层次4:研究控制反应的因素资料法Fe2+Fe(SO2)63+1秒钟60分钟2.8×10-5 mol/L2.1×10-2 mol/L0.1 mol/L检测不出实验现象Fe3+初始浓度为 0.1 mol/LFe2+Fe(SO2)63+1秒钟60分钟2.8×10-5 mol/L2.1×10-2 mol/L0.1 mol/L检测不出实验现象Fe3++SO2Fe(SO2)63+ Fe2+“竞争关系”4.课堂总结Fe3+的氧化性Fe3++Ag—建立研究思路Fe3++SO2—应用研究思路分类
氧化还原速率
限度实验
证据知识 深化对Fe3+氧化性认识方法 建构研究物质性质的方法研究化学反应5.课后思考——应用与延伸如何研究SO2还原性?如何分析SO2与漂粉精溶液反应出现的复杂现象?六、反思与收获1.必修综合复习课的方式元素化合物、概念、原理、实验解决复杂实际问题基本知识基本方法学生能力在实际应用中得以提升
化学素养在提升中得到发展2.本堂课的推广价值Fe3+的氧化性ClO-的氧化性?+4价 S 的还原性?HNO3的氧化性?……研究对象可以改变,但研究方法不变谢 谢 聆 听
