人教版选修四化学高二上学期期末考试卷二(含解析)
文档属性
| 名称 | 人教版选修四化学高二上学期期末考试卷二(含解析) |  | |
| 格式 | zip | ||
| 文件大小 | 320.4KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-10-17 17:16:33 | ||
图片预览



文档简介
人教版选修四化学高二上学期期末考试卷二(含解析)
第I卷(选择题,共45分)
1.下列处理方法正确的是
A.为除去污水中的重金属离子Hg2+,向其中加入足量充分反应后过滤
B.为降低能耗,工业电解熔融态的Al2O3制Al时,加入冰晶石
C.为充分利用原料,氯碱工业中,将阳极室的饱和氯化钠溶液电解为水后导出
D.为保护公路两旁的铁护栏,将其与电源的负极相连
2.单斜硫和正交硫是硫的两种同素异形体(??)
已知:①S(单斜,S)+O2(g)===SO2(g),△H=-297.16 kJ·mol-1
②S(正交,S)+O2(g)===SO2(g),△H2=-296.83 kJ·mol-1
③S(单斜,S)===S(正交,s),△H3
下列说法正确的是(???)
A.△H3="0.33" kJ·mol-1
B.单斜硫转化为正交硫的反应是吸热反应
C.△H3<0,正交硫比单斜硫稳定
D.△H3>0,单斜硫比正交硫稳定
3.下列热化学方程式中△H的绝对值表示可燃物燃烧热的是( )
A. CO(g)+ O2(g) === CO2(g) △H=-283.0 kJ?mol-1
B. CH4(g)+ 2O2(g) === CO2(g)+2H2O(g) △H=-802.3 kJ?mol-1
C. 2H2(g)+ O2(g) === 2H2O(l) △H=-571.6kJ?mol-1
D. C(s)+O2(g) === CO(g) △H=-110.5kJ?mol-1
4.已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ。有机物乙烷在一定条件下分解的反应可表示为:
若在反应中消耗了1 mol乙烷,则有关该反应的说法正确的是21教育网
A.该反应放出251.2 kJ的热量 B.该反应吸收251.2 kJ的热量
C.该反应放出125.6 kJ的热量 D.该反应吸收125.6 kJ的热量
5.在2A+B3C+4D反应中,表示该反应速率最快的是
A.υ(A)=0.5 mol·L?1·s?1????? B.υ(B)=0.5 mol·L?1·s?1
C.υ(C)=0.8 mol·L?1·s?1????? D.υ(D)=1 mol·L?1·s?1
6.已知C(s)+ CO2(g) 2CO(g)正反应为吸热反应,下列措施能使正反应速率加快的是( )
①增加少量C(s) ②升高温度 ③容器不变,再通入CO2 ④缩小体积增大压强
7.在恒温下一定体积的密闭容器中,可以充分说明反应P(气)+Q(气)R(气)+S(固)已达到平衡的是 ( )
A.反应容器内的压强不随时间改变
B.反应容器内P、Q、R、S四者共存
C.P的生成速率和Q的生成速率相等
D.反应容器内的气体总物质的量随时间变化而变化
8.在密闭容器中进行反应:M(g)+N(g) R(g)+2L,此反应符合下图关系,该反应是下列哪种情况
A.正反应吸热,L是固体或液体
B.正反应吸热,L是气体
C.正反应放热,L是固体或液体
D.正反应放热,L是气体
9.常温下,等物质的量浓度、等体积的盐酸分别用pH=9和pH=10的氨水完全中和时,消耗氨水的体积分别为V1和V2,则V1、V2的关系中正确的是
A.V1=10V2 B.V1>10V2 C.V1<10V2 D.V2>10V1
10.分别放置在如下图所示的装置(都盛有0.1 mol·L-1的H2SO4溶液)中的四个相同的纯锌片,腐蚀最慢的是【来源:21·世纪·教育·网】
A B C D
11.银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:
,在此电池放电时,负极上发生反应的物质是( )
A.Ag B.Zn(OH)2 C.Ag20 D.Zn
12.用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量相应的溶质能使溶液恢复到电解前浓度的是()
A.AgNO3 B.Na2SO4 C.CuCl2 D.KCl
13.以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是
A.镀锌层破损后即对铁制品失去保护作用
B.未通电前上述电镀装置可构成原电池,电镀过程是该原电池的充电过程
C.电镀时保持电流恒定,升高温度不改变电解反应速率
D.因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系
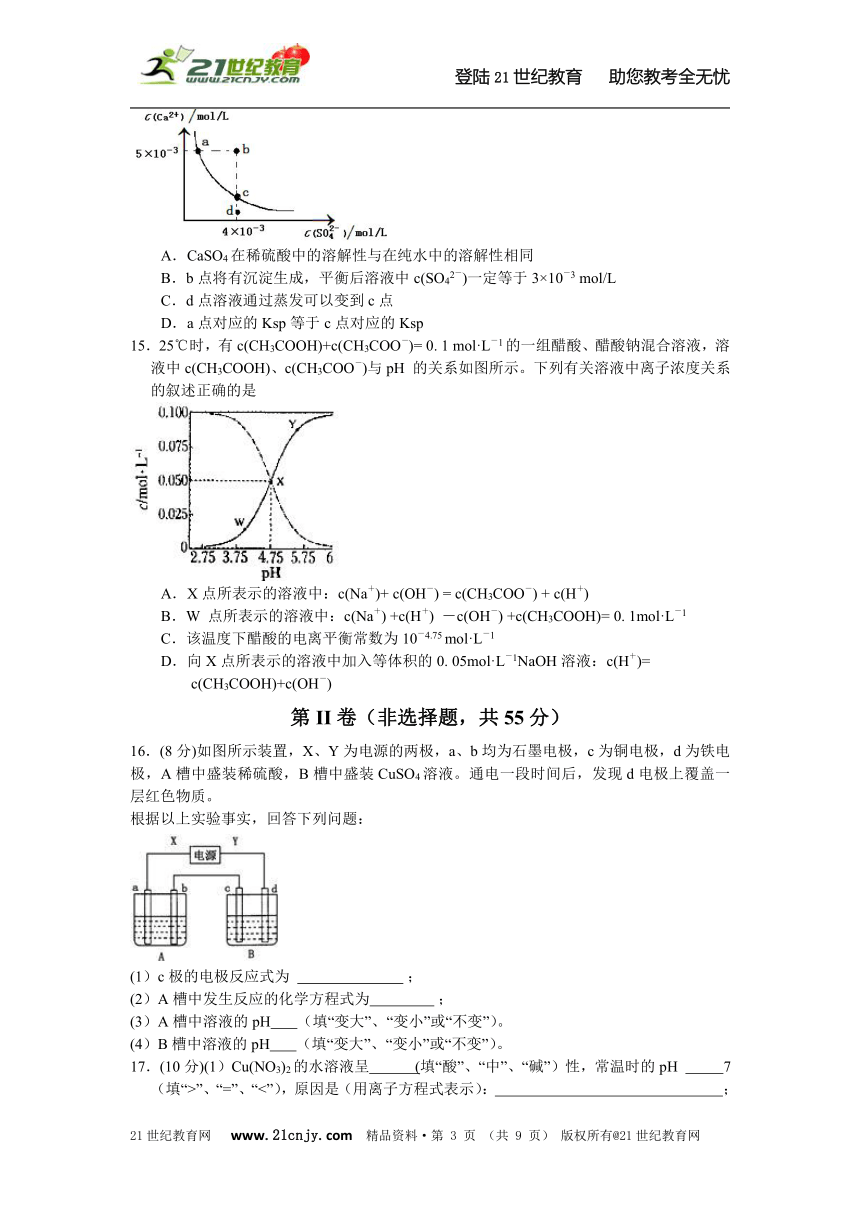
14.常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图。下列说法正确的是
A.CaSO4在稀硫酸中的溶解性与在纯水中的溶解性相同
B.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×10-3 mol/L
C.d点溶液通过蒸发可以变到c点
D.a点对应的Ksp等于c点对应的Ksp
15.25℃时,有c(CH3COOH)+c(CH3COO-)= 0. 1 mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是21*cnjy*com
A.X点所表示的溶液中:c(Na+)+ c(OH-) = c(CH3COO-) + c(H+)
B.W 点所表示的溶液中:c(Na+) +c(H+) -c(OH-) +c(CH3COOH)= 0. 1mol·L-1
C.该温度下醋酸的电离平衡常数为10-4.75 mol·L-1
D.向X点所表示的溶液中加入等体积的0. 05mol·L-1NaOH溶液:c(H+)= c(CH3COOH)+c(OH-) 21·cn·jy·com
第II卷(非选择题,共55分)
16.(8分)如图所示装置,X、Y为电源的两极,a、b均为石墨电极,c为铜电极,d为铁电极,A槽中盛装稀硫酸,B槽中盛装CuSO4溶液。通电一段时间后,发现d电极上覆盖一层红色物质。
根据以上实验事实,回答下列问题:
(1)c极的电极反应式为 ?????????????????????????????;
(2)A槽中发生反应的化学方程式为??????????????????;
(3)A槽中溶液的pH???????(填“变大”、“变小”或“不变”)。
(4)B槽中溶液的pH???????(填“变大”、“变小”或“不变”)。【出处:21教育名师】
17.(10分)(1)Cu(NO3)2的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈 性 ,原因是(用离子方程式表示):______ ,把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。
18.(12分)科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)写出CO燃烧的热化学方程式_____ ________;
(2)写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_____________;
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
①温度升高该反应的平衡常数 (增大、减小、不变)
②B过程用H2表示该反应的化学反应速率是 mol·L-1·min-1
(4)在直接以甲醇为燃料的电池中,电解质溶液为碱性,总反应为:CH3OH+3/2O2+2OH-=CO32-+3H2O,负极的反应式为 。【来源:21cnj*y.co*m】
19.(15分)工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42—等杂质,提纯工艺线路如图所示:【版权所有:21教育】
Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
Ⅱ.有关物质的溶度积如下
物质
CaCO3
MgCO3
Ca(0H)2
Mg(OH)2
Fe(OH)3
Ksp
4.96×10-9
6.82×10-6
4.68×10-6
5.61×10-12
2.64×10-39
回答下列问题:
(1)加入NaOH溶液时,反应的离子方程式为 。向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)= 。
(2)“母液”中除了含有Na+、CO32—外,还含有 等离子。
(3)有人从“绿色化学”角度设想将“母液”沿流程中虚线进行循环使用。请你分析在实际工业生产中是否可行: (填“可行”或“不可行”),并说明理由: 。
(4)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g)=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) =+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式: 。
20.(10分)698 K时,向某V L的密闭容器中充入2 mol H2(g)和2 mol I2(g),发生反应:H2(g)+I2(g) 2HI(g) ΔH=-26.5 kJ·mol-1,测得各物质的物质的量浓度与时间变化的关系如图所示。21教育名师原创作品
请回答下列问题:
(1)V=__________。
(2)该反应达到最大限度的时间是________,该时间内平均反应速率v(HI)=________。
(3)该反应达到平衡状态时,________(填“吸收”或“放出”)的热量为__________。
参考答案及解析
1.B
【解析】A项:加入Pb粉虽能置换出Hg,但Pb2+会留在溶液中,故错。C项:应该为:电解后的淡盐水从阳极导出,可重新用于配制食盐水,故错。D项:铁护栏连上电会很危险,故错。故选B。
【解析】同一个化学反应,用不同的物质表示其反应速率时,速率数值可能不同,但表示的意义是相同的,所以比较反应速率快慢时,应该根据速率之比是相应的化学计量数之比先换算成用同一种物质表示,然后才能直接比较速率数值。所以根据反应的方程式可知,如果都要物质C表示反应速率,则分别是0。75mol/(L·s)、1.5mol/(L·s)、0.8 mol/(L·s)、0.75mol/(L·s),所以答案选B。
6.D21cnjy.com
【解析】考查外界条件对反应速率的影响。浓度对反应速率的影响,不适用于固体和纯液体,①不能。温度升高,速率加快,②可以。增大CO2的浓度,反应速率增大,③可以。有气体参加和生成,所以增大压强,反应速率加快,④可以。答案是D。
7.A
【解析】反应P(气)+Q(气)R(气)+S(固),压强不变,各组分的浓度不变都是平衡状态的标志。反应容器内的气体总物质的量随时间变化而不再变化为平衡状态的标志。
8.A
【解析】根据图像可知,在温度相同时,压强越大,反应物的含量越低,说明增大压强平衡向正反应方向移动,因此L一定不是气体。同样分析在压强相同时,温度越高,反应物的含量越低,说明升高温度平衡向正反应方向移动,因此正反应是吸热反应。所以答案选A。
9.B
【解析】等物质的量浓度、等体积的盐酸分别用pH=9和pH=10的氨水完全中和时,消耗氨水的体积分别为V1和V2,则V1、V2的关系中正确的是V1>10V2 ,因为浓度越大,电离程度越小,所以pH=9和pH=10的氨水前者的氨水浓度大于后者的十倍所以消耗的盐酸的量的关系肯定是V1>10V2 ,故选B。
10.D21世纪教育网版权所有
【解析】D中锌和电源的负极相连,是阴极,属于外加电流的阴极保护法,腐蚀最慢。答案选D。
11.D
【解析】放电相当于原电池,在原电池中负极失去电子,被氧化发生氧化反应。根据方程式可判断放电时锌失去电子,被氧化,所以负极上发生反应的物质是锌。答案选D。
12.C
【解析】四种电解类型分别是:
(1)分解水型:含氧酸、强碱、活泼金属的含氧酸盐(如NaOH、H2SO4、K2SO4等)的电解。
阴极:4H++4e-=2H2↑?? 阳极:4OH--4e-=O2↑+2H2O???总反应:2H2O2H2↑+O2↑
阴极产物:H2;阳极产物:O2。 电解质溶液复原加入物质:H2O。
pH变化情况:原来酸性的溶液pH变小,原来碱性的溶液pH变大,强酸(含氧酸)强碱的正盐溶液pH不变。
(2)分解电解质型:无氧酸(除HF外)、不活泼金属的无氧酸盐(氟化物除外)的电解,如HCl、CuCl2等。
阴极:Cu2++2e-=Cu???? 阳极:2Cl--2e-=Cl2↑???总反应:CuCl2Cu+Cl2↑
阴极产物:酸为H2,盐为金属;阳极产物:卤素等非金属单质。
电解液复原加入物质为原溶质,如电解CuCl2溶液,需加CuCl2。
pH变化情况:如电解无氧酸溶液pH变大但不会超过7;如为盐溶液的电解则视无氧酸根的情况而定。
阴极产物:析出不活泼金属单质;阳极产物是该盐对应的含氧酸和氧气,本例中分别是Cu以及H2SO4、O2.
电解液复原加入物质为不活泼金属的氧化物(金属价态与原盐中相同)。如电解CuSO4溶液,复原需加入CuO。
pH变化情况:溶液pH显著变小。
13.Cwww.21-cn-jy.com
【解析】镀锌层破损后即对铁制品失去保护作用,发生原电池反应锌保护铁,电镀过程是该原电池的放电过程。因部分电能转化为热能,电镀时通过的电量与锌的析出量有确定关系。
14.
【解析】稀硫酸中c(SO42-)大,抑制溶解,A不正确。B点溶液中离子积大于9×10-6,所以一定有沉淀析出。由于起始时c(SO42-)小于c(Ca2+),所以平衡时c(SO42-)仍然小于c(Ca2+),即c(SO42-)小于3×10-3 mol/L,C不正确。蒸发过程中c(SO42-)应该是增大的,所以选项C不正确。溶度积常数只与温度有关系,所以选项D正确,答案选D。
15.C
【解析】A、根据图像可知,X点溶液显酸性,则根据电荷守恒可知c(Na+)+ c(H+)= c(CH3COO-) + c(OH-),选项A不正确;B、W点溶液显酸性,同样根据电荷守恒可知 c(Na+)+ c(H+)= c(CH3COO-) + c(OH-),所以c(Na+) +c(H+) -c(OH-) +c(CH3COOH)=2 c(CH3COOH)<0.1mol/L,B不正确;C、该温度下醋酸的电离平衡常数=,则根据X点的pH可知,该温度下醋酸的电离平衡常数为10-4.75 mol/L,选项C正确;D、向X点所表示的溶液中加入等体积的0. 05mol·L-1NaOH溶液,醋酸恰好反应生成醋酸钠,即溶液是醋酸钠溶液,所以根据质子守恒可知c(OH-)= c(CH3COOH)+ c(H+),D不正确,答案选C。www-2-1-cnjy-com
16.(1)Cu→Cu2++2e-
(2)2H2O=O2↑+H2↑
(3)变小?(4)不变
【解析】题干中“d电极上覆盖一层红色物质”,此物质为Cu。则d极为阴极,c极为阳极,b极为阴极,a极为阳极。X为电源的正极,Y为电源的负极。
故C极发生的反应为Cu→Cu2++2e-;A槽中的溶液为稀硫酸,电解稀硫酸实际上是电解水,故发生的反应为2H2O=O2↑+H2↑;由于水的减少,c(H+)变大,pH变小。
17.(10分)(1) 酸,< ,Cu2+ + H2O Cu(OH)2 + 2H+ ,抑制
(2)酸,Al3++3H2O Al(OH)3+3H+, Al2O3 (3)NaOH
【解析】(1)Cu(NO3)2是强酸弱碱盐,铜离子水解,水溶液呈酸性,pH小于7。水解方程式是Cu2+ + H2O Cu(OH)2 + 2H+;硝酸银溶于水,银离子水解,溶液显酸性。所以将AgNO3固体先溶于较浓的硝酸中的目的是抑制银离子的水解。21·世纪*教育网
(2)氯化铝溶于水,铝离子水解,溶液显酸性,水解方程式是Al3++3H2O Al(OH)3+3H+。水解吸热,加热促进水解,且生成的氯化氢挥发,进一步促进水解,所以最终得到的是氢氧化铝,灼烧得到氧化铝。2-1-c-n-j-y
(3)硫化钠溶于水,硫离子水解,溶液显碱性。所以在配制硫化钠溶液时,为了防止发生
由图像可知,在T2温度下反应先达到平衡,但甲醇的量相对少,即升温平衡左移,正反应是放热反应,平衡常数减小。2·1·c·n·j·y
依据反应速率的公式可知:υ(甲醇)=n(B)/[2×t(B)],而υ(氢气)=3n(B)/[2×t(B)]
(4)燃料电池中总反应为:CH3OH+3/2O2+2OH-==CO32-+3H2O,
负极的反应式为:CH3OH-6e-+8OH-==CO32-+6H2O
正极的反应式为:O2+2H2O+4e-=4OH-
19.(1)MgCO3+2OH- = Mg(OH)2+ CO32—(书写Fe3++3 OH-=Fe(OH)3↓、Mg2++2 OH-=Mg(OH)2↓不得分)(3分)(3分) 21*cnjy*com
(2)Cl-、(2分)
(3)不可行(2分) 若“母液”循环使用,则溶液中c(Cl-)和c()增大,最后所得产物Na2CO3混有杂质(2分)
(4)Na2CO3·H2O(s)=Na2CO3(s)+ H2O(g) △H=+58.73 kJ·mol-1 (3分)
【解析】由溶度积表知,MgCO3的Ksp最大,在溶液中溶解的最多,其它物质与MgCO3相(2)根据图像可知,当反应进行到5s时,各种物质的浓度不再发生变化,说明反应达到平衡状态;5s内HI的浓度改变了1.58mol/L,所以HI的反应速率是1.58mol/L÷5s=0.316 mol·L-1·s-1。
(3)根据图像可知,氢气的浓度减少了0.79mol/L,所以消耗氢气的物质的量是0.79mol/L×2L=1.58mol,因此反应放出的热量是1.58mol×26.5 kJ·mol-1=41.87 kJ。
第I卷(选择题,共45分)
1.下列处理方法正确的是
A.为除去污水中的重金属离子Hg2+,向其中加入足量充分反应后过滤
B.为降低能耗,工业电解熔融态的Al2O3制Al时,加入冰晶石
C.为充分利用原料,氯碱工业中,将阳极室的饱和氯化钠溶液电解为水后导出
D.为保护公路两旁的铁护栏,将其与电源的负极相连
2.单斜硫和正交硫是硫的两种同素异形体(??)
已知:①S(单斜,S)+O2(g)===SO2(g),△H=-297.16 kJ·mol-1
②S(正交,S)+O2(g)===SO2(g),△H2=-296.83 kJ·mol-1
③S(单斜,S)===S(正交,s),△H3
下列说法正确的是(???)
A.△H3="0.33" kJ·mol-1
B.单斜硫转化为正交硫的反应是吸热反应
C.△H3<0,正交硫比单斜硫稳定
D.△H3>0,单斜硫比正交硫稳定
3.下列热化学方程式中△H的绝对值表示可燃物燃烧热的是( )
A. CO(g)+ O2(g) === CO2(g) △H=-283.0 kJ?mol-1
B. CH4(g)+ 2O2(g) === CO2(g)+2H2O(g) △H=-802.3 kJ?mol-1
C. 2H2(g)+ O2(g) === 2H2O(l) △H=-571.6kJ?mol-1
D. C(s)+O2(g) === CO(g) △H=-110.5kJ?mol-1
4.已知断裂1 mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ。有机物乙烷在一定条件下分解的反应可表示为:
若在反应中消耗了1 mol乙烷,则有关该反应的说法正确的是21教育网
A.该反应放出251.2 kJ的热量 B.该反应吸收251.2 kJ的热量
C.该反应放出125.6 kJ的热量 D.该反应吸收125.6 kJ的热量
5.在2A+B3C+4D反应中,表示该反应速率最快的是
A.υ(A)=0.5 mol·L?1·s?1????? B.υ(B)=0.5 mol·L?1·s?1
C.υ(C)=0.8 mol·L?1·s?1????? D.υ(D)=1 mol·L?1·s?1
6.已知C(s)+ CO2(g) 2CO(g)正反应为吸热反应,下列措施能使正反应速率加快的是( )
①增加少量C(s) ②升高温度 ③容器不变,再通入CO2 ④缩小体积增大压强
7.在恒温下一定体积的密闭容器中,可以充分说明反应P(气)+Q(气)R(气)+S(固)已达到平衡的是 ( )
A.反应容器内的压强不随时间改变
B.反应容器内P、Q、R、S四者共存
C.P的生成速率和Q的生成速率相等
D.反应容器内的气体总物质的量随时间变化而变化
8.在密闭容器中进行反应:M(g)+N(g) R(g)+2L,此反应符合下图关系,该反应是下列哪种情况
A.正反应吸热,L是固体或液体
B.正反应吸热,L是气体
C.正反应放热,L是固体或液体
D.正反应放热,L是气体
9.常温下,等物质的量浓度、等体积的盐酸分别用pH=9和pH=10的氨水完全中和时,消耗氨水的体积分别为V1和V2,则V1、V2的关系中正确的是
A.V1=10V2 B.V1>10V2 C.V1<10V2 D.V2>10V1
10.分别放置在如下图所示的装置(都盛有0.1 mol·L-1的H2SO4溶液)中的四个相同的纯锌片,腐蚀最慢的是【来源:21·世纪·教育·网】
A B C D
11.银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:
,在此电池放电时,负极上发生反应的物质是( )
A.Ag B.Zn(OH)2 C.Ag20 D.Zn
12.用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量相应的溶质能使溶液恢复到电解前浓度的是()
A.AgNO3 B.Na2SO4 C.CuCl2 D.KCl
13.以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是
A.镀锌层破损后即对铁制品失去保护作用
B.未通电前上述电镀装置可构成原电池,电镀过程是该原电池的充电过程
C.电镀时保持电流恒定,升高温度不改变电解反应速率
D.因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系
14.常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图。下列说法正确的是
A.CaSO4在稀硫酸中的溶解性与在纯水中的溶解性相同
B.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×10-3 mol/L
C.d点溶液通过蒸发可以变到c点
D.a点对应的Ksp等于c点对应的Ksp
15.25℃时,有c(CH3COOH)+c(CH3COO-)= 0. 1 mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是21*cnjy*com
A.X点所表示的溶液中:c(Na+)+ c(OH-) = c(CH3COO-) + c(H+)
B.W 点所表示的溶液中:c(Na+) +c(H+) -c(OH-) +c(CH3COOH)= 0. 1mol·L-1
C.该温度下醋酸的电离平衡常数为10-4.75 mol·L-1
D.向X点所表示的溶液中加入等体积的0. 05mol·L-1NaOH溶液:c(H+)= c(CH3COOH)+c(OH-) 21·cn·jy·com
第II卷(非选择题,共55分)
16.(8分)如图所示装置,X、Y为电源的两极,a、b均为石墨电极,c为铜电极,d为铁电极,A槽中盛装稀硫酸,B槽中盛装CuSO4溶液。通电一段时间后,发现d电极上覆盖一层红色物质。
根据以上实验事实,回答下列问题:
(1)c极的电极反应式为 ?????????????????????????????;
(2)A槽中发生反应的化学方程式为??????????????????;
(3)A槽中溶液的pH???????(填“变大”、“变小”或“不变”)。
(4)B槽中溶液的pH???????(填“变大”、“变小”或“不变”)。【出处:21教育名师】
17.(10分)(1)Cu(NO3)2的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈 性 ,原因是(用离子方程式表示):______ ,把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。
18.(12分)科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。请回答下列问题:
(1)写出CO燃烧的热化学方程式_____ ________;
(2)写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_____________;
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
①温度升高该反应的平衡常数 (增大、减小、不变)
②B过程用H2表示该反应的化学反应速率是 mol·L-1·min-1
(4)在直接以甲醇为燃料的电池中,电解质溶液为碱性,总反应为:CH3OH+3/2O2+2OH-=CO32-+3H2O,负极的反应式为 。【来源:21cnj*y.co*m】
19.(15分)工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42—等杂质,提纯工艺线路如图所示:【版权所有:21教育】
Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
Ⅱ.有关物质的溶度积如下
物质
CaCO3
MgCO3
Ca(0H)2
Mg(OH)2
Fe(OH)3
Ksp
4.96×10-9
6.82×10-6
4.68×10-6
5.61×10-12
2.64×10-39
回答下列问题:
(1)加入NaOH溶液时,反应的离子方程式为 。向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)= 。
(2)“母液”中除了含有Na+、CO32—外,还含有 等离子。
(3)有人从“绿色化学”角度设想将“母液”沿流程中虚线进行循环使用。请你分析在实际工业生产中是否可行: (填“可行”或“不可行”),并说明理由: 。
(4)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g)=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) =+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式: 。
20.(10分)698 K时,向某V L的密闭容器中充入2 mol H2(g)和2 mol I2(g),发生反应:H2(g)+I2(g) 2HI(g) ΔH=-26.5 kJ·mol-1,测得各物质的物质的量浓度与时间变化的关系如图所示。21教育名师原创作品
请回答下列问题:
(1)V=__________。
(2)该反应达到最大限度的时间是________,该时间内平均反应速率v(HI)=________。
(3)该反应达到平衡状态时,________(填“吸收”或“放出”)的热量为__________。
参考答案及解析
1.B
【解析】A项:加入Pb粉虽能置换出Hg,但Pb2+会留在溶液中,故错。C项:应该为:电解后的淡盐水从阳极导出,可重新用于配制食盐水,故错。D项:铁护栏连上电会很危险,故错。故选B。
【解析】同一个化学反应,用不同的物质表示其反应速率时,速率数值可能不同,但表示的意义是相同的,所以比较反应速率快慢时,应该根据速率之比是相应的化学计量数之比先换算成用同一种物质表示,然后才能直接比较速率数值。所以根据反应的方程式可知,如果都要物质C表示反应速率,则分别是0。75mol/(L·s)、1.5mol/(L·s)、0.8 mol/(L·s)、0.75mol/(L·s),所以答案选B。
6.D21cnjy.com
【解析】考查外界条件对反应速率的影响。浓度对反应速率的影响,不适用于固体和纯液体,①不能。温度升高,速率加快,②可以。增大CO2的浓度,反应速率增大,③可以。有气体参加和生成,所以增大压强,反应速率加快,④可以。答案是D。
7.A
【解析】反应P(气)+Q(气)R(气)+S(固),压强不变,各组分的浓度不变都是平衡状态的标志。反应容器内的气体总物质的量随时间变化而不再变化为平衡状态的标志。
8.A
【解析】根据图像可知,在温度相同时,压强越大,反应物的含量越低,说明增大压强平衡向正反应方向移动,因此L一定不是气体。同样分析在压强相同时,温度越高,反应物的含量越低,说明升高温度平衡向正反应方向移动,因此正反应是吸热反应。所以答案选A。
9.B
【解析】等物质的量浓度、等体积的盐酸分别用pH=9和pH=10的氨水完全中和时,消耗氨水的体积分别为V1和V2,则V1、V2的关系中正确的是V1>10V2 ,因为浓度越大,电离程度越小,所以pH=9和pH=10的氨水前者的氨水浓度大于后者的十倍所以消耗的盐酸的量的关系肯定是V1>10V2 ,故选B。
10.D21世纪教育网版权所有
【解析】D中锌和电源的负极相连,是阴极,属于外加电流的阴极保护法,腐蚀最慢。答案选D。
11.D
【解析】放电相当于原电池,在原电池中负极失去电子,被氧化发生氧化反应。根据方程式可判断放电时锌失去电子,被氧化,所以负极上发生反应的物质是锌。答案选D。
12.C
【解析】四种电解类型分别是:
(1)分解水型:含氧酸、强碱、活泼金属的含氧酸盐(如NaOH、H2SO4、K2SO4等)的电解。
阴极:4H++4e-=2H2↑?? 阳极:4OH--4e-=O2↑+2H2O???总反应:2H2O2H2↑+O2↑
阴极产物:H2;阳极产物:O2。 电解质溶液复原加入物质:H2O。
pH变化情况:原来酸性的溶液pH变小,原来碱性的溶液pH变大,强酸(含氧酸)强碱的正盐溶液pH不变。
(2)分解电解质型:无氧酸(除HF外)、不活泼金属的无氧酸盐(氟化物除外)的电解,如HCl、CuCl2等。
阴极:Cu2++2e-=Cu???? 阳极:2Cl--2e-=Cl2↑???总反应:CuCl2Cu+Cl2↑
阴极产物:酸为H2,盐为金属;阳极产物:卤素等非金属单质。
电解液复原加入物质为原溶质,如电解CuCl2溶液,需加CuCl2。
pH变化情况:如电解无氧酸溶液pH变大但不会超过7;如为盐溶液的电解则视无氧酸根的情况而定。
阴极产物:析出不活泼金属单质;阳极产物是该盐对应的含氧酸和氧气,本例中分别是Cu以及H2SO4、O2.
电解液复原加入物质为不活泼金属的氧化物(金属价态与原盐中相同)。如电解CuSO4溶液,复原需加入CuO。
pH变化情况:溶液pH显著变小。
13.Cwww.21-cn-jy.com
【解析】镀锌层破损后即对铁制品失去保护作用,发生原电池反应锌保护铁,电镀过程是该原电池的放电过程。因部分电能转化为热能,电镀时通过的电量与锌的析出量有确定关系。
14.
【解析】稀硫酸中c(SO42-)大,抑制溶解,A不正确。B点溶液中离子积大于9×10-6,所以一定有沉淀析出。由于起始时c(SO42-)小于c(Ca2+),所以平衡时c(SO42-)仍然小于c(Ca2+),即c(SO42-)小于3×10-3 mol/L,C不正确。蒸发过程中c(SO42-)应该是增大的,所以选项C不正确。溶度积常数只与温度有关系,所以选项D正确,答案选D。
15.C
【解析】A、根据图像可知,X点溶液显酸性,则根据电荷守恒可知c(Na+)+ c(H+)= c(CH3COO-) + c(OH-),选项A不正确;B、W点溶液显酸性,同样根据电荷守恒可知 c(Na+)+ c(H+)= c(CH3COO-) + c(OH-),所以c(Na+) +c(H+) -c(OH-) +c(CH3COOH)=2 c(CH3COOH)<0.1mol/L,B不正确;C、该温度下醋酸的电离平衡常数=,则根据X点的pH可知,该温度下醋酸的电离平衡常数为10-4.75 mol/L,选项C正确;D、向X点所表示的溶液中加入等体积的0. 05mol·L-1NaOH溶液,醋酸恰好反应生成醋酸钠,即溶液是醋酸钠溶液,所以根据质子守恒可知c(OH-)= c(CH3COOH)+ c(H+),D不正确,答案选C。www-2-1-cnjy-com
16.(1)Cu→Cu2++2e-
(2)2H2O=O2↑+H2↑
(3)变小?(4)不变
【解析】题干中“d电极上覆盖一层红色物质”,此物质为Cu。则d极为阴极,c极为阳极,b极为阴极,a极为阳极。X为电源的正极,Y为电源的负极。
故C极发生的反应为Cu→Cu2++2e-;A槽中的溶液为稀硫酸,电解稀硫酸实际上是电解水,故发生的反应为2H2O=O2↑+H2↑;由于水的减少,c(H+)变大,pH变小。
17.(10分)(1) 酸,< ,Cu2+ + H2O Cu(OH)2 + 2H+ ,抑制
(2)酸,Al3++3H2O Al(OH)3+3H+, Al2O3 (3)NaOH
【解析】(1)Cu(NO3)2是强酸弱碱盐,铜离子水解,水溶液呈酸性,pH小于7。水解方程式是Cu2+ + H2O Cu(OH)2 + 2H+;硝酸银溶于水,银离子水解,溶液显酸性。所以将AgNO3固体先溶于较浓的硝酸中的目的是抑制银离子的水解。21·世纪*教育网
(2)氯化铝溶于水,铝离子水解,溶液显酸性,水解方程式是Al3++3H2O Al(OH)3+3H+。水解吸热,加热促进水解,且生成的氯化氢挥发,进一步促进水解,所以最终得到的是氢氧化铝,灼烧得到氧化铝。2-1-c-n-j-y
(3)硫化钠溶于水,硫离子水解,溶液显碱性。所以在配制硫化钠溶液时,为了防止发生
由图像可知,在T2温度下反应先达到平衡,但甲醇的量相对少,即升温平衡左移,正反应是放热反应,平衡常数减小。2·1·c·n·j·y
依据反应速率的公式可知:υ(甲醇)=n(B)/[2×t(B)],而υ(氢气)=3n(B)/[2×t(B)]
(4)燃料电池中总反应为:CH3OH+3/2O2+2OH-==CO32-+3H2O,
负极的反应式为:CH3OH-6e-+8OH-==CO32-+6H2O
正极的反应式为:O2+2H2O+4e-=4OH-
19.(1)MgCO3+2OH- = Mg(OH)2+ CO32—(书写Fe3++3 OH-=Fe(OH)3↓、Mg2++2 OH-=Mg(OH)2↓不得分)(3分)(3分) 21*cnjy*com
(2)Cl-、(2分)
(3)不可行(2分) 若“母液”循环使用,则溶液中c(Cl-)和c()增大,最后所得产物Na2CO3混有杂质(2分)
(4)Na2CO3·H2O(s)=Na2CO3(s)+ H2O(g) △H=+58.73 kJ·mol-1 (3分)
【解析】由溶度积表知,MgCO3的Ksp最大,在溶液中溶解的最多,其它物质与MgCO3相(2)根据图像可知,当反应进行到5s时,各种物质的浓度不再发生变化,说明反应达到平衡状态;5s内HI的浓度改变了1.58mol/L,所以HI的反应速率是1.58mol/L÷5s=0.316 mol·L-1·s-1。
(3)根据图像可知,氢气的浓度减少了0.79mol/L,所以消耗氢气的物质的量是0.79mol/L×2L=1.58mol,因此反应放出的热量是1.58mol×26.5 kJ·mol-1=41.87 kJ。
