沪教全国版九年级化学第3章 3.2 组成物质的化学元素 同步练习(详细答案)
文档属性
| 名称 | 沪教全国版九年级化学第3章 3.2 组成物质的化学元素 同步练习(详细答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 264.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-10-18 00:00:00 | ||
图片预览

文档简介
3.2
组成物质的化学元素
一.选择题(共15小题)
1.(2016 衡阳)下列物质中,属于氧化物的是( )
A.镁
B.空气
C.硝酸钾
D.二氧化锰
2.(2016 上海)属于纯净物的是( )
A.盐汽水
B.矿泉水
C.自来水
D.蒸馏水
3.(2016 天津)下列物质中属于混合物的是( )
A.河水
B.氯酸钾
C.三氧化硫
D.五氧化二磷
4.(2016 吉林)青蒿素(化学式C15H22O5)是中国科学家从植物中成功分离出的抗疟药的有效成分,它属于( )
A.单质
B.纯净物
C.氧化物
D.混合物
5.(2016 苏州)下列物质属于混合物的是( )
A.氧气
B.氧化铜
C.硫酸钠
D.空气
6.(2016 齐齐哈尔)下列微观模拟图中●和○分别表示不同元素的原子,其中表示单质的是( )
A.
B.
C.
D.
7.(2016 扬州)下列物质属于化合物的是( )
A.硫
B.水
C.铜
D.空气
8.(2016 泰州)“含氟牙膏”中的“氟”指的是( )
A.元素
B.原子
C.离子
D.单质
9.(2016 齐齐哈尔)不同种元素最本质的区别是( )
A.中子数不同
B.质子数不同
C.相对原子质量不同
D.核外电子数不同
10.(2016 株洲)元素观是化学的重要观念之一.下列有关元素的说法中错误的是( )
A.元素是具有相同核电荷数的一类原子的总称
B.元素周期表,元素的原子序数与该元素原子核电荷数在数值上相同
C.同种元素的原子核内质子数与中子数一定相等
D.在物质发生化学变化时,原子的种类不变,元素也不会改变
11.(2016 百色)豆腐是人们喜爱的食品,其中含铁和钙,这里所指的“铁”、“钙”理解为( )
A.分子
B.原子
C.单质
D.元素
12.(2016 南京)在元素周期表中硅元素的某些信息如图所示,下列有关硅的说法错误的是( )
A.属于金属元素
B.元素符号为“Si”
C.原子序数为“14”
D.相对原子质量为“28.09”
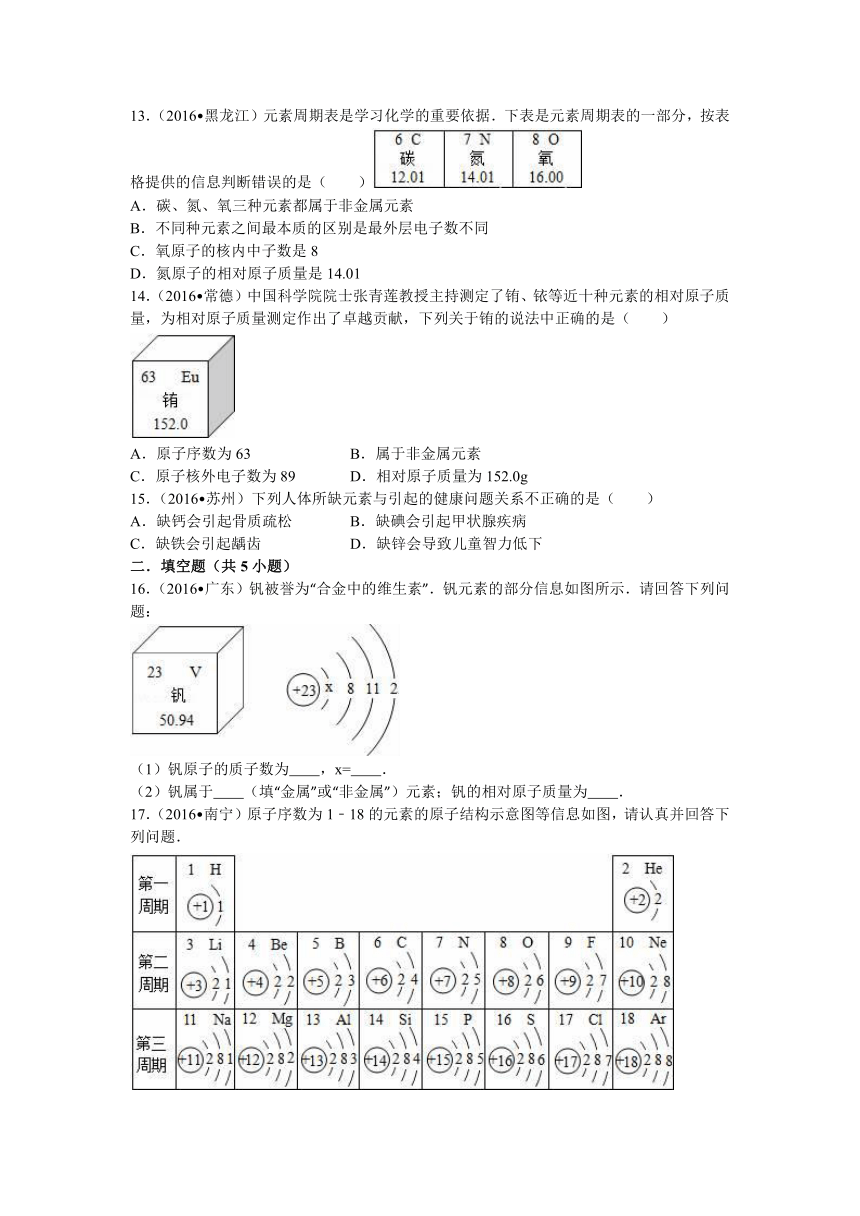
13.(2016 黑龙江)元素周期表是学习化学的重要依据.下表是元素周期表的一部分,按表格提供的信息判断错误的是( )
A.碳、氮、氧三种元素都属于非金属元素
B.不同种元素之间最本质的区别是最外层电子数不同
C.氧原子的核内中子数是8
D.氮原子的相对原子质量是14.01
14.(2016 常德)中国科学院院士张青莲教授主持测定了铕、铱等近十种元素的相对原子质量,为相对原子质量测定作出了卓越贡献,下列关于铕的说法中正确的是( )
A.原子序数为63
B.属于非金属元素
C.原子核外电子数为89
D.相对原子质量为152.0g
15.(2016 苏州)下列人体所缺元素与引起的健康问题关系不正确的是( )
A.缺钙会引起骨质疏松
B.缺碘会引起甲状腺疾病
C.缺铁会引起龋齿
D.缺锌会导致儿童智力低下
二.填空题(共5小题)
16.(2016 广东)钒被誉为“合金中的维生素”.钒元素的部分信息如图所示.请回答下列问题:
(1)钒原子的质子数为 ,x= .
(2)钒属于 (填“金属”或“非金属”)元素;钒的相对原子质量为 .
17.(2016 南宁)原子序数为1﹣18的元素的原子结构示意图等信息如图,请认真并回答下列问题.
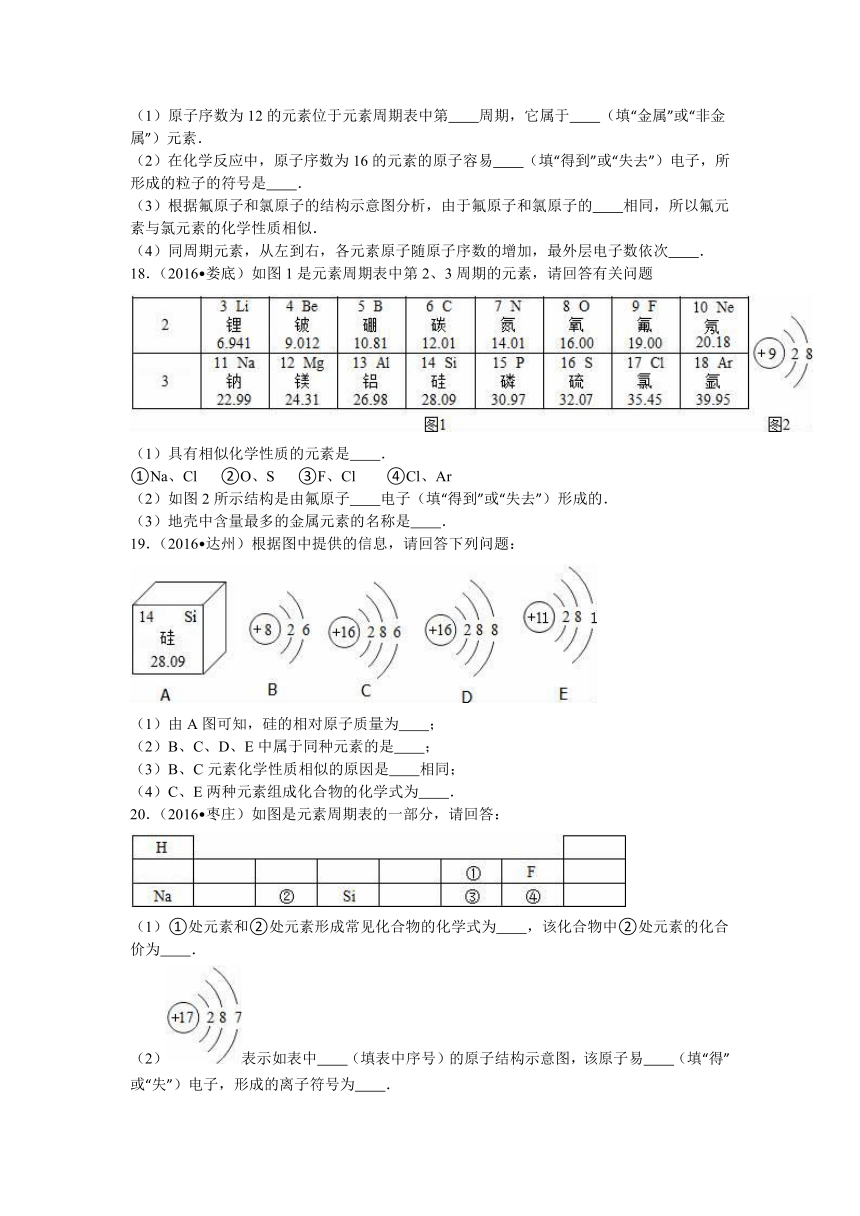
(1)原子序数为12的元素位于元素周期表中第 周期,它属于 (填“金属”或“非金属”)元素.
(2)在化学反应中,原子序数为16的元素的原子容易 (填“得到”或“失去”)电子,所形成的粒子的符号是 .
(3)根据氟原子和氯原子的结构示意图分析,由于氟原子和氯原子的 相同,所以氟元素与氯元素的化学性质相似.
(4)同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次 .
18.(2016 娄底)如图1是元素周期表中第2、3周期的元素,请回答有关问题
(1)具有相似化学性质的元素是 .
①Na、Cl
②O、S
③F、Cl
④Cl、Ar
(2)如图2所示结构是由氟原子 电子(填“得到”或“失去”)形成的.
(3)地壳中含量最多的金属元素的名称是 .
19.(2016 达州)根据图中提供的信息,请回答下列问题:
(1)由A图可知,硅的相对原子质量为 ;
(2)B、C、D、E中属于同种元素的是 ;
(3)B、C元素化学性质相似的原因是 相同;
(4)C、E两种元素组成化合物的化学式为 .
20.(2016 枣庄)如图是元素周期表的一部分,请回答:
(1)①处元素和②处元素形成常见化合物的化学式为 ,该化合物中②处元素的化合价为 .
(2)表示如表中 (填表中序号)的原子结构示意图,该原子易 (填“得”或“失”)电子,形成的离子符号为 .
三.推断题(共2小题)
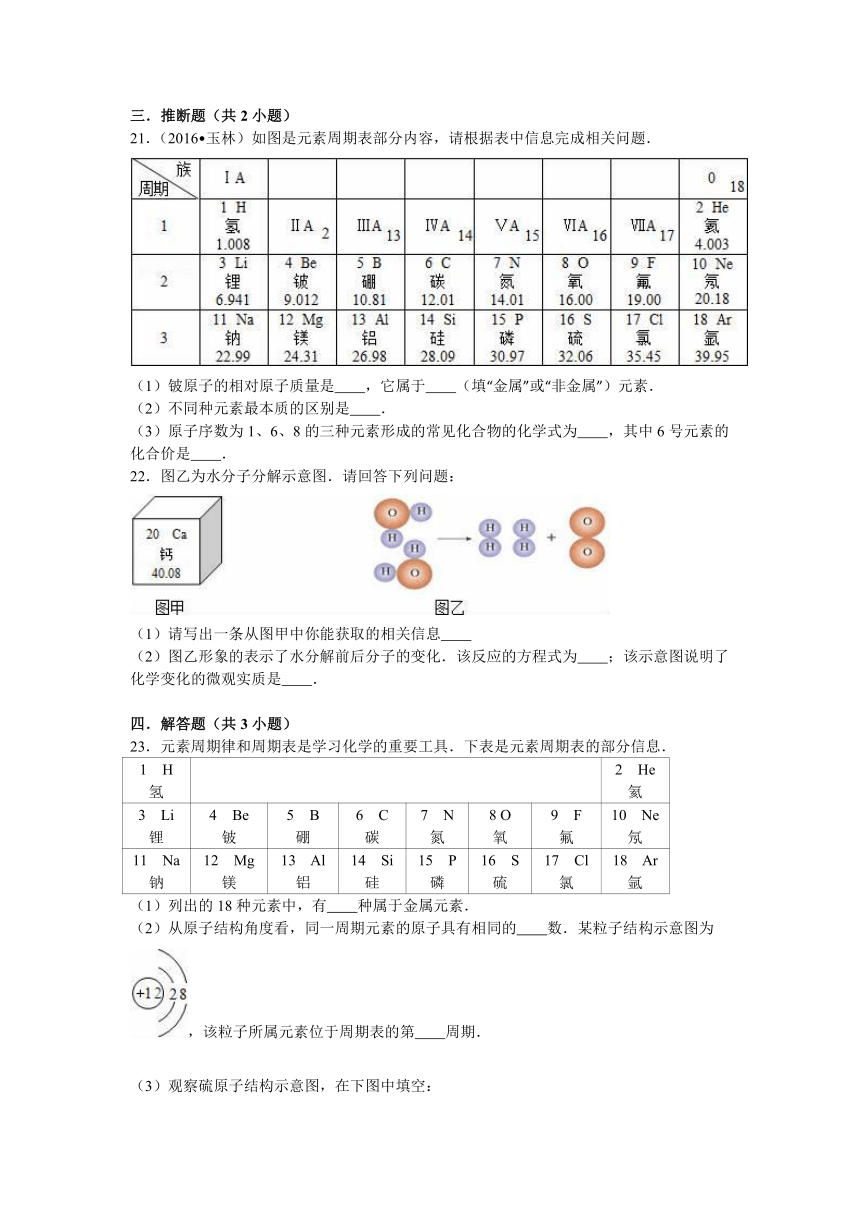
21.(2016 玉林)如图是元素周期表部分内容,请根据表中信息完成相关问题.
(1)铍原子的相对原子质量是 ,它属于 (填“金属”或“非金属”)元素.
(2)不同种元素最本质的区别是 .
(3)原子序数为1、6、8的三种元素形成的常见化合物的化学式为 ,其中6号元素的化合价是 .
22.图乙为水分子分解示意图.请回答下列问题:
(1)请写出一条从图甲中你能获取的相关信息
(2)图乙形象的表示了水分解前后分子的变化.该反应的方程式为 ;该示意图说明了化学变化的微观实质是 .
四.解答题(共3小题)
23.元素周期律和周期表是学习化学的重要工具.下表是元素周期表的部分信息.
1
H氢
2
He氦
3
Li锂
4
Be铍
5
B硼
6
C碳
7
N氮
8
O氧
9
F氟
10
Ne氖
11
Na钠
12
Mg镁
13
Al铝
14
Si硅
15
P磷
16
S硫
17
Cl氯
18
Ar氩
(1)列出的18种元素中,有 种属于金属元素.
(2)从原子结构角度看,同一周期元素的原子具有相同的 数.某粒子结构示意图为,该粒子所属元素位于周期表的第 周期.
(3)观察硫原子结构示意图,在下图中填空:
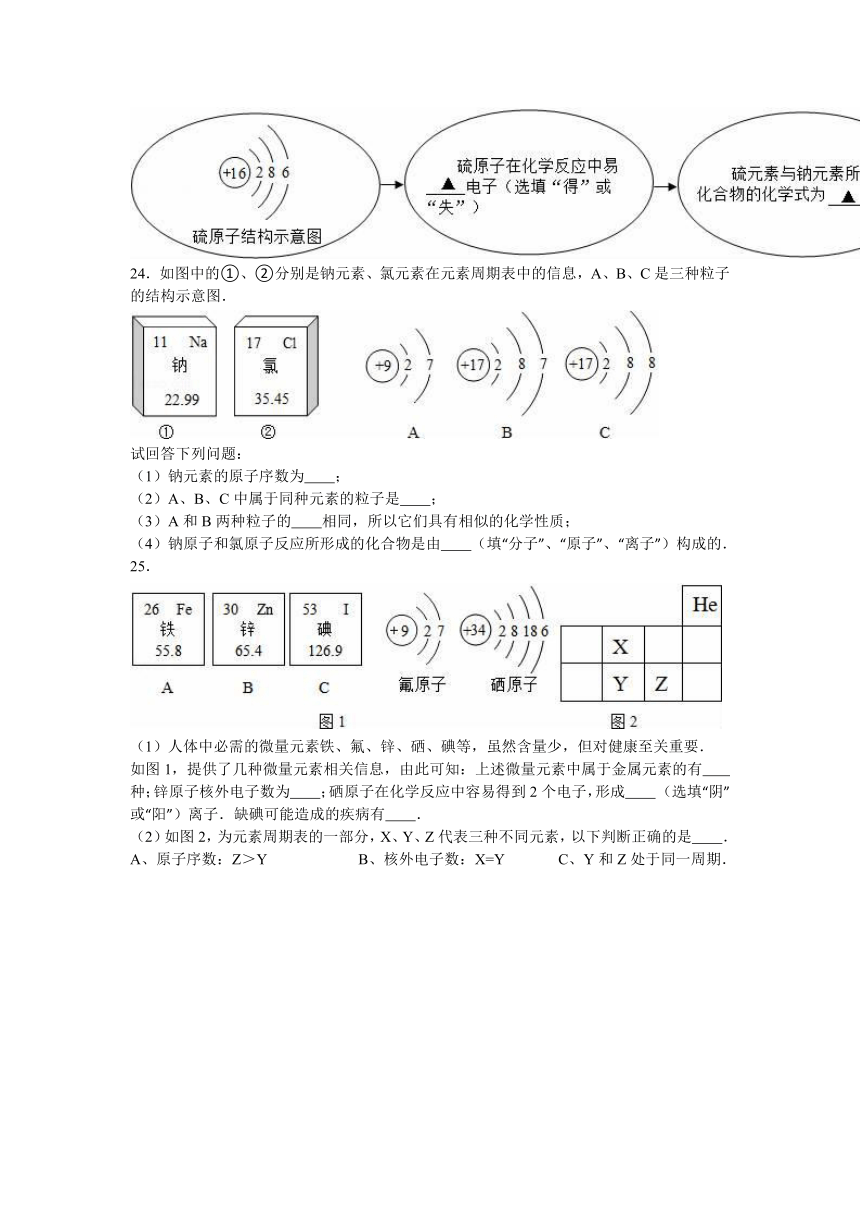
24.如图中的①、②分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图.
试回答下列问题:
(1)钠元素的原子序数为 ;
(2)A、B、C中属于同种元素的粒子是 ;
(3)A和B两种粒子的 相同,所以它们具有相似的化学性质;
(4)钠原子和氯原子反应所形成的化合物是由 (填“分子”、“原子”、“离子”)构成的.
25.
(1)人体中必需的微量元素铁、氟、锌、硒、碘等,虽然含量少,但对健康至关重要.
如图1,提供了几种微量元素相关信息,由此可知:上述微量元素中属于金属元素的有 种;锌原子核外电子数为 ;硒原子在化学反应中容易得到2个电子,形成
(选填“阴”或“阳”)离子.缺碘可能造成的疾病有 .
(2)如图2,为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是 .
A、原子序数:Z>Y B、核外电子数:X=Y
C、Y和Z处于同一周期.
参考答案与解析
一.选择题(共15小题)
1.(2016 衡阳)下列物质中,属于氧化物的是( )
A.镁
B.空气
C.硝酸钾
D.二氧化锰
【分析】本题考查氧化物的识别,根据氧化物的概念可知氧化物只有两种元素,且必须有氧元素.
【解答】解:A中只有一种元素,属于单质,故A错.
B中有氮气、氧气、二氧化碳等物质,属于混合物,故B错.
C中有三种元素,也含氧元素,但不属于氧化物,属于盐,故C错.
D中有两种元素,其一为氧元素,属于氧化物,故D正确.
故选D.
【点评】本题较简单,主要从概念上来抓住判断的关键点,两个关键点缺一不可,要同时具备.
2.(2016 上海)属于纯净物的是( )
A.盐汽水
B.矿泉水
C.自来水
D.蒸馏水
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.
【解答】解:A、盐汽水中有盐、碳酸等物质,属于混合物,故选项错误;
B、矿泉水中有矿物质和水,属于混合物,故选项错误;
C、自来水中有可溶性杂质和不溶性杂质,属于混合物,故选项错误;
D、蒸馏水中只有水分子,属于纯净物中的氧化物,故选项正确;
故选D
【点评】本考点考查了物质的分类,与生活实际联系比较密切.要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.
3.(2016 天津)下列物质中属于混合物的是( )
A.河水
B.氯酸钾
C.三氧化硫
D.五氧化二磷
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.
【解答】解:A、河水中有可溶性杂质和不溶性杂质,属于混合物,故选项正确;
B、氯酸钾属于纯净物中的化合物,故选项错误;
C、三氧化硫属于纯净物中的氧化物,故选项错误;
D、五氧化二磷属于纯净物中的氧化物,故选项错误;
故选A
【点评】本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.
4.(2016 吉林)青蒿素(化学式C15H22O5)是中国科学家从植物中成功分离出的抗疟药的有效成分,它属于( )
A.单质
B.纯净物
C.氧化物
D.混合物
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.青蒿素(化学式C15H22O5)是一种物质,属于纯净物中的化合物.
【解答】解:A、由同种元素组成的纯净物叫单质,故选项错误;
B、青蒿素(化学式C15H22O5)是一种物质,属于纯净物中的化合物,故选项正确;
C、氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素,故选项错误;
D、混合物是由两种或两种以上的物质组成,故选项错误;
故选B
【点评】本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.
5.(2016 苏州)下列物质属于混合物的是( )
A.氧气
B.氧化铜
C.硫酸钠
D.空气
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.
【解答】解:A、氧气属于纯净物中的单质,故选项错误;
B、氧化铜属于纯净物中的氧化物,故选项错误;
C、硫酸钠属于纯净物中的化合物,故选项错误;
D、空气中有氧气、氮气等物质,属于混合物,故选项正确;
故选D
【点评】本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.
6.(2016 齐齐哈尔)下列微观模拟图中●和○分别表示不同元素的原子,其中表示单质的是( )
A.
B.
C.
D.
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.
【解答】解:A、图A表示两种单质的混合物,故选项错误;
B、图B表示一种单质和一种化合物组成的混合物,故选项错误;
C、图C表示纯净物中的单质,故选项正确;
D、图D表示纯净物中的化合物,故选项错误;
故选C
【点评】本考点考查了物质的分类和微观图示的辨别,要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.
7.(2016 扬州)下列物质属于化合物的是( )
A.硫
B.水
C.铜
D.空气
【分析】本题考查利用化合物的概念来判断物质是否为化合物,抓住化合物中至少两种元素,且只有一种物质组成.
【解答】解:
A、硫由一种元素组成,属于单质,故A错;
B、水由氢元素和氧元素组成,属于化合物,故B正确;
C、铜由一种元素组成,属于单质,故C错;
D、空气中含有氮气、氧气、二氧化碳等物质,属于混合物,故D错.
故选B.
【点评】应抓住概念的要点来判断物质的类别,了解常见物质的组成.
8.(2016 泰州)“含氟牙膏”中的“氟”指的是( )
A.元素
B.原子
C.离子
D.单质
【分析】食品、药品、营养品、矿泉水等物质中的“氟”等不是以分子、原子、离子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
【解答】解:“含氟牙膏”,这里的氟指的是不是以分子、原子、离子等形式存在,这里所指的“氟”是强调存在的元素,与具体形态无关.
故选A.
【点评】本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键.
9.(2016 齐齐哈尔)不同种元素最本质的区别是( )
A.中子数不同
B.质子数不同
C.相对原子质量不同
D.核外电子数不同
【分析】在原子中,质子数=核外电子数,但不同种元素之间的本质区别是质子数不同而不是电子数,更不能是中子数和相对原子质量
【解答】解:元素是具有相同核电荷数(即核内质子数)的一类原子的总称,不同种元素之间的本质区别是质子数不同,各选项中不同种元素最本质的区别是质子数不同;
故选:B.
【点评】本题考查学生在原子中,质子数=核外电子数,不同种元素之间的本质区别是质子数不同,此题利用元素的概念进行分析,可帮助学生的解题能力.
10.(2016 株洲)元素观是化学的重要观念之一.下列有关元素的说法中错误的是( )
A.元素是具有相同核电荷数的一类原子的总称
B.元素周期表,元素的原子序数与该元素原子核电荷数在数值上相同
C.同种元素的原子核内质子数与中子数一定相等
D.在物质发生化学变化时,原子的种类不变,元素也不会改变
【分析】A、根据元素的定义进行判断.
B、依据元素周期表是按照原子序数依次增多的顺序排列起来的,原子序数即原子核电荷数即可.
C、根据同种元素的质子数一定相等,中子数不一定相等进行分析.
D、根据在物质发生化学变化时,原子的种类不变,元素种类也不会改变判断.
【解答】解:A、元素的概念是具有相同核电荷数(即核内质子数)的一类原子的总称.所以选项正确.
B、元素周期表是按照原子序数依次增多的顺序排列起来的,原子序数即原子核电荷数,故B正确;
C、同种元素的质子数一定相等,中子数不一定相等,错误;
D、在物质发生化学变化时,原子的种类不变,元素也不会改变,故正确;
故选C
【点评】本题考查了元素的定义、元素周期表的有关内容、质量守恒的原因等知识,题目较易.
11.(2016 百色)豆腐是人们喜爱的食品,其中含铁和钙,这里所指的“铁”、“钙”理解为( )
A.分子
B.原子
C.单质
D.元素
【分析】根据已有的知识进行分析,物质是由元素组成的,据此解答.
【解答】解:物质是由元素组成的,这里的“钙、铁”指的是元素,观察选项,故选D.
【点评】本题考查了物质组成的知识,完成此题,可以依据已有的知识进行.
12.(2016 南京)在元素周期表中硅元素的某些信息如图所示,下列有关硅的说法错误的是( )
A.属于金属元素
B.元素符号为“Si”
C.原子序数为“14”
D.相对原子质量为“28.09”
【分析】根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,进行分析判断即可.
【解答】解:A、根据元素周期表中的一格中获取的信息,该元素的名称是硅,属于非金属元素,故选项说法错误.
B、根据元素周期表中的一格中获取的信息,该元素的元素符号是Si,故选项说法正确.
C、根据元素周期表中的一格中获取的信息,该元素的原子序数为14,故选项说法正确.
D、根据元素周期表中的一格中获取的信息,可知元素的相对原子质量为28.09,故选项说法正确.
故选A.
【点评】本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力.
13.(2016 黑龙江)元素周期表是学习化学的重要依据.下表是元素周期表的一部分,按表格提供的信息判断错误的是( )
A.碳、氮、氧三种元素都属于非金属元素
B.不同种元素之间最本质的区别是最外层电子数不同
C.氧原子的核内中子数是8
D.氮原子的相对原子质量是14.01
【分析】根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,进行分析判断即可.
【解答】解:A、根据元素周期表一部分中获取的信息,磷和硫都带有“石”旁,属于非金属元素,故说法正确;
B、根据元素周期表一部分中获取的信息,可知不同种元素之间最本质的区别是质子数不同,故说法错误;
C、根据元素周期表一部分中获取的信息,可知氧元素的中子数为=16﹣8,故说法正确.
D、根据元素周期表一部分中获取的信息,可知,氮原子的相对原子质量是14.01,故说法正确;
故选B.
【点评】本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力.
14.(2016 常德)中国科学院院士张青莲教授主持测定了铕、铱等近十种元素的相对原子质量,为相对原子质量测定作出了卓越贡献,下列关于铕的说法中正确的是( )
A.原子序数为63
B.属于非金属元素
C.原子核外电子数为89
D.相对原子质量为152.0g
【分析】根据元素周期表中的一个小格所提供的信息进行分析解答本题.
【解答】解:A.由元素周期表的信息可知,其原子序数为63,故正确;
B.铕元素带“钅”字旁,属于金属元素,故错误;
C.在原子中,原子序数=质子数=核外电子数,所以铕原子核外有63个电子,故错误;
D.相对原子质量的单位不是“g”而是“1”,通常省略不写,故错误.
故选A.
【点评】本题考查了元素周期表中看图回答最简单的元素名称、符号、原子序数、相对原子质量,学生必须掌握的知识.
15.(2016 苏州)下列人体所缺元素与引起的健康问题关系不正确的是( )
A.缺钙会引起骨质疏松
B.缺碘会引起甲状腺疾病
C.缺铁会引起龋齿
D.缺锌会导致儿童智力低下
【分析】A、根据钙的生理功能和缺乏症进行分析判断.
B、根据碘的生理功能和缺乏症进行分析判断.
C、根据铁的生理功能和缺乏症进行分析判断.
D、根据锌的生理功能和缺乏症进行分析判断.
【解答】解:A、钙主要存在于骨胳和牙齿中,使骨和牙齿具有坚硬的结构支架,缺乏幼儿和青少年会患佝偻病,老年人会患骨质疏松,故选项正确.
B、碘是合成甲状腺激素的主要元素,缺乏会患甲状腺肿大,故选项正确.
C、铁是合成血红蛋白的主要元素,缺乏会患贫血,故选项错误.
D、锌影响人体发育,缺锌会引起食欲不振,生长迟缓,发育不良,故选项正确.
故选C.
【点评】化学元素与人体健康的关系是中考考查的热点之一,掌握人体化学元素的分类、生理功能、缺乏症等是正确解题的关键.
二.填空题(共5小题)
16.(2016 广东)钒被誉为“合金中的维生素”.钒元素的部分信息如图所示.请回答下列问题:
(1)钒原子的质子数为 ,x= .
(2)钒属于 (填“金属”或“非金属”)元素;钒的相对原子质量为 .
【分析】根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,结合原子结构示意图的信息进行分析判断即可.
【解答】解:(1)由元素周期表的信息可知,钒的原子序数为23,原子序数=质子数,所以质子数为23;在原子中,质子数=核外电子数,所以x=23﹣8﹣11﹣2=2;故填:23;2;
(2)由元素名称的偏旁“金”字可知,该元素属于金属元素;由元素周期表的信息可知,其相对原子质量为50.94;故填:金属,50.94.
【点评】本题难度不大,考查学生灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)进行分析解题的能力.
17.(2016 南宁)原子序数为1﹣18的元素的原子结构示意图等信息如图,请认真并回答下列问题.
(1)原子序数为12的元素位于元素周期表中第 周期,它属于 (填“金属”或“非金属”)元素.
(2)在化学反应中,原子序数为16的元素的原子容易 (填“得到”或“失去”)电子,所形成的粒子的符号是 .
(3)根据氟原子和氯原子的结构示意图分析,由于氟原子和氯原子的 相同,所以氟元素与氯元素的化学性质相似.
(4)同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次 .
【分析】(1)根据原子核外的电子层数等于其所在周期数以及元素的分类来分析;
(2)原子序数为16的原子核内质子数为16;若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子;
(3)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,进行分析解答;
(4)根据元素周期表的规律来分析.
【解答】解:(1)12号元素是镁元素,其原子核外有3个电子层,所以在元素周期表中位于第三周期,镁属于金属元素;故填:三;金属;
(2)16号元素是硫,其原子最外层有6个电子,在化学反应中易得到2个电子形成带两个单位负电荷的硫离子;故填:得到;S2﹣;
(3)元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,氟元素和氯元素化学性质相似的原因是它们的原子的最外层电子数相同.故填:最外层电子数;
(4)同一周期元素之间从左到右,各元素原子随原子序数的增加,最外层电子数从1到8依次递增;故填:从1到8依次递增.
【点评】本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示意图的意义是正确解题的关键.
18.(2016 娄底)如图1是元素周期表中第2、3周期的元素,请回答有关问题
(1)具有相似化学性质的元素是 .
①Na、Cl
②O、S
③F、Cl
④Cl、Ar
(2)如图2所示结构是由氟原子 电子(填“得到”或“失去”)形成的.
(3)地壳中含量最多的金属元素的名称是 .
【分析】(1)根据同一族的元素具有相似的化学性质,进行分析解答.
(2)图中粒子质子数=9,核外电子数=10,质子数<核外电子数,为阴离子,进行分析解答.
(3)地壳中含量最多的金属元素是铝元素,写出其元素符号即可.
【解答】解:(1)同一族的元素具有相似的化学性质,由O、S和F、Cl分别位于同一族,具有相似的化学性质.
(2)图中粒子质子数=9,核外电子数=10,质子数<核外电子数,为阴离子,是氟原子得到1个电子得到的.
(3)地壳中含量最多的金属元素是铝元素,其元素符号为:铝.
故答案为:(1)②③;(2)得到;(3)铝.
【点评】本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、粒子结构示意图的含义是正确解答本题的关键.
19.(2016 达州)根据图中提供的信息,请回答下列问题:
(1)由A图可知,硅的相对原子质量为 ;
(2)B、C、D、E中属于同种元素的是 ;
(3)B、C元素化学性质相似的原因是 相同;
(4)C、E两种元素组成化合物的化学式为 .
【分析】(1)根据图中元素周期表可以获得的信息:汉字下面的数字表示相对原子质量,进行分析解答.
(2)元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的粒子是质子数相同,据此进行分析解答.
(3)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,据此进行分析解答.
(4)C的核内质子数为16,为硫原子;E的核内质子数为11,为钠元素;结合化合价的数值等于离子所带电荷的数值,且符号一致,进行分析解答.
【解答】解:(1)由图中元素周期表可以获得的信息:汉字下面的数字表示相对原子质量,硅的相对原子质量为28.09.
(2)元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),同种元素的粒子是质子数相同,CD的质子数相同,属于同种元素.
(3)元素的化学性质跟它的原子的最外层电子数目关系非常密切,B、C元素化学性质相似的原因是最外层电子数相同.
(4)C的核内质子数为16,为硫元素;硫原子的最外层电子数为6,在化学反应中易得到2个电子而形成2个单位负电荷的阴离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为﹣2价.E的核内质子数为11,为钠元素;钠原子的最外层电子数为1,在化学反应中易失去1个电子而形成带1个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+1价.则C、E两种元素组成化合物的化学式为Na2S.
故答案为:(1)28.09;(2)CD;(3)最外层电子数;(4)Na2S.
【点评】本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、粒子结构示意图的含义是正确解答本题的关键.
20.(2016 枣庄)如图是元素周期表的一部分,请回答:
(1)①处元素和②处元素形成常见化合物的化学式为 ,该化合物中②处元素的化合价为 .
(2)表示如表中 (填表中序号)的原子结构示意图,该原子易 (填“得”或“失”)电子,形成的离子符号为 .
【分析】(1)根据元素在元素周期表中的位置来确定元素种类,然后结合其常显化合价来书写化学式;
(2)根据原子结构示意图的意义以及离子符号的写法来分析.
【解答】解:(1)①是氧元素,在化合物中常显﹣2价,②是铝元素,常显+3价;二者组成的化合物氧化铝的化学式为Al2O3;故填:Al2O3;+3;
(2)由原子结构示意图可知,这是17号元素﹣﹣氯原子的结构示意图,元素位于元素周期表的④位置;其最外层有7个电子,在化学反应中易得到1个电子,而形成带一个单位负电荷的氯离子;故填:④;得;Cl﹣.
【点评】本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示意图的意义是正确解题的关键.
三.推断题(共2小题)
21.(2016 玉林)如图是元素周期表部分内容,请根据表中信息完成相关问题.
(1)铍原子的相对原子质量是 ,它属于 (填“金属”或“非金属”)元素.
(2)不同种元素最本质的区别是 .
(3)原子序数为1、6、8的三种元素形成的常见化合物的化学式为 ,其中6号元素的化合价是 .
【分析】(1)根据元素周期表中一个格的意义分析回答;
(2)根据元素的定义分析;
(3)根据原子序数确定元素及其组成的化合物,根据化合价原则求出元素的化合价.
【解答】解:(1)由元素周期表中一个格的意义可知,铍原子的相对原子质量是9.012,它的名称中带有“钅”字旁,属于金属元素.
(2)不同种元素最本质的区别是质子数不同,
(3)原子序数为1、6、8的三种元素分别是氢、碳、氧元素,形成的常见化合物是碳酸,化学式为:H2CO3,由于氢显+1价,氧显﹣2价,由化合价原则可推出其中6号碳元素的化合价是+4.
故答为:(1)9.012,金属.(2)质子数不同,(3)H2CO3,+4.
【点评】本题的难度不大,了解元素周期表的意义、元素的定义和化合价原则是解答本题的基础知识.
22.图乙为水分子分解示意图.请回答下列问题:
(1)请写出一条从图甲中你能获取的相关信息
(2)图乙形象的表示了水分解前后分子的变化.该反应的方程式为 ;该示意图说明了化学变化的微观实质是 .
【分析】(1)根据元素周期表中的一个小格所提供的信息:元素名称、符号、原子序数、相对原子质量,写出其中一个即可;
(2)根据化学方程式的写,配,注,等书写反应的化学方程式即可解答;
根据化学反应的实质是反应物的分子破坏成原子,原子又重新组合成新的生成物的分子,进行解答.
【解答】解:(1)根据元素周期表中的一个小格所提供的信息:元素名称为钙或元素符号为Ca
或钙元素原子序数为20或钙原子的核内质子数为20或钙原子的相对原子质量为40.08,;
故答案为:钙原子的核内质子数为20(答案合理即可);
(2)根据化学方程式的写,配,注,等书写反应的化学方程式为:2H2O2H2↑+O2↑;
根据化学反应的实质是反应物的分子破坏成原子,原子又重新组合成新的生成物的分子;
故答案为:2H2O2H2↑+O2↑;分子发生破裂,原子重新组合成新的分子.
【点评】本题主要考查学生对化学方程式的书写及化学反应的实质的理解与掌握.
四.解答题(共3小题)
23.元素周期律和周期表是学习化学的重要工具.下表是元素周期表的部分信息.
1
H氢
2
He氦
3
Li锂
4
Be铍
5
B硼
6
C碳
7
N氮
8
O氧
9
F氟
10
Ne氖
11
Na钠
12
Mg镁
13
Al铝
14
Si硅
15
P磷
16
S硫
17
Cl氯
18
Ar氩
(1)列出的18种元素中,有 种属于金属元素.
(2)从原子结构角度看,同一周期元素的原子具有相同的 数.某粒子结构示意图为,该粒子所属元素位于周期表的第 周期.
(3)观察硫原子结构示意图,在下图中填空:
【分析】(1)由汉语名称的“偏旁”可知,属于金属元素的有几种;
(2)同一周期的元素具有相同的电子层数;
(3)非金属元素的最外层电子多余四个,易得电子,而变成阴离子,金属元素易失去电子而变成阳离子;
【解答】解:(1)根据汉语名称带钅字旁的为金属元素,所以共有5种金属元素;
(2)从原子结构角度看,同一周期元素的原子具有相同的电子层数,比较图中的电子和质子数可以知道,失掉了两个电子,所以其原子应该有三个电子层;
(3)硫元素最外层为六个电子,易得两个电子而变成阴离子,而钠元素的最外层有一个电子已失去而带一个单位的正电荷,变成阳离子,故其组成的化学式为:Na2S;
故答案为:(1)5
(2)电子层;
三;
(3)得;Na2S;
【点评】了解元素周期表的特点及其应用;了解元素的简单分类;了解原子结构示意图与离子结构示意图的特点.
24.如图中的①、②分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图.
试回答下列问题:
(1)钠元素的原子序数为 ;
(2)A、B、C中属于同种元素的粒子是 ;
(3)A和B两种粒子的 相同,所以它们具有相似的化学性质;
(4)钠原子和氯原子反应所形成的化合物是由 (填“分子”、“原子”、“离子”)构成的.
【分析】(1)根据图中元素周期表可以获得的信息:原子序数为11;
(2)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的是核电荷数(即核内质子数),据此进行分析解答;
(3)根据元素的化学性质跟它的原子的最外层电子数目有关,决定元素的化学性质的是原子的最外层电子数,进行分析解答.
(4)钠原子和氯原子反应是靠的是电子形成的,所形成的化合物是氯化钠是离子化合物;
【解答】解:(1)由钠元素的元素周期表中的信息可知钠元素的原子序数为11;
(2)根据决定元素种类的是核电荷数(即核内质子数),因为AB的核内质子数相同,所以BC属于同种元素的粒子;
(3)决定元素的化学性质的是原子的最外层电子数,A粒子B粒子的最外层电子数相同,A粒子化学性质与B粒子化学性质相似;
(4)钠原子和氯原子反应是靠的是电子形成的,所形成的化合物是氯化钠是离子化合物;故氯化钠是由钠离子和氯离子构成的;
答案:(1)11;(2)BC;(3)最外层电子数;(4)离子.
【点评】本题考查学生对在原子中,原子序数,质子数,核外电子数,核电荷数之间的关系及元素的最外层电子数决定元素的化学性质的理解与掌握.
25.
(1)人体中必需的微量元素铁、氟、锌、硒、碘等,虽然含量少,但对健康至关重要.
如图1,提供了几种微量元素相关信息,由此可知:上述微量元素中属于金属元素的有 种;锌原子核外电子数为 ;硒原子在化学反应中容易得到2个电子,形成
(选填“阴”或“阳”)离子.缺碘可能造成的疾病有 .
(2)如图2,为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是 .
A、原子序数:Z>Y B、核外电子数:X=Y
C、Y和Z处于同一周期.
【分析】(1)熟记微量元素,根据元素的名称可以判断出元素的种类,其中金属元素指的是带有“金”字偏旁的元素,可据此解答;根据原子的核外电子数=核内质子数=原子序数来完成解答;根据离子的形成过程来完成解答;
(2)元素周期表中,横行表示周期,纵行表示族,位于同一周期的元素具有相同的电子层数,位于同一族的元素最外层电子数相同,在同一周期里,越往右原子序数越大.
【解答】解:(1)上述三种元素中为金属元素的有:铁元素和锌元素;从图中可以知道锌原子为30号元素,所以根据原子的核外电子数=核内质子数=原子序数,可以知道锌原子的核外电子数为30;硒原子得到电子使质子数小于电子数,而电子带负电,所以使硒原子带上了两个单位的负电荷,形成阴离子,缺碘易患甲状腺肿大;故答案为:2;30;阴;甲状腺肿大;
(2)A、元素周期表中,横行表示周期,Y和Z在同一横行,所以位于同一周期里,且Z在Y的右侧,越往右原子序数越大,故A正确;
B、原子核外电子数=原子序数,由于X与Y属于不同的元素,所以原子序数不同,故核外电子数也不同,故B错误;
C、Y和Z在同一横行,所以位于同一周期,故C正确;
故答案为:A、C.
【点评】此题考查了元素的分类和元素周期表的相关知识,是一道综合题目.
组成物质的化学元素
一.选择题(共15小题)
1.(2016 衡阳)下列物质中,属于氧化物的是( )
A.镁
B.空气
C.硝酸钾
D.二氧化锰
2.(2016 上海)属于纯净物的是( )
A.盐汽水
B.矿泉水
C.自来水
D.蒸馏水
3.(2016 天津)下列物质中属于混合物的是( )
A.河水
B.氯酸钾
C.三氧化硫
D.五氧化二磷
4.(2016 吉林)青蒿素(化学式C15H22O5)是中国科学家从植物中成功分离出的抗疟药的有效成分,它属于( )
A.单质
B.纯净物
C.氧化物
D.混合物
5.(2016 苏州)下列物质属于混合物的是( )
A.氧气
B.氧化铜
C.硫酸钠
D.空气
6.(2016 齐齐哈尔)下列微观模拟图中●和○分别表示不同元素的原子,其中表示单质的是( )
A.
B.
C.
D.
7.(2016 扬州)下列物质属于化合物的是( )
A.硫
B.水
C.铜
D.空气
8.(2016 泰州)“含氟牙膏”中的“氟”指的是( )
A.元素
B.原子
C.离子
D.单质
9.(2016 齐齐哈尔)不同种元素最本质的区别是( )
A.中子数不同
B.质子数不同
C.相对原子质量不同
D.核外电子数不同
10.(2016 株洲)元素观是化学的重要观念之一.下列有关元素的说法中错误的是( )
A.元素是具有相同核电荷数的一类原子的总称
B.元素周期表,元素的原子序数与该元素原子核电荷数在数值上相同
C.同种元素的原子核内质子数与中子数一定相等
D.在物质发生化学变化时,原子的种类不变,元素也不会改变
11.(2016 百色)豆腐是人们喜爱的食品,其中含铁和钙,这里所指的“铁”、“钙”理解为( )
A.分子
B.原子
C.单质
D.元素
12.(2016 南京)在元素周期表中硅元素的某些信息如图所示,下列有关硅的说法错误的是( )
A.属于金属元素
B.元素符号为“Si”
C.原子序数为“14”
D.相对原子质量为“28.09”
13.(2016 黑龙江)元素周期表是学习化学的重要依据.下表是元素周期表的一部分,按表格提供的信息判断错误的是( )
A.碳、氮、氧三种元素都属于非金属元素
B.不同种元素之间最本质的区别是最外层电子数不同
C.氧原子的核内中子数是8
D.氮原子的相对原子质量是14.01
14.(2016 常德)中国科学院院士张青莲教授主持测定了铕、铱等近十种元素的相对原子质量,为相对原子质量测定作出了卓越贡献,下列关于铕的说法中正确的是( )
A.原子序数为63
B.属于非金属元素
C.原子核外电子数为89
D.相对原子质量为152.0g
15.(2016 苏州)下列人体所缺元素与引起的健康问题关系不正确的是( )
A.缺钙会引起骨质疏松
B.缺碘会引起甲状腺疾病
C.缺铁会引起龋齿
D.缺锌会导致儿童智力低下
二.填空题(共5小题)
16.(2016 广东)钒被誉为“合金中的维生素”.钒元素的部分信息如图所示.请回答下列问题:
(1)钒原子的质子数为 ,x= .
(2)钒属于 (填“金属”或“非金属”)元素;钒的相对原子质量为 .
17.(2016 南宁)原子序数为1﹣18的元素的原子结构示意图等信息如图,请认真并回答下列问题.
(1)原子序数为12的元素位于元素周期表中第 周期,它属于 (填“金属”或“非金属”)元素.
(2)在化学反应中,原子序数为16的元素的原子容易 (填“得到”或“失去”)电子,所形成的粒子的符号是 .
(3)根据氟原子和氯原子的结构示意图分析,由于氟原子和氯原子的 相同,所以氟元素与氯元素的化学性质相似.
(4)同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次 .
18.(2016 娄底)如图1是元素周期表中第2、3周期的元素,请回答有关问题
(1)具有相似化学性质的元素是 .
①Na、Cl
②O、S
③F、Cl
④Cl、Ar
(2)如图2所示结构是由氟原子 电子(填“得到”或“失去”)形成的.
(3)地壳中含量最多的金属元素的名称是 .
19.(2016 达州)根据图中提供的信息,请回答下列问题:
(1)由A图可知,硅的相对原子质量为 ;
(2)B、C、D、E中属于同种元素的是 ;
(3)B、C元素化学性质相似的原因是 相同;
(4)C、E两种元素组成化合物的化学式为 .
20.(2016 枣庄)如图是元素周期表的一部分,请回答:
(1)①处元素和②处元素形成常见化合物的化学式为 ,该化合物中②处元素的化合价为 .
(2)表示如表中 (填表中序号)的原子结构示意图,该原子易 (填“得”或“失”)电子,形成的离子符号为 .
三.推断题(共2小题)
21.(2016 玉林)如图是元素周期表部分内容,请根据表中信息完成相关问题.
(1)铍原子的相对原子质量是 ,它属于 (填“金属”或“非金属”)元素.
(2)不同种元素最本质的区别是 .
(3)原子序数为1、6、8的三种元素形成的常见化合物的化学式为 ,其中6号元素的化合价是 .
22.图乙为水分子分解示意图.请回答下列问题:
(1)请写出一条从图甲中你能获取的相关信息
(2)图乙形象的表示了水分解前后分子的变化.该反应的方程式为 ;该示意图说明了化学变化的微观实质是 .
四.解答题(共3小题)
23.元素周期律和周期表是学习化学的重要工具.下表是元素周期表的部分信息.
1
H氢
2
He氦
3
Li锂
4
Be铍
5
B硼
6
C碳
7
N氮
8
O氧
9
F氟
10
Ne氖
11
Na钠
12
Mg镁
13
Al铝
14
Si硅
15
P磷
16
S硫
17
Cl氯
18
Ar氩
(1)列出的18种元素中,有 种属于金属元素.
(2)从原子结构角度看,同一周期元素的原子具有相同的 数.某粒子结构示意图为,该粒子所属元素位于周期表的第 周期.
(3)观察硫原子结构示意图,在下图中填空:
24.如图中的①、②分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图.
试回答下列问题:
(1)钠元素的原子序数为 ;
(2)A、B、C中属于同种元素的粒子是 ;
(3)A和B两种粒子的 相同,所以它们具有相似的化学性质;
(4)钠原子和氯原子反应所形成的化合物是由 (填“分子”、“原子”、“离子”)构成的.
25.
(1)人体中必需的微量元素铁、氟、锌、硒、碘等,虽然含量少,但对健康至关重要.
如图1,提供了几种微量元素相关信息,由此可知:上述微量元素中属于金属元素的有 种;锌原子核外电子数为 ;硒原子在化学反应中容易得到2个电子,形成
(选填“阴”或“阳”)离子.缺碘可能造成的疾病有 .
(2)如图2,为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是 .
A、原子序数:Z>Y B、核外电子数:X=Y
C、Y和Z处于同一周期.
参考答案与解析
一.选择题(共15小题)
1.(2016 衡阳)下列物质中,属于氧化物的是( )
A.镁
B.空气
C.硝酸钾
D.二氧化锰
【分析】本题考查氧化物的识别,根据氧化物的概念可知氧化物只有两种元素,且必须有氧元素.
【解答】解:A中只有一种元素,属于单质,故A错.
B中有氮气、氧气、二氧化碳等物质,属于混合物,故B错.
C中有三种元素,也含氧元素,但不属于氧化物,属于盐,故C错.
D中有两种元素,其一为氧元素,属于氧化物,故D正确.
故选D.
【点评】本题较简单,主要从概念上来抓住判断的关键点,两个关键点缺一不可,要同时具备.
2.(2016 上海)属于纯净物的是( )
A.盐汽水
B.矿泉水
C.自来水
D.蒸馏水
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.
【解答】解:A、盐汽水中有盐、碳酸等物质,属于混合物,故选项错误;
B、矿泉水中有矿物质和水,属于混合物,故选项错误;
C、自来水中有可溶性杂质和不溶性杂质,属于混合物,故选项错误;
D、蒸馏水中只有水分子,属于纯净物中的氧化物,故选项正确;
故选D
【点评】本考点考查了物质的分类,与生活实际联系比较密切.要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.
3.(2016 天津)下列物质中属于混合物的是( )
A.河水
B.氯酸钾
C.三氧化硫
D.五氧化二磷
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.
【解答】解:A、河水中有可溶性杂质和不溶性杂质,属于混合物,故选项正确;
B、氯酸钾属于纯净物中的化合物,故选项错误;
C、三氧化硫属于纯净物中的氧化物,故选项错误;
D、五氧化二磷属于纯净物中的氧化物,故选项错误;
故选A
【点评】本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.
4.(2016 吉林)青蒿素(化学式C15H22O5)是中国科学家从植物中成功分离出的抗疟药的有效成分,它属于( )
A.单质
B.纯净物
C.氧化物
D.混合物
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.青蒿素(化学式C15H22O5)是一种物质,属于纯净物中的化合物.
【解答】解:A、由同种元素组成的纯净物叫单质,故选项错误;
B、青蒿素(化学式C15H22O5)是一种物质,属于纯净物中的化合物,故选项正确;
C、氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素,故选项错误;
D、混合物是由两种或两种以上的物质组成,故选项错误;
故选B
【点评】本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.
5.(2016 苏州)下列物质属于混合物的是( )
A.氧气
B.氧化铜
C.硫酸钠
D.空气
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.
【解答】解:A、氧气属于纯净物中的单质,故选项错误;
B、氧化铜属于纯净物中的氧化物,故选项错误;
C、硫酸钠属于纯净物中的化合物,故选项错误;
D、空气中有氧气、氮气等物质,属于混合物,故选项正确;
故选D
【点评】本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.
6.(2016 齐齐哈尔)下列微观模拟图中●和○分别表示不同元素的原子,其中表示单质的是( )
A.
B.
C.
D.
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.
【解答】解:A、图A表示两种单质的混合物,故选项错误;
B、图B表示一种单质和一种化合物组成的混合物,故选项错误;
C、图C表示纯净物中的单质,故选项正确;
D、图D表示纯净物中的化合物,故选项错误;
故选C
【点评】本考点考查了物质的分类和微观图示的辨别,要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.
7.(2016 扬州)下列物质属于化合物的是( )
A.硫
B.水
C.铜
D.空气
【分析】本题考查利用化合物的概念来判断物质是否为化合物,抓住化合物中至少两种元素,且只有一种物质组成.
【解答】解:
A、硫由一种元素组成,属于单质,故A错;
B、水由氢元素和氧元素组成,属于化合物,故B正确;
C、铜由一种元素组成,属于单质,故C错;
D、空气中含有氮气、氧气、二氧化碳等物质,属于混合物,故D错.
故选B.
【点评】应抓住概念的要点来判断物质的类别,了解常见物质的组成.
8.(2016 泰州)“含氟牙膏”中的“氟”指的是( )
A.元素
B.原子
C.离子
D.单质
【分析】食品、药品、营养品、矿泉水等物质中的“氟”等不是以分子、原子、离子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
【解答】解:“含氟牙膏”,这里的氟指的是不是以分子、原子、离子等形式存在,这里所指的“氟”是强调存在的元素,与具体形态无关.
故选A.
【点评】本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键.
9.(2016 齐齐哈尔)不同种元素最本质的区别是( )
A.中子数不同
B.质子数不同
C.相对原子质量不同
D.核外电子数不同
【分析】在原子中,质子数=核外电子数,但不同种元素之间的本质区别是质子数不同而不是电子数,更不能是中子数和相对原子质量
【解答】解:元素是具有相同核电荷数(即核内质子数)的一类原子的总称,不同种元素之间的本质区别是质子数不同,各选项中不同种元素最本质的区别是质子数不同;
故选:B.
【点评】本题考查学生在原子中,质子数=核外电子数,不同种元素之间的本质区别是质子数不同,此题利用元素的概念进行分析,可帮助学生的解题能力.
10.(2016 株洲)元素观是化学的重要观念之一.下列有关元素的说法中错误的是( )
A.元素是具有相同核电荷数的一类原子的总称
B.元素周期表,元素的原子序数与该元素原子核电荷数在数值上相同
C.同种元素的原子核内质子数与中子数一定相等
D.在物质发生化学变化时,原子的种类不变,元素也不会改变
【分析】A、根据元素的定义进行判断.
B、依据元素周期表是按照原子序数依次增多的顺序排列起来的,原子序数即原子核电荷数即可.
C、根据同种元素的质子数一定相等,中子数不一定相等进行分析.
D、根据在物质发生化学变化时,原子的种类不变,元素种类也不会改变判断.
【解答】解:A、元素的概念是具有相同核电荷数(即核内质子数)的一类原子的总称.所以选项正确.
B、元素周期表是按照原子序数依次增多的顺序排列起来的,原子序数即原子核电荷数,故B正确;
C、同种元素的质子数一定相等,中子数不一定相等,错误;
D、在物质发生化学变化时,原子的种类不变,元素也不会改变,故正确;
故选C
【点评】本题考查了元素的定义、元素周期表的有关内容、质量守恒的原因等知识,题目较易.
11.(2016 百色)豆腐是人们喜爱的食品,其中含铁和钙,这里所指的“铁”、“钙”理解为( )
A.分子
B.原子
C.单质
D.元素
【分析】根据已有的知识进行分析,物质是由元素组成的,据此解答.
【解答】解:物质是由元素组成的,这里的“钙、铁”指的是元素,观察选项,故选D.
【点评】本题考查了物质组成的知识,完成此题,可以依据已有的知识进行.
12.(2016 南京)在元素周期表中硅元素的某些信息如图所示,下列有关硅的说法错误的是( )
A.属于金属元素
B.元素符号为“Si”
C.原子序数为“14”
D.相对原子质量为“28.09”
【分析】根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,进行分析判断即可.
【解答】解:A、根据元素周期表中的一格中获取的信息,该元素的名称是硅,属于非金属元素,故选项说法错误.
B、根据元素周期表中的一格中获取的信息,该元素的元素符号是Si,故选项说法正确.
C、根据元素周期表中的一格中获取的信息,该元素的原子序数为14,故选项说法正确.
D、根据元素周期表中的一格中获取的信息,可知元素的相对原子质量为28.09,故选项说法正确.
故选A.
【点评】本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力.
13.(2016 黑龙江)元素周期表是学习化学的重要依据.下表是元素周期表的一部分,按表格提供的信息判断错误的是( )
A.碳、氮、氧三种元素都属于非金属元素
B.不同种元素之间最本质的区别是最外层电子数不同
C.氧原子的核内中子数是8
D.氮原子的相对原子质量是14.01
【分析】根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,进行分析判断即可.
【解答】解:A、根据元素周期表一部分中获取的信息,磷和硫都带有“石”旁,属于非金属元素,故说法正确;
B、根据元素周期表一部分中获取的信息,可知不同种元素之间最本质的区别是质子数不同,故说法错误;
C、根据元素周期表一部分中获取的信息,可知氧元素的中子数为=16﹣8,故说法正确.
D、根据元素周期表一部分中获取的信息,可知,氮原子的相对原子质量是14.01,故说法正确;
故选B.
【点评】本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力.
14.(2016 常德)中国科学院院士张青莲教授主持测定了铕、铱等近十种元素的相对原子质量,为相对原子质量测定作出了卓越贡献,下列关于铕的说法中正确的是( )
A.原子序数为63
B.属于非金属元素
C.原子核外电子数为89
D.相对原子质量为152.0g
【分析】根据元素周期表中的一个小格所提供的信息进行分析解答本题.
【解答】解:A.由元素周期表的信息可知,其原子序数为63,故正确;
B.铕元素带“钅”字旁,属于金属元素,故错误;
C.在原子中,原子序数=质子数=核外电子数,所以铕原子核外有63个电子,故错误;
D.相对原子质量的单位不是“g”而是“1”,通常省略不写,故错误.
故选A.
【点评】本题考查了元素周期表中看图回答最简单的元素名称、符号、原子序数、相对原子质量,学生必须掌握的知识.
15.(2016 苏州)下列人体所缺元素与引起的健康问题关系不正确的是( )
A.缺钙会引起骨质疏松
B.缺碘会引起甲状腺疾病
C.缺铁会引起龋齿
D.缺锌会导致儿童智力低下
【分析】A、根据钙的生理功能和缺乏症进行分析判断.
B、根据碘的生理功能和缺乏症进行分析判断.
C、根据铁的生理功能和缺乏症进行分析判断.
D、根据锌的生理功能和缺乏症进行分析判断.
【解答】解:A、钙主要存在于骨胳和牙齿中,使骨和牙齿具有坚硬的结构支架,缺乏幼儿和青少年会患佝偻病,老年人会患骨质疏松,故选项正确.
B、碘是合成甲状腺激素的主要元素,缺乏会患甲状腺肿大,故选项正确.
C、铁是合成血红蛋白的主要元素,缺乏会患贫血,故选项错误.
D、锌影响人体发育,缺锌会引起食欲不振,生长迟缓,发育不良,故选项正确.
故选C.
【点评】化学元素与人体健康的关系是中考考查的热点之一,掌握人体化学元素的分类、生理功能、缺乏症等是正确解题的关键.
二.填空题(共5小题)
16.(2016 广东)钒被誉为“合金中的维生素”.钒元素的部分信息如图所示.请回答下列问题:
(1)钒原子的质子数为 ,x= .
(2)钒属于 (填“金属”或“非金属”)元素;钒的相对原子质量为 .
【分析】根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,结合原子结构示意图的信息进行分析判断即可.
【解答】解:(1)由元素周期表的信息可知,钒的原子序数为23,原子序数=质子数,所以质子数为23;在原子中,质子数=核外电子数,所以x=23﹣8﹣11﹣2=2;故填:23;2;
(2)由元素名称的偏旁“金”字可知,该元素属于金属元素;由元素周期表的信息可知,其相对原子质量为50.94;故填:金属,50.94.
【点评】本题难度不大,考查学生灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)进行分析解题的能力.
17.(2016 南宁)原子序数为1﹣18的元素的原子结构示意图等信息如图,请认真并回答下列问题.
(1)原子序数为12的元素位于元素周期表中第 周期,它属于 (填“金属”或“非金属”)元素.
(2)在化学反应中,原子序数为16的元素的原子容易 (填“得到”或“失去”)电子,所形成的粒子的符号是 .
(3)根据氟原子和氯原子的结构示意图分析,由于氟原子和氯原子的 相同,所以氟元素与氯元素的化学性质相似.
(4)同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次 .
【分析】(1)根据原子核外的电子层数等于其所在周期数以及元素的分类来分析;
(2)原子序数为16的原子核内质子数为16;若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子;
(3)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,进行分析解答;
(4)根据元素周期表的规律来分析.
【解答】解:(1)12号元素是镁元素,其原子核外有3个电子层,所以在元素周期表中位于第三周期,镁属于金属元素;故填:三;金属;
(2)16号元素是硫,其原子最外层有6个电子,在化学反应中易得到2个电子形成带两个单位负电荷的硫离子;故填:得到;S2﹣;
(3)元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,氟元素和氯元素化学性质相似的原因是它们的原子的最外层电子数相同.故填:最外层电子数;
(4)同一周期元素之间从左到右,各元素原子随原子序数的增加,最外层电子数从1到8依次递增;故填:从1到8依次递增.
【点评】本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示意图的意义是正确解题的关键.
18.(2016 娄底)如图1是元素周期表中第2、3周期的元素,请回答有关问题
(1)具有相似化学性质的元素是 .
①Na、Cl
②O、S
③F、Cl
④Cl、Ar
(2)如图2所示结构是由氟原子 电子(填“得到”或“失去”)形成的.
(3)地壳中含量最多的金属元素的名称是 .
【分析】(1)根据同一族的元素具有相似的化学性质,进行分析解答.
(2)图中粒子质子数=9,核外电子数=10,质子数<核外电子数,为阴离子,进行分析解答.
(3)地壳中含量最多的金属元素是铝元素,写出其元素符号即可.
【解答】解:(1)同一族的元素具有相似的化学性质,由O、S和F、Cl分别位于同一族,具有相似的化学性质.
(2)图中粒子质子数=9,核外电子数=10,质子数<核外电子数,为阴离子,是氟原子得到1个电子得到的.
(3)地壳中含量最多的金属元素是铝元素,其元素符号为:铝.
故答案为:(1)②③;(2)得到;(3)铝.
【点评】本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、粒子结构示意图的含义是正确解答本题的关键.
19.(2016 达州)根据图中提供的信息,请回答下列问题:
(1)由A图可知,硅的相对原子质量为 ;
(2)B、C、D、E中属于同种元素的是 ;
(3)B、C元素化学性质相似的原因是 相同;
(4)C、E两种元素组成化合物的化学式为 .
【分析】(1)根据图中元素周期表可以获得的信息:汉字下面的数字表示相对原子质量,进行分析解答.
(2)元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的粒子是质子数相同,据此进行分析解答.
(3)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,据此进行分析解答.
(4)C的核内质子数为16,为硫原子;E的核内质子数为11,为钠元素;结合化合价的数值等于离子所带电荷的数值,且符号一致,进行分析解答.
【解答】解:(1)由图中元素周期表可以获得的信息:汉字下面的数字表示相对原子质量,硅的相对原子质量为28.09.
(2)元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),同种元素的粒子是质子数相同,CD的质子数相同,属于同种元素.
(3)元素的化学性质跟它的原子的最外层电子数目关系非常密切,B、C元素化学性质相似的原因是最外层电子数相同.
(4)C的核内质子数为16,为硫元素;硫原子的最外层电子数为6,在化学反应中易得到2个电子而形成2个单位负电荷的阴离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为﹣2价.E的核内质子数为11,为钠元素;钠原子的最外层电子数为1,在化学反应中易失去1个电子而形成带1个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+1价.则C、E两种元素组成化合物的化学式为Na2S.
故答案为:(1)28.09;(2)CD;(3)最外层电子数;(4)Na2S.
【点评】本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、粒子结构示意图的含义是正确解答本题的关键.
20.(2016 枣庄)如图是元素周期表的一部分,请回答:
(1)①处元素和②处元素形成常见化合物的化学式为 ,该化合物中②处元素的化合价为 .
(2)表示如表中 (填表中序号)的原子结构示意图,该原子易 (填“得”或“失”)电子,形成的离子符号为 .
【分析】(1)根据元素在元素周期表中的位置来确定元素种类,然后结合其常显化合价来书写化学式;
(2)根据原子结构示意图的意义以及离子符号的写法来分析.
【解答】解:(1)①是氧元素,在化合物中常显﹣2价,②是铝元素,常显+3价;二者组成的化合物氧化铝的化学式为Al2O3;故填:Al2O3;+3;
(2)由原子结构示意图可知,这是17号元素﹣﹣氯原子的结构示意图,元素位于元素周期表的④位置;其最外层有7个电子,在化学反应中易得到1个电子,而形成带一个单位负电荷的氯离子;故填:④;得;Cl﹣.
【点评】本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示意图的意义是正确解题的关键.
三.推断题(共2小题)
21.(2016 玉林)如图是元素周期表部分内容,请根据表中信息完成相关问题.
(1)铍原子的相对原子质量是 ,它属于 (填“金属”或“非金属”)元素.
(2)不同种元素最本质的区别是 .
(3)原子序数为1、6、8的三种元素形成的常见化合物的化学式为 ,其中6号元素的化合价是 .
【分析】(1)根据元素周期表中一个格的意义分析回答;
(2)根据元素的定义分析;
(3)根据原子序数确定元素及其组成的化合物,根据化合价原则求出元素的化合价.
【解答】解:(1)由元素周期表中一个格的意义可知,铍原子的相对原子质量是9.012,它的名称中带有“钅”字旁,属于金属元素.
(2)不同种元素最本质的区别是质子数不同,
(3)原子序数为1、6、8的三种元素分别是氢、碳、氧元素,形成的常见化合物是碳酸,化学式为:H2CO3,由于氢显+1价,氧显﹣2价,由化合价原则可推出其中6号碳元素的化合价是+4.
故答为:(1)9.012,金属.(2)质子数不同,(3)H2CO3,+4.
【点评】本题的难度不大,了解元素周期表的意义、元素的定义和化合价原则是解答本题的基础知识.
22.图乙为水分子分解示意图.请回答下列问题:
(1)请写出一条从图甲中你能获取的相关信息
(2)图乙形象的表示了水分解前后分子的变化.该反应的方程式为 ;该示意图说明了化学变化的微观实质是 .
【分析】(1)根据元素周期表中的一个小格所提供的信息:元素名称、符号、原子序数、相对原子质量,写出其中一个即可;
(2)根据化学方程式的写,配,注,等书写反应的化学方程式即可解答;
根据化学反应的实质是反应物的分子破坏成原子,原子又重新组合成新的生成物的分子,进行解答.
【解答】解:(1)根据元素周期表中的一个小格所提供的信息:元素名称为钙或元素符号为Ca
或钙元素原子序数为20或钙原子的核内质子数为20或钙原子的相对原子质量为40.08,;
故答案为:钙原子的核内质子数为20(答案合理即可);
(2)根据化学方程式的写,配,注,等书写反应的化学方程式为:2H2O2H2↑+O2↑;
根据化学反应的实质是反应物的分子破坏成原子,原子又重新组合成新的生成物的分子;
故答案为:2H2O2H2↑+O2↑;分子发生破裂,原子重新组合成新的分子.
【点评】本题主要考查学生对化学方程式的书写及化学反应的实质的理解与掌握.
四.解答题(共3小题)
23.元素周期律和周期表是学习化学的重要工具.下表是元素周期表的部分信息.
1
H氢
2
He氦
3
Li锂
4
Be铍
5
B硼
6
C碳
7
N氮
8
O氧
9
F氟
10
Ne氖
11
Na钠
12
Mg镁
13
Al铝
14
Si硅
15
P磷
16
S硫
17
Cl氯
18
Ar氩
(1)列出的18种元素中,有 种属于金属元素.
(2)从原子结构角度看,同一周期元素的原子具有相同的 数.某粒子结构示意图为,该粒子所属元素位于周期表的第 周期.
(3)观察硫原子结构示意图,在下图中填空:
【分析】(1)由汉语名称的“偏旁”可知,属于金属元素的有几种;
(2)同一周期的元素具有相同的电子层数;
(3)非金属元素的最外层电子多余四个,易得电子,而变成阴离子,金属元素易失去电子而变成阳离子;
【解答】解:(1)根据汉语名称带钅字旁的为金属元素,所以共有5种金属元素;
(2)从原子结构角度看,同一周期元素的原子具有相同的电子层数,比较图中的电子和质子数可以知道,失掉了两个电子,所以其原子应该有三个电子层;
(3)硫元素最外层为六个电子,易得两个电子而变成阴离子,而钠元素的最外层有一个电子已失去而带一个单位的正电荷,变成阳离子,故其组成的化学式为:Na2S;
故答案为:(1)5
(2)电子层;
三;
(3)得;Na2S;
【点评】了解元素周期表的特点及其应用;了解元素的简单分类;了解原子结构示意图与离子结构示意图的特点.
24.如图中的①、②分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图.
试回答下列问题:
(1)钠元素的原子序数为 ;
(2)A、B、C中属于同种元素的粒子是 ;
(3)A和B两种粒子的 相同,所以它们具有相似的化学性质;
(4)钠原子和氯原子反应所形成的化合物是由 (填“分子”、“原子”、“离子”)构成的.
【分析】(1)根据图中元素周期表可以获得的信息:原子序数为11;
(2)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的是核电荷数(即核内质子数),据此进行分析解答;
(3)根据元素的化学性质跟它的原子的最外层电子数目有关,决定元素的化学性质的是原子的最外层电子数,进行分析解答.
(4)钠原子和氯原子反应是靠的是电子形成的,所形成的化合物是氯化钠是离子化合物;
【解答】解:(1)由钠元素的元素周期表中的信息可知钠元素的原子序数为11;
(2)根据决定元素种类的是核电荷数(即核内质子数),因为AB的核内质子数相同,所以BC属于同种元素的粒子;
(3)决定元素的化学性质的是原子的最外层电子数,A粒子B粒子的最外层电子数相同,A粒子化学性质与B粒子化学性质相似;
(4)钠原子和氯原子反应是靠的是电子形成的,所形成的化合物是氯化钠是离子化合物;故氯化钠是由钠离子和氯离子构成的;
答案:(1)11;(2)BC;(3)最外层电子数;(4)离子.
【点评】本题考查学生对在原子中,原子序数,质子数,核外电子数,核电荷数之间的关系及元素的最外层电子数决定元素的化学性质的理解与掌握.
25.
(1)人体中必需的微量元素铁、氟、锌、硒、碘等,虽然含量少,但对健康至关重要.
如图1,提供了几种微量元素相关信息,由此可知:上述微量元素中属于金属元素的有 种;锌原子核外电子数为 ;硒原子在化学反应中容易得到2个电子,形成
(选填“阴”或“阳”)离子.缺碘可能造成的疾病有 .
(2)如图2,为元素周期表的一部分,X、Y、Z代表三种不同元素,以下判断正确的是 .
A、原子序数:Z>Y B、核外电子数:X=Y
C、Y和Z处于同一周期.
【分析】(1)熟记微量元素,根据元素的名称可以判断出元素的种类,其中金属元素指的是带有“金”字偏旁的元素,可据此解答;根据原子的核外电子数=核内质子数=原子序数来完成解答;根据离子的形成过程来完成解答;
(2)元素周期表中,横行表示周期,纵行表示族,位于同一周期的元素具有相同的电子层数,位于同一族的元素最外层电子数相同,在同一周期里,越往右原子序数越大.
【解答】解:(1)上述三种元素中为金属元素的有:铁元素和锌元素;从图中可以知道锌原子为30号元素,所以根据原子的核外电子数=核内质子数=原子序数,可以知道锌原子的核外电子数为30;硒原子得到电子使质子数小于电子数,而电子带负电,所以使硒原子带上了两个单位的负电荷,形成阴离子,缺碘易患甲状腺肿大;故答案为:2;30;阴;甲状腺肿大;
(2)A、元素周期表中,横行表示周期,Y和Z在同一横行,所以位于同一周期里,且Z在Y的右侧,越往右原子序数越大,故A正确;
B、原子核外电子数=原子序数,由于X与Y属于不同的元素,所以原子序数不同,故核外电子数也不同,故B错误;
C、Y和Z在同一横行,所以位于同一周期,故C正确;
故答案为:A、C.
【点评】此题考查了元素的分类和元素周期表的相关知识,是一道综合题目.
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
