江西万载株潭中学2017届高三化学选修五第一章认识有机化合物能力提升检测试题
文档属性
| 名称 | 江西万载株潭中学2017届高三化学选修五第一章认识有机化合物能力提升检测试题 |
|
|
| 格式 | zip | ||
| 文件大小 | 153.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-10-23 00:00:00 | ||
图片预览





文档简介
江西万载株潭中学2017届高三化学选修五第一章认识有机化合物能力提升检测试题
第I卷
选择题
一、选择题(每小题4分,共48分)。
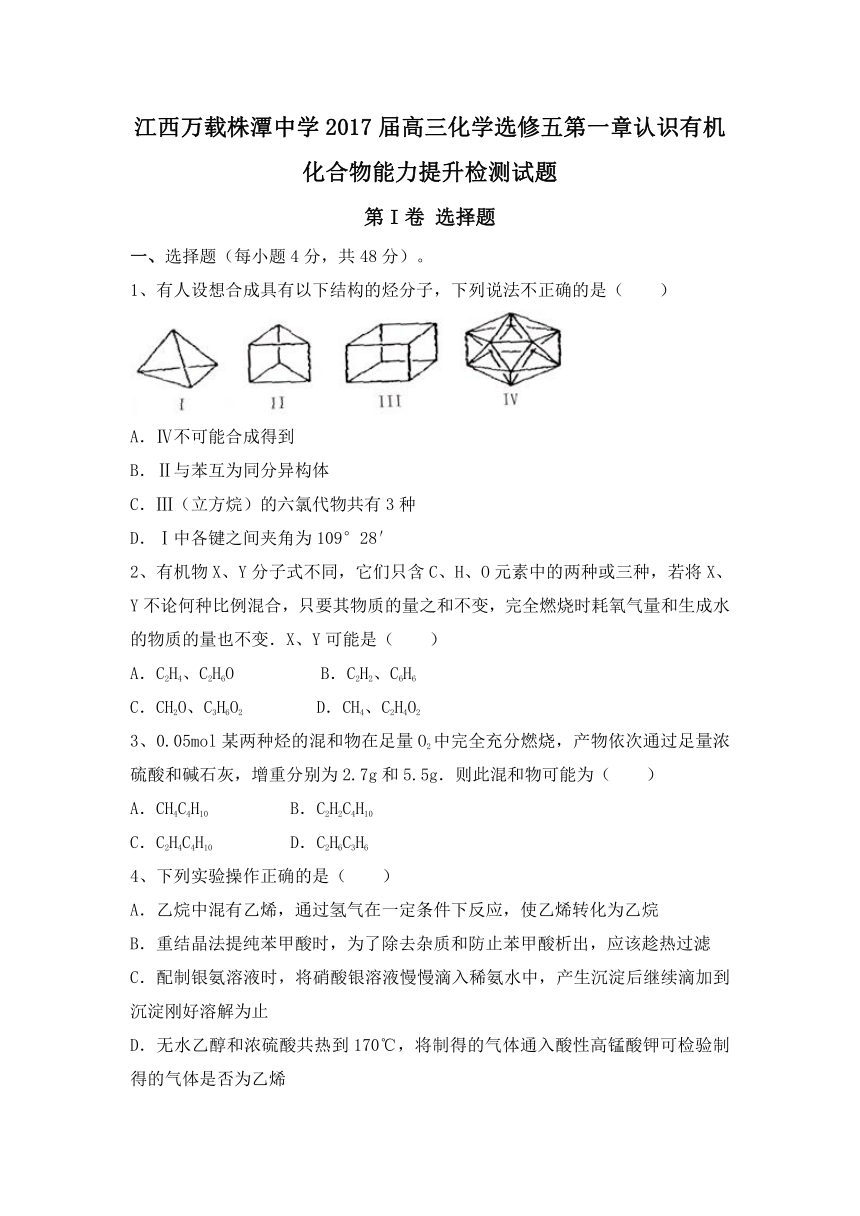
1、有人设想合成具有以下结构的烃分子,下列说法不正确的是( )
A.Ⅳ不可能合成得到
B.Ⅱ与苯互为同分异构体
C.Ⅲ(立方烷)的六氯代物共有3种
D.Ⅰ中各键之间夹角为109°28′
2、有机物X、Y分子式不同,它们只含C、H、O元素中的两种或三种,若将X、Y不论何种比例混合,只要其物质的量之和不变,完全燃烧时耗氧气量和生成水的物质的量也不变.X、Y可能是( )
A.C2H4、C2H6O
B.C2H2、C6H6
C.CH2O、C3H6O2
D.CH4、C2H4O2
3、0.05mol某两种烃的混和物在足量O2中完全充分燃烧,产物依次通过足量浓硫酸和碱石灰,增重分别为2.7g和5.5g.则此混和物可能为( )
A.CH4C4H10
B.C2H2C4H10
C.C2H4C4H10
D.C2H6C3H6
4、下列实验操作正确的是( )
A.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷
B.重结晶法提纯苯甲酸时,为了除去杂质和防止苯甲酸析出,应该趁热过滤
C.配制银氨溶液时,将硝酸银溶液慢慢滴入稀氨水中,产生沉淀后继续滴加到沉淀刚好溶解为止
D.无水乙醇和浓硫酸共热到170℃,将制得的气体通入酸性高锰酸钾可检验制得的气体是否为乙烯
5、下列叙述正确的是( )24
A.和分子组成相差一个﹣CH2﹣,因此是同系物关系M
B.和
均是芳香烃,既是芳香烃又是芳香族化合物T
C.分子式为C4H8的有机物可能存在4个C﹣C单键8
D.分子式为C2H6O的红外光谱图上发现有C﹣H键和C﹣O键的振动吸收,由此可以初步推测:有机物结构简式一定为C2H5﹣OH7
6、下列有机物命名正确的是( )M
A.
2﹣乙基甲烷y
B.CH3CH2CH2OH
1﹣丁醇I
C.
对二甲苯/
D.
2﹣甲基﹣2﹣丙烯N
7、下列关于有机物的说法或表述中不正确的是( )I
A.等质量的乙烷、乙烯、乙炔在氧气中完全燃烧,乙烷消耗的氧气最多3
B.可借助于核磁共振氢谱区分乙醇和二甲醚这两种物质i
C.CH3CH(CH3)CH(CH3)CH(C2H5)CH2CH3的名称:2,3﹣二甲基﹣4﹣乙基己烷h
D.石油裂解是高分子生成小分子的过程B
8、下列说法正确的是( )i
A.按系统命名法,化合物的名称是2,3,5,5﹣四甲基﹣4,4﹣二乙基己烷V
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等V
C.苯和甲苯互为同系物,均能使KMnO4酸性溶液褪色b
D.结构片段的高聚物是由加聚反应形成,其单体分子式为C7H60q
9、下列说法中正确的是( )4
A.CCl4的比例模型示意图为i
B.的名称为2,6﹣二甲基3乙基庚烷A
C.化合物有4种一氯代物=
D.1mol最多能与4molNaOH完全反应=
10、如图是一种分子式为C4H8O2的有机物的红外光谱图,符合条件的有机物有( )
A.2种
B.3种
C.4种
D.5种
11、由一氧化碳、甲烷和乙烷组成的混合气体8.96L(标准状况),在足量氧气中充分燃烧后,生成气体先通过足量浓硫酸,再通过足量氢氧化钠溶液,测知氢氧化钠溶液增重26.4g,则原混合气体中乙烷的物质的量为( )
A.0.1mol
B.大于或等于0.2mol,小于0.3mol
C.0.2mol
D.大于0.1mol小于0.3mol
12、将一定量的乙二醇(分子式为C2H6O2)完全燃烧后的所有产物,全部通入过量的石灰水中,完全被吸收,经过滤得到20g沉淀.滤液的质量比原石灰水的质量减少了(不考虑过滤时液体质量的损失)( )
A.4g
B.5.8g
C.11.2g
D.14.2g
第II卷
非选择题
二、非选择题(共52分)
13、按要求填空
(1)写出
4﹣甲基﹣2﹣乙基﹣1﹣戊烯的结构简式
;
(2)对羟基苯甲酸乙酯
;
(3)
系统名称为
;
(4)同时符合下列四个要求的水杨酸(邻羟基苯甲酸)的同分异构体共有
种.其核磁共振氢谱峰面积比为
.
①含有苯环;
②能发生银镜反应,不能发生水解反应;③在稀NaOH溶液中,1mol该同分异构体能与
2molNaOH发生反应;④只能生成两种一氯代产物.
14、(1)常温下,一种烷烃A和一种单烯烃B组成混和气体,A或B分子最多只含有4个碳原子,且B分子的碳原子数比A分子的多.将1L该混和气体充分燃烧,在同温同压下得到2.5LCO2气体.试推断原混和气体中A和B所有可能的组合及其体积比,并将结果填入下表:
组合编号
A的分子式
B的分子式
A和B的体积比VA:VB
(2)烃C与烃A互为同系物,分子中含有11个C原子,8个甲基,则烃C的系统名称为
,该烃的二氯代物有
种.
15、(1)键线式
表示的分子式
结构简式
名称是
.
(2)含有杂质的工业乙醇的蒸馏装置中,玻璃仪器有酒精灯、蒸馏瓶、
、
、尾接管、锥形瓶
(3)写出丁基的结构简式有
(4)0.1mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6mol,则该烃的分子式为
.若该烃能使溴水褪色,且能在催化剂作用下与H2发生加成反应,生成2,2﹣二甲基丁烷,则此烃属于
烃,结构简式为
,名称是
,该加成反应的化学方程式为
.
16、(1)相同物质的量的①C2H4②C2H6O完全燃烧,消耗氧气物质的量关系为
(填编号,用“>”或“=”表示).
(2)的分子式为
.
(3)在1个分子中,处于同一平面上的原子数最多可能有
个.
(4)系统命名为
.
(5)高聚的单体为
、
.
17、(Ⅰ)某烃A的相对分子质量为84.回答下列问题:
(1)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号)
;
a.C7H12O2
b.C6H14c.C6H14O
d.C7H14O3
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种.A的结构简式为
;
(3)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为
;
(Ⅱ)1mol分子式为CmHn的有机物在氧气中完全燃烧,生成CO2和H2O的物质的量相等,并消耗168L氧气(标况下).该有机化合物的分子式
;
(Ⅲ)某有机物A是烃的含氧衍生物,为测定其组成有如下实验结果:
①在一定温度和压强下将A汽化,其质量是同温、同压下氢气质量的76倍;
②称取7.6g有机物A,在过量氧气中完全燃烧.将反应后的混合气体通过足量浓H2SO4后体积变为10.64L,浓硫酸增重3.6g.再将余下的气体通过盛有足量碱石灰的干燥管,气体体积减少至1.68L(气体体积均在标准状况下测定).确定A的分子式
.
参考答案
1.
D
解:A、分子Ⅳ中碳原子形成5个共价键,所以不可能合成,故A正确;
B、Ⅱ的分子式为C6H6,与苯分子式相同,结构不同,互为同分异构体,故B正确;
C、分子的二氯代物有3种,所二氯取代产物和六氯取代产物种数一样,所以Ⅲ(立方烷)的六氯代物共有3种,故C正确;
D、正四面体空间结构的分子中,化学键的键角是109°28′,但是图示物质是三角锥型的分子,键角不是109°28′,故D错误.
故选D.
2.D
解:A.C2H4、C2H6O含有的H数目不同,物质的量比值不同,生成的水的物质的量不同,故A错误;
B.C2H2、C6H6含有的H数目不同,二者物质的量比值不同,生成的水的物质的量不同,且耗氧量也不同,故B错误.
C.CH2O、C3H6O2含有的H数目不同,二者物质的量比值不同,生成的水的物质的量不同,且耗氧量不同,故C错误;
D.CH4、C2H4O2含有的H数目相同,在分子组成上相差1个“CO2”基团,只要其物质的量之和不变,完全燃烧时耗氧气量和生成水的物质的量也不变,故D正确;
故选:D.
3.D
解:烃完全燃烧生成二氧化碳和水,产物通过足量浓硫酸增重2.7g为水的质量,
所以水的物质的量为=0.15mol;
通过足量碱石灰增重5.5g为二氧化碳质量.
所以二氧化碳的物质的量为=0.125mol.
所以平均分子组成中碳原子数为:=2.5,氢原子数为=6
即平均分子组成为C2.5H6.
A、若CH4和C4H10,由碳原子可知为二者为1:1混合,其平均分子组成中H原子数目为7,由于平均分子组成中含有6个H原子,故A错误;
B、若C2H2和C4H10,由氢原子可知二者为1:1混合,其平均分子组成中C原子数目为3,由于平均分子组成中含有2.5个C原子,故B错误;
C、若C2H4和C4H10,由碳原子可知C2H4和C4H10按3:1混合,由氢原子可知C2H4和C4H10按2:1混合,混合比例不同,故不可能,故C错误;
D、若C2H6和C3H6,由氢原子可知按任意比混合,由碳原子可知为二者为1:1混合,故二者1:1混合,平均分子组成为
C2.5H6,故D正确.
故选:D.
4.B
解:A.乙烷中乙烯的含量未知,不能确定通入氢气的量,易引入杂质,且反应在实验室难以完成,故A错误;
B.趁热过滤,减少苯甲酸的损失,则重结晶法提纯苯甲酸时,为除去杂质和防止苯甲酸析出,应该趁热过滤,故B正确;
C.配制银氨溶液时,氨水不能加入过量,应至沉淀刚好溶解为止,故C错误;
D.无水乙醇和浓硫酸共热至170℃,发生消去反应生成乙烯,乙醇易挥发,乙烯、乙醇均能被酸性高锰酸钾氧化,不能检验,应除去乙醇,再检验乙烯,故D错误.
故选B.
5.C
解:A.中羟基直接与苯环相连,属于酚类,而所以醇类,二者的结构不同,所以二者一定不属于同系物,故A错误;
B.为苯,属于芳香烃,而为环己烷,不属于芳香烃,中含有氧原子,也不属于芳香烃,故B错误;
C.分子式为C4H8的有机物中可能含有一个环,即可能为环烷烃,如环丁烷,分子中含有4个碳氢键,故C正确;
D.分子式为C2H6O的红外光谱图上发现有C﹣H键和C﹣O键的振动吸收,由于二甲醚CH3﹣O﹣CH3中也含有C﹣H键和C﹣O键,无法判断该有机物是否为乙醇,故D错误;
故选C.
6.C
解:A、有机物的名称是2﹣甲基丁烷,故A错误;
B、CH3CH2CH2OH含三个碳原子,它的名称是1﹣丙醇,故B错误;
C、对于结构中含有苯环的,可以根据其相对位置,用“邻”、“间”、“对”进行命名,其名称是对二甲苯,故C正确;
D、含有官能团的有机物命名时,从离官能团最近的碳原子开始编号,即命名为2﹣甲基﹣1﹣丙烯,故D错误.
故选C.
7.D
解:A.等质量的烃燃烧,耗氧量取决于H%,H%越大耗氧量越大,乙烷的含氢量最大,则消耗的氧气的量最多,故A正确;
B.乙醇和二甲醚的氢原子种类不同,则核磁共振氢谱不同,可鉴别,故B正确;
C.CH3CH(CH3)CH(CH3)CH(C2H5)CH2CH3的主链含有6个C原子,含有2个甲基和1个乙基,名称为2,3﹣二甲基﹣4﹣乙基己烷,故C正确;
D.高分子化合物的相对分子质量在10000以上,石油不是高分子化合物,故D错误.
故选D.
8.B
解:A、烷烃命名时,要选最长的碳链为主链,故主链上有6个碳原子,从离支链近的一端给主链上碳原子编号,则在2号碳原子上有2个甲基,在3号碳原子上有1个甲基和1个乙基,在4号和5号碳原子上各有一个甲基,故名称为:2,2,3,4,5﹣五甲基﹣3﹣乙基己烷,故A错误;
B、有机物CxHyOz的耗氧量为(x+y/2﹣z/4),则1mol苯消耗6.5mol氧气,1mol苯甲酸消耗6.5mol氧气,故等物质的量的两者的耗氧量相同,故B正确;
C、苯和甲苯互为同系物,甲苯能被酸性KMnO4氧化成苯甲酸,溶液褪色,但苯与酸性KMnO4不反应,不能使KMnO4酸性溶液褪色,故C错误;
D、此结构片段为酚醛树脂的结构片段,其单体为苯酚和甲醛,故D错误.
故选B.
9.B
解:A.氯原子比碳原子半径大,故A错误;
B.符合命名规则,故B正确;
C.有3种氢原子,有3种一氯代物,故C错误;
D.水解产物中共含有2个酚羟基、1个羧基和碳酸,则0.1
mol的最多能与含5.0
molNaOH的水溶液完全反应,故D错误.
故选B.
10.A
解:由红外光谱图可看出该分子中有不对称CH3﹣和﹣CH2﹣,含有C=O双键,C﹣O﹣C单键,因此该分子中有2个CH3,1个﹣CH2﹣,所以A的结构简式为CH3COOCH2CH3或是CH3CH2COOCH3,故选A.
11.C
解:一氧化碳、甲烷和乙烷组成的混合气体8.96L(标准状况),混合气体的物质的量为:=0.4mol,
浓硫酸吸收水、NaOH溶液吸收二氧化碳,故NaOH溶液增重26.4g为二氧化碳质量,所以二氧化碳的物质的量为:=0.6mol,
所以平均组成中平均碳原子数为:=1.5,
一氧化碳、甲烷分子中都含有一个碳原子,可以看做1个组分,
设CO、甲烷的总物质的量为x,乙烷的物质的量为y,则:=1.5,
解得:x=y,
则原混合气体中乙烷的物质的量为:0.4mol×=0.2mol,
故选C.
12.B
解:n(CO2)=n(CaCO3)==0.2mol,m(CO2)=0.2mol×44g/mol=8.8g,
则n(H2O)=×nn(CO2)=0.3mol,m(H2O)=0.3mol×18g/mol=5.4g,
设反应前溶液的质量为xg,滤液的质量为yg,
根据化学反应遵循质量守和定律,
则有:m(CO2)+m(H2O)+x=m(CaCO3)+y,
即:8.8+5.4+x=20+y,
x﹣y=20﹣8.8﹣5.4=5.8,
故选B.
13.(1).
(2);
(3)2,3﹣二甲基﹣1﹣丁烯;
(4)2;1:2:2:1.
解:(1)4﹣甲基﹣2﹣乙基﹣1﹣戊烯的结构简式为:CH3CH(CH3)CH2C(CH2CH3)=CH2,将碳、氢元素符号省略,只表示分子中键的连接情况,每个拐点或终点均表示有1个碳原子,得到的键线式为:,
故答案为:.
(2)对羟基苯甲酸乙酯,是苯环上对位有羟基,羧基和乙醇发生酯化反应生成酯,结构简式为:,
故答案为:;
(3)
系统命名得到名称2,3﹣二甲基﹣1﹣丁烯,
故答案为:2,3﹣二甲基﹣1﹣丁烯;
(4)可与FeCl3溶液发生显色反应,说明含有酚羟基,能发生银镜反应,不能发生水解反应,说明含有﹣CHO、不含酯基,且含苯环、一氯代物有两种,符合条件的的同分异构体有、,共2种,有机物分子中的等效氢原子种类决定了其核磁共振氢谱总共峰的数目为:1:2:2:1,
故答案为:2;1:2:2:1.
14.(1)
组合编号
A的分子式
B的分子式
A和B的体积比VA:VB
①
CH4
C3H6
1:3
②
CH4
C4H8
1:1
③
C2H6
C3H6
1:1
④
C2H6
C4H8
3:1
(2)
2,2,3,3,4,4﹣六甲基戊烷;
6.
(1)因1升混合气体充分燃烧后生成2.5升CO2,且B分子的碳原子数比A分子的多,混合气体只能由碳原子数小于2.5的烷烃(CH4和C2H6)和碳原子数大于2.5的烯烃(C3H6和C4H8)组成.它们有四种可能的组合:CH4、C3H6;CH4、C4H8;C2H6、C3H6;C2H6、C4H8,
如为CH4、C3H6,则=2.5,VA:VB=1:3,
如为CH4、C4H8,则=2.5,VA:VB=1:1;
如为C2H6、C3H6,则=2.5,VA:VB=1:1;
如为C2H6、C4H8,则=2.5,VA:VB=3:1,
故答案为:
组合编号
A的分子式
B的分子式
A和B的体积比VA:VB
①
CH4
C3H6
1:3
②
CH4
C4H8
1:1
③
C2H6
C3H6
1:1
④
C2H6
C4H8
3:1
(2)烃C与烃A互为同系物,应为烷烃,分子中含有11个C原子,8个甲基,为2,2,3,3,4,4﹣六甲基戊烷,2个氯原子可在相同或不同的碳原子上,如图:,有1、1;2、2;1、4;1、2;2、5;1、3,共6种不同的位置,则有6种同分异构体,
故答案为:2,2,3,3,4,4﹣六甲基戊烷;
6.
15.(1)C6H14;(CH3)2CHCH2CH2CH3;2﹣甲基戊烷;
(2)温度计;冷凝管;
(3)﹣CH2CH2CH2CH3、﹣CH(CH3)CH2CH3、﹣CH2CH(CH3)2、﹣C(CH3)3;
(4)C6H12;单烯;(CH3)3CCH=CH2;3,3﹣二甲基﹣1﹣丁烯;C(CH3)3CH=CH2+H2→C(CH3)3CH2CH3.
(1)分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,结构简式为:(CH3)2CHCH2CH2CH3,命名为:2﹣甲基戊烷,
故答案为:C6H14;(CH3)2CHCH2CH2CH3;2﹣甲基戊烷;
(2)含有杂质的工业乙醇的蒸馏装置中,需要使用的玻璃仪器为:酒精灯、蒸馏瓶、温度计、冷凝管、尾接管、锥形瓶,还缺少温度计和冷凝管,
故答案为:温度计;冷凝管;
(3)丁烷含有正丁烷和异丁烷两种同分异构体,正丁烷去掉一个H后剩下的部分可为:﹣CH2CH2CH2CH3或﹣CH(CH3)CH2CH3;
异丁烷去掉一个H后剩下的部分可为:﹣CH2CH(CH3)2或﹣C(CH3)3,
故答案为:﹣CH2CH2CH2CH3、﹣CH(CH3)CH2CH3、﹣CH2CH(CH3)2、﹣C(CH3)3;
(4)0.1mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6mol,根据原子守恒可知,该烃的分子中N(C)==6,N(H)==12,故该烃的分子式为C6H12;
该烃能使溴水褪色,说明分子中含有1个C=C键,该烃属于烯烃,在催化剂作用下与H2加成生成2,2﹣二甲基丁烷(),相邻两个碳原子都含有H原子为C=C双键位置,该烃的结构简式为:(CH3)3CCH=CH2,名称为3,3﹣二甲基﹣1﹣丁烯;
与氢气发生加成反应的化学方程式为:C(CH3)3CH=CH2+H2→C(CH3)3CH2CH3,
故答案为:C6H12;单烯;(CH3)3CCH=CH2;3,3﹣二甲基﹣1﹣丁烯;C(CH3)3CH=CH2+H2→C(CH3)3CH2CH3.
16.(1)=;
(2)C12H16O;
(3)16;
(4)4,4﹣二甲基﹣2﹣戊醇;
(5)CH2=CH2;CH3﹣CH=CH2.
(1)相同物质的量的①C2H4②C2H6O完全燃烧,其中C2H6O可以写成C2H4(H2O),所以耗氧的量与C2H4的耗氧的量相等,故答案为:=;
(2)的分子式中有12个碳原子、一个氧原子,不饱和度为5,所以氢原子数为12×2+2﹣5×2=16,所以分子式为C12H16O,
故答案为:C12H16O;
(3)当苯和双键所在的平面共平面时,处于同一平面上的原子数最多,所以16个原子共平面,故答案为:16;
(4)﹣OH在2号位置,主链为5,有两个甲基,有机物名称为4,4﹣二甲基﹣2﹣戊醇,故答案为:4,4﹣二甲基﹣2﹣戊醇;
(5)为加聚反应产物,将中括号去掉,按照“见双键,四个碳,无双键,两个碳”划线断开,然后将半键闭合可得该有机物的单体分别为:CH3﹣CH=CH2、CH2=CH2,
故答案为:CH2=CH2;CH3﹣CH=CH2.
17.(Ⅰ)(1)b;(2);(3).(Ⅱ)C5H10;(Ⅲ)C8H8O3.
(Ⅰ)烃A的相对分子质量为84,=6,则该烃可能为烯烃或环烷烃,分子式应为C6H12,
(1)总物质的量一定,充分燃烧消耗氧气的量不相等,则1molC6H12消耗氧气为x+=6+=9mol,
a.1molC7H12O2消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故a不选;
b.1molC6H14消耗氧气为9.5mol,总物质的量一定,充分燃烧消耗氧气的量不相等,故b选;
c.1molC6H14O消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故c不选;
d.1molC7H14O3消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故d不选;
故答案为:b;
(2)烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种,则结构对称,只含一种H,即含4个甲基,A为,
故答案为:;
(3)A不能使溴水褪色,且其一氯代物只有一种,则不含C=C,只有一种H,应为环烃,其结构简式为,故答案为:.
(Ⅱ)生成CO2和H2O的物质的量相等,则该烃的最简式为CH2,令该烃的组成为CxH2x,根据CxH2x+O2xCO2+xH2O可知,1molCxH2x消耗氧气的物质的量为mol,故mol×22.4L/mol=168L,解得x=5,故该烃为C5H10,
故答案为:C5H10;
(Ⅲ)Mr(A)=76×Mr(H2)=76×2=152,
浓硫酸增重3.6g,则反应中生成的水的质量是3.6g,
n(H)==0.4mol,
再将余下的气体通过盛有足量碱石灰的干燥管,气体体积减少至1.68L(气体体积均在标准状况下测定).所以反应中生成的CO2是10.64L﹣1.68L=8.96L,
n(C)==0.4mol,
则根据原子守恒可知,
n(O)==0.15mol,
n(C):n(H):n(O)=0.4mol:0.4mol:0.15mol=8:8:3,
A的实验式是C8H8O3,式量为152,即实验式就是分子式,即分子式为C8H8O3,
故答案为:C8H8O3.
第I卷
选择题
一、选择题(每小题4分,共48分)。
1、有人设想合成具有以下结构的烃分子,下列说法不正确的是( )
A.Ⅳ不可能合成得到
B.Ⅱ与苯互为同分异构体
C.Ⅲ(立方烷)的六氯代物共有3种
D.Ⅰ中各键之间夹角为109°28′
2、有机物X、Y分子式不同,它们只含C、H、O元素中的两种或三种,若将X、Y不论何种比例混合,只要其物质的量之和不变,完全燃烧时耗氧气量和生成水的物质的量也不变.X、Y可能是( )
A.C2H4、C2H6O
B.C2H2、C6H6
C.CH2O、C3H6O2
D.CH4、C2H4O2
3、0.05mol某两种烃的混和物在足量O2中完全充分燃烧,产物依次通过足量浓硫酸和碱石灰,增重分别为2.7g和5.5g.则此混和物可能为( )
A.CH4C4H10
B.C2H2C4H10
C.C2H4C4H10
D.C2H6C3H6
4、下列实验操作正确的是( )
A.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷
B.重结晶法提纯苯甲酸时,为了除去杂质和防止苯甲酸析出,应该趁热过滤
C.配制银氨溶液时,将硝酸银溶液慢慢滴入稀氨水中,产生沉淀后继续滴加到沉淀刚好溶解为止
D.无水乙醇和浓硫酸共热到170℃,将制得的气体通入酸性高锰酸钾可检验制得的气体是否为乙烯
5、下列叙述正确的是( )24
A.和分子组成相差一个﹣CH2﹣,因此是同系物关系M
B.和
均是芳香烃,既是芳香烃又是芳香族化合物T
C.分子式为C4H8的有机物可能存在4个C﹣C单键8
D.分子式为C2H6O的红外光谱图上发现有C﹣H键和C﹣O键的振动吸收,由此可以初步推测:有机物结构简式一定为C2H5﹣OH7
6、下列有机物命名正确的是( )M
A.
2﹣乙基甲烷y
B.CH3CH2CH2OH
1﹣丁醇I
C.
对二甲苯/
D.
2﹣甲基﹣2﹣丙烯N
7、下列关于有机物的说法或表述中不正确的是( )I
A.等质量的乙烷、乙烯、乙炔在氧气中完全燃烧,乙烷消耗的氧气最多3
B.可借助于核磁共振氢谱区分乙醇和二甲醚这两种物质i
C.CH3CH(CH3)CH(CH3)CH(C2H5)CH2CH3的名称:2,3﹣二甲基﹣4﹣乙基己烷h
D.石油裂解是高分子生成小分子的过程B
8、下列说法正确的是( )i
A.按系统命名法,化合物的名称是2,3,5,5﹣四甲基﹣4,4﹣二乙基己烷V
B.等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等V
C.苯和甲苯互为同系物,均能使KMnO4酸性溶液褪色b
D.结构片段的高聚物是由加聚反应形成,其单体分子式为C7H60q
9、下列说法中正确的是( )4
A.CCl4的比例模型示意图为i
B.的名称为2,6﹣二甲基3乙基庚烷A
C.化合物有4种一氯代物=
D.1mol最多能与4molNaOH完全反应=
10、如图是一种分子式为C4H8O2的有机物的红外光谱图,符合条件的有机物有( )
A.2种
B.3种
C.4种
D.5种
11、由一氧化碳、甲烷和乙烷组成的混合气体8.96L(标准状况),在足量氧气中充分燃烧后,生成气体先通过足量浓硫酸,再通过足量氢氧化钠溶液,测知氢氧化钠溶液增重26.4g,则原混合气体中乙烷的物质的量为( )
A.0.1mol
B.大于或等于0.2mol,小于0.3mol
C.0.2mol
D.大于0.1mol小于0.3mol
12、将一定量的乙二醇(分子式为C2H6O2)完全燃烧后的所有产物,全部通入过量的石灰水中,完全被吸收,经过滤得到20g沉淀.滤液的质量比原石灰水的质量减少了(不考虑过滤时液体质量的损失)( )
A.4g
B.5.8g
C.11.2g
D.14.2g
第II卷
非选择题
二、非选择题(共52分)
13、按要求填空
(1)写出
4﹣甲基﹣2﹣乙基﹣1﹣戊烯的结构简式
;
(2)对羟基苯甲酸乙酯
;
(3)
系统名称为
;
(4)同时符合下列四个要求的水杨酸(邻羟基苯甲酸)的同分异构体共有
种.其核磁共振氢谱峰面积比为
.
①含有苯环;
②能发生银镜反应,不能发生水解反应;③在稀NaOH溶液中,1mol该同分异构体能与
2molNaOH发生反应;④只能生成两种一氯代产物.
14、(1)常温下,一种烷烃A和一种单烯烃B组成混和气体,A或B分子最多只含有4个碳原子,且B分子的碳原子数比A分子的多.将1L该混和气体充分燃烧,在同温同压下得到2.5LCO2气体.试推断原混和气体中A和B所有可能的组合及其体积比,并将结果填入下表:
组合编号
A的分子式
B的分子式
A和B的体积比VA:VB
(2)烃C与烃A互为同系物,分子中含有11个C原子,8个甲基,则烃C的系统名称为
,该烃的二氯代物有
种.
15、(1)键线式
表示的分子式
结构简式
名称是
.
(2)含有杂质的工业乙醇的蒸馏装置中,玻璃仪器有酒精灯、蒸馏瓶、
、
、尾接管、锥形瓶
(3)写出丁基的结构简式有
(4)0.1mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6mol,则该烃的分子式为
.若该烃能使溴水褪色,且能在催化剂作用下与H2发生加成反应,生成2,2﹣二甲基丁烷,则此烃属于
烃,结构简式为
,名称是
,该加成反应的化学方程式为
.
16、(1)相同物质的量的①C2H4②C2H6O完全燃烧,消耗氧气物质的量关系为
(填编号,用“>”或“=”表示).
(2)的分子式为
.
(3)在1个分子中,处于同一平面上的原子数最多可能有
个.
(4)系统命名为
.
(5)高聚的单体为
、
.
17、(Ⅰ)某烃A的相对分子质量为84.回答下列问题:
(1)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号)
;
a.C7H12O2
b.C6H14c.C6H14O
d.C7H14O3
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种.A的结构简式为
;
(3)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为
;
(Ⅱ)1mol分子式为CmHn的有机物在氧气中完全燃烧,生成CO2和H2O的物质的量相等,并消耗168L氧气(标况下).该有机化合物的分子式
;
(Ⅲ)某有机物A是烃的含氧衍生物,为测定其组成有如下实验结果:
①在一定温度和压强下将A汽化,其质量是同温、同压下氢气质量的76倍;
②称取7.6g有机物A,在过量氧气中完全燃烧.将反应后的混合气体通过足量浓H2SO4后体积变为10.64L,浓硫酸增重3.6g.再将余下的气体通过盛有足量碱石灰的干燥管,气体体积减少至1.68L(气体体积均在标准状况下测定).确定A的分子式
.
参考答案
1.
D
解:A、分子Ⅳ中碳原子形成5个共价键,所以不可能合成,故A正确;
B、Ⅱ的分子式为C6H6,与苯分子式相同,结构不同,互为同分异构体,故B正确;
C、分子的二氯代物有3种,所二氯取代产物和六氯取代产物种数一样,所以Ⅲ(立方烷)的六氯代物共有3种,故C正确;
D、正四面体空间结构的分子中,化学键的键角是109°28′,但是图示物质是三角锥型的分子,键角不是109°28′,故D错误.
故选D.
2.D
解:A.C2H4、C2H6O含有的H数目不同,物质的量比值不同,生成的水的物质的量不同,故A错误;
B.C2H2、C6H6含有的H数目不同,二者物质的量比值不同,生成的水的物质的量不同,且耗氧量也不同,故B错误.
C.CH2O、C3H6O2含有的H数目不同,二者物质的量比值不同,生成的水的物质的量不同,且耗氧量不同,故C错误;
D.CH4、C2H4O2含有的H数目相同,在分子组成上相差1个“CO2”基团,只要其物质的量之和不变,完全燃烧时耗氧气量和生成水的物质的量也不变,故D正确;
故选:D.
3.D
解:烃完全燃烧生成二氧化碳和水,产物通过足量浓硫酸增重2.7g为水的质量,
所以水的物质的量为=0.15mol;
通过足量碱石灰增重5.5g为二氧化碳质量.
所以二氧化碳的物质的量为=0.125mol.
所以平均分子组成中碳原子数为:=2.5,氢原子数为=6
即平均分子组成为C2.5H6.
A、若CH4和C4H10,由碳原子可知为二者为1:1混合,其平均分子组成中H原子数目为7,由于平均分子组成中含有6个H原子,故A错误;
B、若C2H2和C4H10,由氢原子可知二者为1:1混合,其平均分子组成中C原子数目为3,由于平均分子组成中含有2.5个C原子,故B错误;
C、若C2H4和C4H10,由碳原子可知C2H4和C4H10按3:1混合,由氢原子可知C2H4和C4H10按2:1混合,混合比例不同,故不可能,故C错误;
D、若C2H6和C3H6,由氢原子可知按任意比混合,由碳原子可知为二者为1:1混合,故二者1:1混合,平均分子组成为
C2.5H6,故D正确.
故选:D.
4.B
解:A.乙烷中乙烯的含量未知,不能确定通入氢气的量,易引入杂质,且反应在实验室难以完成,故A错误;
B.趁热过滤,减少苯甲酸的损失,则重结晶法提纯苯甲酸时,为除去杂质和防止苯甲酸析出,应该趁热过滤,故B正确;
C.配制银氨溶液时,氨水不能加入过量,应至沉淀刚好溶解为止,故C错误;
D.无水乙醇和浓硫酸共热至170℃,发生消去反应生成乙烯,乙醇易挥发,乙烯、乙醇均能被酸性高锰酸钾氧化,不能检验,应除去乙醇,再检验乙烯,故D错误.
故选B.
5.C
解:A.中羟基直接与苯环相连,属于酚类,而所以醇类,二者的结构不同,所以二者一定不属于同系物,故A错误;
B.为苯,属于芳香烃,而为环己烷,不属于芳香烃,中含有氧原子,也不属于芳香烃,故B错误;
C.分子式为C4H8的有机物中可能含有一个环,即可能为环烷烃,如环丁烷,分子中含有4个碳氢键,故C正确;
D.分子式为C2H6O的红外光谱图上发现有C﹣H键和C﹣O键的振动吸收,由于二甲醚CH3﹣O﹣CH3中也含有C﹣H键和C﹣O键,无法判断该有机物是否为乙醇,故D错误;
故选C.
6.C
解:A、有机物的名称是2﹣甲基丁烷,故A错误;
B、CH3CH2CH2OH含三个碳原子,它的名称是1﹣丙醇,故B错误;
C、对于结构中含有苯环的,可以根据其相对位置,用“邻”、“间”、“对”进行命名,其名称是对二甲苯,故C正确;
D、含有官能团的有机物命名时,从离官能团最近的碳原子开始编号,即命名为2﹣甲基﹣1﹣丙烯,故D错误.
故选C.
7.D
解:A.等质量的烃燃烧,耗氧量取决于H%,H%越大耗氧量越大,乙烷的含氢量最大,则消耗的氧气的量最多,故A正确;
B.乙醇和二甲醚的氢原子种类不同,则核磁共振氢谱不同,可鉴别,故B正确;
C.CH3CH(CH3)CH(CH3)CH(C2H5)CH2CH3的主链含有6个C原子,含有2个甲基和1个乙基,名称为2,3﹣二甲基﹣4﹣乙基己烷,故C正确;
D.高分子化合物的相对分子质量在10000以上,石油不是高分子化合物,故D错误.
故选D.
8.B
解:A、烷烃命名时,要选最长的碳链为主链,故主链上有6个碳原子,从离支链近的一端给主链上碳原子编号,则在2号碳原子上有2个甲基,在3号碳原子上有1个甲基和1个乙基,在4号和5号碳原子上各有一个甲基,故名称为:2,2,3,4,5﹣五甲基﹣3﹣乙基己烷,故A错误;
B、有机物CxHyOz的耗氧量为(x+y/2﹣z/4),则1mol苯消耗6.5mol氧气,1mol苯甲酸消耗6.5mol氧气,故等物质的量的两者的耗氧量相同,故B正确;
C、苯和甲苯互为同系物,甲苯能被酸性KMnO4氧化成苯甲酸,溶液褪色,但苯与酸性KMnO4不反应,不能使KMnO4酸性溶液褪色,故C错误;
D、此结构片段为酚醛树脂的结构片段,其单体为苯酚和甲醛,故D错误.
故选B.
9.B
解:A.氯原子比碳原子半径大,故A错误;
B.符合命名规则,故B正确;
C.有3种氢原子,有3种一氯代物,故C错误;
D.水解产物中共含有2个酚羟基、1个羧基和碳酸,则0.1
mol的最多能与含5.0
molNaOH的水溶液完全反应,故D错误.
故选B.
10.A
解:由红外光谱图可看出该分子中有不对称CH3﹣和﹣CH2﹣,含有C=O双键,C﹣O﹣C单键,因此该分子中有2个CH3,1个﹣CH2﹣,所以A的结构简式为CH3COOCH2CH3或是CH3CH2COOCH3,故选A.
11.C
解:一氧化碳、甲烷和乙烷组成的混合气体8.96L(标准状况),混合气体的物质的量为:=0.4mol,
浓硫酸吸收水、NaOH溶液吸收二氧化碳,故NaOH溶液增重26.4g为二氧化碳质量,所以二氧化碳的物质的量为:=0.6mol,
所以平均组成中平均碳原子数为:=1.5,
一氧化碳、甲烷分子中都含有一个碳原子,可以看做1个组分,
设CO、甲烷的总物质的量为x,乙烷的物质的量为y,则:=1.5,
解得:x=y,
则原混合气体中乙烷的物质的量为:0.4mol×=0.2mol,
故选C.
12.B
解:n(CO2)=n(CaCO3)==0.2mol,m(CO2)=0.2mol×44g/mol=8.8g,
则n(H2O)=×nn(CO2)=0.3mol,m(H2O)=0.3mol×18g/mol=5.4g,
设反应前溶液的质量为xg,滤液的质量为yg,
根据化学反应遵循质量守和定律,
则有:m(CO2)+m(H2O)+x=m(CaCO3)+y,
即:8.8+5.4+x=20+y,
x﹣y=20﹣8.8﹣5.4=5.8,
故选B.
13.(1).
(2);
(3)2,3﹣二甲基﹣1﹣丁烯;
(4)2;1:2:2:1.
解:(1)4﹣甲基﹣2﹣乙基﹣1﹣戊烯的结构简式为:CH3CH(CH3)CH2C(CH2CH3)=CH2,将碳、氢元素符号省略,只表示分子中键的连接情况,每个拐点或终点均表示有1个碳原子,得到的键线式为:,
故答案为:.
(2)对羟基苯甲酸乙酯,是苯环上对位有羟基,羧基和乙醇发生酯化反应生成酯,结构简式为:,
故答案为:;
(3)
系统命名得到名称2,3﹣二甲基﹣1﹣丁烯,
故答案为:2,3﹣二甲基﹣1﹣丁烯;
(4)可与FeCl3溶液发生显色反应,说明含有酚羟基,能发生银镜反应,不能发生水解反应,说明含有﹣CHO、不含酯基,且含苯环、一氯代物有两种,符合条件的的同分异构体有、,共2种,有机物分子中的等效氢原子种类决定了其核磁共振氢谱总共峰的数目为:1:2:2:1,
故答案为:2;1:2:2:1.
14.(1)
组合编号
A的分子式
B的分子式
A和B的体积比VA:VB
①
CH4
C3H6
1:3
②
CH4
C4H8
1:1
③
C2H6
C3H6
1:1
④
C2H6
C4H8
3:1
(2)
2,2,3,3,4,4﹣六甲基戊烷;
6.
(1)因1升混合气体充分燃烧后生成2.5升CO2,且B分子的碳原子数比A分子的多,混合气体只能由碳原子数小于2.5的烷烃(CH4和C2H6)和碳原子数大于2.5的烯烃(C3H6和C4H8)组成.它们有四种可能的组合:CH4、C3H6;CH4、C4H8;C2H6、C3H6;C2H6、C4H8,
如为CH4、C3H6,则=2.5,VA:VB=1:3,
如为CH4、C4H8,则=2.5,VA:VB=1:1;
如为C2H6、C3H6,则=2.5,VA:VB=1:1;
如为C2H6、C4H8,则=2.5,VA:VB=3:1,
故答案为:
组合编号
A的分子式
B的分子式
A和B的体积比VA:VB
①
CH4
C3H6
1:3
②
CH4
C4H8
1:1
③
C2H6
C3H6
1:1
④
C2H6
C4H8
3:1
(2)烃C与烃A互为同系物,应为烷烃,分子中含有11个C原子,8个甲基,为2,2,3,3,4,4﹣六甲基戊烷,2个氯原子可在相同或不同的碳原子上,如图:,有1、1;2、2;1、4;1、2;2、5;1、3,共6种不同的位置,则有6种同分异构体,
故答案为:2,2,3,3,4,4﹣六甲基戊烷;
6.
15.(1)C6H14;(CH3)2CHCH2CH2CH3;2﹣甲基戊烷;
(2)温度计;冷凝管;
(3)﹣CH2CH2CH2CH3、﹣CH(CH3)CH2CH3、﹣CH2CH(CH3)2、﹣C(CH3)3;
(4)C6H12;单烯;(CH3)3CCH=CH2;3,3﹣二甲基﹣1﹣丁烯;C(CH3)3CH=CH2+H2→C(CH3)3CH2CH3.
(1)分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,结构简式为:(CH3)2CHCH2CH2CH3,命名为:2﹣甲基戊烷,
故答案为:C6H14;(CH3)2CHCH2CH2CH3;2﹣甲基戊烷;
(2)含有杂质的工业乙醇的蒸馏装置中,需要使用的玻璃仪器为:酒精灯、蒸馏瓶、温度计、冷凝管、尾接管、锥形瓶,还缺少温度计和冷凝管,
故答案为:温度计;冷凝管;
(3)丁烷含有正丁烷和异丁烷两种同分异构体,正丁烷去掉一个H后剩下的部分可为:﹣CH2CH2CH2CH3或﹣CH(CH3)CH2CH3;
异丁烷去掉一个H后剩下的部分可为:﹣CH2CH(CH3)2或﹣C(CH3)3,
故答案为:﹣CH2CH2CH2CH3、﹣CH(CH3)CH2CH3、﹣CH2CH(CH3)2、﹣C(CH3)3;
(4)0.1mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6mol,根据原子守恒可知,该烃的分子中N(C)==6,N(H)==12,故该烃的分子式为C6H12;
该烃能使溴水褪色,说明分子中含有1个C=C键,该烃属于烯烃,在催化剂作用下与H2加成生成2,2﹣二甲基丁烷(),相邻两个碳原子都含有H原子为C=C双键位置,该烃的结构简式为:(CH3)3CCH=CH2,名称为3,3﹣二甲基﹣1﹣丁烯;
与氢气发生加成反应的化学方程式为:C(CH3)3CH=CH2+H2→C(CH3)3CH2CH3,
故答案为:C6H12;单烯;(CH3)3CCH=CH2;3,3﹣二甲基﹣1﹣丁烯;C(CH3)3CH=CH2+H2→C(CH3)3CH2CH3.
16.(1)=;
(2)C12H16O;
(3)16;
(4)4,4﹣二甲基﹣2﹣戊醇;
(5)CH2=CH2;CH3﹣CH=CH2.
(1)相同物质的量的①C2H4②C2H6O完全燃烧,其中C2H6O可以写成C2H4(H2O),所以耗氧的量与C2H4的耗氧的量相等,故答案为:=;
(2)的分子式中有12个碳原子、一个氧原子,不饱和度为5,所以氢原子数为12×2+2﹣5×2=16,所以分子式为C12H16O,
故答案为:C12H16O;
(3)当苯和双键所在的平面共平面时,处于同一平面上的原子数最多,所以16个原子共平面,故答案为:16;
(4)﹣OH在2号位置,主链为5,有两个甲基,有机物名称为4,4﹣二甲基﹣2﹣戊醇,故答案为:4,4﹣二甲基﹣2﹣戊醇;
(5)为加聚反应产物,将中括号去掉,按照“见双键,四个碳,无双键,两个碳”划线断开,然后将半键闭合可得该有机物的单体分别为:CH3﹣CH=CH2、CH2=CH2,
故答案为:CH2=CH2;CH3﹣CH=CH2.
17.(Ⅰ)(1)b;(2);(3).(Ⅱ)C5H10;(Ⅲ)C8H8O3.
(Ⅰ)烃A的相对分子质量为84,=6,则该烃可能为烯烃或环烷烃,分子式应为C6H12,
(1)总物质的量一定,充分燃烧消耗氧气的量不相等,则1molC6H12消耗氧气为x+=6+=9mol,
a.1molC7H12O2消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故a不选;
b.1molC6H14消耗氧气为9.5mol,总物质的量一定,充分燃烧消耗氧气的量不相等,故b选;
c.1molC6H14O消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故c不选;
d.1molC7H14O3消耗氧气为9mol,总物质的量一定,充分燃烧消耗氧气的量相等,故d不选;
故答案为:b;
(2)烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种,则结构对称,只含一种H,即含4个甲基,A为,
故答案为:;
(3)A不能使溴水褪色,且其一氯代物只有一种,则不含C=C,只有一种H,应为环烃,其结构简式为,故答案为:.
(Ⅱ)生成CO2和H2O的物质的量相等,则该烃的最简式为CH2,令该烃的组成为CxH2x,根据CxH2x+O2xCO2+xH2O可知,1molCxH2x消耗氧气的物质的量为mol,故mol×22.4L/mol=168L,解得x=5,故该烃为C5H10,
故答案为:C5H10;
(Ⅲ)Mr(A)=76×Mr(H2)=76×2=152,
浓硫酸增重3.6g,则反应中生成的水的质量是3.6g,
n(H)==0.4mol,
再将余下的气体通过盛有足量碱石灰的干燥管,气体体积减少至1.68L(气体体积均在标准状况下测定).所以反应中生成的CO2是10.64L﹣1.68L=8.96L,
n(C)==0.4mol,
则根据原子守恒可知,
n(O)==0.15mol,
n(C):n(H):n(O)=0.4mol:0.4mol:0.15mol=8:8:3,
A的实验式是C8H8O3,式量为152,即实验式就是分子式,即分子式为C8H8O3,
故答案为:C8H8O3.
