人教版化学必修一课件:4.3硫和氮的氧化物(共18张PPT)
文档属性
| 名称 | 人教版化学必修一课件:4.3硫和氮的氧化物(共18张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 62.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-10-24 07:15:00 | ||
图片预览




文档简介
课件18张PPT。目前计入我国空气污染指数的项目暂定为哪三样?可吸入颗粒物、二氧化硫、氮的氧化物第三节 硫和氮的氧化物一、硫1、在自然界的存在形态化合态:地壳的岩石中游离态:火山口附近硫铁矿:FeS2黄铜矿:CuFeS2石膏:CaSO4.2H2O芒硝:Na2SO4.10H2O2、硫单质:黄色晶体、质脆、易研磨成粉末
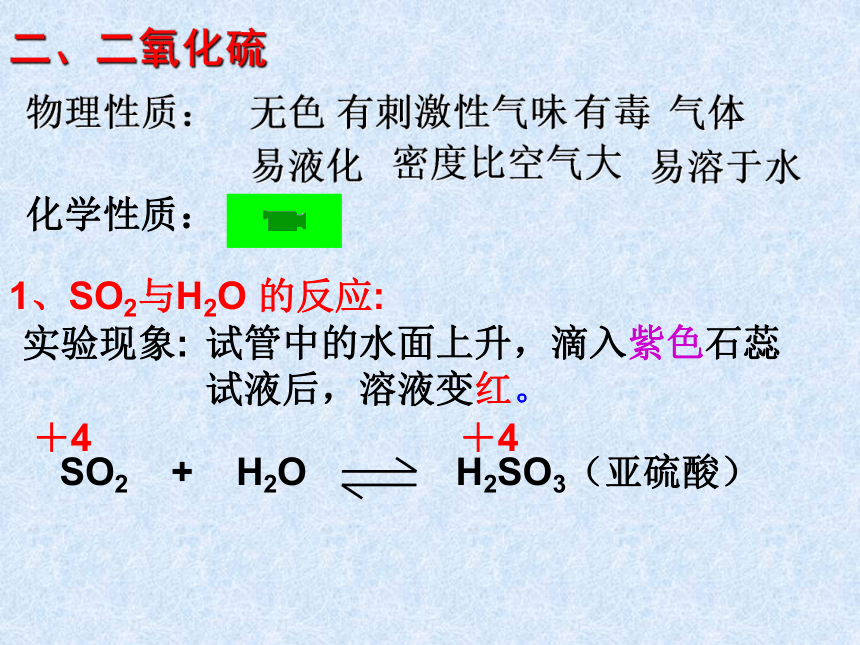
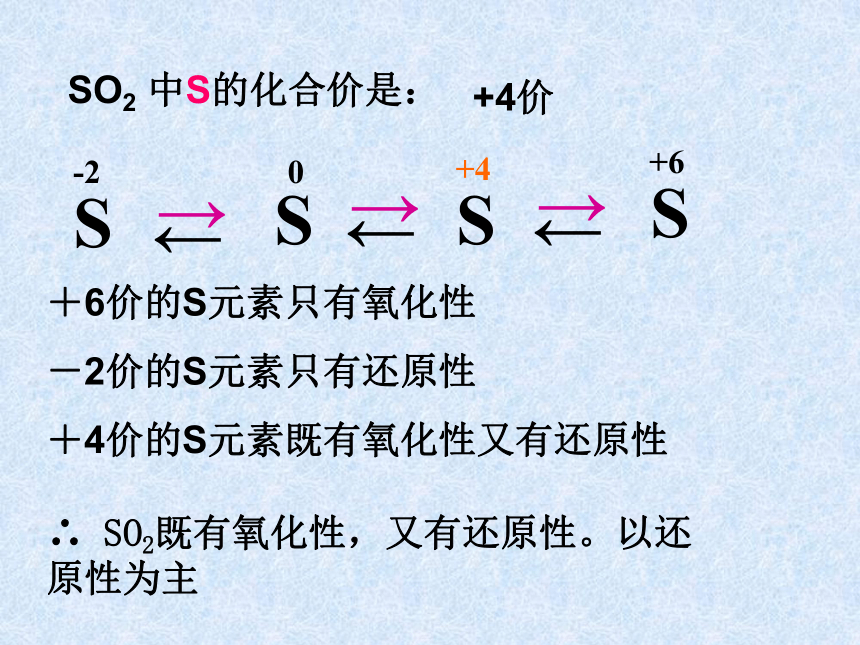
不溶于水,微溶于酒精,易溶于二硫化碳蛋白质明亮的蓝紫色微弱的淡蓝色3、硫在空气中燃烧发出 火焰,在纯净的氧气中燃烧发出 火焰,生成一种刺激性气味的气体是 ,化学方程式为二、二氧化硫物理性质:气体无色有刺激性气味有毒易液化密度比空气大易溶于水化学性质:1、SO2与H2O 的反应:实验现象:试管中的水面上升,滴入紫色石蕊试液后,溶液变红。SO2 + H2O H2SO3(亚硫酸)+4+4SO2 中S的化合价是:∴ SO2既有氧化性,又有还原性。以还原性为主+4价+6价的S元素只有氧化性
-2价的S元素只有还原性
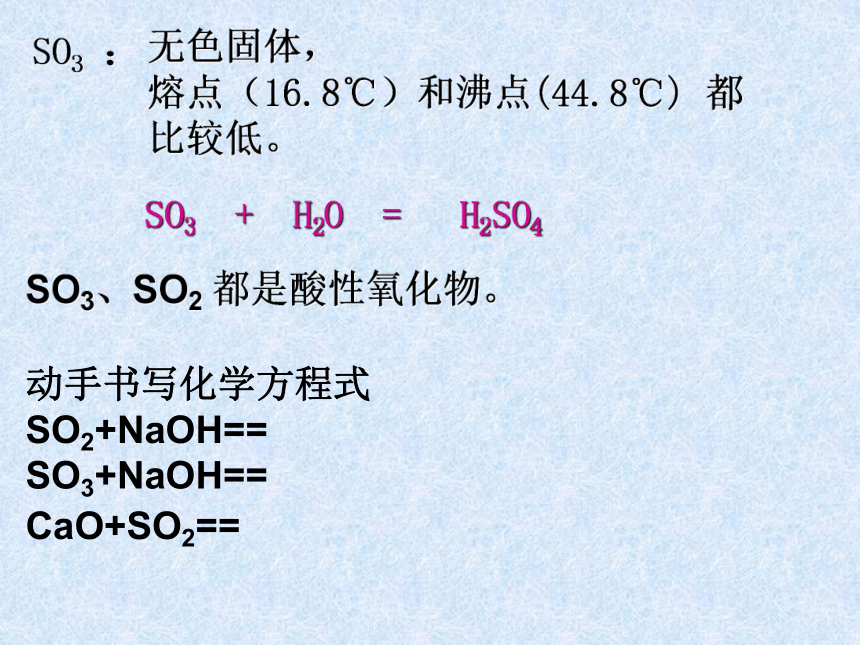
+4价的S元素既有氧化性又有还原性2、还原性 与O2的反应:疑问:通常情况下SO2与O2能否大量共存?思考:已知亚硫酸溶液、亚硫酸钠粉末暴露在空气中容易变质,请写出其化学方程式? 2 H2SO3+O2== 2H2SO42Na2SO3+O2==2Na2SO4+4+6无色固体, 熔点(16.8℃)和沸点(44.8℃) 都比较低。 SO3 + H2O = H2SO4 SO3 :动手书写化学方程式
SO2+NaOH==
SO3+NaOH==SO3、SO2 都是酸性氧化物。CaO+SO2==3、SO2的漂白性:实验现象:品红溶液褪色 加热后,又恢复原来的颜色。该实验说明了什么问题?结论:SO2具有漂白性SO2的漂白原理是什么?与HClO、Na2O2、活性碳是否相同?1.下列叙述中,正确的是( ) A. SO2在空气中易被氧化为SO3 B. 在常温下, SO2的气体摩尔 体积是22.4L C. SO2 与SO3都能与水剧烈反应 D. SO2可用于漂白纸浆, SO3不能。练习:D2、在下列变化中,
不属于化学变化的是( )
A、SO2使品红溶液褪色
B、氯水使有色布条褪色
C、活性炭使红墨水褪色
D、O3使某些染料褪色C3、下列说法正确的是( )
A、SO2能使酸性KMnO4溶液褪色
B、可以用澄清石灰水鉴别SO2与CO2
C、硫粉在过量的纯氧中燃烧可以生成SO3
D、少量的SO2通入浓的CaCl2溶液能生成白色沉淀N2O、NO、N2O3、NO2、N2O4、N2O5氮的氧化物:分析氮元素的化合价-3 0 +1 +2 +3 +4 +4 +5无色,无味,有毒气体红棕色,刺激性气味,有毒气体不溶于水易 溶于水不与水反应3NO2+H2O=2HNO3+NO遇空气立即变红2NO+O2==2NO2遇空气不反应N2+O2 2NO(无色)三、一氧化氮与二氧化氮+2+4思考与交流:
1、一装满二氧化氮的试管倒置在水中一段时间,可观察到的现象是___________。2、科学探究:现给你一试管二氧化氮气体,其他药品和仪器自选,请你设计实验步骤,尽可能使二氧化氮被水吸收。见教材P92将一支充满NO2的试管倒放在盛有水的水槽中红棕色气体逐渐消失,水位上升到整个试管的2/33NO2+H2O=2HNO3+NO制取少量氧气2KClO3==2KCl+3O2↑将氧气慢慢通入倒放的试管中无色气体变为红棕色,又变为无色气体,液面不断上升,直至充满2NO+O2==2NO23、通入多少氧气时,正好充满整个试管?1、正常雨水pH应在什么范围? 2、形成酸雨的主要原因? 3、空气二氧化硫的主要来源?四、二氧化硫和二氧化氮的污染阅读教材后探讨:约为5.6化石燃料的燃烧(煤、石油)含硫矿石的冶炼制硫酸、磷肥、纸浆等工业废气三、一氧化氮:NO无色,无味,有毒气体不溶于水1、物理性质:2、化学性质:遇空气立即变红2NO+O2==2NO23、自然界的形成:N2+O2 2NO(无色)NO:
,,很不稳定。2NO+O2=2NO2
NO2:
红棕色,刺激性气体,有毒,易 溶于水,溶于水时,生成HNO3和NO
3NO2+H2O=2HNO3+NO
(NO2不是HNO3的酸酐,
分析电子转移, 氧化剂和还原剂的比)
B:与氧气反应
N2+O2 2NO(无色)
2NO+O2=2NO2(红棕色)
你还能列举与氧气反应再反应的情况吗
不溶于水,微溶于酒精,易溶于二硫化碳蛋白质明亮的蓝紫色微弱的淡蓝色3、硫在空气中燃烧发出 火焰,在纯净的氧气中燃烧发出 火焰,生成一种刺激性气味的气体是 ,化学方程式为二、二氧化硫物理性质:气体无色有刺激性气味有毒易液化密度比空气大易溶于水化学性质:1、SO2与H2O 的反应:实验现象:试管中的水面上升,滴入紫色石蕊试液后,溶液变红。SO2 + H2O H2SO3(亚硫酸)+4+4SO2 中S的化合价是:∴ SO2既有氧化性,又有还原性。以还原性为主+4价+6价的S元素只有氧化性
-2价的S元素只有还原性
+4价的S元素既有氧化性又有还原性2、还原性 与O2的反应:疑问:通常情况下SO2与O2能否大量共存?思考:已知亚硫酸溶液、亚硫酸钠粉末暴露在空气中容易变质,请写出其化学方程式? 2 H2SO3+O2== 2H2SO42Na2SO3+O2==2Na2SO4+4+6无色固体, 熔点(16.8℃)和沸点(44.8℃) 都比较低。 SO3 + H2O = H2SO4 SO3 :动手书写化学方程式
SO2+NaOH==
SO3+NaOH==SO3、SO2 都是酸性氧化物。CaO+SO2==3、SO2的漂白性:实验现象:品红溶液褪色 加热后,又恢复原来的颜色。该实验说明了什么问题?结论:SO2具有漂白性SO2的漂白原理是什么?与HClO、Na2O2、活性碳是否相同?1.下列叙述中,正确的是( ) A. SO2在空气中易被氧化为SO3 B. 在常温下, SO2的气体摩尔 体积是22.4L C. SO2 与SO3都能与水剧烈反应 D. SO2可用于漂白纸浆, SO3不能。练习:D2、在下列变化中,
不属于化学变化的是( )
A、SO2使品红溶液褪色
B、氯水使有色布条褪色
C、活性炭使红墨水褪色
D、O3使某些染料褪色C3、下列说法正确的是( )
A、SO2能使酸性KMnO4溶液褪色
B、可以用澄清石灰水鉴别SO2与CO2
C、硫粉在过量的纯氧中燃烧可以生成SO3
D、少量的SO2通入浓的CaCl2溶液能生成白色沉淀N2O、NO、N2O3、NO2、N2O4、N2O5氮的氧化物:分析氮元素的化合价-3 0 +1 +2 +3 +4 +4 +5无色,无味,有毒气体红棕色,刺激性气味,有毒气体不溶于水易 溶于水不与水反应3NO2+H2O=2HNO3+NO遇空气立即变红2NO+O2==2NO2遇空气不反应N2+O2 2NO(无色)三、一氧化氮与二氧化氮+2+4思考与交流:
1、一装满二氧化氮的试管倒置在水中一段时间,可观察到的现象是___________。2、科学探究:现给你一试管二氧化氮气体,其他药品和仪器自选,请你设计实验步骤,尽可能使二氧化氮被水吸收。见教材P92将一支充满NO2的试管倒放在盛有水的水槽中红棕色气体逐渐消失,水位上升到整个试管的2/33NO2+H2O=2HNO3+NO制取少量氧气2KClO3==2KCl+3O2↑将氧气慢慢通入倒放的试管中无色气体变为红棕色,又变为无色气体,液面不断上升,直至充满2NO+O2==2NO23、通入多少氧气时,正好充满整个试管?1、正常雨水pH应在什么范围? 2、形成酸雨的主要原因? 3、空气二氧化硫的主要来源?四、二氧化硫和二氧化氮的污染阅读教材后探讨:约为5.6化石燃料的燃烧(煤、石油)含硫矿石的冶炼制硫酸、磷肥、纸浆等工业废气三、一氧化氮:NO无色,无味,有毒气体不溶于水1、物理性质:2、化学性质:遇空气立即变红2NO+O2==2NO23、自然界的形成:N2+O2 2NO(无色)NO:
,,很不稳定。2NO+O2=2NO2
NO2:
红棕色,刺激性气体,有毒,易 溶于水,溶于水时,生成HNO3和NO
3NO2+H2O=2HNO3+NO
(NO2不是HNO3的酸酐,
分析电子转移, 氧化剂和还原剂的比)
B:与氧气反应
N2+O2 2NO(无色)
2NO+O2=2NO2(红棕色)
你还能列举与氧气反应再反应的情况吗
