人教版九年级化学上册 第三单元 课题2 原子的结构 优质课教学课件 (共17张PPT)
文档属性
| 名称 | 人教版九年级化学上册 第三单元 课题2 原子的结构 优质课教学课件 (共17张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 644.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-10-24 21:18:39 | ||
图片预览



文档简介
课件17张PPT。 物质构成的奥秘 课题2 原子的结构课前复习 1、物质是由 、 或 构成的分子原子离子2、水是由 构成的,
每个水分子又是由 和 构成的。
过氧化氢是由 构成的;
每个过氧化氢分子又是由 和 构成的。
水(H2O)和过氧化氢(H2O2)都是由 和
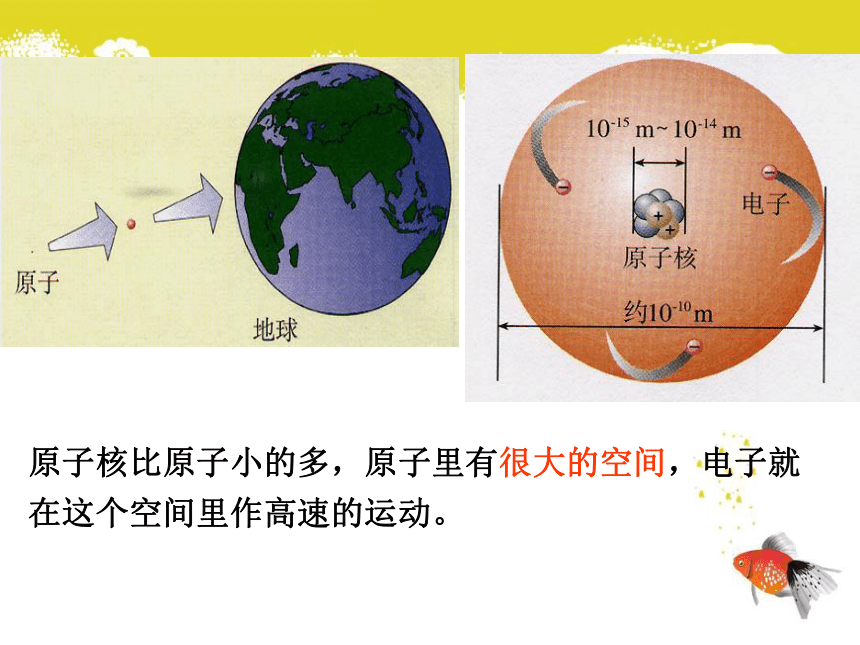
组成的。(本内容根据需要合理安排)3、在化学反应中,分子 而原子 。可分不可分 水分子2个氢原子1个氧原子过氧化氢分子 2个氢原子2个氧原子氢元素氧元素原子核比原子小的多,原子里有很大的空间,电子就
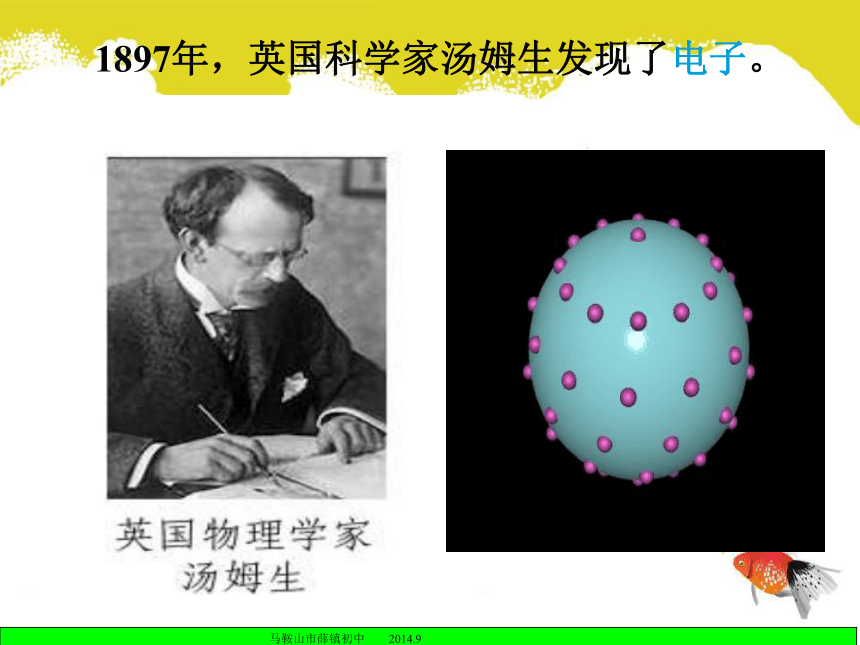
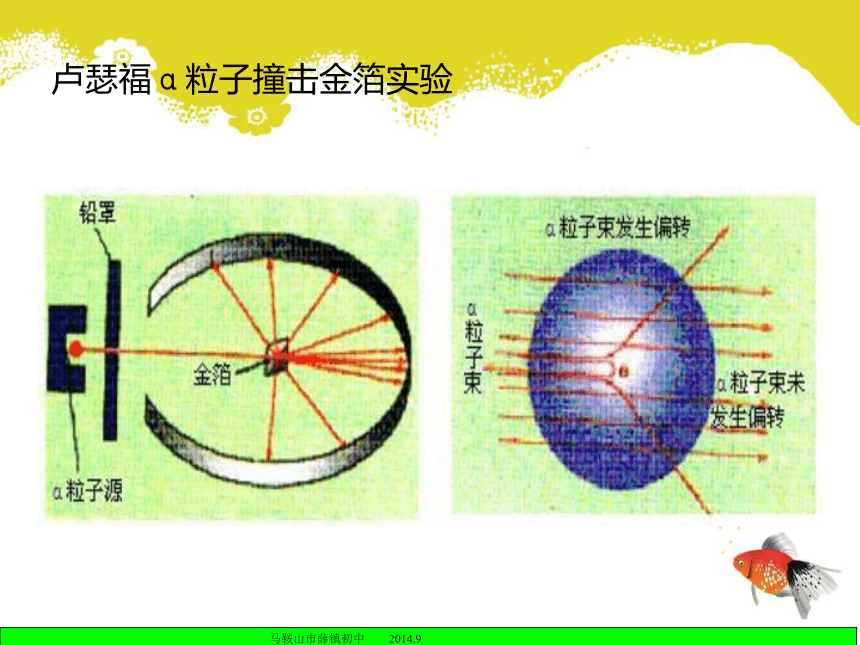
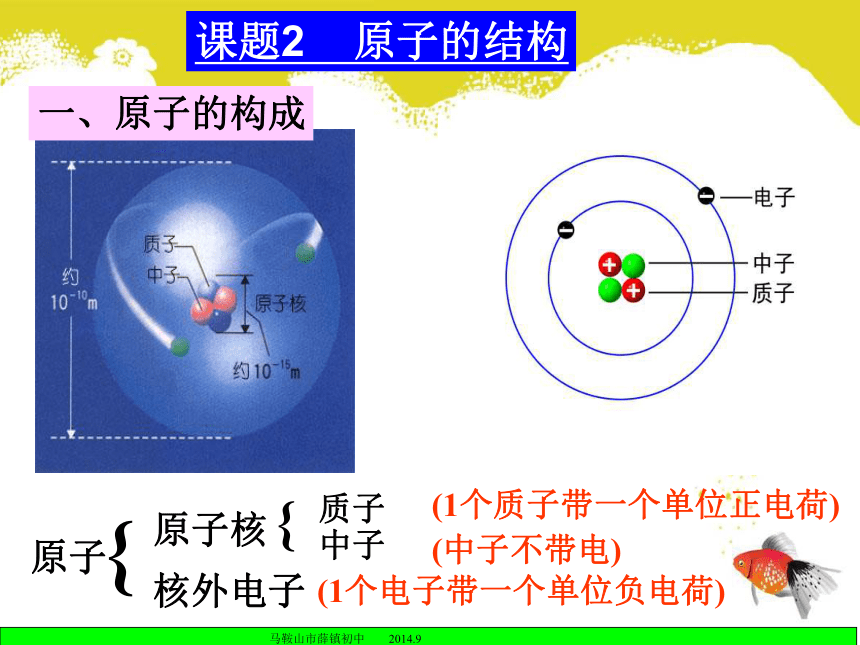
在这个空间里作高速的运动。 19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体。1897年,英国科学家汤姆生发现了电子。卢瑟福α粒子撞击金箔实验课题2 原子的结构原子原子核核外电子 质子 中子{
{(1个质子带一个单位正电荷)(1个电子带一个单位负电荷)(中子不带电)一、原子的构成在原子中,核电荷数 质子数 核外电子数==不同种类的原子,核内的质子数与核外的电子数都不相同原子不显电性原子序数注意:一定相等一定相等不一定相等不一定相等不是,氢原子除外,氢原子中没有中子。质子数不同一个5、以氧原子为例,
①、说明构成原子的粒子有哪几种?
②、它们是怎样构成原子的?
③、为什么整个氧原子不显电性?三种,质子、中子和电子。质子和中子构成原子核居于原子中心,
核外电子围绕原子核做高速运动构成原子。因为原子核所带的电量与核外电子的电量相等,
但电性相反,因此整个原子不显电性。6、某原子的质子数为11,中子数比质子数多1,则该
原子中所含粒子总数为 。34112165611二、相对原子质量(原子量)标准:一个碳12原子的实际质量的1/12
1.993×10-26千克×1/12
=1.66×10-27千克某原子的相
对原子质量(Ar)=该原子的实际质量(千克)标准(1.66×10-27千克)单位:为1(一般不写)例、一个标准碳原子的质量为Akg,一个硫原子的质量
为Bkg,镁的相对原子质量为C,则硫原子的相对原子
质量为 ;一个镁原子的质量为 千克。12B/AAC/12相对原子质量(Ar)==相对原子质量质子数+中子数原子的质量主要集中在原子核上课堂练习:1、完成下表661288167771111231616162626301、在化学变化中可以再分的微粒是( )
A、分子 B、原子 C、中子 D、电子
2、决定相对原子质量大小的主要微粒是( )
A、质子和电子 B、质子和中子
C、中子和电子 D、电子
3、一个碳原子的实际质量为1.993×10-26千克,
碳的相对原子质量是( )
A、12克 B、1/12 C、12 D、1.993×10-26/12
4、一个核内有6个质子和6个中子的碳原子的实际质量
为m千克,则实际质量为n千克的另一种原子的相对原子
质量为( )
A、n/12m B、12n/m千克 C、12n/m D、12ABCC
每个水分子又是由 和 构成的。
过氧化氢是由 构成的;
每个过氧化氢分子又是由 和 构成的。
水(H2O)和过氧化氢(H2O2)都是由 和
组成的。(本内容根据需要合理安排)3、在化学反应中,分子 而原子 。可分不可分 水分子2个氢原子1个氧原子过氧化氢分子 2个氢原子2个氧原子氢元素氧元素原子核比原子小的多,原子里有很大的空间,电子就
在这个空间里作高速的运动。 19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体。1897年,英国科学家汤姆生发现了电子。卢瑟福α粒子撞击金箔实验课题2 原子的结构原子原子核核外电子 质子 中子{
{(1个质子带一个单位正电荷)(1个电子带一个单位负电荷)(中子不带电)一、原子的构成在原子中,核电荷数 质子数 核外电子数==不同种类的原子,核内的质子数与核外的电子数都不相同原子不显电性原子序数注意:一定相等一定相等不一定相等不一定相等不是,氢原子除外,氢原子中没有中子。质子数不同一个5、以氧原子为例,
①、说明构成原子的粒子有哪几种?
②、它们是怎样构成原子的?
③、为什么整个氧原子不显电性?三种,质子、中子和电子。质子和中子构成原子核居于原子中心,
核外电子围绕原子核做高速运动构成原子。因为原子核所带的电量与核外电子的电量相等,
但电性相反,因此整个原子不显电性。6、某原子的质子数为11,中子数比质子数多1,则该
原子中所含粒子总数为 。34112165611二、相对原子质量(原子量)标准:一个碳12原子的实际质量的1/12
1.993×10-26千克×1/12
=1.66×10-27千克某原子的相
对原子质量(Ar)=该原子的实际质量(千克)标准(1.66×10-27千克)单位:为1(一般不写)例、一个标准碳原子的质量为Akg,一个硫原子的质量
为Bkg,镁的相对原子质量为C,则硫原子的相对原子
质量为 ;一个镁原子的质量为 千克。12B/AAC/12相对原子质量(Ar)==相对原子质量质子数+中子数原子的质量主要集中在原子核上课堂练习:1、完成下表661288167771111231616162626301、在化学变化中可以再分的微粒是( )
A、分子 B、原子 C、中子 D、电子
2、决定相对原子质量大小的主要微粒是( )
A、质子和电子 B、质子和中子
C、中子和电子 D、电子
3、一个碳原子的实际质量为1.993×10-26千克,
碳的相对原子质量是( )
A、12克 B、1/12 C、12 D、1.993×10-26/12
4、一个核内有6个质子和6个中子的碳原子的实际质量
为m千克,则实际质量为n千克的另一种原子的相对原子
质量为( )
A、n/12m B、12n/m千克 C、12n/m D、12ABCC
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
