3 配置一定溶质质量分数的溶液 练习
图片预览


文档简介
COOCO.因你而专业.
可圈可点HTTP://.CN
web试卷生成系统谢谢使用
题号
一、填空题
二、选择题
三、多项选择
四、计算题
总分
得分
评卷人
得分
一、填空题
(每空?
分,共?
分)
1、配制360.0g
10%的盐酸,需要36%的盐酸(密度为1.18g/cm3)____毫升,水____毫升.
2、向90g10%的NaCl溶液中加入10gK2SO4搅拌至完全溶解,所得溶液中NaCl的质量分数为____.
3、向40g5%的NaOH溶液中,加入60g10%的NaOH溶液,混合后溶液中NaOH质量分数为____.
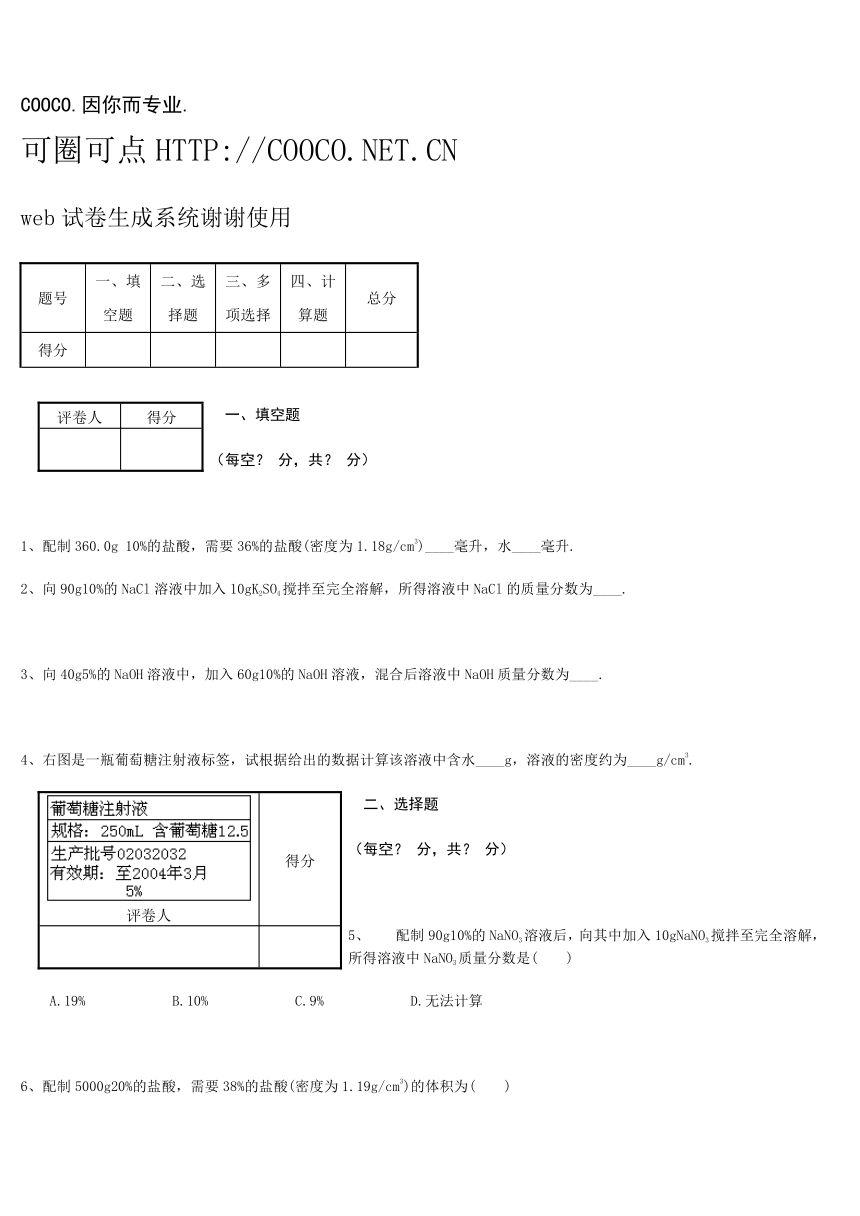
4、右图是一瓶葡萄糖注射液标签,试根据给出的数据计算该溶液中含水____g,溶液的密度约为____g/cm3.
评卷人
得分
二、选择题
(每空?
分,共?
分)
5、 配制90g10%的NaNO3溶液后,向其中加入10gNaNO3搅拌至完全溶解,所得溶液中NaNO3质量分数是( )
A.19% B.10% C.9% D.无法计算
6、配制5000g20%的盐酸,需要38%的盐酸(密度为1.19g/cm3)的体积为( )
A.2211mL
B.1000mL
C.2200mL D.2632mL
7、某酒精溶液中乙醇所含的氢原子数与水所含的氢原子数相等,则该酒精溶液中溶质的质量分数为( )
A.50% B.25% C.46%
D.33.3%
8、一份2%的NaCl溶液蒸发掉40g水后,溶质质量分数变为10%,则原溶液中溶质质量为( )
A.1g
B.2g
C.5g D.8g
9、20℃时,NaCl的溶解度为36g,该温度下,NaCl溶液中溶质质量分数不可能为( )
A.20% B.26.5% C.25%
D.30%
评卷人
得分
三、多项选择
(每空?
分,共?
分)
10、把40g5%的CaCl2溶液溶质质量分数增大到10%,应采用的方法是( )
A.把溶剂蒸发掉一半 B.加入2gCaCl2固体
C.加入40g15%的CaCl2溶液
D.把溶剂蒸发掉20g
评卷人
得分
四、计算题
(每空?
分,共?
分)
11、 现有100g溶质质量分数为15%的过氧乙酸溶液,欲配制成溶质质量分数为1.5%的溶液来使用,需加水多少克?
12、配制2000g20%的稀硫酸用以除锈,需98%的浓硫酸和水各多少毫升?
13、实验室用95%的浓硫酸与5%的稀硫酸来配制20%的硫酸180g,需要95%的硫酸和5%的硫酸各多少克?
14、200g稀硫酸与足量锌反应,生成0.4g氢气.求:①原硫酸溶液中溶质的质量分数.②所得溶液中溶质质量分数.
15、把16.9gNaCl和Na2CO3的混合物加入到100g7.3%的盐酸中,恰好完全反应.求反应后所得溶液中溶质的质量分数.
16、为了给水果消毒,某同学要把30g15%的KMnO4溶液稀释成0.3%的溶液,需加水多少克?
17、将9gKNO3完全溶于21g水中,并将其均分为三份,计算:(1)取一份,其中溶质质量分数是多少?(2)取一份,使其溶质质量分数增大一倍,需加入KNO3多少克?(3)取一份,欲使其溶质质量分数减小一半,需加水多少克?
18、t℃时,4.8g镁与一定量的稀盐酸恰好完全反应,所得溶液溶质质量分数为25%.求所用盐酸中氯化氢的质量分数.
19、取22.2g石灰石样品,放入盛有126g稀盐酸的烧杯中,石灰石中的CaCO3与盐酸恰好完全反应(杂质不反应,也不溶解),烧杯内物质质量变为139.4g.求反应后所得溶液中溶质的质量分数.
20、常温下,将18.9gKCl和K2CO3的混合物溶于149g水中,向其中加入36.5g稀盐酸,恰好完全反应,得到200g不饱和溶液.求反应后所得溶液中溶质的质量分数.
21、将10g不纯的MgCl2样品(杂质不溶于水),放入50g水中,充分搅拌,待样品中MgCl2全部溶解后过滤.将所得滤液与63.3gNaOH溶液恰好完全反应,生成5.8g白色沉淀.
求:(1)样品中MgCl2的质量
(2)反应后所得溶液中溶质的质量分数
22、甲、乙、丙三位同学分别取铁粉和铜粉的均匀混合物与某稀硫酸反应,所得数据如下:
甲
乙
丙
金属混合物质量(g)
10
10
20
稀硫酸质量(g)
100
120
100
反应后,过滤得干燥固体质量(g)
2
2
12
计算:(1)金属混合物中铁的质量分数;
(2)甲制得硫酸亚铁质量;
(3)该稀硫酸中溶质的质量分数.
参考答案
一、填空题
1、 84.7 260.0
2、 9%
3、 8%
4、237.5 1
二、选择题
5、 A
6、 A
7、C
8、A
9、D
三、多项选择
10、 CD
四、计算题
11、解:设需加水质量为x,
100g×15%=(100g+x)×1.5%
x=900g
12、解:设需浓硫酸的质量为x
2000g×20%=x×98%
x=408.2g
浓硫酸体积=408.2g÷1.84g/cm3=221.8mL
水的体积=(2000g-408.2g)÷1g/cm3=1591.8mL
13、解:设需要95%,5%硫酸的质量分别为x,y
x=30g y=150g
14、解:设参加反应的H2SO4质量为x,生成ZnSO4的质量为y.
Zn+H2SO4=ZnSO4+H2↑
98 161 2
x
y 0.4g
x=19.6g
y=32.2g
(1)
(2)
15、解:盐酸中溶质质量为:100g×7.3%=7.3g
设Na2CO3质量为x,生成NaCl质量为y,CO2质量为m,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 117 44
x 7.3g y
m
x=10.6g y=11.7g
m=4.4g
所得溶液溶质质量分数为:
16、 1470g
17、30% 7.5g 10g
18、20.4%
19、16.2%
20、10%
21、(1)9.5g (2)10g
22、(1)80% (2)21.7g (3)14%
可圈可点HTTP://.CN
web试卷生成系统谢谢使用
题号
一、填空题
二、选择题
三、多项选择
四、计算题
总分
得分
评卷人
得分
一、填空题
(每空?
分,共?
分)
1、配制360.0g
10%的盐酸,需要36%的盐酸(密度为1.18g/cm3)____毫升,水____毫升.
2、向90g10%的NaCl溶液中加入10gK2SO4搅拌至完全溶解,所得溶液中NaCl的质量分数为____.
3、向40g5%的NaOH溶液中,加入60g10%的NaOH溶液,混合后溶液中NaOH质量分数为____.
4、右图是一瓶葡萄糖注射液标签,试根据给出的数据计算该溶液中含水____g,溶液的密度约为____g/cm3.
评卷人
得分
二、选择题
(每空?
分,共?
分)
5、 配制90g10%的NaNO3溶液后,向其中加入10gNaNO3搅拌至完全溶解,所得溶液中NaNO3质量分数是( )
A.19% B.10% C.9% D.无法计算
6、配制5000g20%的盐酸,需要38%的盐酸(密度为1.19g/cm3)的体积为( )
A.2211mL
B.1000mL
C.2200mL D.2632mL
7、某酒精溶液中乙醇所含的氢原子数与水所含的氢原子数相等,则该酒精溶液中溶质的质量分数为( )
A.50% B.25% C.46%
D.33.3%
8、一份2%的NaCl溶液蒸发掉40g水后,溶质质量分数变为10%,则原溶液中溶质质量为( )
A.1g
B.2g
C.5g D.8g
9、20℃时,NaCl的溶解度为36g,该温度下,NaCl溶液中溶质质量分数不可能为( )
A.20% B.26.5% C.25%
D.30%
评卷人
得分
三、多项选择
(每空?
分,共?
分)
10、把40g5%的CaCl2溶液溶质质量分数增大到10%,应采用的方法是( )
A.把溶剂蒸发掉一半 B.加入2gCaCl2固体
C.加入40g15%的CaCl2溶液
D.把溶剂蒸发掉20g
评卷人
得分
四、计算题
(每空?
分,共?
分)
11、 现有100g溶质质量分数为15%的过氧乙酸溶液,欲配制成溶质质量分数为1.5%的溶液来使用,需加水多少克?
12、配制2000g20%的稀硫酸用以除锈,需98%的浓硫酸和水各多少毫升?
13、实验室用95%的浓硫酸与5%的稀硫酸来配制20%的硫酸180g,需要95%的硫酸和5%的硫酸各多少克?
14、200g稀硫酸与足量锌反应,生成0.4g氢气.求:①原硫酸溶液中溶质的质量分数.②所得溶液中溶质质量分数.
15、把16.9gNaCl和Na2CO3的混合物加入到100g7.3%的盐酸中,恰好完全反应.求反应后所得溶液中溶质的质量分数.
16、为了给水果消毒,某同学要把30g15%的KMnO4溶液稀释成0.3%的溶液,需加水多少克?
17、将9gKNO3完全溶于21g水中,并将其均分为三份,计算:(1)取一份,其中溶质质量分数是多少?(2)取一份,使其溶质质量分数增大一倍,需加入KNO3多少克?(3)取一份,欲使其溶质质量分数减小一半,需加水多少克?
18、t℃时,4.8g镁与一定量的稀盐酸恰好完全反应,所得溶液溶质质量分数为25%.求所用盐酸中氯化氢的质量分数.
19、取22.2g石灰石样品,放入盛有126g稀盐酸的烧杯中,石灰石中的CaCO3与盐酸恰好完全反应(杂质不反应,也不溶解),烧杯内物质质量变为139.4g.求反应后所得溶液中溶质的质量分数.
20、常温下,将18.9gKCl和K2CO3的混合物溶于149g水中,向其中加入36.5g稀盐酸,恰好完全反应,得到200g不饱和溶液.求反应后所得溶液中溶质的质量分数.
21、将10g不纯的MgCl2样品(杂质不溶于水),放入50g水中,充分搅拌,待样品中MgCl2全部溶解后过滤.将所得滤液与63.3gNaOH溶液恰好完全反应,生成5.8g白色沉淀.
求:(1)样品中MgCl2的质量
(2)反应后所得溶液中溶质的质量分数
22、甲、乙、丙三位同学分别取铁粉和铜粉的均匀混合物与某稀硫酸反应,所得数据如下:
甲
乙
丙
金属混合物质量(g)
10
10
20
稀硫酸质量(g)
100
120
100
反应后,过滤得干燥固体质量(g)
2
2
12
计算:(1)金属混合物中铁的质量分数;
(2)甲制得硫酸亚铁质量;
(3)该稀硫酸中溶质的质量分数.
参考答案
一、填空题
1、 84.7 260.0
2、 9%
3、 8%
4、237.5 1
二、选择题
5、 A
6、 A
7、C
8、A
9、D
三、多项选择
10、 CD
四、计算题
11、解:设需加水质量为x,
100g×15%=(100g+x)×1.5%
x=900g
12、解:设需浓硫酸的质量为x
2000g×20%=x×98%
x=408.2g
浓硫酸体积=408.2g÷1.84g/cm3=221.8mL
水的体积=(2000g-408.2g)÷1g/cm3=1591.8mL
13、解:设需要95%,5%硫酸的质量分别为x,y
x=30g y=150g
14、解:设参加反应的H2SO4质量为x,生成ZnSO4的质量为y.
Zn+H2SO4=ZnSO4+H2↑
98 161 2
x
y 0.4g
x=19.6g
y=32.2g
(1)
(2)
15、解:盐酸中溶质质量为:100g×7.3%=7.3g
设Na2CO3质量为x,生成NaCl质量为y,CO2质量为m,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 117 44
x 7.3g y
m
x=10.6g y=11.7g
m=4.4g
所得溶液溶质质量分数为:
16、 1470g
17、30% 7.5g 10g
18、20.4%
19、16.2%
20、10%
21、(1)9.5g (2)10g
22、(1)80% (2)21.7g (3)14%
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
