扬州市梅林中学《把握核心素养方向标促进学生可持续发展》课件(共26张PPT)
文档属性
| 名称 | 扬州市梅林中学《把握核心素养方向标促进学生可持续发展》课件(共26张PPT) |  | |
| 格式 | ppt | ||
| 文件大小 | 714.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-10-27 22:12:38 | ||
图片预览



文档简介
(共26张PPT)
把握核心素养方向标
促进学生可持续发展
一、分值和考试时间
城市 南京 苏州 无锡 常州 镇江 南通 盐城 泰州 扬州 徐州 淮安 连云港 宿迁
分值 80 100 50 100 100 60 70 60 100 60 60 60 40
时间 60 100 50 100 100 60 60 60 100 60 60 60 理
化
120
二、试卷结构分析
第Ⅰ卷:选择题
第Ⅱ卷:非选择题
化学中考试卷
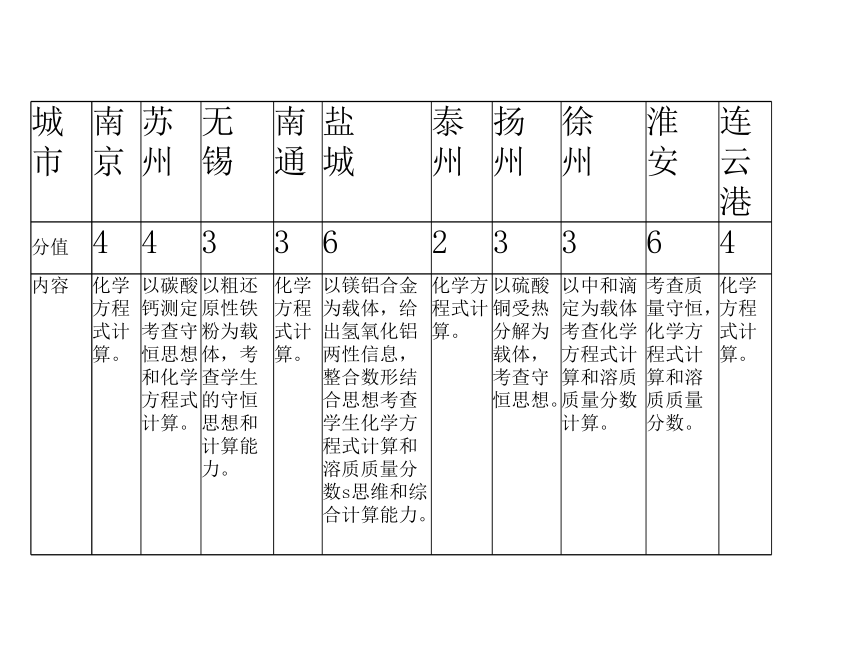
城市 南京 苏州 无
锡 南通 盐
城 泰州 扬
州 徐
州 淮
安 连云港
分值 4 4 3 3 6 2 3 3 6 4
内容 化学方程式计算。 以碳酸钙测定考查守恒思想和化学方程式计算。 以粗还原性铁粉为载体,考查学生的守恒思想和计算能力。 化学方程式计算。 以镁铝合金为载体,给出氢氧化铝两性信息,整合数形结合思想考查学生化学方程式计算和溶质质量分数s思维和综合计算能力。 化学方程式计算。 以硫酸铜受热分解为载体,考查守恒思想。 以中和滴定为载体考查化学方程式计算和溶质质量分数计算。 考查质量守恒,化学方程式计算和溶质质量分数。 化学方程式计算。
计算题
溶质质量分数
化学方程式
酸碱盐知识
数形结合
全新信息
体系选择
EXAMINATIOAN
CHEMICAI DISCIPLNES
化学思想
计算能力
One
Two
Three
思维能力
镇江30(三)4
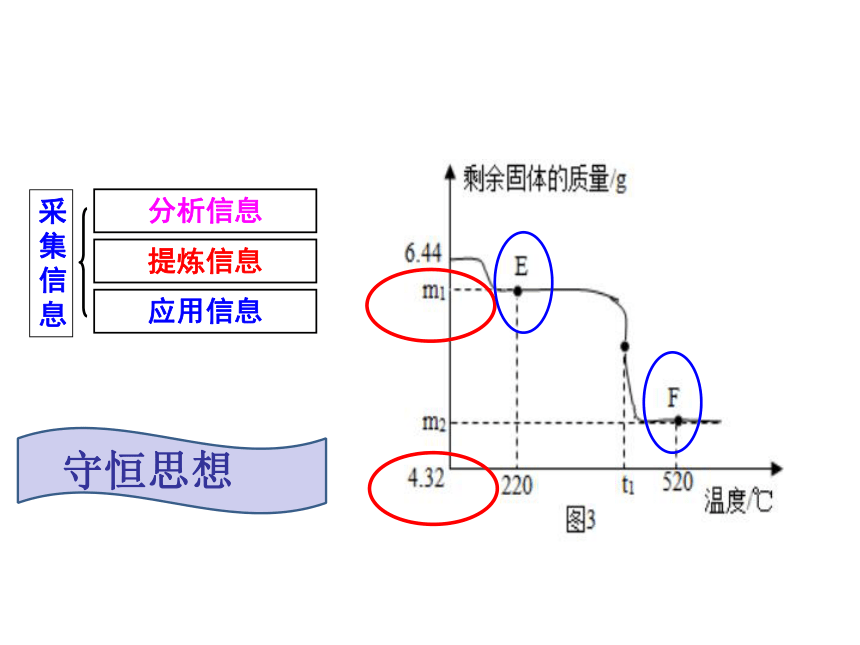
兴趣小组称取此固体6.44g,[查阅资料]
①Fe(OH)2在150℃~200℃时完全分解为FeO;
②FeSO4在450℃~500℃时完全分解为Fe2O3,2FeSO4=Fe2O3+SO2↑+SO3↑
2FeSO4 2Fe(OH)2 Fe2O3〔相对分子质量为644]
分析信息
提炼信息
应用信息
采集信息
守恒思想
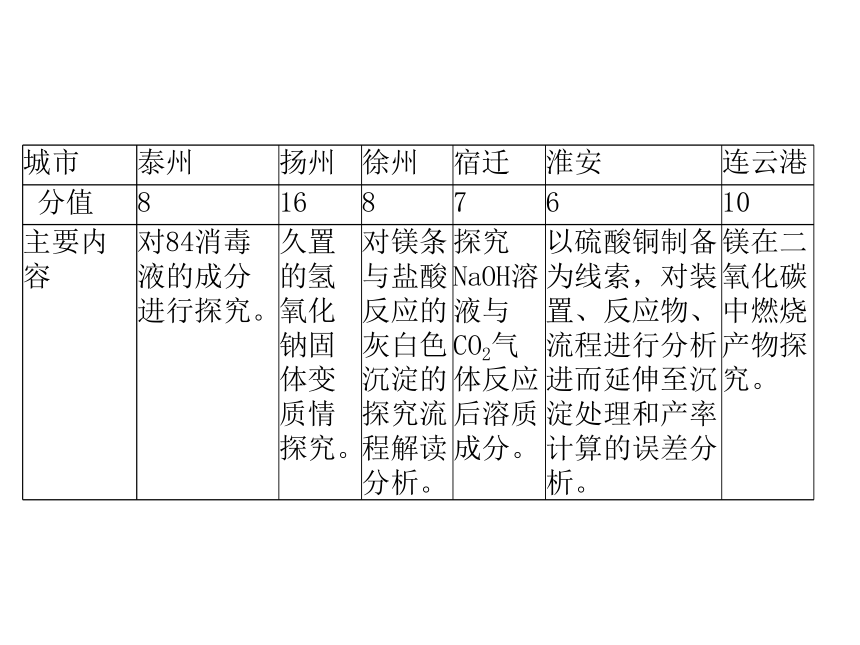
城市 泰州 扬州 徐州 宿迁 淮安 连云港
分值 8 16 8 7 6 10
主要内容 对84消毒液的成分进行探究。 久置的氢氧化钠固体变质情探究。 对镁条与盐酸反应的灰白色沉淀的探究流程解读分析。 探究NaOH溶液与CO2气体反应后溶质成分。 以硫酸铜制备为线索,对装置、反应物、流程进行分析进而延伸至沉淀处理和产率计算的误差分析。 镁在二氧化碳中燃烧产物探究。
城市 南京 苏州 无锡 常州 镇江 南通
分值 11 9 12 8 14 10
主要内容 以经典的拉瓦锡研究空气成分实验为引子,利用教材中实验装置对红磷和白磷不同的实验效果进行分析,展示用铁粉进行空气中氧气测定的可行性并进行分析。 探究白磷在水中燃烧的实验装置的改进过程分析。 对绿矾制备氧化铁、四氧化三铁及还原性铁粉的流程、操作、原理进行分析和展示。 从镁与稀盐酸反应的异常现象入手,对产生的原因、异常物质的成分进行分析和计算。 以钢铁材料为线索,对铁及其化合物的实验产物进行定性分析,对实验中出现的灰绿色含铁固体成分进行定量测定,对设计的实验装置和流程、现象分析,利用数形结合思想计算相关物质的量。 验证水的组成及探究水在电极端所发生的变化,将宏观现象与微观粒子产生联系。
三、点击命题亮点
(一)题干内容紧跟时代,素材鲜活。
以常州卷为例,试卷中的选择题5-7题以近年来开发的“石头纸”为素材,;第28题则用压强传感器获得的数据进行题干设计,反映了测量和定量分析的手段与时俱进;第29题则回归生活,DIY冰淇淋。
(二)关注学生核心素养,形式灵活。
以扬州卷为例,命题遵循课程标准的三维目标理念,关注学生核心素养,考查学生收集和处理信息的能力、分析和解决实际问题能力,有浓厚的化学味;能引导教师在学习中注重学科基本思想和实验方法的传授。
扬州第25题:
反应液温度(℃)
所得 CaO 活性最高。要得出正确结论,煅烧时还需控制的条件是 。
(2)以电石渣[主要成分为Ca(OH)2,还含有少量MgO等杂质]为原料制备高纯CaCO3的流程如下:
①右图为NH4Cl浓度对钙、镁浸出率的影响可知:较适宜的NH4Cl溶液的质量分数为 ;浸取时主要反应的化学方程式为 。
钙和镁的浸出率(%)
②流程中虚线内部分若改用 溶液(填化学式),可一步得到与原流程完全相同的生成物。
③流程中虚线内部分若改用Na2CO3溶液,也能得到高纯CaCO3。试从生成物的角度分析原流程的优点:a.NH3可循环利用;b. 。
【点评】此题通过对简单工艺流程的阅读与分析,强化了实验基本操作、目的、条件控制、化学方程式的书写与意义、绿色化学思想等综合能力,依据已有化学知识结合新信息来解答,对考生的阅读、理解能力要求较高。预计难度0.65。
(三)聚焦化学实验考查,内容真实。
如南京中考第21题:空气中氧气含量测定的再认识。
立意 能力
【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1)。该实验中选择使用汞的优点有 。
A.实验过程中没有污染
B.在汞槽中起到液封作用
C.生成的化合物加热分解又能得到汞和氧气
D.能将密闭装置内空气中的氧气集合耗尽
【实验与交流】在老师的指导下,小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%,请从燃烧条件的角度回答产生上述结果的主要原因白磷的着火点比红磷的着火点低
【实验探究1】小明根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量,于是进行了实验(装置如图3)通过7天测得的数据计算空气中氧气的含量为19.13%.
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点及原因:
装置内残留的氧气更少,实验结果更准确
实验前的体积 实验后的体积
集气瓶内空气 烧杯内蒸馏水 烧杯内剩余蒸馏水
131mL 90.0mL 63.6mL
2016无锡下列化肥中,从外观即可与其他化肥相区别的是( )
A.硫酸钾 B.硝酸铵 C.磷矿粉 D.氯化钾
EXAMINATIOAN
CHEMICAI DSCIPLINES
泰州17(5)制取气体前应先检查装置的气密性,若按F图所示操作,结果在导管口未看到气泡,其可能原因与下列因素无关的是
a.将烧杯换成水槽 b.导管深入水中位置过深,气体无法逸出
c.将水换成冰水 d.先用手捂住试管壁,再将导管另一端插入水中.
紧扣课标教材
体现基础启蒙
强化实验探究
突出学科特征
联系社会生活
彰显学科价值
重视化学思维体现能力立意
中考命题
关注学段衔接
兼顾学生发展
把握学生心理
体现人文关怀
把握核心素养方向标
促进学生可持续发展
一、分值和考试时间
城市 南京 苏州 无锡 常州 镇江 南通 盐城 泰州 扬州 徐州 淮安 连云港 宿迁
分值 80 100 50 100 100 60 70 60 100 60 60 60 40
时间 60 100 50 100 100 60 60 60 100 60 60 60 理
化
120
二、试卷结构分析
第Ⅰ卷:选择题
第Ⅱ卷:非选择题
化学中考试卷
城市 南京 苏州 无
锡 南通 盐
城 泰州 扬
州 徐
州 淮
安 连云港
分值 4 4 3 3 6 2 3 3 6 4
内容 化学方程式计算。 以碳酸钙测定考查守恒思想和化学方程式计算。 以粗还原性铁粉为载体,考查学生的守恒思想和计算能力。 化学方程式计算。 以镁铝合金为载体,给出氢氧化铝两性信息,整合数形结合思想考查学生化学方程式计算和溶质质量分数s思维和综合计算能力。 化学方程式计算。 以硫酸铜受热分解为载体,考查守恒思想。 以中和滴定为载体考查化学方程式计算和溶质质量分数计算。 考查质量守恒,化学方程式计算和溶质质量分数。 化学方程式计算。
计算题
溶质质量分数
化学方程式
酸碱盐知识
数形结合
全新信息
体系选择
EXAMINATIOAN
CHEMICAI DISCIPLNES
化学思想
计算能力
One
Two
Three
思维能力
镇江30(三)4
兴趣小组称取此固体6.44g,[查阅资料]
①Fe(OH)2在150℃~200℃时完全分解为FeO;
②FeSO4在450℃~500℃时完全分解为Fe2O3,2FeSO4=Fe2O3+SO2↑+SO3↑
2FeSO4 2Fe(OH)2 Fe2O3〔相对分子质量为644]
分析信息
提炼信息
应用信息
采集信息
守恒思想
城市 泰州 扬州 徐州 宿迁 淮安 连云港
分值 8 16 8 7 6 10
主要内容 对84消毒液的成分进行探究。 久置的氢氧化钠固体变质情探究。 对镁条与盐酸反应的灰白色沉淀的探究流程解读分析。 探究NaOH溶液与CO2气体反应后溶质成分。 以硫酸铜制备为线索,对装置、反应物、流程进行分析进而延伸至沉淀处理和产率计算的误差分析。 镁在二氧化碳中燃烧产物探究。
城市 南京 苏州 无锡 常州 镇江 南通
分值 11 9 12 8 14 10
主要内容 以经典的拉瓦锡研究空气成分实验为引子,利用教材中实验装置对红磷和白磷不同的实验效果进行分析,展示用铁粉进行空气中氧气测定的可行性并进行分析。 探究白磷在水中燃烧的实验装置的改进过程分析。 对绿矾制备氧化铁、四氧化三铁及还原性铁粉的流程、操作、原理进行分析和展示。 从镁与稀盐酸反应的异常现象入手,对产生的原因、异常物质的成分进行分析和计算。 以钢铁材料为线索,对铁及其化合物的实验产物进行定性分析,对实验中出现的灰绿色含铁固体成分进行定量测定,对设计的实验装置和流程、现象分析,利用数形结合思想计算相关物质的量。 验证水的组成及探究水在电极端所发生的变化,将宏观现象与微观粒子产生联系。
三、点击命题亮点
(一)题干内容紧跟时代,素材鲜活。
以常州卷为例,试卷中的选择题5-7题以近年来开发的“石头纸”为素材,;第28题则用压强传感器获得的数据进行题干设计,反映了测量和定量分析的手段与时俱进;第29题则回归生活,DIY冰淇淋。
(二)关注学生核心素养,形式灵活。
以扬州卷为例,命题遵循课程标准的三维目标理念,关注学生核心素养,考查学生收集和处理信息的能力、分析和解决实际问题能力,有浓厚的化学味;能引导教师在学习中注重学科基本思想和实验方法的传授。
扬州第25题:
反应液温度(℃)
所得 CaO 活性最高。要得出正确结论,煅烧时还需控制的条件是 。
(2)以电石渣[主要成分为Ca(OH)2,还含有少量MgO等杂质]为原料制备高纯CaCO3的流程如下:
①右图为NH4Cl浓度对钙、镁浸出率的影响可知:较适宜的NH4Cl溶液的质量分数为 ;浸取时主要反应的化学方程式为 。
钙和镁的浸出率(%)
②流程中虚线内部分若改用 溶液(填化学式),可一步得到与原流程完全相同的生成物。
③流程中虚线内部分若改用Na2CO3溶液,也能得到高纯CaCO3。试从生成物的角度分析原流程的优点:a.NH3可循环利用;b. 。
【点评】此题通过对简单工艺流程的阅读与分析,强化了实验基本操作、目的、条件控制、化学方程式的书写与意义、绿色化学思想等综合能力,依据已有化学知识结合新信息来解答,对考生的阅读、理解能力要求较高。预计难度0.65。
(三)聚焦化学实验考查,内容真实。
如南京中考第21题:空气中氧气含量测定的再认识。
立意 能力
【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1)。该实验中选择使用汞的优点有 。
A.实验过程中没有污染
B.在汞槽中起到液封作用
C.生成的化合物加热分解又能得到汞和氧气
D.能将密闭装置内空气中的氧气集合耗尽
【实验与交流】在老师的指导下,小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%,请从燃烧条件的角度回答产生上述结果的主要原因白磷的着火点比红磷的着火点低
【实验探究1】小明根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量,于是进行了实验(装置如图3)通过7天测得的数据计算空气中氧气的含量为19.13%.
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点及原因:
装置内残留的氧气更少,实验结果更准确
实验前的体积 实验后的体积
集气瓶内空气 烧杯内蒸馏水 烧杯内剩余蒸馏水
131mL 90.0mL 63.6mL
2016无锡下列化肥中,从外观即可与其他化肥相区别的是( )
A.硫酸钾 B.硝酸铵 C.磷矿粉 D.氯化钾
EXAMINATIOAN
CHEMICAI DSCIPLINES
泰州17(5)制取气体前应先检查装置的气密性,若按F图所示操作,结果在导管口未看到气泡,其可能原因与下列因素无关的是
a.将烧杯换成水槽 b.导管深入水中位置过深,气体无法逸出
c.将水换成冰水 d.先用手捂住试管壁,再将导管另一端插入水中.
紧扣课标教材
体现基础启蒙
强化实验探究
突出学科特征
联系社会生活
彰显学科价值
重视化学思维体现能力立意
中考命题
关注学段衔接
兼顾学生发展
把握学生心理
体现人文关怀
同课章节目录
