沪教全国版九年级化学第4章《认识化学变化》检测试卷
文档属性
| 名称 | 沪教全国版九年级化学第4章《认识化学变化》检测试卷 |

|
|
| 格式 | zip | ||
| 文件大小 | 59.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-11-06 00:00:00 | ||
图片预览

文档简介
第4章《认识化学变化》检测试卷
满分:100分 时间:60分钟
可能用到的相对原子质量:H-1 O-16 Mg-24 P-31 Al-27 Mn-25
一、单项选择题(每小题只有一个正确答案。每小题2分,共20分)
1.不适宜用质量守恒定律解释的现象是 ( )
A.煤炭燃烧后变成煤灰,质量变小了
B.樟脑球放在衣柜中一段时间后变小了
C.镁带燃烧后生成的固体质量增加
D.高锰酸钾受热,其固体的总质量逐渐减小
2.小华在一次探究实验中将一小粒金属钠投入盛有蒸馏水的烧杯中,发现反应剧烈并生成大量气体,则该气体可能是 ( )
A.H2 B.CH4 C.He D.NH3
3.如下图所示,每两分子的甲反应后生成一分子的乙和两分子的丙。已知甲、乙、丙分别为不同的纯净物,则丙物质的化学式是 ( )
A.A2 B.AB2
C.A2B D.A4B2
4.煤油中含有噻吩,噻吩(用X表示)有令人不愉快的气味,其燃烧的化学方程式可表示为X+6O24CO2+SO2+2H2O,则x的化学式为 ( )
A.CH4S B.C2H6S
C.C4H4S D.C6H6S
5.已知化学方程式X+2O2CO2+2H2O,下列对x的判断正确的是 ( )
A.X中一定含碳、氢元素,可能含氧元素
B.X中一定含碳、氢、氧三种元素
C.X中碳、氢元素的质量比为1:4
D.X的化学式是CH4
6.煤的气化是提高煤的利用率、减少环境污染的有效措施。煤的气化过程中发生了化学反应C+H2O(气)H2+CO,反应前后,发生了变化的是 ( )
A.元素的种类 B.碳、氢元素的化合价
C.原子的数目 D.物质的总质量
7.镁条在空气中燃烧,此反应中有关的量随时间变化的图像正确的是 ( )
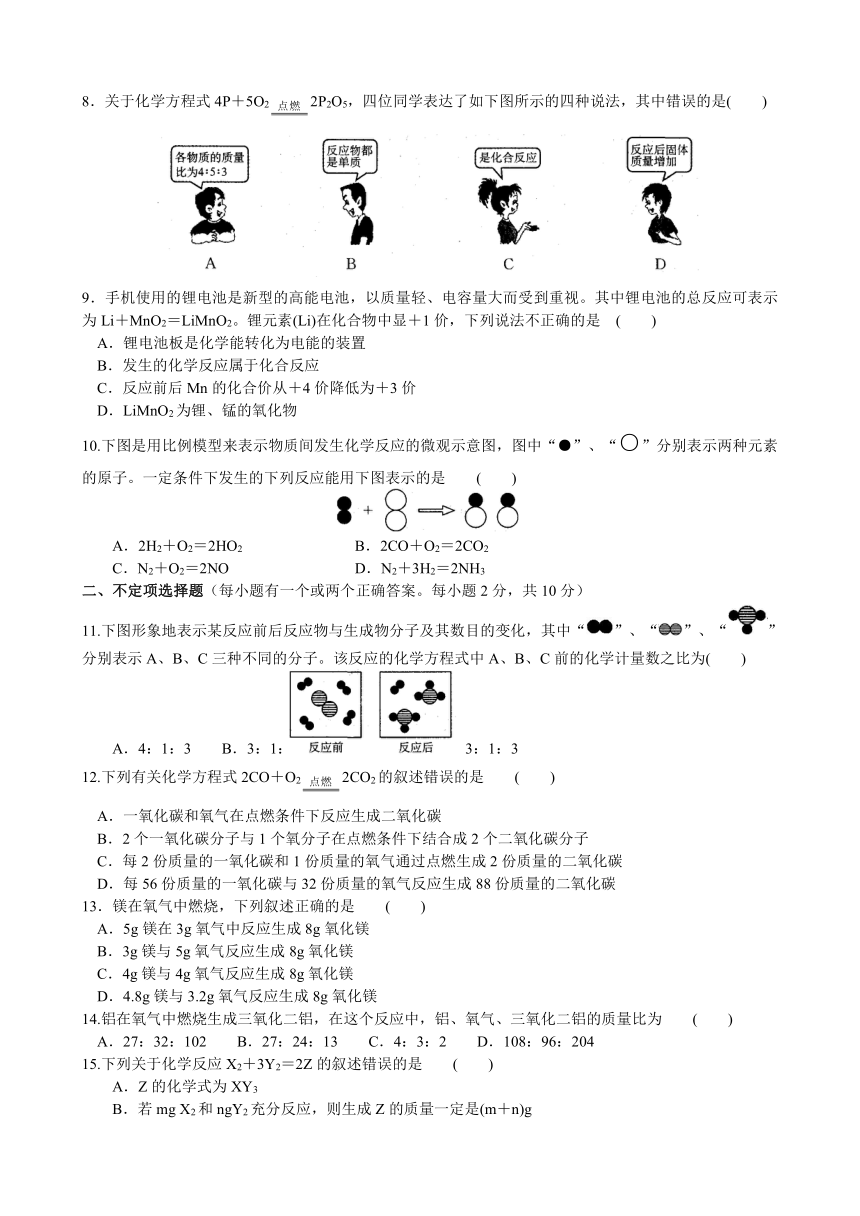
8.关于化学方程式4P+5O22P2O5,四位同学表达了如下图所示的四种说法,其中错误的是( )
9.手机使用的锂电池是新型的高能电池,以质量轻、电容量大而受到重视。其中锂电池的总反应可表示为Li+MnO2=LiMnO2。锂元素(Li)在化合物中显+1价,下列说法不正确的是 ( )
A.锂电池板是化学能转化为电能的装置
B.发生的化学反应属于化合反应
C.反应前后Mn的化合价从+4价降低为+3价
D.LiMnO2为锂、锰的氧化物
10.下图是用比例模型来表示物质间发生化学反应的微观示意图,图中“●”、“○”分别表示两种元素的原子。一定条件下发生的下列反应能用下图表示的是 ( )
A.2H2+O2=2HO2 B.2CO+O2=2CO2
C.N2+O2=2NO D.N2+3H2=2NH3
二、不定项选择题(每小题有一个或两个正确答案。每小题2分,共10分)
11.下图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中“”、“”、“”分别表示A、B、C三种不同的分子。该反应的化学方程式中A、B、C前的化学计量数之比为( )
A.4:1:3 B.3:1:2 C.4:1:2 D.3:1:3
12.下列有关化学方程式2CO+O22CO2的叙述错误的是 ( )
A.一氧化碳和氧气在点燃条件下反应生成二氧化碳
B.2个一氧化碳分子与1个氧分子在点燃条件下结合成2个二氧化碳分子
C.每2份质量的一氧化碳和1份质量的氧气通过点燃生成2份质量的二氧化碳
D.每56份质量的一氧化碳与32份质量的氧气反应生成88份质量的二氧化碳
13.镁在氧气中燃烧,下列叙述正确的是 ( )
A.5g镁在3g氧气中反应生成8g氧化镁
B.3g镁与5g氧气反应生成8g氧化镁
C.4g镁与4g氧气反应生成8g氧化镁
D.4.8g镁与3.2g氧气反应生成8g氧化镁
14.铝在氧气中燃烧生成三氧化二铝,在这个反应中,铝、氧气、三氧化二铝的质量比为 ( )
A.27:32:102 B.27:24:13 C.4:3:2 D.108:96:204
15.下列关于化学反应X2+3Y2=2Z的叙述错误的是 ( )
A.Z的化学式为XY3
B.若mg X2和ngY2充分反应,则生成Z的质量一定是(m+n)g
C.若X2和Y2的相对分子质量分别为M和N,则Z的相对分子质量为(M+N)
D.若ag X2完全反应生成bgZ,则同时消耗(b-a)g Y2
三、填空题(每空3分,共54分)
16.某同学写了以下化学方程式:
①Mg+O2MgO2
②H2OH2↑+O2↑
③C+O2↑CO2↑
④4P+5O22P2O5↓
⑤3Fe+2O2=Fe3O4
⑥S+O2=SO2
根据化学方程式错误的不同,将其序号填入以下相应的空白处:
(1)未配平的是_______。
(2)化学式写错的是
(3)“↑”或“↓”使用不当的是_______。
(4)未注明反应条件或条件不正确的是_______。
17.在4P+5O22P2O5反应中,可以说每_______个磷原子与_______个氧分子发生化合反应,生成_______个五氧化二磷分子;也可以说每_______份质量的磷与_______份质量的氧气反应,生成_______份质量的五氧化二磷。
18.构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水。ClO2是新一代饮用水的消毒剂,我国成功研制出制取ClO2的新方法,其反应的微观过程图如下:
试回答:
(1) ClO2叫作_______,其中氯元素的化合价为_______。
(2)根据反应的微观过程图写出反应的化学方程式:_______。
19.高级汽车中常配置有一种汽车安全气袋,内部贮存有硝酸铵。当汽车高速行驶中受到猛烈撞击时,硝酸铵迅速分解产生大量一氧化二氮(N2O)气体和另一种氧化物充满气袋,填补在乘员与挡风玻璃、方向盘之间,防止乘员受伤。
(1)硝酸铵受撞击发生分解反应的化学方程式是_______。
(2)此反应中反应物和生成物中氮元素的化合价从左到右依次为_______。
20.为测定空气中氧气所占的体积分数,某同学设计了如下图所示实验。在一个耐热活塞的底部放一小块(足量)白磷,然后迅速将活塞下压,可以观察到的现象为_______;冷却至原来温度时,慢慢松开手,活塞最终将回到刻度_______处,白磷燃烧的原因是_______。
四、计算题(第21题6分,第22题10分,共16分)
21.实验室需要制取48g氧气,应至少用多少克的高锰酸钾?
22.为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,杂质中不含钙元素)。
有关实验数据如下表所示:
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为多少克?
(2)求该石灰石中碳酸钙的质量分数。
(3)求该石灰石中钙元素的质量分数。
参考答案
一、单项选择题
1.B 2.A 3.C 4.C 5.D 6.B 7.D 8.A 9.D 10.C
二、不定项选择题
11.B 12.BC 13.D 14.D 15.BC
三、填空题
16.(1)② (2)① (3)③④ (4)⑤⑥
17.4 5 2 124 160 284
18.(1)二氧化氯 +4 (2)Cl2+2NaClO2=2ClO2+2NaCl
19.(1) NH4NO3=N2O+2H2O (2)-3、+5、+1
20.白磷燃烧,产生大量的白烟 4 下压活塞做功,空气的内能增加,温度升高,达到白磷的着火点
四、计算题
21.474g
22.(1)4.4g (9)83.3% (3)33.3%
满分:100分 时间:60分钟
可能用到的相对原子质量:H-1 O-16 Mg-24 P-31 Al-27 Mn-25
一、单项选择题(每小题只有一个正确答案。每小题2分,共20分)
1.不适宜用质量守恒定律解释的现象是 ( )
A.煤炭燃烧后变成煤灰,质量变小了
B.樟脑球放在衣柜中一段时间后变小了
C.镁带燃烧后生成的固体质量增加
D.高锰酸钾受热,其固体的总质量逐渐减小
2.小华在一次探究实验中将一小粒金属钠投入盛有蒸馏水的烧杯中,发现反应剧烈并生成大量气体,则该气体可能是 ( )
A.H2 B.CH4 C.He D.NH3
3.如下图所示,每两分子的甲反应后生成一分子的乙和两分子的丙。已知甲、乙、丙分别为不同的纯净物,则丙物质的化学式是 ( )
A.A2 B.AB2
C.A2B D.A4B2
4.煤油中含有噻吩,噻吩(用X表示)有令人不愉快的气味,其燃烧的化学方程式可表示为X+6O24CO2+SO2+2H2O,则x的化学式为 ( )
A.CH4S B.C2H6S
C.C4H4S D.C6H6S
5.已知化学方程式X+2O2CO2+2H2O,下列对x的判断正确的是 ( )
A.X中一定含碳、氢元素,可能含氧元素
B.X中一定含碳、氢、氧三种元素
C.X中碳、氢元素的质量比为1:4
D.X的化学式是CH4
6.煤的气化是提高煤的利用率、减少环境污染的有效措施。煤的气化过程中发生了化学反应C+H2O(气)H2+CO,反应前后,发生了变化的是 ( )
A.元素的种类 B.碳、氢元素的化合价
C.原子的数目 D.物质的总质量
7.镁条在空气中燃烧,此反应中有关的量随时间变化的图像正确的是 ( )
8.关于化学方程式4P+5O22P2O5,四位同学表达了如下图所示的四种说法,其中错误的是( )
9.手机使用的锂电池是新型的高能电池,以质量轻、电容量大而受到重视。其中锂电池的总反应可表示为Li+MnO2=LiMnO2。锂元素(Li)在化合物中显+1价,下列说法不正确的是 ( )
A.锂电池板是化学能转化为电能的装置
B.发生的化学反应属于化合反应
C.反应前后Mn的化合价从+4价降低为+3价
D.LiMnO2为锂、锰的氧化物
10.下图是用比例模型来表示物质间发生化学反应的微观示意图,图中“●”、“○”分别表示两种元素的原子。一定条件下发生的下列反应能用下图表示的是 ( )
A.2H2+O2=2HO2 B.2CO+O2=2CO2
C.N2+O2=2NO D.N2+3H2=2NH3
二、不定项选择题(每小题有一个或两个正确答案。每小题2分,共10分)
11.下图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中“”、“”、“”分别表示A、B、C三种不同的分子。该反应的化学方程式中A、B、C前的化学计量数之比为( )
A.4:1:3 B.3:1:2 C.4:1:2 D.3:1:3
12.下列有关化学方程式2CO+O22CO2的叙述错误的是 ( )
A.一氧化碳和氧气在点燃条件下反应生成二氧化碳
B.2个一氧化碳分子与1个氧分子在点燃条件下结合成2个二氧化碳分子
C.每2份质量的一氧化碳和1份质量的氧气通过点燃生成2份质量的二氧化碳
D.每56份质量的一氧化碳与32份质量的氧气反应生成88份质量的二氧化碳
13.镁在氧气中燃烧,下列叙述正确的是 ( )
A.5g镁在3g氧气中反应生成8g氧化镁
B.3g镁与5g氧气反应生成8g氧化镁
C.4g镁与4g氧气反应生成8g氧化镁
D.4.8g镁与3.2g氧气反应生成8g氧化镁
14.铝在氧气中燃烧生成三氧化二铝,在这个反应中,铝、氧气、三氧化二铝的质量比为 ( )
A.27:32:102 B.27:24:13 C.4:3:2 D.108:96:204
15.下列关于化学反应X2+3Y2=2Z的叙述错误的是 ( )
A.Z的化学式为XY3
B.若mg X2和ngY2充分反应,则生成Z的质量一定是(m+n)g
C.若X2和Y2的相对分子质量分别为M和N,则Z的相对分子质量为(M+N)
D.若ag X2完全反应生成bgZ,则同时消耗(b-a)g Y2
三、填空题(每空3分,共54分)
16.某同学写了以下化学方程式:
①Mg+O2MgO2
②H2OH2↑+O2↑
③C+O2↑CO2↑
④4P+5O22P2O5↓
⑤3Fe+2O2=Fe3O4
⑥S+O2=SO2
根据化学方程式错误的不同,将其序号填入以下相应的空白处:
(1)未配平的是_______。
(2)化学式写错的是
(3)“↑”或“↓”使用不当的是_______。
(4)未注明反应条件或条件不正确的是_______。
17.在4P+5O22P2O5反应中,可以说每_______个磷原子与_______个氧分子发生化合反应,生成_______个五氧化二磷分子;也可以说每_______份质量的磷与_______份质量的氧气反应,生成_______份质量的五氧化二磷。
18.构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水。ClO2是新一代饮用水的消毒剂,我国成功研制出制取ClO2的新方法,其反应的微观过程图如下:
试回答:
(1) ClO2叫作_______,其中氯元素的化合价为_______。
(2)根据反应的微观过程图写出反应的化学方程式:_______。
19.高级汽车中常配置有一种汽车安全气袋,内部贮存有硝酸铵。当汽车高速行驶中受到猛烈撞击时,硝酸铵迅速分解产生大量一氧化二氮(N2O)气体和另一种氧化物充满气袋,填补在乘员与挡风玻璃、方向盘之间,防止乘员受伤。
(1)硝酸铵受撞击发生分解反应的化学方程式是_______。
(2)此反应中反应物和生成物中氮元素的化合价从左到右依次为_______。
20.为测定空气中氧气所占的体积分数,某同学设计了如下图所示实验。在一个耐热活塞的底部放一小块(足量)白磷,然后迅速将活塞下压,可以观察到的现象为_______;冷却至原来温度时,慢慢松开手,活塞最终将回到刻度_______处,白磷燃烧的原因是_______。
四、计算题(第21题6分,第22题10分,共16分)
21.实验室需要制取48g氧气,应至少用多少克的高锰酸钾?
22.为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,杂质中不含钙元素)。
有关实验数据如下表所示:
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为多少克?
(2)求该石灰石中碳酸钙的质量分数。
(3)求该石灰石中钙元素的质量分数。
参考答案
一、单项选择题
1.B 2.A 3.C 4.C 5.D 6.B 7.D 8.A 9.D 10.C
二、不定项选择题
11.B 12.BC 13.D 14.D 15.BC
三、填空题
16.(1)② (2)① (3)③④ (4)⑤⑥
17.4 5 2 124 160 284
18.(1)二氧化氯 +4 (2)Cl2+2NaClO2=2ClO2+2NaCl
19.(1) NH4NO3=N2O+2H2O (2)-3、+5、+1
20.白磷燃烧,产生大量的白烟 4 下压活塞做功,空气的内能增加,温度升高,达到白磷的着火点
四、计算题
21.474g
22.(1)4.4g (9)83.3% (3)33.3%
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
