黑龙江省友谊县红兴隆管理局第一高级中学2016-2017学年高二上学期期中考试化学试题
文档属性
| 名称 | 黑龙江省友谊县红兴隆管理局第一高级中学2016-2017学年高二上学期期中考试化学试题 |  | |
| 格式 | zip | ||
| 文件大小 | 150.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-11-17 15:27:54 | ||
图片预览


文档简介
红兴隆管理局第一高级中学2016-2017学年度
第一学期高二年级期中考试化学试卷
卷面分值:100分
时间:70分钟。
可能用到的相对原子质量:
H:1
Cu:64
C:12
第Ⅰ卷(选择题,共60分)
一、选择题(本题包括20小题,每小题3分,共60分。每小题只有一个选项符合题意。)
1.
用括号内试剂除去下列各物质中的少量杂质,正确的是
( )
A.溴苯中的溴(苯)
B.MgCl2酸性溶液中少量的FeCl3
(Mg(OH)2)
C.硝基苯中的苯(硝酸)
D.甲烷中的乙烯(酸性高锰酸钾溶液)
2.
下列说法中正确的是
( )
A.向0.1 mol L-1氨水中加入少量水,pH减小,c(OH-)/c(NH3·H2O)减小
B.保存FeSO4溶液时,加入稀HNO3抑制Fe2+水解
C.FeCl3溶液蒸干、灼烧至恒重,最终得到FeCl3固体
D.将纯水加热的过程中,Kw变大,pH变小
3.
化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)CuS(s)+Mn2+(aq),下列说法错误的是
( )
A.MnS的Ksp比CuS的Ksp大
B.该反应达到平衡时c(Mn2+)=c(Cu2+)
C.往平衡体系中加入少量CuSO4固体后,C(Mn2+)变大
D.该反应的平衡常数
4.
下列过程或现象与盐类水解无关的是
( )
A.纯碱溶液去油污
B.加热稀醋酸溶液其pH
稍有减小
C.小苏打溶液与AlCl3溶液混合产生气体和沉淀
D.浓的硫化钠溶液有臭味
5.
能证明乙酸是弱酸的实验事实是
( )
A.CH3COOH溶液与Zn反应放出H2
B.0.1
mol/L
CH3COOH溶液可使紫色石蕊变红
C.CH3COOH溶液与NaCO3反应生成CO2
D.0.1
mol/L
CH3COONa溶液的pH大于7
6.
室温,将pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后,溶液呈
( )
A.碱性
B.中性
C.酸性
D.无法确定
7.
在用Zn片、Cu片和稀硫酸组成的电池装置中,下列说法中正确的是
( )
A.溶液中的阳离子向正极移动,阴离子向负极移动
B.经过一段时问工作后'电解液的pH值减小
C.锌片是正极,铜片上有气泡产生
D.电流方向是从锌片流向铜片
8.
下列有关四个常用电化学装置的叙述正确的是
( )
A.图Ⅰ所示电池中,MnO2作催化剂
B.图Ⅱ所示电池放电过程中,硫酸浓度不断增大
C.图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图Ⅳ所示电池中,Ag2O作氧化剂,在电池工作过程中被还原为Ag
9.在一定条件下能发生取代反应和加成反应,但不能使酸性高锰酸钾溶液褪色的是
( )
A.乙烷
B.甲烷
C.苯
D.乙烯
10.
某电动汽车配载一种可充放电的锂离子电池。放电时电池的总反应为Li1-xCoO2+LixC6=LiCoO2+
C6(x<1)。下列关于该电池的说法不正确的是
( )
A.放电时,Li+在电解质中由负极向正极迁移
B.充电时,若转移1mole-,石墨C6电极将增重7xg
C.放电时,负极的电极反应式为LixC6-xe-=
xLi++
C6
D.充电时,阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+Li+
11.下列关于乙烯的说法不正确的是
( )
A.乙烯是一种基本化工原料,其产量可用来衡量一个国家的石油化工发展水平
B.乙烯是一种植物生长调节剂,可作为水果的催熟剂
C.乙烯通入溴水中因发生取代反应而使溴水褪色
D.乙烯可以和水发生加成反应生成乙醇
12.
下列说法不正确的是
(
)
A.为避免船体遭受腐蚀,在船舶的外壳装上若干锌块,称为牺牲阳极的阴极保护法
B.原电池工作时,电流的方向由正极→负载→负极→原电池中电解质溶液→正极
C.纯银在空气中久置变黑发生的是化学腐蚀
D.在铁制品上镀铜时,铁制品作电镀池的阳极,铜盐为电镀液
13.
下列叙述正确的是
( )
A.在原电池的负极和电解池的阴极上都是发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2
C.用惰性电极电解饱和KBr溶液,若有1
mol电子转移,则生成1
molKOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
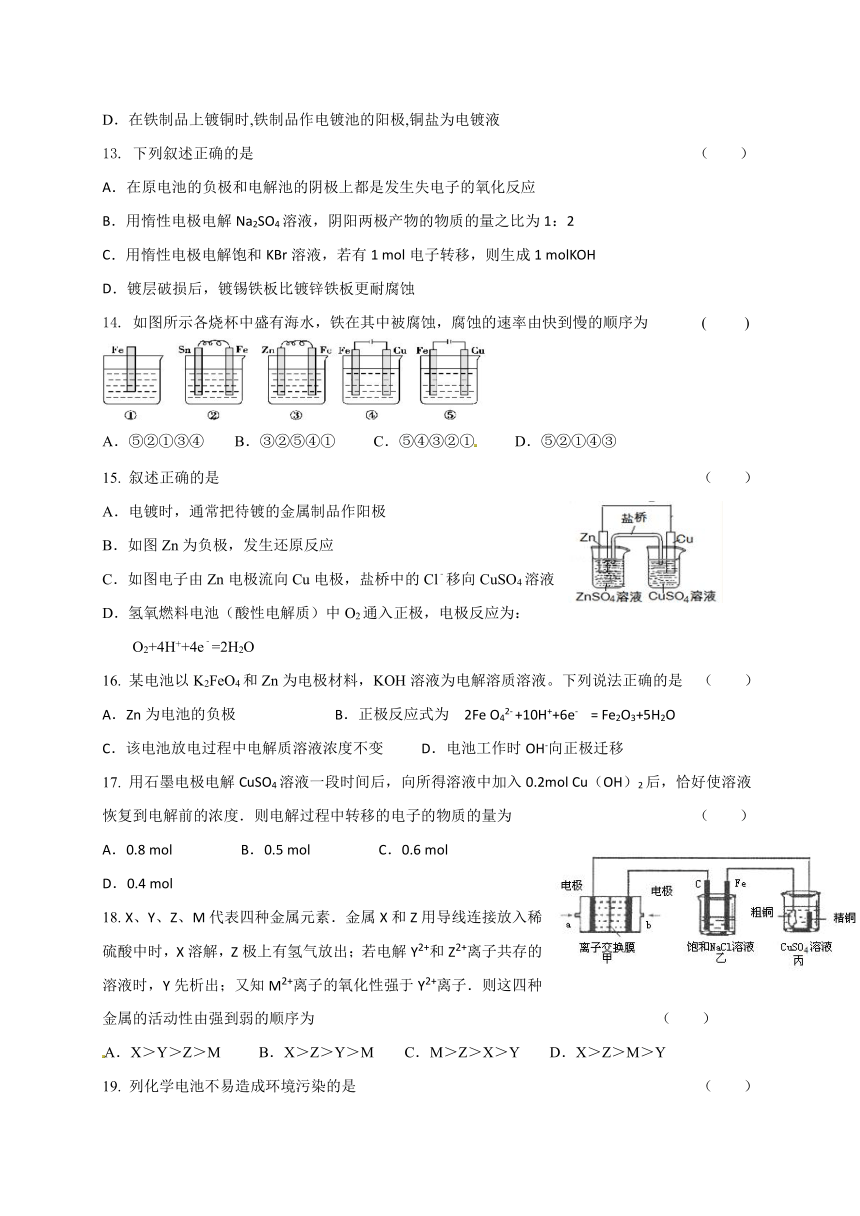
14.
如图所示各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由快到慢的顺序为
(
)
A.⑤②①③④
B.③②⑤④①
C.⑤④③②①
D.⑤②①④③
15.
叙述正确的是
( )
A.电镀时,通常把待镀的金属制品作阳极
B.如图Zn为负极,发生还原反应
C.如图电子由Zn电极流向Cu电极,盐桥中的Cl﹣移向CuSO4溶液
D.氢氧燃料电池(酸性电解质)中O2通入正极,电极反应为:
O2+4H++4e﹣=2H2O
16.
某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液。下列说法正确的是
( )
A.Zn为电池的负极
B.正极反应式为
2Fe
O42-
+10H++6e-
=
Fe2O3+5H2O
C.该电池放电过程中电解质溶液浓度不变
D.电池工作时OH-向正极迁移
17.
用石墨电极电解CuSO4溶液一段时间后,向所得溶液中加入0.2mol
Cu(OH)2后,恰好使溶液恢复到电解前的浓度.则电解过程中转移的电子的物质的量为
( )
A.0.8
mol
B.0.5
mol
C.0.6
mol
D.0.4
mol
18.
X、Y、Z、M代表四种金属元素.金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+离子共存的溶液时,Y先析出;又知M2+离子的氧化性强于Y2+离子.则这四种金属的活动性由强到弱的顺序为
( )
A.X>Y>Z>M
B.X>Z>Y>M
C.M>Z>X>Y
D.X>Z>M>Y
19.
列化学电池不易造成环境污染的是
( )
A.氢氧燃料电池
B.锌锰电池
C.镍镉电池
D.铅蓄电池
20.
Mg–AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是
( )
A.
负极反应式为Mg–2e–=Mg2+
B.
电池放电时Cl–由正极向负极迁移
C.
正极反应式为Ag++e–=Ag
D.
负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑
第Ⅱ卷(非选择题,共40分)
二、非选择题
21.(9分)请写出下列反应的化学反应方程式,并判断其反应类型。
(1)乙烯与溴的反应:
,属于
反应。
(2)由乙烯制聚乙烯:
,属于
反应。
(3)由苯制取溴苯:
,属于
反应。
22.(7分)
请回答下列问题:
(1)NH4Cl溶液显
性,原因是
(用离子方程式表示),NH4Cl溶液中离子浓度由大到小的顺序为
.
(2)将浓度均为0.10mol/L的CH3COOH溶液和NaOH溶液混合后,若pH>7,则该溶液中c(CH3COO-)
c(Na+).(填“>”、“<”、“=”).
23.
(12分)如图为用惰性电极电解CuCl2溶液,并验证其产物的实验装置,回答下问题:
(1)惰性电极Ⅰ为电解池的
(选填“阴”或“阳”)极。
(2)反应开始一段时间后,惰性电极Ⅰ上实验现象为
。
KI—淀粉溶液会变
色。
(3)惰性电极Ⅱ上发生的电极反应为
。
(4)该电解反应方程式为
。
(5)可以将惰性电极Ⅰ换为
。
A.
铜棒
B.铁棒
C.钠块
24.
(12分)如图所示的装置,将电路接通后,向(乙)中滴人酚酞溶液,在Fe极附近显红色.试回答下列问题:
(1)(甲)装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则b处通入的是
(填“CH4”或“O2”),a处电极上发生的电极反应式是
;
(2)在(乙)装置中,石墨(C)电极上发生
(填“氧化”或“还原”)
反应;(乙)装置中总反应的离子方程式是:
。
(3)如果(丙)装置中精铜电极的质量增加了6.4g,则(甲)装置中消耗的
CH4的质量为
,
(乙)装置中,铁电极上产生的气体在标准状况下为
。
红兴隆管理局第一高级中学
2016-2017学年度第一学期高二年级期中考试化学试卷答案
1B
2D
3
B
4B
5D
6C
7A
8
D
9C
10B
11C
12
D
13C
14A
15D
16A
17A
18B
19A
20C
21.(1)CH2=CH2+Br2→CH2BrCH2Br
(2分)
加成反应(1分)
(2)nCH2=CH2
(2分)
加聚反应(1分)
(3)
(2分)
取代反应(1分)
22.(1)酸(1分);NH4++H2O NH3 H2O+H+;(2分)c(Cl﹣)>c(NH4+)>c(H+)>c(OH﹣)(2分);(2)<(2分)
23.(每空2分)(1)阴
(2)析出红色物质
蓝(3)2Cl--2e-
=
Cl2↑
(4)CuCl2
Cu
+
Cl2↑
或
Cu2++2Cl-
Cu
+
Cl2↑
(5)AB
24.
(每空2分)(1):O2;CH4+10OH﹣-8e﹣=CO32-+7H2O;(2)氧化;2Cl﹣+2H2O2OH﹣+Cl2↑+H2↑;(3)0.4g;
2.24L
第一学期高二年级期中考试化学试卷
卷面分值:100分
时间:70分钟。
可能用到的相对原子质量:
H:1
Cu:64
C:12
第Ⅰ卷(选择题,共60分)
一、选择题(本题包括20小题,每小题3分,共60分。每小题只有一个选项符合题意。)
1.
用括号内试剂除去下列各物质中的少量杂质,正确的是
( )
A.溴苯中的溴(苯)
B.MgCl2酸性溶液中少量的FeCl3
(Mg(OH)2)
C.硝基苯中的苯(硝酸)
D.甲烷中的乙烯(酸性高锰酸钾溶液)
2.
下列说法中正确的是
( )
A.向0.1 mol L-1氨水中加入少量水,pH减小,c(OH-)/c(NH3·H2O)减小
B.保存FeSO4溶液时,加入稀HNO3抑制Fe2+水解
C.FeCl3溶液蒸干、灼烧至恒重,最终得到FeCl3固体
D.将纯水加热的过程中,Kw变大,pH变小
3.
化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)CuS(s)+Mn2+(aq),下列说法错误的是
( )
A.MnS的Ksp比CuS的Ksp大
B.该反应达到平衡时c(Mn2+)=c(Cu2+)
C.往平衡体系中加入少量CuSO4固体后,C(Mn2+)变大
D.该反应的平衡常数
4.
下列过程或现象与盐类水解无关的是
( )
A.纯碱溶液去油污
B.加热稀醋酸溶液其pH
稍有减小
C.小苏打溶液与AlCl3溶液混合产生气体和沉淀
D.浓的硫化钠溶液有臭味
5.
能证明乙酸是弱酸的实验事实是
( )
A.CH3COOH溶液与Zn反应放出H2
B.0.1
mol/L
CH3COOH溶液可使紫色石蕊变红
C.CH3COOH溶液与NaCO3反应生成CO2
D.0.1
mol/L
CH3COONa溶液的pH大于7
6.
室温,将pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后,溶液呈
( )
A.碱性
B.中性
C.酸性
D.无法确定
7.
在用Zn片、Cu片和稀硫酸组成的电池装置中,下列说法中正确的是
( )
A.溶液中的阳离子向正极移动,阴离子向负极移动
B.经过一段时问工作后'电解液的pH值减小
C.锌片是正极,铜片上有气泡产生
D.电流方向是从锌片流向铜片
8.
下列有关四个常用电化学装置的叙述正确的是
( )
A.图Ⅰ所示电池中,MnO2作催化剂
B.图Ⅱ所示电池放电过程中,硫酸浓度不断增大
C.图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图Ⅳ所示电池中,Ag2O作氧化剂,在电池工作过程中被还原为Ag
9.在一定条件下能发生取代反应和加成反应,但不能使酸性高锰酸钾溶液褪色的是
( )
A.乙烷
B.甲烷
C.苯
D.乙烯
10.
某电动汽车配载一种可充放电的锂离子电池。放电时电池的总反应为Li1-xCoO2+LixC6=LiCoO2+
C6(x<1)。下列关于该电池的说法不正确的是
( )
A.放电时,Li+在电解质中由负极向正极迁移
B.充电时,若转移1mole-,石墨C6电极将增重7xg
C.放电时,负极的电极反应式为LixC6-xe-=
xLi++
C6
D.充电时,阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+Li+
11.下列关于乙烯的说法不正确的是
( )
A.乙烯是一种基本化工原料,其产量可用来衡量一个国家的石油化工发展水平
B.乙烯是一种植物生长调节剂,可作为水果的催熟剂
C.乙烯通入溴水中因发生取代反应而使溴水褪色
D.乙烯可以和水发生加成反应生成乙醇
12.
下列说法不正确的是
(
)
A.为避免船体遭受腐蚀,在船舶的外壳装上若干锌块,称为牺牲阳极的阴极保护法
B.原电池工作时,电流的方向由正极→负载→负极→原电池中电解质溶液→正极
C.纯银在空气中久置变黑发生的是化学腐蚀
D.在铁制品上镀铜时,铁制品作电镀池的阳极,铜盐为电镀液
13.
下列叙述正确的是
( )
A.在原电池的负极和电解池的阴极上都是发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2
C.用惰性电极电解饱和KBr溶液,若有1
mol电子转移,则生成1
molKOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
14.
如图所示各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由快到慢的顺序为
(
)
A.⑤②①③④
B.③②⑤④①
C.⑤④③②①
D.⑤②①④③
15.
叙述正确的是
( )
A.电镀时,通常把待镀的金属制品作阳极
B.如图Zn为负极,发生还原反应
C.如图电子由Zn电极流向Cu电极,盐桥中的Cl﹣移向CuSO4溶液
D.氢氧燃料电池(酸性电解质)中O2通入正极,电极反应为:
O2+4H++4e﹣=2H2O
16.
某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液。下列说法正确的是
( )
A.Zn为电池的负极
B.正极反应式为
2Fe
O42-
+10H++6e-
=
Fe2O3+5H2O
C.该电池放电过程中电解质溶液浓度不变
D.电池工作时OH-向正极迁移
17.
用石墨电极电解CuSO4溶液一段时间后,向所得溶液中加入0.2mol
Cu(OH)2后,恰好使溶液恢复到电解前的浓度.则电解过程中转移的电子的物质的量为
( )
A.0.8
mol
B.0.5
mol
C.0.6
mol
D.0.4
mol
18.
X、Y、Z、M代表四种金属元素.金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+离子共存的溶液时,Y先析出;又知M2+离子的氧化性强于Y2+离子.则这四种金属的活动性由强到弱的顺序为
( )
A.X>Y>Z>M
B.X>Z>Y>M
C.M>Z>X>Y
D.X>Z>M>Y
19.
列化学电池不易造成环境污染的是
( )
A.氢氧燃料电池
B.锌锰电池
C.镍镉电池
D.铅蓄电池
20.
Mg–AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是
( )
A.
负极反应式为Mg–2e–=Mg2+
B.
电池放电时Cl–由正极向负极迁移
C.
正极反应式为Ag++e–=Ag
D.
负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑
第Ⅱ卷(非选择题,共40分)
二、非选择题
21.(9分)请写出下列反应的化学反应方程式,并判断其反应类型。
(1)乙烯与溴的反应:
,属于
反应。
(2)由乙烯制聚乙烯:
,属于
反应。
(3)由苯制取溴苯:
,属于
反应。
22.(7分)
请回答下列问题:
(1)NH4Cl溶液显
性,原因是
(用离子方程式表示),NH4Cl溶液中离子浓度由大到小的顺序为
.
(2)将浓度均为0.10mol/L的CH3COOH溶液和NaOH溶液混合后,若pH>7,则该溶液中c(CH3COO-)
c(Na+).(填“>”、“<”、“=”).
23.
(12分)如图为用惰性电极电解CuCl2溶液,并验证其产物的实验装置,回答下问题:
(1)惰性电极Ⅰ为电解池的
(选填“阴”或“阳”)极。
(2)反应开始一段时间后,惰性电极Ⅰ上实验现象为
。
KI—淀粉溶液会变
色。
(3)惰性电极Ⅱ上发生的电极反应为
。
(4)该电解反应方程式为
。
(5)可以将惰性电极Ⅰ换为
。
A.
铜棒
B.铁棒
C.钠块
24.
(12分)如图所示的装置,将电路接通后,向(乙)中滴人酚酞溶液,在Fe极附近显红色.试回答下列问题:
(1)(甲)装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则b处通入的是
(填“CH4”或“O2”),a处电极上发生的电极反应式是
;
(2)在(乙)装置中,石墨(C)电极上发生
(填“氧化”或“还原”)
反应;(乙)装置中总反应的离子方程式是:
。
(3)如果(丙)装置中精铜电极的质量增加了6.4g,则(甲)装置中消耗的
CH4的质量为
,
(乙)装置中,铁电极上产生的气体在标准状况下为
。
红兴隆管理局第一高级中学
2016-2017学年度第一学期高二年级期中考试化学试卷答案
1B
2D
3
B
4B
5D
6C
7A
8
D
9C
10B
11C
12
D
13C
14A
15D
16A
17A
18B
19A
20C
21.(1)CH2=CH2+Br2→CH2BrCH2Br
(2分)
加成反应(1分)
(2)nCH2=CH2
(2分)
加聚反应(1分)
(3)
(2分)
取代反应(1分)
22.(1)酸(1分);NH4++H2O NH3 H2O+H+;(2分)c(Cl﹣)>c(NH4+)>c(H+)>c(OH﹣)(2分);(2)<(2分)
23.(每空2分)(1)阴
(2)析出红色物质
蓝(3)2Cl--2e-
=
Cl2↑
(4)CuCl2
Cu
+
Cl2↑
或
Cu2++2Cl-
Cu
+
Cl2↑
(5)AB
24.
(每空2分)(1):O2;CH4+10OH﹣-8e﹣=CO32-+7H2O;(2)氧化;2Cl﹣+2H2O2OH﹣+Cl2↑+H2↑;(3)0.4g;
2.24L
同课章节目录
