高一化学人教版必修1第1.2.2 气体摩尔体积 课时同步附解析
文档属性
| 名称 | 高一化学人教版必修1第1.2.2 气体摩尔体积 课时同步附解析 |  | |
| 格式 | zip | ||
| 文件大小 | 57.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-11-30 14:04:40 | ||
图片预览


文档简介
绝密★启用前
人教版必修一第一章第二节第二课时
气体摩尔体积
一、选择题
1.下列有关物理量相应的单位表达错误的是( )
A.
摩尔质量g/mol
B.
气体摩尔体积L/mol
C.
溶解度g/100g
D.
密度g/cm3
2.下列说法正确的是( )
A.1
mol任何气体的体积都是22.4
L
B.在标准状况下,某气体的体积为22.4
L,则该气体的物质的量为1
mol,所含的分子数目约为6.02×1023
C.当温度高于0
℃时,一定量任何气体的体积都大于22.4
L
D.当压强大于101
kPa时,1
mol任何气体的体积都小于22.4
L
3.标准状况下,下列物质占体积最大的是( )
A.98
g
H2SO4
B.6.02×1023个CO2
C.44.8
L
HCl
D.6
g
H2
4.空气可近似认为N2和O2按体积比为4∶1组成的混合气体,则空气的平均相对分子质量约为( )
A.28
B.29
C.32
D.60
5.下列各组物质中,所含分子数一定相同的是( )
A.1
g
H2和8
g
O2
B.0.1
mol
HCl和2.24
L
He
C.150
℃、1.01×105
Pa时,18
L
H2O和18
L
CO2
D.常温常压下,28
g
CO和6.02×1022个CO分子
6.在同温、同压下,A容器中的氧气和B容器中的氨气所含的原子个数相同,则A、B两容器中气体体积之比为( )
A.1∶2
B.2∶1
C.2∶3
D.3∶2
7.(双选题)关于m
g
H2和n
g
He的下列说法正确的是( )
A.同温同压下,H2和He的体积比为m∶2n
B.同温同压下,若m=n,则H2与He的物质的量比为2∶1
C.体积相同时,He的质量一定大于H2
D.同温同压下,若二者的物质的量相等,其体积也相等
8.某物质在一定条件下加热分解,产物都是气体。分解方程式为:2AB+2C+2D。测得生成的混合气体的平均相对分子质量为2a,则A的相对分子质量为( )
A.7a
B.5a
C.2.5a
D.2a
9.下列叙述正确的是( )
A.一定温度、压强下,气体体积由其分子的大小决定
B.一定温度、压强下,气体体积由气体的物质的量的多少决定
C.气体摩尔体积是指1
mol
任何气体所占的体积为
22.4
L
D.不同的气体,若体积不等,则它们所含的分子数一定不相等
10.在两个容积相同的容器中,一个盛装氯化氢气体,另一个盛装氢气和氯气的混合气体。在同温同压下,两容器内的气体一定具有相同的( )
A.原子数
B.密度
C.质量
D.相对分子质量
11.在相同的温度和压强下,4个容积相同的容器中分别装有4种气体:a.CO2;b.O2;
c.N2;d.CH4。则4个容器中气体的质量由大到小的顺序是( )
A.c>d>b>a
B.b>a>d>c
C.a>b>c>d
D.d>c>a>b
12.在一定温度和压强下,1体积的A2气体和3体积的B2气体化合成2体积的C气体,则C的化学式为( )
A.AB3
B.AB
C.A3B
D.A2B3
二、非选择题
13.N2、CO2、SO2三种气体的物质的量比为1∶1∶1时,它们的分子个数比为________;质量比为________;同温、同压下体积之比为________。
14.在标准状况下,由CO和CO2组成的混合气体为6.72
L,质量为12
g,此混合物中CO和CO2物质的量之比是________,
CO的质量分数是________,混合气体的平均相对分子质量是________。
15.同温同压下,同质量的X、Y两种气体,相对分子质量分别为A、B,则:
(1)X与Y的体积比为________,分子个数比为________,密度比为________。
(2)同温同压下的X、Y两种气体体积相同,则X与Y的质量比为________,物质的量比为________。
16.现有14.4
g
CO和CO2的混合气体,在标准状况下其体积为8.96
L。回答下列问题:
(1)该混合气体的平均摩尔质量为________。
(2)混合气体中碳原子的个数为________(用NA表示阿伏加德罗常数的值)。
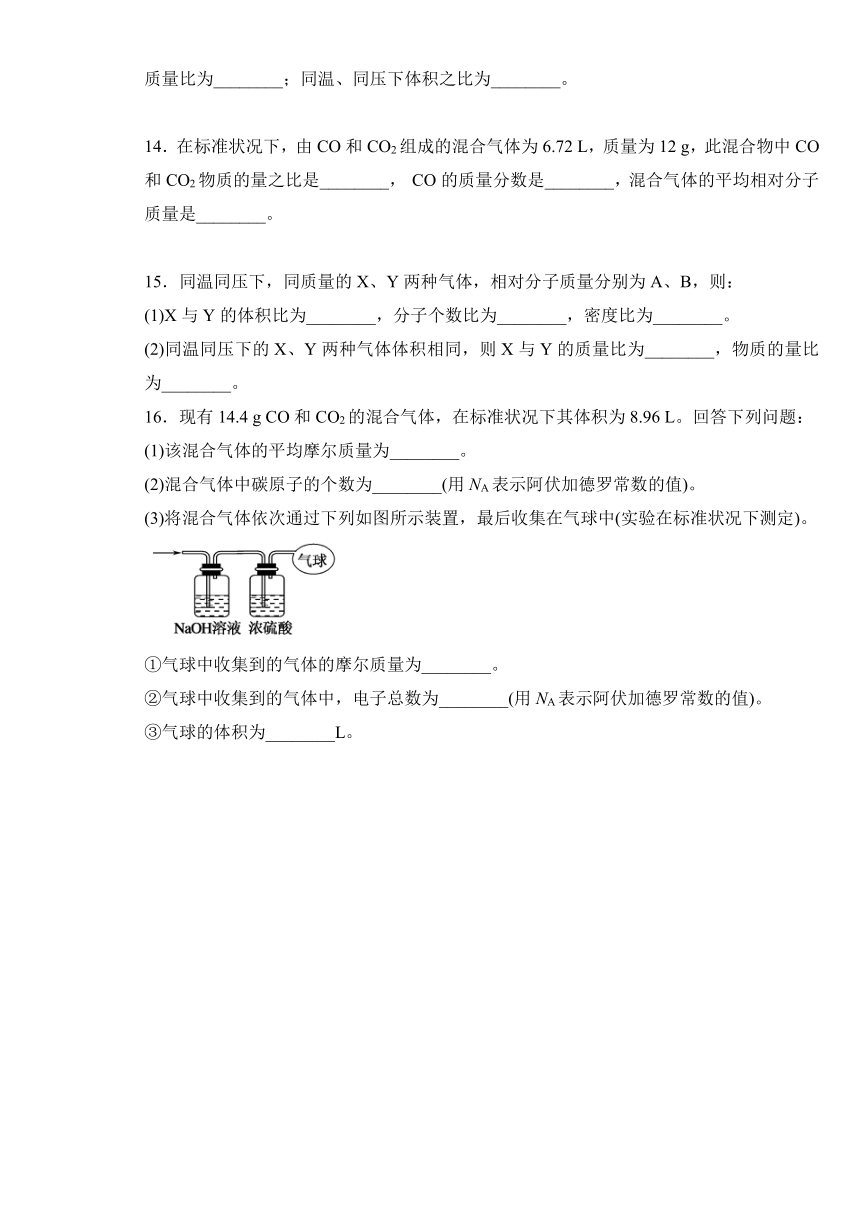
(3)将混合气体依次通过下列如图所示装置,最后收集在气球中(实验在标准状况下测定)。
①气球中收集到的气体的摩尔质量为________。
②气球中收集到的气体中,电子总数为________(用NA表示阿伏加德罗常数的值)。
③气球的体积为________L。
人教版必修一第一章第二节第二课时
气体摩尔体积
参考答案及解析
1.
【答案】C
【解析】溶解度的单位为g。
【题型】选择题
【难度】容易
2.
【答案】B
【解析】A未指明气体所处的状况;C未指明压强;D未指明温度,气体摩尔体积同时受温度和压强的影响,故A、C、D都不正确。
【题型】选择题
【难度】容易
3.
【答案】D
【解析】四种物质的物质的量分别为:1mol、1mol、2mol、3mol,且硫酸为液态,故体积最大的为D项。
【题型】选择题
【难度】容易
4.
【答案】B
【解析】N2的相对分子质量为28,O2的相对分子质量为32,根据平均值规律,空气的平均相对分子质量应大于28,小于32。
【题型】选择题
【难度】一般
5.
【答案】C
【解析】根据N=n·NA知,若N相同,则n相同。A项,1
g
H2为0.5
mol,8
g
O2为0.25
mol,故分子数不相同;B项,未指明是标准状况,2.24
L
He不一定是0.1
mol,;C项,温度相同,压强相同,体积相同,分子数一定相同;D项,28
g
CO的物质的量为1
mol,而6.02×1022个CO的物质的量为0.1
mol,两者分子数不相同。
【题型】选择题
【难度】容易
6.
【答案】B
【解析】n(O2)×2=n(NH3)×4,故n(O2)∶n(NH3)=2∶1,=,故选B。
【题型】选择题
【难度】一般
7.
【答案】BD
【解析】A项,==;B项,==;C项,条件不同无法比较;D项正确。
【题型】选择题
【难度】一般
8.
【答案】B
【解析】据质量守恒定律可知,若反应前为2
mol
A分解,则反应后生成5
mol混合气体,则2MA=5=5×2a,MA=5a。
【题型】选择题
【难度】一般
9.
【答案】B
【解析】气体的分子间距离较大,一定温度和一定压强下,气体的体积由分子数多少决定,故A项错误,B项正确;气体摩尔体积是指1
mol
任何气体在一定温度和压强下所占的体积,22.4
L是标准状况下的气体摩尔体积,故C项错误;气体的分子数与气体的体积,所处的温度、压强有关,体积不同。若温度、压强不同,则分子数有可能相同,故D项错误。
【题型】选择题
【难度】一般
10.
【答案】A
【解析】同温同压下,相同体积的气体所含分子数相等,由于H2、Cl2、HCl都是双原子分子,故它们所含原子数也相等。两种气体的而相对分子质量不一定相同,则质量不一定相同,密度不一定相同,B、C、D项错误。
【题型】选择题
【难度】容易
11.
【答案】C
【解析】同温、同压、相同体积的气体具有相同的物质的量,其质量的大小与四种气体的摩尔质量成正比,C项正确
【题型】选择题
【难度】容易
12.
【答案】A
【解析】反应的化学方程式为A2+3B2=2C,根据质量守恒定律可知:C的化学式为AB3,A项正确。
【题型】选择题
【难度】容易
13.
【答案】1∶1∶1 7∶11∶16 1∶1∶1
【解析】三种气体的物质的量相同,则分子个数相同,即分子个数之比为1∶1∶1;质量之比为摩尔质量之比,为7∶11∶16;同温同压同物质的量的气体具有相同的体积,即体积比为1∶1∶1
【题型】填空题
【难度】容易
14.
【答案】1∶3 17.5% 40
【解析】气体的总物质的量为n=V/Vm=6.72
L/22.4
L/mol=0.3mol,所以n(CO)+n(CO2)=0.3
mol;n(CO)·28
g/mol+n(CO2)·44
g/mol=12
g,求得n(CO)=0.075
mol,n(CO2)=0.225
mol。CO的质量分数为,
【题型】填空题
【难度】一般
15.
【答案】(1)B∶A B∶A A∶B
【解析】由pV=nRT可得出结论:气体体积比等于物质的量之比,等于气体分子个数比,进而可推导出结果。
(2)A∶B 1∶1
【题型】填空题
【难度】一般
16.
【答案】(1)36
g·mol-1 (2)0.4NA (3)①28
g·mol-1 ②2.8NA ③4.48
【解析】(1)混合气体的物质的量为=0.4
mol,混合气体的平均摩尔质量
==36
g·mol-1。(2)0.4
mol
CO和CO2的混合气体中,碳原子为0.4
mol。(3)①将混合气体依次通过NaOH溶液和浓硫酸,则最后收集到的气体是CO。②设原混合气体中CO的物质的量为n1,CO2的物质的量为n2。,解得,因此气球中收集到0.2
mol
CO,含有2.8
mol电子。③0.2
mol
CO在标准状况下的体积为4.48
L。
【题型】填空题
【难度】较难
人教版必修一第一章第二节第二课时
气体摩尔体积
一、选择题
1.下列有关物理量相应的单位表达错误的是( )
A.
摩尔质量g/mol
B.
气体摩尔体积L/mol
C.
溶解度g/100g
D.
密度g/cm3
2.下列说法正确的是( )
A.1
mol任何气体的体积都是22.4
L
B.在标准状况下,某气体的体积为22.4
L,则该气体的物质的量为1
mol,所含的分子数目约为6.02×1023
C.当温度高于0
℃时,一定量任何气体的体积都大于22.4
L
D.当压强大于101
kPa时,1
mol任何气体的体积都小于22.4
L
3.标准状况下,下列物质占体积最大的是( )
A.98
g
H2SO4
B.6.02×1023个CO2
C.44.8
L
HCl
D.6
g
H2
4.空气可近似认为N2和O2按体积比为4∶1组成的混合气体,则空气的平均相对分子质量约为( )
A.28
B.29
C.32
D.60
5.下列各组物质中,所含分子数一定相同的是( )
A.1
g
H2和8
g
O2
B.0.1
mol
HCl和2.24
L
He
C.150
℃、1.01×105
Pa时,18
L
H2O和18
L
CO2
D.常温常压下,28
g
CO和6.02×1022个CO分子
6.在同温、同压下,A容器中的氧气和B容器中的氨气所含的原子个数相同,则A、B两容器中气体体积之比为( )
A.1∶2
B.2∶1
C.2∶3
D.3∶2
7.(双选题)关于m
g
H2和n
g
He的下列说法正确的是( )
A.同温同压下,H2和He的体积比为m∶2n
B.同温同压下,若m=n,则H2与He的物质的量比为2∶1
C.体积相同时,He的质量一定大于H2
D.同温同压下,若二者的物质的量相等,其体积也相等
8.某物质在一定条件下加热分解,产物都是气体。分解方程式为:2AB+2C+2D。测得生成的混合气体的平均相对分子质量为2a,则A的相对分子质量为( )
A.7a
B.5a
C.2.5a
D.2a
9.下列叙述正确的是( )
A.一定温度、压强下,气体体积由其分子的大小决定
B.一定温度、压强下,气体体积由气体的物质的量的多少决定
C.气体摩尔体积是指1
mol
任何气体所占的体积为
22.4
L
D.不同的气体,若体积不等,则它们所含的分子数一定不相等
10.在两个容积相同的容器中,一个盛装氯化氢气体,另一个盛装氢气和氯气的混合气体。在同温同压下,两容器内的气体一定具有相同的( )
A.原子数
B.密度
C.质量
D.相对分子质量
11.在相同的温度和压强下,4个容积相同的容器中分别装有4种气体:a.CO2;b.O2;
c.N2;d.CH4。则4个容器中气体的质量由大到小的顺序是( )
A.c>d>b>a
B.b>a>d>c
C.a>b>c>d
D.d>c>a>b
12.在一定温度和压强下,1体积的A2气体和3体积的B2气体化合成2体积的C气体,则C的化学式为( )
A.AB3
B.AB
C.A3B
D.A2B3
二、非选择题
13.N2、CO2、SO2三种气体的物质的量比为1∶1∶1时,它们的分子个数比为________;质量比为________;同温、同压下体积之比为________。
14.在标准状况下,由CO和CO2组成的混合气体为6.72
L,质量为12
g,此混合物中CO和CO2物质的量之比是________,
CO的质量分数是________,混合气体的平均相对分子质量是________。
15.同温同压下,同质量的X、Y两种气体,相对分子质量分别为A、B,则:
(1)X与Y的体积比为________,分子个数比为________,密度比为________。
(2)同温同压下的X、Y两种气体体积相同,则X与Y的质量比为________,物质的量比为________。
16.现有14.4
g
CO和CO2的混合气体,在标准状况下其体积为8.96
L。回答下列问题:
(1)该混合气体的平均摩尔质量为________。
(2)混合气体中碳原子的个数为________(用NA表示阿伏加德罗常数的值)。
(3)将混合气体依次通过下列如图所示装置,最后收集在气球中(实验在标准状况下测定)。
①气球中收集到的气体的摩尔质量为________。
②气球中收集到的气体中,电子总数为________(用NA表示阿伏加德罗常数的值)。
③气球的体积为________L。
人教版必修一第一章第二节第二课时
气体摩尔体积
参考答案及解析
1.
【答案】C
【解析】溶解度的单位为g。
【题型】选择题
【难度】容易
2.
【答案】B
【解析】A未指明气体所处的状况;C未指明压强;D未指明温度,气体摩尔体积同时受温度和压强的影响,故A、C、D都不正确。
【题型】选择题
【难度】容易
3.
【答案】D
【解析】四种物质的物质的量分别为:1mol、1mol、2mol、3mol,且硫酸为液态,故体积最大的为D项。
【题型】选择题
【难度】容易
4.
【答案】B
【解析】N2的相对分子质量为28,O2的相对分子质量为32,根据平均值规律,空气的平均相对分子质量应大于28,小于32。
【题型】选择题
【难度】一般
5.
【答案】C
【解析】根据N=n·NA知,若N相同,则n相同。A项,1
g
H2为0.5
mol,8
g
O2为0.25
mol,故分子数不相同;B项,未指明是标准状况,2.24
L
He不一定是0.1
mol,;C项,温度相同,压强相同,体积相同,分子数一定相同;D项,28
g
CO的物质的量为1
mol,而6.02×1022个CO的物质的量为0.1
mol,两者分子数不相同。
【题型】选择题
【难度】容易
6.
【答案】B
【解析】n(O2)×2=n(NH3)×4,故n(O2)∶n(NH3)=2∶1,=,故选B。
【题型】选择题
【难度】一般
7.
【答案】BD
【解析】A项,==;B项,==;C项,条件不同无法比较;D项正确。
【题型】选择题
【难度】一般
8.
【答案】B
【解析】据质量守恒定律可知,若反应前为2
mol
A分解,则反应后生成5
mol混合气体,则2MA=5=5×2a,MA=5a。
【题型】选择题
【难度】一般
9.
【答案】B
【解析】气体的分子间距离较大,一定温度和一定压强下,气体的体积由分子数多少决定,故A项错误,B项正确;气体摩尔体积是指1
mol
任何气体在一定温度和压强下所占的体积,22.4
L是标准状况下的气体摩尔体积,故C项错误;气体的分子数与气体的体积,所处的温度、压强有关,体积不同。若温度、压强不同,则分子数有可能相同,故D项错误。
【题型】选择题
【难度】一般
10.
【答案】A
【解析】同温同压下,相同体积的气体所含分子数相等,由于H2、Cl2、HCl都是双原子分子,故它们所含原子数也相等。两种气体的而相对分子质量不一定相同,则质量不一定相同,密度不一定相同,B、C、D项错误。
【题型】选择题
【难度】容易
11.
【答案】C
【解析】同温、同压、相同体积的气体具有相同的物质的量,其质量的大小与四种气体的摩尔质量成正比,C项正确
【题型】选择题
【难度】容易
12.
【答案】A
【解析】反应的化学方程式为A2+3B2=2C,根据质量守恒定律可知:C的化学式为AB3,A项正确。
【题型】选择题
【难度】容易
13.
【答案】1∶1∶1 7∶11∶16 1∶1∶1
【解析】三种气体的物质的量相同,则分子个数相同,即分子个数之比为1∶1∶1;质量之比为摩尔质量之比,为7∶11∶16;同温同压同物质的量的气体具有相同的体积,即体积比为1∶1∶1
【题型】填空题
【难度】容易
14.
【答案】1∶3 17.5% 40
【解析】气体的总物质的量为n=V/Vm=6.72
L/22.4
L/mol=0.3mol,所以n(CO)+n(CO2)=0.3
mol;n(CO)·28
g/mol+n(CO2)·44
g/mol=12
g,求得n(CO)=0.075
mol,n(CO2)=0.225
mol。CO的质量分数为,
【题型】填空题
【难度】一般
15.
【答案】(1)B∶A B∶A A∶B
【解析】由pV=nRT可得出结论:气体体积比等于物质的量之比,等于气体分子个数比,进而可推导出结果。
(2)A∶B 1∶1
【题型】填空题
【难度】一般
16.
【答案】(1)36
g·mol-1 (2)0.4NA (3)①28
g·mol-1 ②2.8NA ③4.48
【解析】(1)混合气体的物质的量为=0.4
mol,混合气体的平均摩尔质量
==36
g·mol-1。(2)0.4
mol
CO和CO2的混合气体中,碳原子为0.4
mol。(3)①将混合气体依次通过NaOH溶液和浓硫酸,则最后收集到的气体是CO。②设原混合气体中CO的物质的量为n1,CO2的物质的量为n2。,解得,因此气球中收集到0.2
mol
CO,含有2.8
mol电子。③0.2
mol
CO在标准状况下的体积为4.48
L。
【题型】填空题
【难度】较难
