3.3物质组成的表示 课件(40张PPT)
文档属性
| 名称 | 3.3物质组成的表示 课件(40张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 4.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-12-02 16:11:25 | ||
图片预览










文档简介
课件40张PPT。物质组成的表示 1.下列物质你们都较熟悉,请写出它们的化学符号:
①氧气______;②氮气______;③二氧化碳______;
④水______;⑤氧化铜______;
⑥一氧化碳______;⑦甲烷______;⑧氨气______。
提示:①O2 ②N2 ③CO2 ④H2O
⑤CuO ⑥CO ⑦CH4 ⑧NH32.指出下列符号的意义:
①H:_______________________________________________;
②2O:______________________________________________;
③Na+:_____________________________________________;
④3H+:_____________________________________________。
提示:①氢元素或1个氢原子 ②2个氧原子
③钠离子带一个单位的正电荷 ④3个氢离子3.请说出下列物质的构成:①水 ②金 ③氯化钠
提示:①水由水分子构成;②金由金原子构成;③氯化钠由氯离子和钠离子构成。【探究主题一】化学式及其意义
阅读教材标题一内容,并将下列空白处填写完整:
1.概念:用元素符号和数字表示__________的式子。
2.作用:任何纯净物都有___________,都可以用化学式来表示
其组成。
例如:金属铜由_______构成,化学式为___;食盐由_________
_______聚集而成,化学式为_______,水由水分子聚集而成,
化学式为_____。物质组成固定的组成铜原子Cu氯离子和钠离子NaClH2O3.化学式的意义
(1)表示___________。
(2)表示__________________。
(3)表示各元素的原子或离子之间的数量关系。
注意:由分子构成的物质,还表示该物质的1个分子。
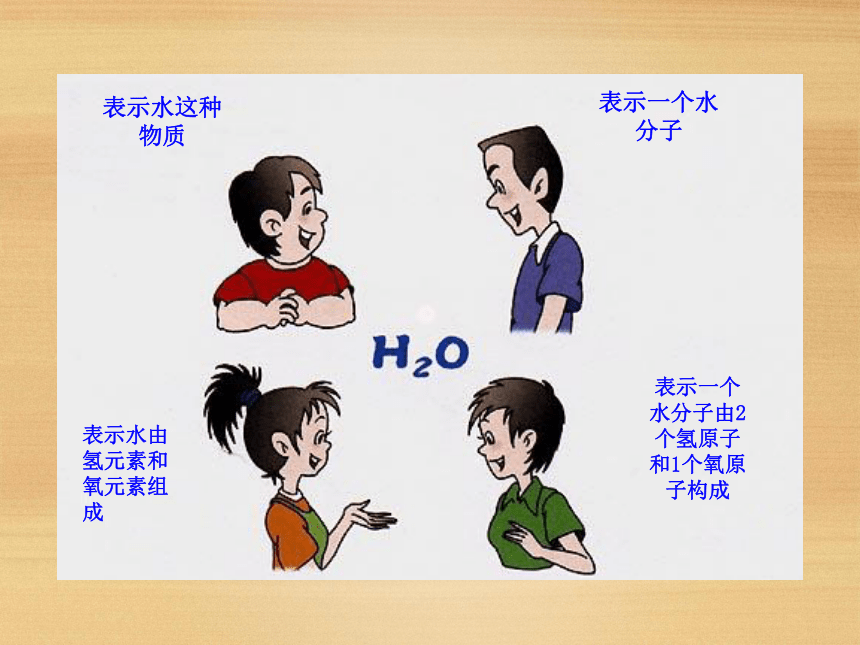
这种物质这种物质的组成元素表示水这种物质表示水由氢元素和氧元素组成表示一个水分子由2个氢原子和1个氧原子构成表示一个水分子注意:若化学式前加数字就只具有微观意义,如2H2O:只表示2个水分子。
4.表示
由分子构成的物质,一般将它们的分子式作为其化学式。在分子式中,元素符号右下角的数字表示每个分子中所含该种原子的数目。水的化学式(H2O)具有的意义:
表示___________
宏观 表示水由________和________组成
H2O
表示____________
微观 表示1个水分子由__________和__________构成水这种物质氢元素氧元素一个水分子2个氢原子1个氧原子2H2O 表示2个水分子
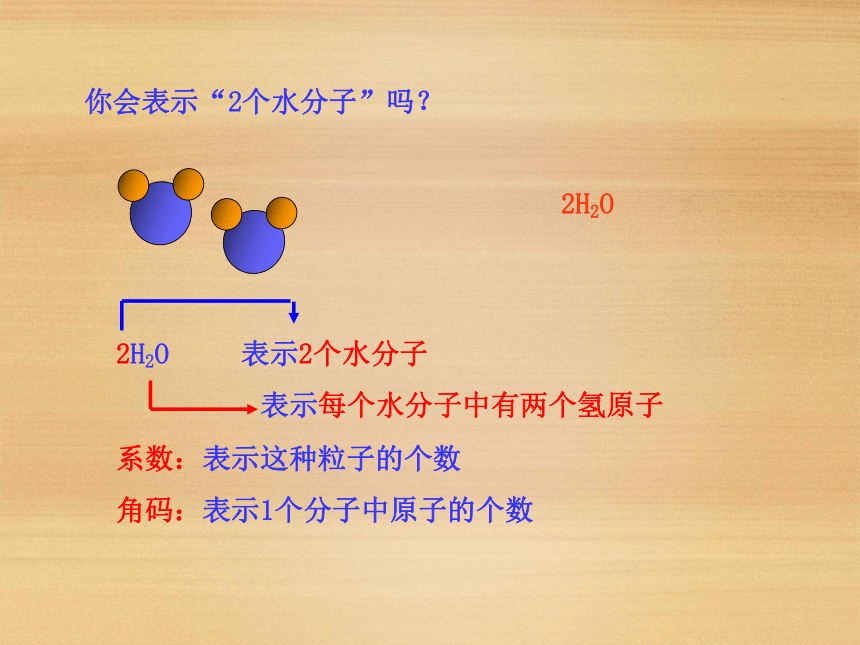
表示每个水分子中有两个氢原子 2H2O你会表示“2个水分子”吗?系数:表示这种粒子的个数
角码:表示1个分子中原子的个数【探究讨论】
1.数字在元素符号周围不同的位置代表不同的含义,你能说出下列符号中“2”的意义吗?
①2H ②2H2O ③2Mg2+提示:元素符号前面的数字表示原子个数,即①中“2”表示2个氢原子;化学式前面的数字表示分子个数,即②中前面的“2”表示2个水分子,化学式中元素符号右下角的数字表示一个分子中含有的这种原子的个数,即②中“H”右下角的数字“2”表示1个水分子中含有2个氢原子;离子符号前面的数字表示离子的个数,即③中前面的“2”表示2个镁离子,元素符号右上角的数字表示每个离子所带电荷数,即③中Mg2+右上角的“2”表示每个镁离子带2个单位的正电荷。2.2011年11月1日,“神舟”八号飞船由“长征”二号火箭顺利发射升空,并实现了与“天宫”一号目标飞行器的完美对接。偏二甲肼是火箭推进器的常用燃料,根据偏二甲肼的化学式C2H6N2,你还知道哪些信息?
提示:应根据化学式表示的意义回答,如偏二甲肼是由碳、氢、氮三种元素组成的;偏二甲肼中碳原子、氢原子和氮原子的个数比为1∶3∶1;一个偏二甲肼分子中含有10个原子等。3.化学式的读法
(1)单质。
一般除稀有气体和双原子分子构成的气体单质在元素名称后加
“气”字外,其余直接读元素的名称。如“O2”读作“____”,
“Fe”读作“___”。
(2)化合物。
由两种元素组成的化合物,其化学式读法与书写顺序相反,
一般读作“某化某”。在读化合物的化学式时,有时要读出
各元素的原子个数,但“1”一般不读出。
比如“CuCl2”读作氯化铜,“P2O5”读作五氧化二磷。氧气铁化学式的读法顺口溜
正确命名化合物,从右向左中文读,
原子个数先读出,其后名称是元素,
中间“化”字来过渡。
原子团的化合物,不读个数是特殊,
“根”字省去不读出,不用“化”字来过渡。
(氢氧根是特殊)【探究主题二】化合价
阅读教材标题二内容,将下列空白处填写完整:
1.元素化合价的确定
化合价可表示原子之间相互化合的比例。
(1)在由离子构成的化合物中,元素的化合价是由这种元素的
______________________________决定的。
例如:钠元素与氯元素化合时一个原子得到或失去电子的数目+1 -1 (2)在依靠共用电子对形成的化合物中,化合价的数值就是_____
__________________。
(3)一种元素可表现多种化合价的原因是原子在不同情况下_____
______或_____________________是不同的。形成共用电子对的数目得失电子形成共用电子对的数目(1)化合价的实质:元素在形成化合物时表现出的化学性质,取决于原子最外层电子数。
(2)化合价是元素原子在形成化合物时表现出的性质,因此,单质分子中元素的化合价为零。
(3)化合价有正价和负价。
(4)在化合物里正负化合价的代数和为零。
(5)化合物中,通常氢为+1价,氧为-2价,金属元素显正价。 2.元素的化合价(6)元素的变价:许多元素的原子在不同的条件下可显示不同的化合价。
例:Cu为+1,+2,Fe为+2(亚铁),+3
(7)熟记原子团的化合价:原子团的化合价是组成元素的化合价的代数和。
(1)原子团:在化学反应中常作为一个整体的原子的集团,又叫根。3.原子团NO3OHSO4CO3NH4-1-1-2-2+1NO3-OH-SO42-CO32-NH4+(2)原子团的符号、化合价和对应的离子符号负一硝酸、氢氧根;负二硫酸、碳酸根;正一价的是铵根。4.化合价与离子符号的关系
如:Mg 和 Mg2++2同种元素的化合价与其离子相比:数值和符号相同,表示方法不同,“标价正上数置后,离子偏右数在前”。5、常见元素化合价的判断规律
(1)在化合物中,金属元素、氢元素表现正价,非金属元素有时
表现正价,有时表现负价。
例如:镁表现___价,铝表现___价,硫可表现为___________价。
(2)在化合物中,各元素的正负化合价的代数和_____。
(3)单质中元素的化合价______。+2+3-2、+4、+6为零为零化合价(顺口溜)
一价氢氯钾钠银,二价氧钙钡镁锌
铜一二、铁二三,铝三硅四要记准
氮磷具有可变价,化学式中来区分(1)确定物质中某元素的化合价的计算步骤题1.试确定氯酸钾中氯元素的化合价先写出化学式KClO3设未知数列等式并求解+1+X+(-2)×3=0答:氯酸钾中氯元素化合价为+5+5X=+5解答解:设KClO3中Cl的化合价为X6.化学式与元素化合价的关系 (2)根据化学式确定元素的化合价: 题2.标出下列物质中各元素的化合价:
①氯化锌 ②金属锌 ③氢氧化钠 ① ZnCl2 ② Zn ③ Na O H+2-10+1-2 +1④ MgO ⑤ K2O ⑥ H2O ⑦ Ca(OH)2+2-2+1-2+1-2+2 -2+1 ④氧化镁 ⑤氧化钾 ⑥水 ⑦ 氢氧化钙(3)根据化合价正确书写化学式
①最小公倍数法(以书写氧化铝化学式为例)
写:正价元素在左,负价元素在右。把化合价标在元素符号的正上方
求:求两种化合价绝对值的最小公倍数,然后求原子个数。最小公倍数原子个数
Al的原子个数=
O原子的个数=
标:将原子个数写在相应元素符号的右下角
验:验证各元素的化合价代数和是否为零
(+3)×2+(-2)×3=0Al2O3 7.书写化学式应注意的问题
(1) ___________写在左边,__________写在右边。
(2)把原子数写在___________。 如果原子数为1,则省略不写。
(3)当____________________的代数和等于零时,化学式才算
正确。
(4)只能写实际存在的物质的化学式。正价元素负价元素元素符号的右下角正价总数与负价总数化学式的书写(顺口溜)
化学式,书写易,化合价态先记忆。
正价前,负价后,这项工作不能漏。
标价数,化最简,十字交叉是关键。
原子团,特殊体,该加括号要牢记。【探究讨论】
1.在化合物中金属元素总显正价,非金属元素总显负价。这种认识是否正确?
提示:不正确。有的化合物中,如非金属元素之间形成的化合物,其中有的非金属元素显正价,否则元素化合价的代数和不为0,如水中氢元素的化合价为+1价。2.同一种元素在不同化合物中的化合价可能不同,是否在同一
种化合物中化合价一定相同?
提示:不一定。同一种元素在不同化合物中的化合价可能不
同,如一氧化碳和二氧化碳中碳元素的化合价分别为+2价和+4
价;同一种元素在同一种化合物中的化合价也可能不同,如硝
酸铵中氮元素的化合价为【探究主题三】物质组成的定量表示
阅读教材标题三内容,将下列空白处填写完整:
1.计算组成物质的各种元素的的质量比
化合物中各元素的质量比=化学式中各原子的相对原子质量×原子个数之比。
如二氧化碳(CO2)中碳元素与氧元素的质量比为:
(______) ∶ (_______)=3∶8
化学式中碳 化学式中氧
原子相对原 原子相对原
子质量之和 子质量之和12×116×22.计算物质中某元素的质量分数
(1)化学式量:某物质化学式中_____________________的总和。对于由分子构成的物质,也叫相对分子质量。
(2)化合物中某元素的质量分数=
如过氧化氢(H2O2)中氢元素的质量分数为各原子的相对原子质量氢原子个数【探究讨论】
相对分子质量是否是分子的质量?
提示:分子的质量等于构成分子的各原子的质量总和,而相对
分子质量是化学式中各原子的相对原子质量的总和,而不是化
学式中各原子的质量的总和,故相对分子质量不是分子的质量,是分子的相对质量,两者的关系为:相对分子质量=【考点一】化学式与化合价
【典例1】(2010·肇庆中考)开封县境内新发现了大型的“钼矿”,金属钼可用于制造火箭、导弹等耐高温材料。如果钼铅矿(PbMoO4)中的铅元素为+2价,则钼元素的化合价为( )
A.+2 B.+3 C.+4 D.+6
【我的记录空间】选D。设钼元素的化合价为x,根据在化合物中正负化合价的代数和为零,则有(+2)+x+(-2)×4=0,解得x=+6。【拓展归纳】
1.根据化学式求其中某元素的化合价
可按如下步骤完成:设出变价元素的化合价,利用不变价元素的化合价,求出变价元素的化合价。例如:求氯酸钾(KClO3)中氯元素的化合价。设氯酸钾中氯元素的化合价为x。已知氯酸钾中钾、氧两元素的化合价分别为+1和-2,则(+1)+x+(-2)×3
=0,x=+5。
2.化学式、元素符号周围小数字表示的意义
(1)原子可直接用元素符号表示,元素符号前的数字,表示该原子的个数。例如:“3Cu”表示三个铜原子。(2)化学式前面的数字表示其粒子的个数。例如:“4H2O”只具
有微观意义,表示四个水分子。
(3)化学式中元素符号右下角的数字,表示该物质一个分子中含
该原子的个数。例如:“N2”中的“2”表示一个氮气分子中含
有两个氮原子。
(4)离子符号在元素符号的右上角,先标出电荷数,再标出电
性,电荷数是1时,可省略不写。例如:“Mg2+”中“2”的意义
是一个镁离子带两个单位正电荷。
(5)化合价标在元素符号正上方,正、负号在前,数值在后。例
如:“ ”表示水中氢元素表现+1价,氧元素表现-2价。【考点二】有关化学式的计算
【典例2】(2010·汕头中考)如图是某品牌补铁剂的标签。请回答:富马酸亚铁颗粒
化学式:C4H2FeO4
每包含富马酸亚铁0.2 g
适应症:缺铁性贫血。
服用量:每次1包~2包(成人),
……(1)富马酸亚铁中含有______种元素, C、H、Fe、O原子个数比
为______。
(2)富马酸亚铁的相对分子质量为______。
(3)若每次服用1包该补铁剂,摄入铁元素的质量为______mg(计
算结果取整数)。【我的记录空间】(1)富马酸亚铁由C、H、Fe、O四种元素组
成;每个C4H2FeO4分子含有4个碳原子、2个氢原子、1个铁原
子、4个氧原子,其原子个数比为4∶2∶1∶4。(2)富马酸亚
铁的相对分子质量=12×4+1×2+56+16×4=170。(3)1包该补
铁剂含铁元素的质量= ×100%×0.2 g=0.066 g=66 mg。
答案: (1)4 4∶2∶1∶4 (2)170 (3)66【规律方法】有关化学式的计算
1.计算相对分子质量时,同种原子的相对原子质量与其原子个数之间用“×”,不同原子的相对原子质量之间用“+”;化学式中有括号时,括号内的各元素的相对原子质量相加之后再乘以括号外面的数字。
2.计算化合物中各元素的质量比时,一定要注意:元素的种类与各元素的原子个数比的顺序要对应。
3.化合物中某元素的质量=化合物的质量×该元素在此化合物中的质量分数。4.在混合物中化合物的质量分数(纯度)=混合物中某元素的质量分数÷化合物中该元素的质量分数。
5.在混合物中某元素的质量分数=含该元素的化合物的质量分数(纯度)×该元素在化合物中的质量分数。
①氧气______;②氮气______;③二氧化碳______;
④水______;⑤氧化铜______;
⑥一氧化碳______;⑦甲烷______;⑧氨气______。
提示:①O2 ②N2 ③CO2 ④H2O
⑤CuO ⑥CO ⑦CH4 ⑧NH32.指出下列符号的意义:
①H:_______________________________________________;
②2O:______________________________________________;
③Na+:_____________________________________________;
④3H+:_____________________________________________。
提示:①氢元素或1个氢原子 ②2个氧原子
③钠离子带一个单位的正电荷 ④3个氢离子3.请说出下列物质的构成:①水 ②金 ③氯化钠
提示:①水由水分子构成;②金由金原子构成;③氯化钠由氯离子和钠离子构成。【探究主题一】化学式及其意义
阅读教材标题一内容,并将下列空白处填写完整:
1.概念:用元素符号和数字表示__________的式子。
2.作用:任何纯净物都有___________,都可以用化学式来表示
其组成。
例如:金属铜由_______构成,化学式为___;食盐由_________
_______聚集而成,化学式为_______,水由水分子聚集而成,
化学式为_____。物质组成固定的组成铜原子Cu氯离子和钠离子NaClH2O3.化学式的意义
(1)表示___________。
(2)表示__________________。
(3)表示各元素的原子或离子之间的数量关系。
注意:由分子构成的物质,还表示该物质的1个分子。
这种物质这种物质的组成元素表示水这种物质表示水由氢元素和氧元素组成表示一个水分子由2个氢原子和1个氧原子构成表示一个水分子注意:若化学式前加数字就只具有微观意义,如2H2O:只表示2个水分子。
4.表示
由分子构成的物质,一般将它们的分子式作为其化学式。在分子式中,元素符号右下角的数字表示每个分子中所含该种原子的数目。水的化学式(H2O)具有的意义:
表示___________
宏观 表示水由________和________组成
H2O
表示____________
微观 表示1个水分子由__________和__________构成水这种物质氢元素氧元素一个水分子2个氢原子1个氧原子2H2O 表示2个水分子
表示每个水分子中有两个氢原子 2H2O你会表示“2个水分子”吗?系数:表示这种粒子的个数
角码:表示1个分子中原子的个数【探究讨论】
1.数字在元素符号周围不同的位置代表不同的含义,你能说出下列符号中“2”的意义吗?
①2H ②2H2O ③2Mg2+提示:元素符号前面的数字表示原子个数,即①中“2”表示2个氢原子;化学式前面的数字表示分子个数,即②中前面的“2”表示2个水分子,化学式中元素符号右下角的数字表示一个分子中含有的这种原子的个数,即②中“H”右下角的数字“2”表示1个水分子中含有2个氢原子;离子符号前面的数字表示离子的个数,即③中前面的“2”表示2个镁离子,元素符号右上角的数字表示每个离子所带电荷数,即③中Mg2+右上角的“2”表示每个镁离子带2个单位的正电荷。2.2011年11月1日,“神舟”八号飞船由“长征”二号火箭顺利发射升空,并实现了与“天宫”一号目标飞行器的完美对接。偏二甲肼是火箭推进器的常用燃料,根据偏二甲肼的化学式C2H6N2,你还知道哪些信息?
提示:应根据化学式表示的意义回答,如偏二甲肼是由碳、氢、氮三种元素组成的;偏二甲肼中碳原子、氢原子和氮原子的个数比为1∶3∶1;一个偏二甲肼分子中含有10个原子等。3.化学式的读法
(1)单质。
一般除稀有气体和双原子分子构成的气体单质在元素名称后加
“气”字外,其余直接读元素的名称。如“O2”读作“____”,
“Fe”读作“___”。
(2)化合物。
由两种元素组成的化合物,其化学式读法与书写顺序相反,
一般读作“某化某”。在读化合物的化学式时,有时要读出
各元素的原子个数,但“1”一般不读出。
比如“CuCl2”读作氯化铜,“P2O5”读作五氧化二磷。氧气铁化学式的读法顺口溜
正确命名化合物,从右向左中文读,
原子个数先读出,其后名称是元素,
中间“化”字来过渡。
原子团的化合物,不读个数是特殊,
“根”字省去不读出,不用“化”字来过渡。
(氢氧根是特殊)【探究主题二】化合价
阅读教材标题二内容,将下列空白处填写完整:
1.元素化合价的确定
化合价可表示原子之间相互化合的比例。
(1)在由离子构成的化合物中,元素的化合价是由这种元素的
______________________________决定的。
例如:钠元素与氯元素化合时一个原子得到或失去电子的数目+1 -1 (2)在依靠共用电子对形成的化合物中,化合价的数值就是_____
__________________。
(3)一种元素可表现多种化合价的原因是原子在不同情况下_____
______或_____________________是不同的。形成共用电子对的数目得失电子形成共用电子对的数目(1)化合价的实质:元素在形成化合物时表现出的化学性质,取决于原子最外层电子数。
(2)化合价是元素原子在形成化合物时表现出的性质,因此,单质分子中元素的化合价为零。
(3)化合价有正价和负价。
(4)在化合物里正负化合价的代数和为零。
(5)化合物中,通常氢为+1价,氧为-2价,金属元素显正价。 2.元素的化合价(6)元素的变价:许多元素的原子在不同的条件下可显示不同的化合价。
例:Cu为+1,+2,Fe为+2(亚铁),+3
(7)熟记原子团的化合价:原子团的化合价是组成元素的化合价的代数和。
(1)原子团:在化学反应中常作为一个整体的原子的集团,又叫根。3.原子团NO3OHSO4CO3NH4-1-1-2-2+1NO3-OH-SO42-CO32-NH4+(2)原子团的符号、化合价和对应的离子符号负一硝酸、氢氧根;负二硫酸、碳酸根;正一价的是铵根。4.化合价与离子符号的关系
如:Mg 和 Mg2++2同种元素的化合价与其离子相比:数值和符号相同,表示方法不同,“标价正上数置后,离子偏右数在前”。5、常见元素化合价的判断规律
(1)在化合物中,金属元素、氢元素表现正价,非金属元素有时
表现正价,有时表现负价。
例如:镁表现___价,铝表现___价,硫可表现为___________价。
(2)在化合物中,各元素的正负化合价的代数和_____。
(3)单质中元素的化合价______。+2+3-2、+4、+6为零为零化合价(顺口溜)
一价氢氯钾钠银,二价氧钙钡镁锌
铜一二、铁二三,铝三硅四要记准
氮磷具有可变价,化学式中来区分(1)确定物质中某元素的化合价的计算步骤题1.试确定氯酸钾中氯元素的化合价先写出化学式KClO3设未知数列等式并求解+1+X+(-2)×3=0答:氯酸钾中氯元素化合价为+5+5X=+5解答解:设KClO3中Cl的化合价为X6.化学式与元素化合价的关系 (2)根据化学式确定元素的化合价: 题2.标出下列物质中各元素的化合价:
①氯化锌 ②金属锌 ③氢氧化钠 ① ZnCl2 ② Zn ③ Na O H+2-10+1-2 +1④ MgO ⑤ K2O ⑥ H2O ⑦ Ca(OH)2+2-2+1-2+1-2+2 -2+1 ④氧化镁 ⑤氧化钾 ⑥水 ⑦ 氢氧化钙(3)根据化合价正确书写化学式
①最小公倍数法(以书写氧化铝化学式为例)
写:正价元素在左,负价元素在右。把化合价标在元素符号的正上方
求:求两种化合价绝对值的最小公倍数,然后求原子个数。最小公倍数原子个数
Al的原子个数=
O原子的个数=
标:将原子个数写在相应元素符号的右下角
验:验证各元素的化合价代数和是否为零
(+3)×2+(-2)×3=0Al2O3 7.书写化学式应注意的问题
(1) ___________写在左边,__________写在右边。
(2)把原子数写在___________。 如果原子数为1,则省略不写。
(3)当____________________的代数和等于零时,化学式才算
正确。
(4)只能写实际存在的物质的化学式。正价元素负价元素元素符号的右下角正价总数与负价总数化学式的书写(顺口溜)
化学式,书写易,化合价态先记忆。
正价前,负价后,这项工作不能漏。
标价数,化最简,十字交叉是关键。
原子团,特殊体,该加括号要牢记。【探究讨论】
1.在化合物中金属元素总显正价,非金属元素总显负价。这种认识是否正确?
提示:不正确。有的化合物中,如非金属元素之间形成的化合物,其中有的非金属元素显正价,否则元素化合价的代数和不为0,如水中氢元素的化合价为+1价。2.同一种元素在不同化合物中的化合价可能不同,是否在同一
种化合物中化合价一定相同?
提示:不一定。同一种元素在不同化合物中的化合价可能不
同,如一氧化碳和二氧化碳中碳元素的化合价分别为+2价和+4
价;同一种元素在同一种化合物中的化合价也可能不同,如硝
酸铵中氮元素的化合价为【探究主题三】物质组成的定量表示
阅读教材标题三内容,将下列空白处填写完整:
1.计算组成物质的各种元素的的质量比
化合物中各元素的质量比=化学式中各原子的相对原子质量×原子个数之比。
如二氧化碳(CO2)中碳元素与氧元素的质量比为:
(______) ∶ (_______)=3∶8
化学式中碳 化学式中氧
原子相对原 原子相对原
子质量之和 子质量之和12×116×22.计算物质中某元素的质量分数
(1)化学式量:某物质化学式中_____________________的总和。对于由分子构成的物质,也叫相对分子质量。
(2)化合物中某元素的质量分数=
如过氧化氢(H2O2)中氢元素的质量分数为各原子的相对原子质量氢原子个数【探究讨论】
相对分子质量是否是分子的质量?
提示:分子的质量等于构成分子的各原子的质量总和,而相对
分子质量是化学式中各原子的相对原子质量的总和,而不是化
学式中各原子的质量的总和,故相对分子质量不是分子的质量,是分子的相对质量,两者的关系为:相对分子质量=【考点一】化学式与化合价
【典例1】(2010·肇庆中考)开封县境内新发现了大型的“钼矿”,金属钼可用于制造火箭、导弹等耐高温材料。如果钼铅矿(PbMoO4)中的铅元素为+2价,则钼元素的化合价为( )
A.+2 B.+3 C.+4 D.+6
【我的记录空间】选D。设钼元素的化合价为x,根据在化合物中正负化合价的代数和为零,则有(+2)+x+(-2)×4=0,解得x=+6。【拓展归纳】
1.根据化学式求其中某元素的化合价
可按如下步骤完成:设出变价元素的化合价,利用不变价元素的化合价,求出变价元素的化合价。例如:求氯酸钾(KClO3)中氯元素的化合价。设氯酸钾中氯元素的化合价为x。已知氯酸钾中钾、氧两元素的化合价分别为+1和-2,则(+1)+x+(-2)×3
=0,x=+5。
2.化学式、元素符号周围小数字表示的意义
(1)原子可直接用元素符号表示,元素符号前的数字,表示该原子的个数。例如:“3Cu”表示三个铜原子。(2)化学式前面的数字表示其粒子的个数。例如:“4H2O”只具
有微观意义,表示四个水分子。
(3)化学式中元素符号右下角的数字,表示该物质一个分子中含
该原子的个数。例如:“N2”中的“2”表示一个氮气分子中含
有两个氮原子。
(4)离子符号在元素符号的右上角,先标出电荷数,再标出电
性,电荷数是1时,可省略不写。例如:“Mg2+”中“2”的意义
是一个镁离子带两个单位正电荷。
(5)化合价标在元素符号正上方,正、负号在前,数值在后。例
如:“ ”表示水中氢元素表现+1价,氧元素表现-2价。【考点二】有关化学式的计算
【典例2】(2010·汕头中考)如图是某品牌补铁剂的标签。请回答:富马酸亚铁颗粒
化学式:C4H2FeO4
每包含富马酸亚铁0.2 g
适应症:缺铁性贫血。
服用量:每次1包~2包(成人),
……(1)富马酸亚铁中含有______种元素, C、H、Fe、O原子个数比
为______。
(2)富马酸亚铁的相对分子质量为______。
(3)若每次服用1包该补铁剂,摄入铁元素的质量为______mg(计
算结果取整数)。【我的记录空间】(1)富马酸亚铁由C、H、Fe、O四种元素组
成;每个C4H2FeO4分子含有4个碳原子、2个氢原子、1个铁原
子、4个氧原子,其原子个数比为4∶2∶1∶4。(2)富马酸亚
铁的相对分子质量=12×4+1×2+56+16×4=170。(3)1包该补
铁剂含铁元素的质量= ×100%×0.2 g=0.066 g=66 mg。
答案: (1)4 4∶2∶1∶4 (2)170 (3)66【规律方法】有关化学式的计算
1.计算相对分子质量时,同种原子的相对原子质量与其原子个数之间用“×”,不同原子的相对原子质量之间用“+”;化学式中有括号时,括号内的各元素的相对原子质量相加之后再乘以括号外面的数字。
2.计算化合物中各元素的质量比时,一定要注意:元素的种类与各元素的原子个数比的顺序要对应。
3.化合物中某元素的质量=化合物的质量×该元素在此化合物中的质量分数。4.在混合物中化合物的质量分数(纯度)=混合物中某元素的质量分数÷化合物中该元素的质量分数。
5.在混合物中某元素的质量分数=含该元素的化合物的质量分数(纯度)×该元素在化合物中的质量分数。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
