7溶液复习 课件
图片预览










文档简介
课件35张PPT。阶段复习课
第七单元主题一 溶液的形成
【主题训练1】关于溶液和乳化的下列说法错误的是( )
A.溶液中可以含有多种溶质
B.溶液是均一、稳定的混合物
C.用汽油洗去衣服上的油污是乳化现象
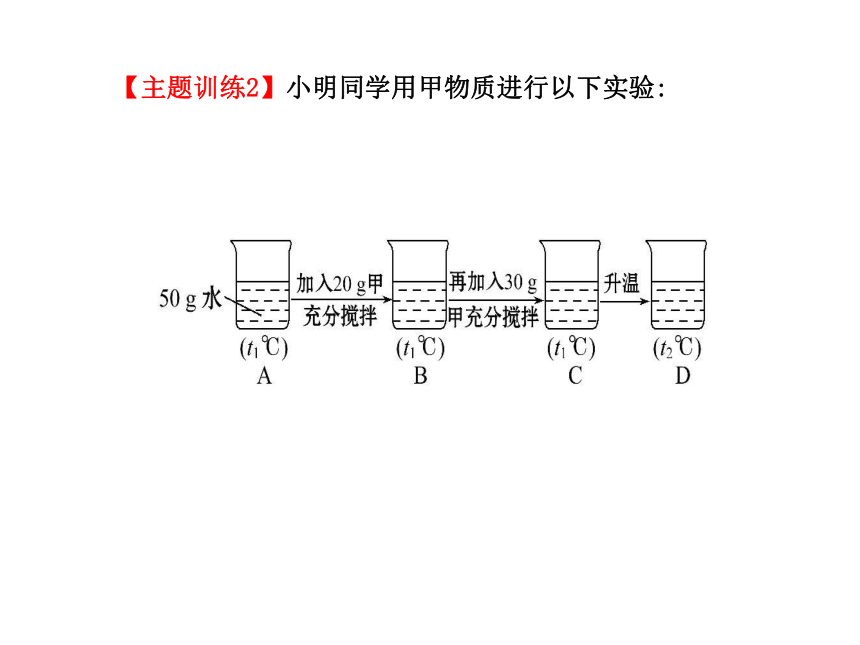
D.溶液不一定是无色的【解析】选C。本题考查学生对溶液和乳化的认知能力。解答本题需明确两点:(1)溶液的概念与特性;(2)乳化现象的发生原理。汽油洗去油污是因为油污溶解在汽油中被除去,故C错误。【主题训练2】小明同学用甲物质进行以下实验:(1)实验过程中,B、C、D对应的溶液为不饱和溶液的是
_____________________________________________。
(2)向B对应的溶液中再加入30 g甲固体的过程中,发现固体全部溶解,D图溶液放置一段时间后又有部分固体析出。你认为“全部溶解”的原因是?? __。【解析】不饱和溶液是指在一定温度下仍能继续溶解溶质的溶液,B中烧杯内含有50 g水和20 g甲物质,加入30 g甲物质后又能溶解,表明B中溶液一定为不饱和溶液,D中溶液中的固体虽全部溶解,但温度发生了变化,能否继续溶解,我们无法得知,故C溶液不一定是不饱和溶液,D中溶液有固体析出,表明此时溶液为t2℃时的饱和溶液,温度之所以发生变化,是因为物质溶解时产生了热量。答案:(1)B
(2)甲物质溶于水时会放出热量,使溶液温度升高【关键点拨】
1.溶解与乳化的比较:2.饱和溶液和不饱和溶液:
(1)概念中的要点:一定温度下;一定量的溶剂;能不能继续溶解溶质。
(2)相互转化(氢氧化钙除外)。
不饱和溶液 饱和溶液【真题体验】
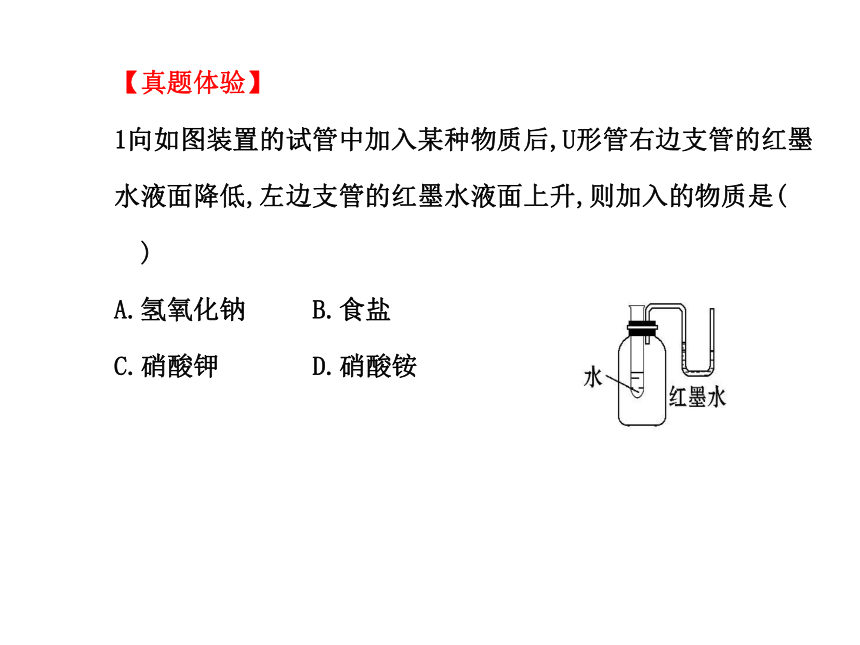
1向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是( )
A.氢氧化钠 B.食盐
C.硝酸钾 D.硝酸铵【解析】选D。本题考查学生对物质溶于水时溶液温度变化的认识。解答本题需明确气体体积受温度的影响变化情况。由题意可知瓶内压强减小,应为瓶内温度降低所致,故而应选硝酸铵。2.溶液对人类的生产、生活都有很重要的意义。下列关于溶液的说法或做法错误的是( )
A.夏天喝的汽水不是溶液
B.蛋汤太咸,加水稀释后口味变淡
C.无色、透明的液体不一定是溶液
D.凉茶水是均一、稳定的混合物【解析】选A。本题主要考查溶液的有关知识。夏天喝的汽水是溶液,是二氧化碳的水溶液,蛋汤稀释后,溶液浓度变小,口味变淡;无色、透明的液体不一定是溶液,如水;凉茶水属于溶液,是均一、稳定的混合物。3.下列说法不正确的是( )
A.溶液都是无色、均一、稳定的液体
B.氯化钠溶液是由钠离子、氯离子和水分子组成的混合物
C.用洗洁精清洗餐具上的油污发生乳化现象
D.用酒精浸泡草药可溶解其中的有效成分【解析】选A。本题考查学生对溶液知识的认识,解答本题的关键应明确3点:(1)溶液的性质和特征;(2)洗洁精洗涤油污的作用原理;(3)除水可以作溶剂外,酒精、汽油等物质也可以作溶剂。A中,溶液一定是均一稳定的混合物,但不一定是无色的;B中,氯化钠溶液是氯化钠固体以钠离子、氯离子的形式扩散到水中形成的,故B正确;C中,用洗洁精清洗油污属于乳化过程;D中,酒精可以作溶剂,溶解某些有机物成分,故D正确。4.配制硝酸钾溶液时得到下表数据,根据表中数据分析,不正确的是( )A.28℃时10克水中最多能溶解硝酸钾4克
B.60℃时等质量水中能溶解的硝酸钾比28℃时多
C.①②所得溶液溶质的质量分数相等
D.③所得溶液一定是硝酸钾的饱和溶液【解析】选D。对比①②可以看出,28℃时10克水中溶解了硝酸钾4克时,再向其中加入硝酸钾不再溶解,因此28℃时10克水中最多能溶解硝酸钾4克,A正确;28℃时10克水中最多能溶解硝酸钾4克,60℃时10克水中能溶解硝酸钾8克,因此60℃时等质量水中能溶解的硝酸钾比28℃时多,B正确;①②中水的质量相同,溶解的硝酸钾的质量相同,因此所得溶液溶质的质量分数相等,C正确;根据表中数据可知,60℃时10克水中溶解了8克硝酸钾,是否还能再溶解无法得知,因此不能判断③所得溶液是否是硝酸钾的饱和溶液,D错误。主题二 溶质质量分数及溶液的配制
【主题训练3】(2013·青岛中考)科学施肥是实现农业增产的重要手段。硝酸铵(NH4NO3)是一种常用的氮肥,其中氮、氢、氧三种元素的质量比为____________。若要配制200 g溶质质量分数为5%的硝酸铵溶液,需要硝酸铵的质量为______g,需要水的质量为______g。【解析】本题考查对有关元素质量比、溶质质量分数的计算。氮、氢、氧三种元素的质量比=(14×2)∶(1×4)∶(16×3)
=7∶1∶12。硝酸铵的质量:200 g×5%=10 g,水的质量:200 g-10 g=190 g。
答案:7∶1∶12 10 190【关键点拨】
1.溶质质量分数公式:
溶质的质量分数= ×100%
= ×100%。2.溶液的配制:
(1)仪器:配制一定溶质质量分数的溶液分为两种情况:一是“固”配“液”,固体需要用托盘天平称量质量;二是“浓”配“稀”,浓溶液的取用需要用量筒量取体积,不需要托盘天平,量筒共用到2次。(2)误差分析。
①所配溶液的溶质质量分数偏大,如量取浓溶液时仰视读数、量取水时俯视读数等。
②所配溶液的溶质质量分数偏小,如称量时“左码右物”并使用游码、量取浓溶液时俯视读数、量取水时仰视读数等。【真题体验】
1.将80 g质量分数为35%的浓盐酸,稀释成10%的稀盐酸,需加水的质量为( )
A.80 g B.100 g C.200 g D.280 g
【解析】选C。可设出水的质量,然后利用溶液在稀释前后溶质的质量不变找出等量关系。解:设需加水的质量为x,则80 g ×35%=(80 g+x)×10%,解得,x=200 g;即需加水的质量为
200 g。2.配制50 g质量分数为6%的氯化钠溶液,下列说法不正确的是( )
A.实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和胶头滴管
B.用托盘天平称量所需氯化钠的质量3.0 g
C.用10 mL量筒量取所需水的体积
D.实验步骤是计算、称量、量取、溶解【解析】选C。配制50 g质量分数为6%的氯化钠溶液,需氯化钠的质量:50 g×6%=3 g,水的质量:50 g-3 g=47 g,合47 mL,应选用50 mL的量筒量取所需的水,C错误。3.室温时,对100 mL氯化钠饱和溶液作如下操作,最终甲、乙两烧杯中溶液( )
A.溶质质量相同 B.溶质质量分数相同
C.均为不饱和溶液 D.溶剂质量相同【解析】选A。本题考查学生对溶液配制及稀释的理解。溶液具有均一性,将100 mL等分为两份,两份完全相同,均为饱和溶液;向乙中加入50 mL水,溶液变为不饱和,但溶质的质量不变。故选A。4.有100 g 10%的盐酸溶液,要使其溶质质量分数增大一倍,应采取的方法是( )
(提示:盐酸易挥发)
A.把溶液的量倒掉一半
B.溶质的质量增大一倍
C.将100 g 10%的盐酸与200 g 25%的盐酸混合
D.蒸发掉溶剂的质量是原溶液质量的一半【解析】选C。A选项溶液具有均一性,把溶液的量倒掉一半,
其溶质质量分数不变,故A错误;B选项根据溶质质量分数=
×100%可知,溶质的质量增大一倍,因溶液的质量也
增加,因此溶质质量分数增大不到一倍,故B错误;C选项将100 g
10%的盐酸与200 g 25%的盐酸混合,溶质质量分数为
×100%=20%,故C正确;D选项蒸发时先
挥发出来的是氯化氢气体,故D错误。5.配制50 g质量分数为5%的氯化钠溶液,下列说法正确的是( )
A.将砝码直接放在左盘,将氯化钠直接放在右盘进行称量
B.量取水时,仰视量筒读数
C.将称好的氯化钠放入量筒中溶解
D.为加快固体溶解,用玻璃棒搅拌【解析】选D。A选项用托盘天平称量氯化钠时,为防止腐蚀托盘,应将氯化钠放在纸片上称量,且应“左物右码”,故选项说法错误。B选项量筒读数时视线要与量筒内液体的凹液面的最低处保持水平,仰视读数,读数比实际偏小,则会导致所量取水的实际体积大于所量的值,溶剂的质量偏大,故所得溶液的质量分数偏小,故选项说法错误。C选项溶解操作应在烧杯中,不能将称好的氯化钠放入量筒中溶解,故选项说法错误。D选项为加快固体溶解,可用玻璃棒搅拌,故选项说法正确。6.请根据溶液的有关知识回答下列问题:
(1)已知硝酸钾在水中的溶解能力随温度升高而增大,则将KNO3饱和溶液变成不饱和溶液可采取的措施有? __。
(2)配制0.9%的生理盐水的主要实验操作步骤有? __。 【解析】(1)将KNO3饱和溶液变成不饱和溶液可采取的措施有:增加溶剂、改变温度;(2)配制0.9%的生理盐水的主要实验操作步骤有:计算、称量、溶解、装瓶贴签。
答案:(1)增加溶剂、改变温度
(2)计算、称量、溶解、装瓶贴签
第七单元主题一 溶液的形成
【主题训练1】关于溶液和乳化的下列说法错误的是( )
A.溶液中可以含有多种溶质
B.溶液是均一、稳定的混合物
C.用汽油洗去衣服上的油污是乳化现象
D.溶液不一定是无色的【解析】选C。本题考查学生对溶液和乳化的认知能力。解答本题需明确两点:(1)溶液的概念与特性;(2)乳化现象的发生原理。汽油洗去油污是因为油污溶解在汽油中被除去,故C错误。【主题训练2】小明同学用甲物质进行以下实验:(1)实验过程中,B、C、D对应的溶液为不饱和溶液的是
_____________________________________________。
(2)向B对应的溶液中再加入30 g甲固体的过程中,发现固体全部溶解,D图溶液放置一段时间后又有部分固体析出。你认为“全部溶解”的原因是?? __。【解析】不饱和溶液是指在一定温度下仍能继续溶解溶质的溶液,B中烧杯内含有50 g水和20 g甲物质,加入30 g甲物质后又能溶解,表明B中溶液一定为不饱和溶液,D中溶液中的固体虽全部溶解,但温度发生了变化,能否继续溶解,我们无法得知,故C溶液不一定是不饱和溶液,D中溶液有固体析出,表明此时溶液为t2℃时的饱和溶液,温度之所以发生变化,是因为物质溶解时产生了热量。答案:(1)B
(2)甲物质溶于水时会放出热量,使溶液温度升高【关键点拨】
1.溶解与乳化的比较:2.饱和溶液和不饱和溶液:
(1)概念中的要点:一定温度下;一定量的溶剂;能不能继续溶解溶质。
(2)相互转化(氢氧化钙除外)。
不饱和溶液 饱和溶液【真题体验】
1向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是( )
A.氢氧化钠 B.食盐
C.硝酸钾 D.硝酸铵【解析】选D。本题考查学生对物质溶于水时溶液温度变化的认识。解答本题需明确气体体积受温度的影响变化情况。由题意可知瓶内压强减小,应为瓶内温度降低所致,故而应选硝酸铵。2.溶液对人类的生产、生活都有很重要的意义。下列关于溶液的说法或做法错误的是( )
A.夏天喝的汽水不是溶液
B.蛋汤太咸,加水稀释后口味变淡
C.无色、透明的液体不一定是溶液
D.凉茶水是均一、稳定的混合物【解析】选A。本题主要考查溶液的有关知识。夏天喝的汽水是溶液,是二氧化碳的水溶液,蛋汤稀释后,溶液浓度变小,口味变淡;无色、透明的液体不一定是溶液,如水;凉茶水属于溶液,是均一、稳定的混合物。3.下列说法不正确的是( )
A.溶液都是无色、均一、稳定的液体
B.氯化钠溶液是由钠离子、氯离子和水分子组成的混合物
C.用洗洁精清洗餐具上的油污发生乳化现象
D.用酒精浸泡草药可溶解其中的有效成分【解析】选A。本题考查学生对溶液知识的认识,解答本题的关键应明确3点:(1)溶液的性质和特征;(2)洗洁精洗涤油污的作用原理;(3)除水可以作溶剂外,酒精、汽油等物质也可以作溶剂。A中,溶液一定是均一稳定的混合物,但不一定是无色的;B中,氯化钠溶液是氯化钠固体以钠离子、氯离子的形式扩散到水中形成的,故B正确;C中,用洗洁精清洗油污属于乳化过程;D中,酒精可以作溶剂,溶解某些有机物成分,故D正确。4.配制硝酸钾溶液时得到下表数据,根据表中数据分析,不正确的是( )A.28℃时10克水中最多能溶解硝酸钾4克
B.60℃时等质量水中能溶解的硝酸钾比28℃时多
C.①②所得溶液溶质的质量分数相等
D.③所得溶液一定是硝酸钾的饱和溶液【解析】选D。对比①②可以看出,28℃时10克水中溶解了硝酸钾4克时,再向其中加入硝酸钾不再溶解,因此28℃时10克水中最多能溶解硝酸钾4克,A正确;28℃时10克水中最多能溶解硝酸钾4克,60℃时10克水中能溶解硝酸钾8克,因此60℃时等质量水中能溶解的硝酸钾比28℃时多,B正确;①②中水的质量相同,溶解的硝酸钾的质量相同,因此所得溶液溶质的质量分数相等,C正确;根据表中数据可知,60℃时10克水中溶解了8克硝酸钾,是否还能再溶解无法得知,因此不能判断③所得溶液是否是硝酸钾的饱和溶液,D错误。主题二 溶质质量分数及溶液的配制
【主题训练3】(2013·青岛中考)科学施肥是实现农业增产的重要手段。硝酸铵(NH4NO3)是一种常用的氮肥,其中氮、氢、氧三种元素的质量比为____________。若要配制200 g溶质质量分数为5%的硝酸铵溶液,需要硝酸铵的质量为______g,需要水的质量为______g。【解析】本题考查对有关元素质量比、溶质质量分数的计算。氮、氢、氧三种元素的质量比=(14×2)∶(1×4)∶(16×3)
=7∶1∶12。硝酸铵的质量:200 g×5%=10 g,水的质量:200 g-10 g=190 g。
答案:7∶1∶12 10 190【关键点拨】
1.溶质质量分数公式:
溶质的质量分数= ×100%
= ×100%。2.溶液的配制:
(1)仪器:配制一定溶质质量分数的溶液分为两种情况:一是“固”配“液”,固体需要用托盘天平称量质量;二是“浓”配“稀”,浓溶液的取用需要用量筒量取体积,不需要托盘天平,量筒共用到2次。(2)误差分析。
①所配溶液的溶质质量分数偏大,如量取浓溶液时仰视读数、量取水时俯视读数等。
②所配溶液的溶质质量分数偏小,如称量时“左码右物”并使用游码、量取浓溶液时俯视读数、量取水时仰视读数等。【真题体验】
1.将80 g质量分数为35%的浓盐酸,稀释成10%的稀盐酸,需加水的质量为( )
A.80 g B.100 g C.200 g D.280 g
【解析】选C。可设出水的质量,然后利用溶液在稀释前后溶质的质量不变找出等量关系。解:设需加水的质量为x,则80 g ×35%=(80 g+x)×10%,解得,x=200 g;即需加水的质量为
200 g。2.配制50 g质量分数为6%的氯化钠溶液,下列说法不正确的是( )
A.实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和胶头滴管
B.用托盘天平称量所需氯化钠的质量3.0 g
C.用10 mL量筒量取所需水的体积
D.实验步骤是计算、称量、量取、溶解【解析】选C。配制50 g质量分数为6%的氯化钠溶液,需氯化钠的质量:50 g×6%=3 g,水的质量:50 g-3 g=47 g,合47 mL,应选用50 mL的量筒量取所需的水,C错误。3.室温时,对100 mL氯化钠饱和溶液作如下操作,最终甲、乙两烧杯中溶液( )
A.溶质质量相同 B.溶质质量分数相同
C.均为不饱和溶液 D.溶剂质量相同【解析】选A。本题考查学生对溶液配制及稀释的理解。溶液具有均一性,将100 mL等分为两份,两份完全相同,均为饱和溶液;向乙中加入50 mL水,溶液变为不饱和,但溶质的质量不变。故选A。4.有100 g 10%的盐酸溶液,要使其溶质质量分数增大一倍,应采取的方法是( )
(提示:盐酸易挥发)
A.把溶液的量倒掉一半
B.溶质的质量增大一倍
C.将100 g 10%的盐酸与200 g 25%的盐酸混合
D.蒸发掉溶剂的质量是原溶液质量的一半【解析】选C。A选项溶液具有均一性,把溶液的量倒掉一半,
其溶质质量分数不变,故A错误;B选项根据溶质质量分数=
×100%可知,溶质的质量增大一倍,因溶液的质量也
增加,因此溶质质量分数增大不到一倍,故B错误;C选项将100 g
10%的盐酸与200 g 25%的盐酸混合,溶质质量分数为
×100%=20%,故C正确;D选项蒸发时先
挥发出来的是氯化氢气体,故D错误。5.配制50 g质量分数为5%的氯化钠溶液,下列说法正确的是( )
A.将砝码直接放在左盘,将氯化钠直接放在右盘进行称量
B.量取水时,仰视量筒读数
C.将称好的氯化钠放入量筒中溶解
D.为加快固体溶解,用玻璃棒搅拌【解析】选D。A选项用托盘天平称量氯化钠时,为防止腐蚀托盘,应将氯化钠放在纸片上称量,且应“左物右码”,故选项说法错误。B选项量筒读数时视线要与量筒内液体的凹液面的最低处保持水平,仰视读数,读数比实际偏小,则会导致所量取水的实际体积大于所量的值,溶剂的质量偏大,故所得溶液的质量分数偏小,故选项说法错误。C选项溶解操作应在烧杯中,不能将称好的氯化钠放入量筒中溶解,故选项说法错误。D选项为加快固体溶解,可用玻璃棒搅拌,故选项说法正确。6.请根据溶液的有关知识回答下列问题:
(1)已知硝酸钾在水中的溶解能力随温度升高而增大,则将KNO3饱和溶液变成不饱和溶液可采取的措施有? __。
(2)配制0.9%的生理盐水的主要实验操作步骤有? __。 【解析】(1)将KNO3饱和溶液变成不饱和溶液可采取的措施有:增加溶剂、改变温度;(2)配制0.9%的生理盐水的主要实验操作步骤有:计算、称量、溶解、装瓶贴签。
答案:(1)增加溶剂、改变温度
(2)计算、称量、溶解、装瓶贴签
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
