人教版九年级化学下册9.2《溶解度》教学课件 (共27张PPT)
文档属性
| 名称 | 人教版九年级化学下册9.2《溶解度》教学课件 (共27张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 11.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-12-08 00:00:00 | ||
图片预览


文档简介
课件27张PPT。第2节
溶 解 度饱和溶液溶解度内容提要学习目标1.通过实验探究,建立饱和溶液与不饱和溶液的概念;了解饱和溶液与不饱和溶液相互转化的方法;
2.了解结晶现象;
3.了解固体溶解度的涵义,会绘制和使用溶解度曲线;
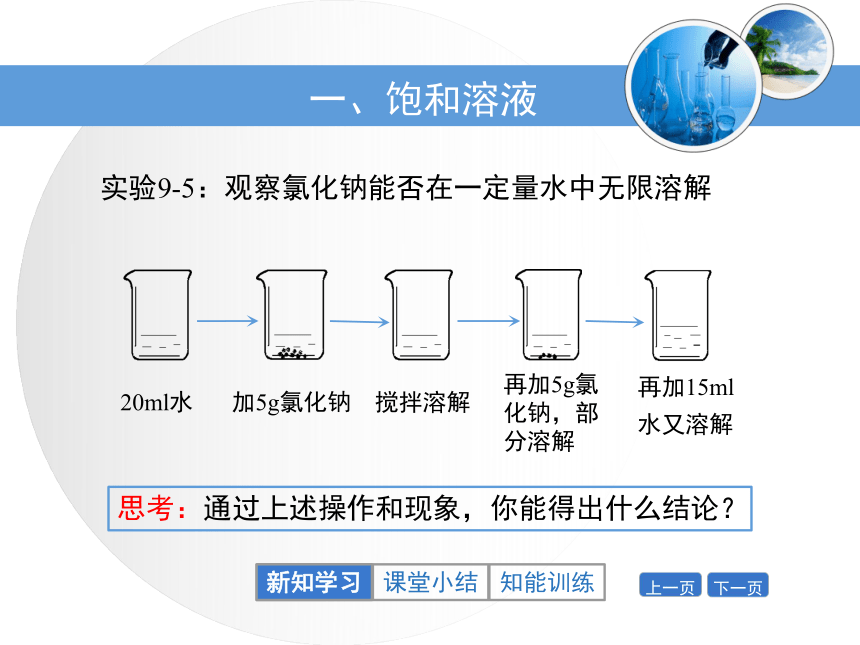
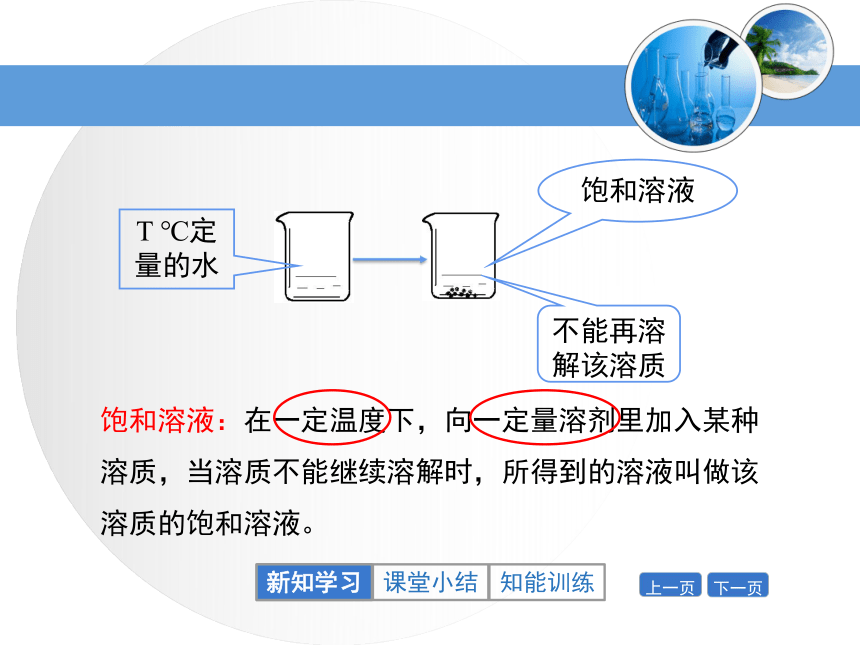
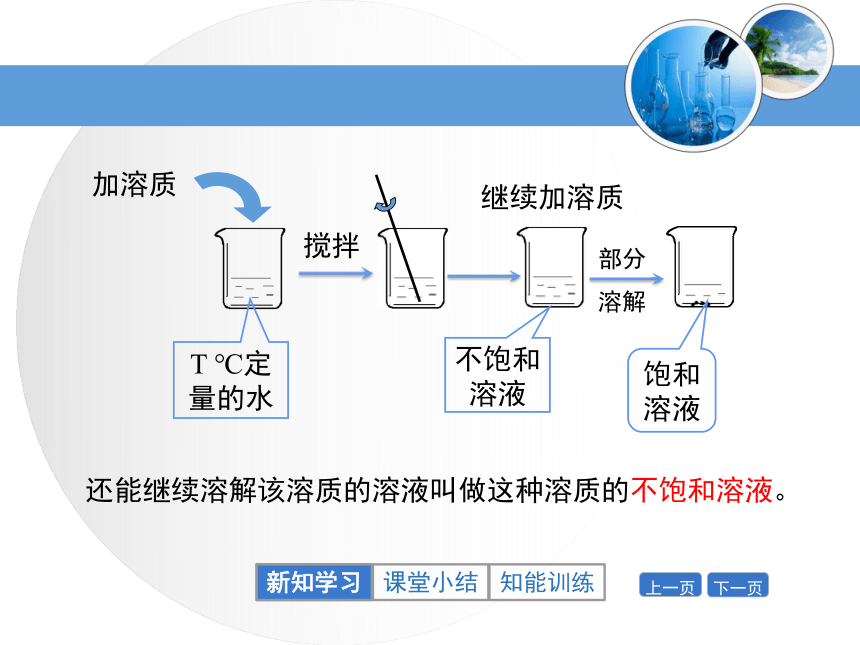
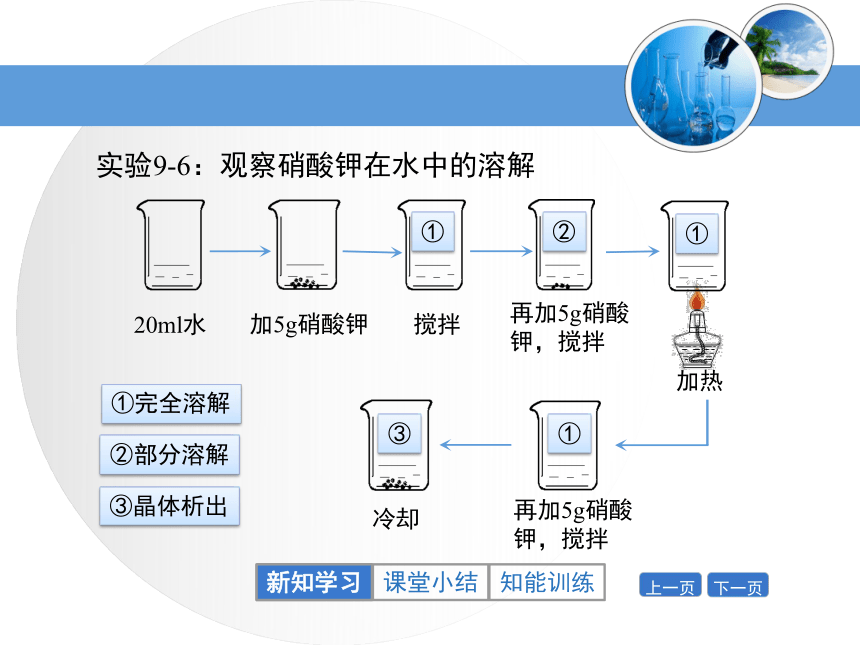
4.知道气体溶解度的表示方法与影响因素。新知学习回顾:什么是溶液,氯化钠溶于水能形成溶液吗?思考:氯化钠能无限制地溶解在一定量的水中吗?一、饱和溶液新知学习实验9-5:观察氯化钠能否在一定量水中无限溶解20ml水思考:通过上述操作和现象,你能得出什么结论?新知学习饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做该溶质的饱和溶液。T ℃定量的水不能再溶解该溶质饱和溶液新知学习T ℃定量的水饱和溶液还能继续溶解该溶质的溶液叫做这种溶质的不饱和溶液。继续加溶质不饱和溶液新知学习实验9-6:观察硝酸钾在水中的溶解20ml水①①完全溶解②部分溶解②①①③③晶体析出新知学习加热后,硝酸钾
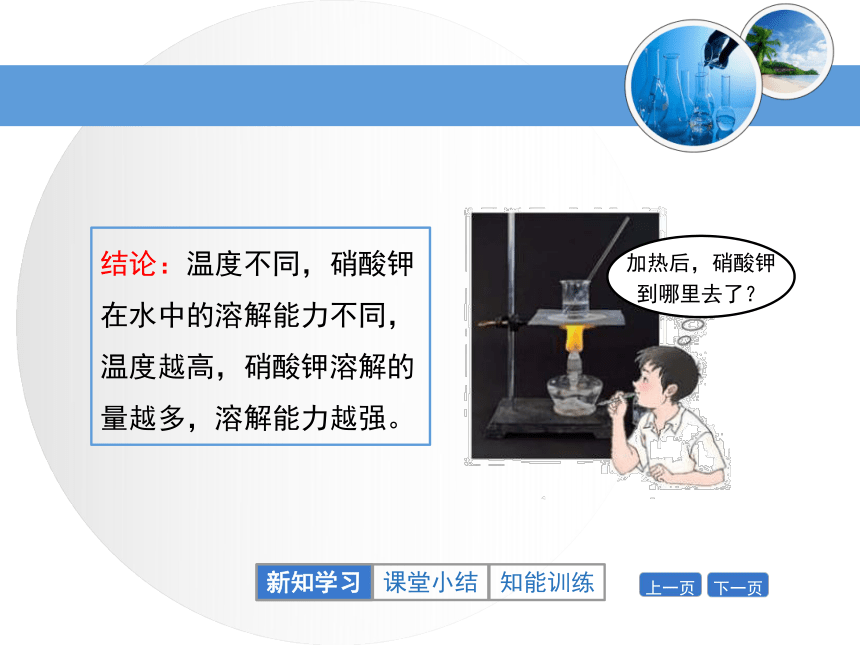
到哪里去了?结论:温度不同,硝酸钾在水中的溶解能力不同,温度越高,硝酸钾溶解的量越多,溶解能力越强。新知学习饱和溶液增加溶剂,改变温度增加溶质,减少溶剂,改变温度不饱和溶液饱和溶液与不饱和溶液的相互转化注意:溶液的浓和稀与溶液是否饱和没有必然的联系。新知学习当热的硝酸钾溶液冷却后,烧杯底部出现了固体。降温结晶结晶:溶质从溶液中析出的过程叫结晶。结晶新知学习蒸发溶剂冷却海水晒盐蒸发结晶新知学习蒸发池结晶池海水海水晒盐过程水分
蒸发贮水池二、溶解度新知学习思考:
1.如何确定一份溶液是否为饱和溶液?
2.如何表示一份饱和溶液中溶解的溶质的量?溶解度:在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。新知学习条件 —— 一定温度标准 —— 100克溶剂 (水)状态 —— 饱和溶液单位 —— 溶质的质量(克)溶解度4要素注意:若某物质在某温度时的溶解度为S克,则此时
M质 = S克,M剂 = 100克,M液= M质+M剂 = 100+S 克。新知学习判断正误:
1.l00g水中最多溶解38g氯化钠,所以氯化钠在水中的溶解度是38g。( )
2.在10℃时,烧杯内水中最多溶有140g硝酸铵,所以硝酸铵在水中的溶解度是140g。( )
3.在60℃,100g水中溶有75g硝酸钾,所以60℃时硝酸钾的溶解度为75g。( )
4.60℃,100g水中最多溶解124g硝酸钾,所以硝酸钾在这温度下的溶解度是124。( )××××缺少:100g溶剂缺少:达到饱和缺少:温度缺少:单位新知学习溶解度与溶解性的关系硝酸钾在不同温度时的溶解度:溶解度的表示方法:(1)表格法、列表法:13.331.620.945.863.985.5110138169202246新知学习(2)溶解度曲线新知学习几种固体物质的溶解度曲线新知学习1.同种物质在不同温度下的溶解度不同。2.曲线的交点表示这两种物质在该温度下的溶解度相同。3.曲线越陡,该物质的溶解度受温度影响越大。4.极少数固体物质溶解度随温度升高而减小,如熟石灰。总结:溶解度曲线中的一些规律新知学习气体在水中的溶解度通常用一定压强、一定温度下1体积水最多溶解气体的体积数来表示。例如:25℃、1 个标准大气压下,1L淡水和1L海水中最多可溶解的氧气体积分别为6.04mL和4.95 mL。
影响气体溶解度的因素有温度、压强等。气体的溶解度新知学习课堂小结课堂小结溶解度海水晒盐知能训练知能训练1.能证明20℃时某一硝酸钾溶液已达到饱和的方法是( )
A.向20℃时该溶液中加入硝酸钾固体,固体不溶解
B.向20℃时该溶液中加入少量水,溶液变稀
C.取少量溶液降温到0℃,有固体析出
D.取少量溶液升温到50℃,无固体析出A知能训练2.下列关于溶解度的说法,不正确的是( )
A.溶解度能够表示物质溶解性的强弱程度
B.溶解度能够表示溶质在溶剂中溶解的程度
C.溶解度能够表示某种物质在某种溶剂中的溶解限量
D.在相同温度、相同溶剂的条件下,要判定不同物质的溶解度相对大小,可以根据其饱和溶液的溶质质量分数B知能训练3.甲、乙、丙三种固体物质的溶解度曲线如图所示,下列有关说法中正确的是( )
A.甲物质的溶解度最大
B.丙物质的溶解度随温度升高而降低
C.乙物质的溶解度不随温度升降而变化
D.t2℃时甲、乙、丙三种物质的溶解度相等BEndThank
you结束
2.了解结晶现象;
3.了解固体溶解度的涵义,会绘制和使用溶解度曲线;
4.知道气体溶解度的表示方法与影响因素。新知学习回顾:什么是溶液,氯化钠溶于水能形成溶液吗?思考:氯化钠能无限制地溶解在一定量的水中吗?一、饱和溶液新知学习实验9-5:观察氯化钠能否在一定量水中无限溶解20ml水思考:通过上述操作和现象,你能得出什么结论?新知学习饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做该溶质的饱和溶液。T ℃定量的水不能再溶解该溶质饱和溶液新知学习T ℃定量的水饱和溶液还能继续溶解该溶质的溶液叫做这种溶质的不饱和溶液。继续加溶质不饱和溶液新知学习实验9-6:观察硝酸钾在水中的溶解20ml水①①完全溶解②部分溶解②①①③③晶体析出新知学习加热后,硝酸钾
到哪里去了?结论:温度不同,硝酸钾在水中的溶解能力不同,温度越高,硝酸钾溶解的量越多,溶解能力越强。新知学习饱和溶液增加溶剂,改变温度增加溶质,减少溶剂,改变温度不饱和溶液饱和溶液与不饱和溶液的相互转化注意:溶液的浓和稀与溶液是否饱和没有必然的联系。新知学习当热的硝酸钾溶液冷却后,烧杯底部出现了固体。降温结晶结晶:溶质从溶液中析出的过程叫结晶。结晶新知学习蒸发溶剂冷却海水晒盐蒸发结晶新知学习蒸发池结晶池海水海水晒盐过程水分
蒸发贮水池二、溶解度新知学习思考:
1.如何确定一份溶液是否为饱和溶液?
2.如何表示一份饱和溶液中溶解的溶质的量?溶解度:在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。新知学习条件 —— 一定温度标准 —— 100克溶剂 (水)状态 —— 饱和溶液单位 —— 溶质的质量(克)溶解度4要素注意:若某物质在某温度时的溶解度为S克,则此时
M质 = S克,M剂 = 100克,M液= M质+M剂 = 100+S 克。新知学习判断正误:
1.l00g水中最多溶解38g氯化钠,所以氯化钠在水中的溶解度是38g。( )
2.在10℃时,烧杯内水中最多溶有140g硝酸铵,所以硝酸铵在水中的溶解度是140g。( )
3.在60℃,100g水中溶有75g硝酸钾,所以60℃时硝酸钾的溶解度为75g。( )
4.60℃,100g水中最多溶解124g硝酸钾,所以硝酸钾在这温度下的溶解度是124。( )××××缺少:100g溶剂缺少:达到饱和缺少:温度缺少:单位新知学习溶解度与溶解性的关系硝酸钾在不同温度时的溶解度:溶解度的表示方法:(1)表格法、列表法:13.331.620.945.863.985.5110138169202246新知学习(2)溶解度曲线新知学习几种固体物质的溶解度曲线新知学习1.同种物质在不同温度下的溶解度不同。2.曲线的交点表示这两种物质在该温度下的溶解度相同。3.曲线越陡,该物质的溶解度受温度影响越大。4.极少数固体物质溶解度随温度升高而减小,如熟石灰。总结:溶解度曲线中的一些规律新知学习气体在水中的溶解度通常用一定压强、一定温度下1体积水最多溶解气体的体积数来表示。例如:25℃、1 个标准大气压下,1L淡水和1L海水中最多可溶解的氧气体积分别为6.04mL和4.95 mL。
影响气体溶解度的因素有温度、压强等。气体的溶解度新知学习课堂小结课堂小结溶解度海水晒盐知能训练知能训练1.能证明20℃时某一硝酸钾溶液已达到饱和的方法是( )
A.向20℃时该溶液中加入硝酸钾固体,固体不溶解
B.向20℃时该溶液中加入少量水,溶液变稀
C.取少量溶液降温到0℃,有固体析出
D.取少量溶液升温到50℃,无固体析出A知能训练2.下列关于溶解度的说法,不正确的是( )
A.溶解度能够表示物质溶解性的强弱程度
B.溶解度能够表示溶质在溶剂中溶解的程度
C.溶解度能够表示某种物质在某种溶剂中的溶解限量
D.在相同温度、相同溶剂的条件下,要判定不同物质的溶解度相对大小,可以根据其饱和溶液的溶质质量分数B知能训练3.甲、乙、丙三种固体物质的溶解度曲线如图所示,下列有关说法中正确的是( )
A.甲物质的溶解度最大
B.丙物质的溶解度随温度升高而降低
C.乙物质的溶解度不随温度升降而变化
D.t2℃时甲、乙、丙三种物质的溶解度相等BEndThank
you结束
同课章节目录
