重庆市人教版高中化学选修4学案-4.1原电池
文档属性
| 名称 | 重庆市人教版高中化学选修4学案-4.1原电池 |
|
|
| 格式 | zip | ||
| 文件大小 | 711.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-12-12 00:00:00 | ||
图片预览


文档简介
第四章
电化学基础
第一节
原电池
【考纲要求】
了解原电池的工作原理,能写出电极反应和电池反应方程式。
【自主学习】
阅读课本P70---P72,思考并完成以下预习内容。
1.以锌铜原电池为例,写出电极反应式和总化学方程式。
2.
单液原电池不能提供持续稳定的电流,可能的原因是什么?该原电池还有哪些缺点?
3.
什么是盐桥?为何要引入盐桥?盐桥在原电池中有何作用?
4.原电池输出电能的能力影响因素有哪些?
5.基于盐桥,原电池还可以如何改进(例如:阳离子交换膜)?
【考点突破】
考点一:原电池的构造及工作原理
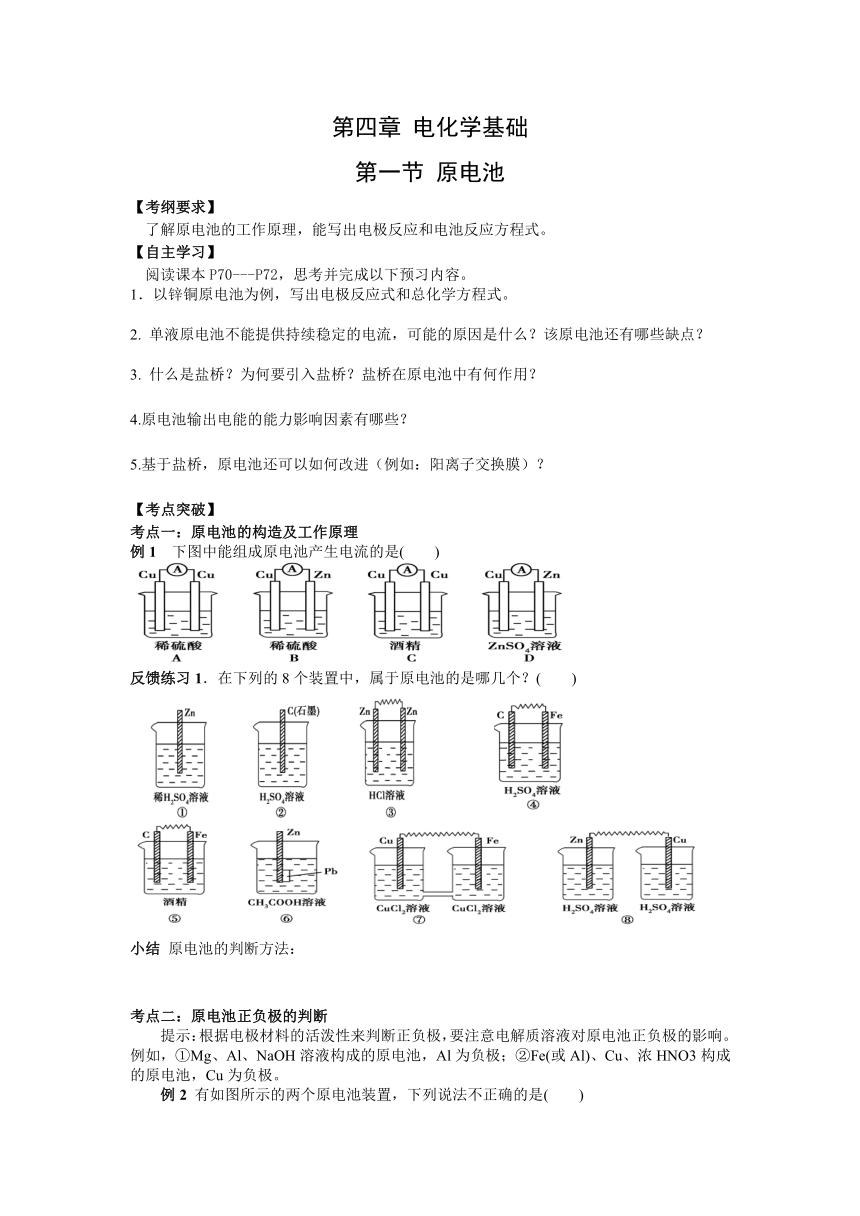
例1 下图中能组成原电池产生电流的是( )
反馈练习1.在下列的8个装置中,属于原电池的是哪几个?( )
小结
原电池的判断方法:
考点二:原电池正负极的判断
提示:根据电极材料的活泼性来判断正负极,要注意电解质溶液对原电池正负极的影响。例如,①Mg、Al、NaOH溶液构成的原电池,Al为负极;②Fe(或Al)、Cu、浓HNO3构成的原电池,Cu为负极。
例2
有如图所示的两个原电池装置,下列说法不正确的是( )
A.A池中负极的电极反应为Mg-2e-===Mg2+
B.Mg在A池中为负极,在B池中为正极
C.B池中电子的流向:Mg→Al
D.原电池工作一段时间后,A池溶液的pH会增大
反馈练习2.铜锌原电池(如图)工作时,下列叙述正确的是( )
A.正极反应为:Zn-2e-===Zn2+
B.电池反应为:Zn+Cu2+===Zn2++Cu
C.在外电路中,电流从负极流向正极
D.盐桥中的K+移向ZnSO4溶液
反馈练习3下列说法中不正确的是
( )
A.由
Al、Cu、稀H2SO4组成原电池,其负极反应式为:
Al-3e-=
Al3+
B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:
Al-3e-=
Al3+
C.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:
Cu-2e-=
Cu2+
D.由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=
Cu2+
小结
原电池正负极判断方法:
考点三:原电池原理的应用(设计原电池、比较金属活泼性、金属防护、加快速率)
例3
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少。据此判断这四种金属活动性由大到小的顺序是( )
A.①③②④
B.①③④②
C.③④②①
D.③①②④
例4
利用反应Zn+2FeCl3==ZnCl2+2FeCl2,
设计一个原电池,在下边方框内画出实验装置图,
并指出正极为________,电极反应式为________;
负极为________,电极反应式为________。
反馈练习4
有A、B、C、D四种金属。将A与B用导线连接起来,浸入电解质溶液中,B不易腐蚀。将A、D分别投入等浓度盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此,判断它们的金属活动性由强到弱的顺序是( )
A.D>C>A>B
B.D>A>B>C
C.D>B>A>C
D.B>A>D>C
反馈练习5
为什么实验室用锌与稀H2SO4反应制H2,在其他条件相同的条件下,用粗锌产生H2的速率会更快?
反馈练习6
为何海船船底要附一块锌?
反馈练习7
某电池的总反应为:
Fe+2Fe3+===3Fe2+,能实现该反应的原电池是( )
正极
负极
电解质溶液
A
Cu
Fe
FeCl3溶液
B
C
Fe
Fe(NO3)2溶液
C
Fe
Zn
Fe2(SO4)3溶液
D
Ag
Fe
CuSO4溶液
【考点巩固】
1.下列化学反应在理论上可设计成原电池的是( )
A.2Al(s)+2NaOH(aq)+2H2O(l)===2NaAlO2(aq)+3H2(g) ΔH<0
B.HNO3(aq)+KOH(aq)===KNO3(aq)+H2O(l) ΔH<0
C.
Ba(OH)2·H2O(s)+2NH4Cl(s)===BaCl2(aq)+2NH3·H2O(aq)+8H2O(l) ΔH>0
D.Na2O(s)+H2O(l)===2NaOH(aq) ΔH<0
2.
将反应Cu(s)+2Ag+(aq)===Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,下列有关叙述正确的是( )
A.KNO3盐桥中的K+移向Cu(NO3)2溶液
B.Ag作负极,Cu作正极
C.工作一段时间后,Cu(NO3)2溶液中c(Cu2+)增大
D.取出盐桥后,电流计的指针依然发生偏转
3.分析下图所示的四个原电池装置,结论正确的是( )
A.(1)(2)中Mg作负极,(3)(4)中Fe作负极
B.(2)中Mg作正极,电极反应式为:
6H2O+6e-===6OH-+3H2↑
C.(3)中Fe作电池负极
D.(4)中Cu作正极,电极反应式为:
2H++2e-===H2↑
4.(双选)根据下图,下列判断中正确的是( )
A.烧杯a中的溶液pH升高
B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-===H2↑
D.烧杯b中发生的反应为2Cl--2e-===Cl2↑
5.银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去。下列说法正确的是( )
A.处理过程中银器一直保持恒重
B.银器为正极,Ag2S被还原生成单质银
C.该过程中总反应为2Al+3Ag2S===6Ag+Al2S3
D.黑色褪去的原因是黑色Ag2S转化为白色AgCl
6.控制适合的条件,将反应Fe3++Ag
Fe2++Ag+设计成如图所示的原电池(盐桥中装有琼脂-硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)。已知,接通后,观察到电流计指针向右偏转。下列判断正确的是( )
A.在外电路中,电子从石墨电极流向银电极
B.盐桥中的K+移向乙烧杯
C.一段时间后,电流计指针反向偏转,越过0刻度,
向左边偏转
D.电流计指针居中后,往甲烧杯中加入一定量的铁粉,
电流计指针将向左偏转
7.将Fe片和石墨用导线相连,一组插入稀硫酸中,一组插入FeCl3的溶液中,分别形成了原电池。
(1)这两个原电池中,正极分别是( )。
A.石墨、石墨
B.石墨、Fe片
C.Fe片、Fe片
D.Fe片、石墨
(2)写出插入稀H2SO4中形成原电池的正极反应式_____________________。
(3)写出插入FeCl3溶液中形成原电池的电池总反应式_____________________
8.由锌片
、铜片和200
mL稀硫酸组成的原电池如下图所示。
(1)原电池的负极反应是_____________________,
正极反应是_____________________。
(2)电流的方向是_____________________。
(3)一段时间后,当在铜片上放出1.68
L(标准状况)气体时,H2SO4恰好消耗一半。则产生这些气体的同时,共消耗________g锌,有________个电子通过了导线,原硫酸的物质的量浓度是________(设溶液体积不变)。
9.
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。
锌片上发生的电极反应:_____________________;
银片上发生的电极反应:_____________________。
(2)若该电池中两电极的总质量为60
g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47
g,试计算:
①产生氢气的体积(标准状况);
②通过导线的电量。(已知NA=6.02×1023/mol,1个电子所带的电量为1.60×10-19C)
第四章
电化学基础
第一节
原电池
【考点突破】
例1
B
反馈练习1
④⑥⑦
例2
C
反馈训练2
B
反馈训练3
C
例3
B
实验装置图如下图所示。 Pt
2Fe3++2e-==2Fe2+
Zn
Zn-2e-==Zn2+
反馈练习4
B
反馈训练5
原电池加快反应速率
反馈练习6
原电池用于金属的防护
反馈练习7
A
【考点巩固】
1
A
2
C
3
B
4
AB
5
B
6
D
7
(1)A (2)2H++2e-===H2↑
(3)2Fe3++Fe===3Fe2+
8
(1)Zn-2e-===Zn2+ 2H++2e-===H2↑
(2)由Cu极流向Zn极
(3)4.875
9.03×1022 0.75
mol·L-1
9
(1)Zn-2e-===Zn2+ 2H++2e-===H2↑
(2)①产生氢气的体积是4.5
L
②通过导线的电量为3.85×104C
电化学基础
第一节
原电池
【考纲要求】
了解原电池的工作原理,能写出电极反应和电池反应方程式。
【自主学习】
阅读课本P70---P72,思考并完成以下预习内容。
1.以锌铜原电池为例,写出电极反应式和总化学方程式。
2.
单液原电池不能提供持续稳定的电流,可能的原因是什么?该原电池还有哪些缺点?
3.
什么是盐桥?为何要引入盐桥?盐桥在原电池中有何作用?
4.原电池输出电能的能力影响因素有哪些?
5.基于盐桥,原电池还可以如何改进(例如:阳离子交换膜)?
【考点突破】
考点一:原电池的构造及工作原理
例1 下图中能组成原电池产生电流的是( )
反馈练习1.在下列的8个装置中,属于原电池的是哪几个?( )
小结
原电池的判断方法:
考点二:原电池正负极的判断
提示:根据电极材料的活泼性来判断正负极,要注意电解质溶液对原电池正负极的影响。例如,①Mg、Al、NaOH溶液构成的原电池,Al为负极;②Fe(或Al)、Cu、浓HNO3构成的原电池,Cu为负极。
例2
有如图所示的两个原电池装置,下列说法不正确的是( )
A.A池中负极的电极反应为Mg-2e-===Mg2+
B.Mg在A池中为负极,在B池中为正极
C.B池中电子的流向:Mg→Al
D.原电池工作一段时间后,A池溶液的pH会增大
反馈练习2.铜锌原电池(如图)工作时,下列叙述正确的是( )
A.正极反应为:Zn-2e-===Zn2+
B.电池反应为:Zn+Cu2+===Zn2++Cu
C.在外电路中,电流从负极流向正极
D.盐桥中的K+移向ZnSO4溶液
反馈练习3下列说法中不正确的是
( )
A.由
Al、Cu、稀H2SO4组成原电池,其负极反应式为:
Al-3e-=
Al3+
B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:
Al-3e-=
Al3+
C.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:
Cu-2e-=
Cu2+
D.由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=
Cu2+
小结
原电池正负极判断方法:
考点三:原电池原理的应用(设计原电池、比较金属活泼性、金属防护、加快速率)
例3
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少。据此判断这四种金属活动性由大到小的顺序是( )
A.①③②④
B.①③④②
C.③④②①
D.③①②④
例4
利用反应Zn+2FeCl3==ZnCl2+2FeCl2,
设计一个原电池,在下边方框内画出实验装置图,
并指出正极为________,电极反应式为________;
负极为________,电极反应式为________。
反馈练习4
有A、B、C、D四种金属。将A与B用导线连接起来,浸入电解质溶液中,B不易腐蚀。将A、D分别投入等浓度盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此,判断它们的金属活动性由强到弱的顺序是( )
A.D>C>A>B
B.D>A>B>C
C.D>B>A>C
D.B>A>D>C
反馈练习5
为什么实验室用锌与稀H2SO4反应制H2,在其他条件相同的条件下,用粗锌产生H2的速率会更快?
反馈练习6
为何海船船底要附一块锌?
反馈练习7
某电池的总反应为:
Fe+2Fe3+===3Fe2+,能实现该反应的原电池是( )
正极
负极
电解质溶液
A
Cu
Fe
FeCl3溶液
B
C
Fe
Fe(NO3)2溶液
C
Fe
Zn
Fe2(SO4)3溶液
D
Ag
Fe
CuSO4溶液
【考点巩固】
1.下列化学反应在理论上可设计成原电池的是( )
A.2Al(s)+2NaOH(aq)+2H2O(l)===2NaAlO2(aq)+3H2(g) ΔH<0
B.HNO3(aq)+KOH(aq)===KNO3(aq)+H2O(l) ΔH<0
C.
Ba(OH)2·H2O(s)+2NH4Cl(s)===BaCl2(aq)+2NH3·H2O(aq)+8H2O(l) ΔH>0
D.Na2O(s)+H2O(l)===2NaOH(aq) ΔH<0
2.
将反应Cu(s)+2Ag+(aq)===Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,下列有关叙述正确的是( )
A.KNO3盐桥中的K+移向Cu(NO3)2溶液
B.Ag作负极,Cu作正极
C.工作一段时间后,Cu(NO3)2溶液中c(Cu2+)增大
D.取出盐桥后,电流计的指针依然发生偏转
3.分析下图所示的四个原电池装置,结论正确的是( )
A.(1)(2)中Mg作负极,(3)(4)中Fe作负极
B.(2)中Mg作正极,电极反应式为:
6H2O+6e-===6OH-+3H2↑
C.(3)中Fe作电池负极
D.(4)中Cu作正极,电极反应式为:
2H++2e-===H2↑
4.(双选)根据下图,下列判断中正确的是( )
A.烧杯a中的溶液pH升高
B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-===H2↑
D.烧杯b中发生的反应为2Cl--2e-===Cl2↑
5.银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去。下列说法正确的是( )
A.处理过程中银器一直保持恒重
B.银器为正极,Ag2S被还原生成单质银
C.该过程中总反应为2Al+3Ag2S===6Ag+Al2S3
D.黑色褪去的原因是黑色Ag2S转化为白色AgCl
6.控制适合的条件,将反应Fe3++Ag
Fe2++Ag+设计成如图所示的原电池(盐桥中装有琼脂-硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)。已知,接通后,观察到电流计指针向右偏转。下列判断正确的是( )
A.在外电路中,电子从石墨电极流向银电极
B.盐桥中的K+移向乙烧杯
C.一段时间后,电流计指针反向偏转,越过0刻度,
向左边偏转
D.电流计指针居中后,往甲烧杯中加入一定量的铁粉,
电流计指针将向左偏转
7.将Fe片和石墨用导线相连,一组插入稀硫酸中,一组插入FeCl3的溶液中,分别形成了原电池。
(1)这两个原电池中,正极分别是( )。
A.石墨、石墨
B.石墨、Fe片
C.Fe片、Fe片
D.Fe片、石墨
(2)写出插入稀H2SO4中形成原电池的正极反应式_____________________。
(3)写出插入FeCl3溶液中形成原电池的电池总反应式_____________________
8.由锌片
、铜片和200
mL稀硫酸组成的原电池如下图所示。
(1)原电池的负极反应是_____________________,
正极反应是_____________________。
(2)电流的方向是_____________________。
(3)一段时间后,当在铜片上放出1.68
L(标准状况)气体时,H2SO4恰好消耗一半。则产生这些气体的同时,共消耗________g锌,有________个电子通过了导线,原硫酸的物质的量浓度是________(设溶液体积不变)。
9.
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。
锌片上发生的电极反应:_____________________;
银片上发生的电极反应:_____________________。
(2)若该电池中两电极的总质量为60
g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47
g,试计算:
①产生氢气的体积(标准状况);
②通过导线的电量。(已知NA=6.02×1023/mol,1个电子所带的电量为1.60×10-19C)
第四章
电化学基础
第一节
原电池
【考点突破】
例1
B
反馈练习1
④⑥⑦
例2
C
反馈训练2
B
反馈训练3
C
例3
B
实验装置图如下图所示。 Pt
2Fe3++2e-==2Fe2+
Zn
Zn-2e-==Zn2+
反馈练习4
B
反馈训练5
原电池加快反应速率
反馈练习6
原电池用于金属的防护
反馈练习7
A
【考点巩固】
1
A
2
C
3
B
4
AB
5
B
6
D
7
(1)A (2)2H++2e-===H2↑
(3)2Fe3++Fe===3Fe2+
8
(1)Zn-2e-===Zn2+ 2H++2e-===H2↑
(2)由Cu极流向Zn极
(3)4.875
9.03×1022 0.75
mol·L-1
9
(1)Zn-2e-===Zn2+ 2H++2e-===H2↑
(2)①产生氢气的体积是4.5
L
②通过导线的电量为3.85×104C
