到实验室去:粗盐中难溶性杂质的去除 课件 (31张PPT)
文档属性
| 名称 | 到实验室去:粗盐中难溶性杂质的去除 课件 (31张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 283.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-12-14 00:00:00 | ||
图片预览










文档简介
课件31张PPT。到实验室去:粗盐中难溶性杂质的去除1.学会除去少量粗盐中的难溶性杂质的方法。
2.初步学会使用过滤、蒸发的方法对混合物进行分离。蒸馏水、粗盐;托盘天平、烧杯、玻璃棒、蒸发皿、坩埚钳、酒精灯、漏斗、药匙、量筒、滤纸、剪刀、铁架台(带铁圈)。
【友情提示】加热操作应避免灼伤人体、损坏仪器,应严格遵守操作规范。1.溶解:用_____量取10 mL水,倒入烧杯中,称取3.0 g粗盐,
加入水中,用_______搅拌,直至粗盐不再溶解为止。得到的
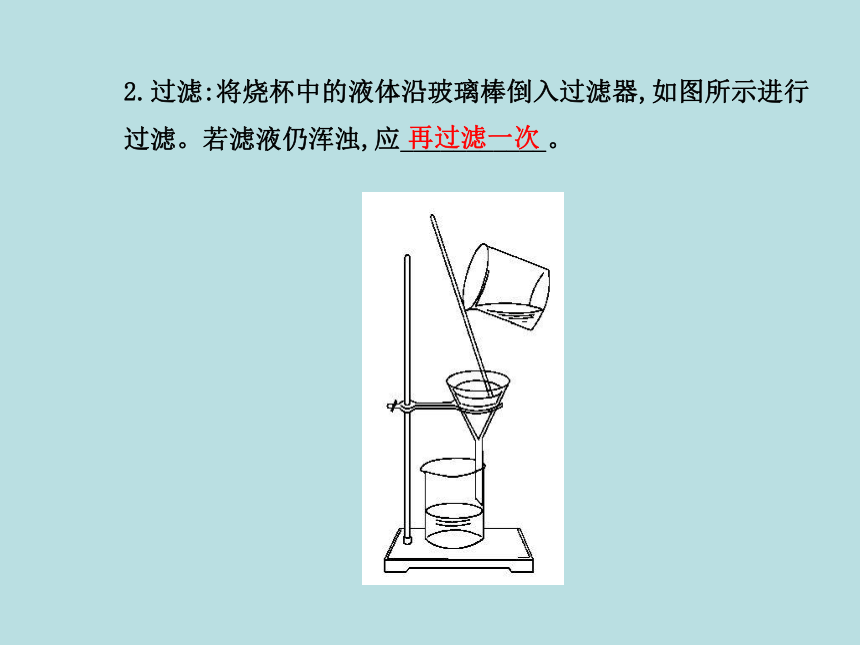
液体呈浑浊状态。量筒玻璃棒2.过滤:将烧杯中的液体沿玻璃棒倒入过滤器,如图所示进行
过滤。若滤液仍浑浊,应___________。再过滤一次漏斗边缘滤纸边缘玻璃棒三层滤纸处烧杯内壁3.蒸发:如图所示,将蒸发皿放到铁圈上,倒入滤液,用酒精灯
加热,用_______搅拌;待蒸发皿中出现较多晶体时,即
_________;用_______将蒸发皿中的晶体转移到指定的容器
内。玻璃棒停止加热玻璃棒(1)过滤操作中为什么要求做到“一贴二低三靠”?
提示:“一贴”即滤纸与漏斗紧贴在一起,这样可避免滤纸和漏斗之间的气泡影响过滤速度;“二低”指滤纸边缘要低于漏斗边缘和液面低于滤纸边缘,这样可避免浑浊液体进入滤液;“三靠”指盛浑浊液体的烧杯要与玻璃棒靠在一起,玻璃棒的下端要与三层滤纸一边靠在一起,漏斗的末端管口要与烧杯内壁靠在一起,这样可防止液体溅出,防止玻璃棒将滤纸捅破。(2)经过滤所得的滤液仍浑浊,可能的原因是什么?下一步应采取什么措施?
提示:滤液仍浑浊,可能的原因有滤纸破损;过滤时液面高于滤纸边缘;仪器不干净等。一次过滤所得的滤液仍浑浊时,应再过滤一次,如果过滤两次后滤液仍然浑浊,需重新制作过滤器再次过滤。
(3)在进行蒸发操作时,为什么看到大量晶体析出时就停止加热?
提示:这样做的目的是防止持续加热造成固体飞溅。(4)在以上几步实验操作中,有几处用到了玻璃棒,分别起了什么作用?
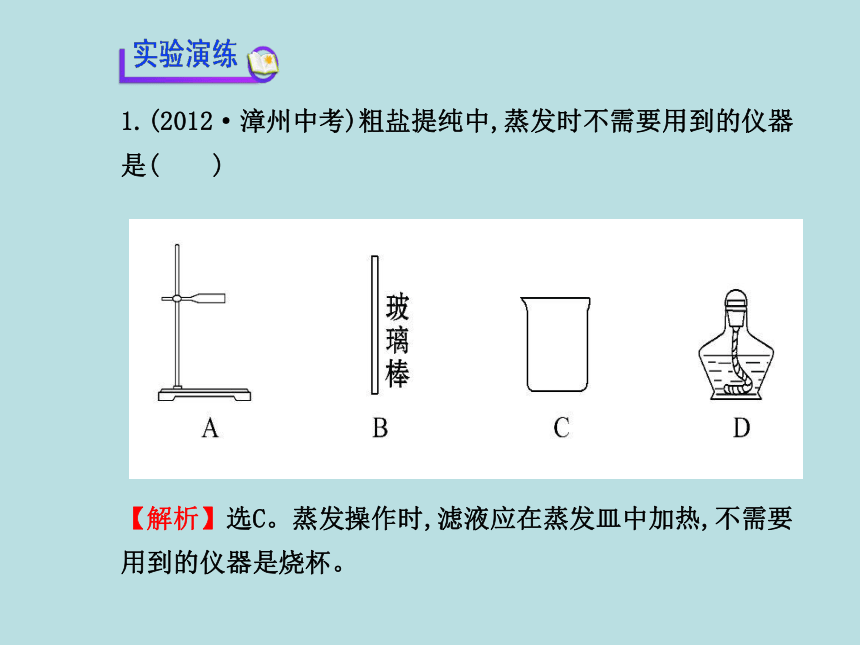
提示:溶解、过滤、蒸发等操作中,都用到了玻璃棒。在溶解中,玻璃棒起加速溶解的作用;在过滤时,玻璃棒起引导液体流下的作用;蒸发时,可用玻璃棒搅拌防止液体暴沸,停止加热后,可用玻璃棒将晶体转移到指定的容器内,此时玻璃棒起转移固体的作用。1.(2012·漳州中考)粗盐提纯中,蒸发时不需要用到的仪器是( )
【解析】选C。蒸发操作时,滤液应在蒸发皿中加热,不需要用到的仪器是烧杯。2.在粗盐提纯的实验中,最后进行氯化钠溶液的蒸发时,一般有如下操作:①固定铁圈位置,②放置蒸发皿,③放置酒精灯,④加热并搅拌,⑤停止加热,借余热蒸干。正确的操作顺序是
( )
A.①②③④⑤ B.①③②④⑤
C.③①②④⑤ D.③②①④⑤
【解析】选C。在进行氯化钠溶液的蒸发操作时,安装仪器的顺序为由下向上,即先放置酒精灯,根据酒精灯的高度确定铁圈的高度,再放置蒸发皿。 3.(2013·金山区二模)粗盐提纯实验中,不合理的操作是
( )
A.用天平称得11.7 g食盐 B.用适量水充分溶解食盐
C.过滤除去不溶性杂质 D.加热至水分全部蒸干为止
【解析】选D。天平的精确度为0.1 g,A合理;溶解食盐时水的量不宜过多或过少,B合理;过滤能除去不溶性杂质,C正确;加热至大部分晶体析出时就可停止加热,利用余热蒸干,D不合理。4.小明在家做“粗盐提纯”的实验,下列对其做法的认识中,错误的是( )
A.将粗盐放入玻璃杯中加水溶解——粒子在不断运动
B.溶解时用筷子搅拌——加快溶解速度
C.用自制净水器过滤粗盐水——过滤后的溶液中溶质只有食盐
D.实验时不用一次性塑料杯或纸杯——保护环境要从身边小事做起【解析】选C。用自制净水器过滤粗盐水只是将溶液中的不溶性固体杂质除去,溶液中仍含有氯化镁、氯化钙等可溶性杂质。5.下列是关于“粗盐提纯”实验的几种说法,其中正确的是
( )
A.为加快过滤速度,应用玻璃棒不断搅拌过滤器内的液体
B.如果经两次过滤滤液仍浑浊,则应检查实验装置并分析原因
C.蒸发滤液时要用玻璃棒不断搅拌,用酒精灯持续加热直到蒸干为止
D.为了节约蒸发时间,蒸发皿里应盛满溶液【解析】选B。用玻璃棒在过滤器内搅拌很容易弄破漏斗中的滤纸,而使实验失败,A操作不正确;经两次过滤滤液仍浑浊,可能是滤纸破损或盛接滤液的烧杯不洁净等,应检查实验装置并分析原因,B是正确的;直到蒸发皿中的液体蒸干再停止加热,会导致灼热的氯化钠固体飞溅,造成事故,C操作不正确;倒入蒸发皿中溶液的量不能超过其容积的2/3,如过多,加热时易逬溅,D操作也不正确。6.(2013·咸宁中考)用下列实验操作可完成两个实验。甲实验为粗盐中难溶性杂质的去除,乙实验为配制溶质的质量分数为10%的氯化钠溶液。下列说法中,正确的是( )A.甲实验的步骤是①④⑤,其中去除杂质的关键步骤是蒸发
B.甲实验各步操作中,玻璃棒的作用都是相同的
C.乙实验若按照②③①的步骤进行操作,则配制的溶液浓度偏大(ρ水=1 g·cm-3)
D.乙实验中,若①所用的烧杯内壁沾有水,对配制的溶液浓度无影响【解析】选C。粗盐中难溶性杂质的去除的步骤是溶解、过滤、蒸发结晶,故步骤为①④⑤,其中去除杂质的关键步骤是过滤;甲实验各步操作中玻璃棒的作用不同,分别为搅拌、引流、搅拌;配制氯化钠溶液时,量取液体体积时,视线偏高,造成量取液体体积偏少,故导致配制的溶液浓度偏大;若①所用的烧杯内壁沾有水,造成溶剂的质量偏大,使配制的溶液浓度偏小。7.(2013·河北中考)某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50 g 5%的氯化钠溶液。
实验一:下图是同学们做粗盐提纯实验的操作示意图。 请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是 。
(2)操作⑥中的错误是 。
(3)粗盐提纯实验的操作顺序为(填操作序号) 、称量精盐并计算产率。(4)操作④中,当观察到 时,停止加热。
实验二:用提纯得到的精盐配制了50 g 5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有 (填序号)。
①氯化钠固体仍然不纯
②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数
④装瓶时,有少量溶液洒出【解析】实验一:(1)玻璃棒在溶解的过程中起到了搅拌加速溶解的作用。(2)过滤操作过程中应该用玻璃棒引流;操作⑥中的错误是没有用玻璃棒引流。(3)粗盐提纯实验的操作顺序为取粗盐进行称量,倒入烧杯中加水,搅拌溶解后过滤,最后蒸发结晶得到精盐,称量精盐,计算产率,故步骤为①⑤②③⑥④。(4)蒸发过程中,蒸发皿中出现较多固体时,停止加热,利用余热将剩余的少量液体蒸干。实验二:所配溶液的溶质质量分数偏小,原因可能是溶质少、溶剂多或两种情况同时存在,氯化钠固体仍然不纯,称得氯化钠比需要的少,称量时砝码端忘垫质量相同的纸片使得称出的氯化钠减少,量取水时,仰视读数,水的体积比需要的多,都会造成所得溶液中溶质的质量分数偏小。装瓶时,有少量溶液洒出,不影响溶液中溶质的质量分数。答案:实验一:(1)加速溶解
(2)未用玻璃棒引流
(3)①⑤②③⑥④
(4)出现较多固体
实验二:①②③8.(2012·自贡中考)氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程:(1)操作③中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是 (填序号)。(2)操作④中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到 等仪器。该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外,你认为还可采取 等措施。(3)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是 (填序号)。
A.食盐没有全部溶解即过滤
B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿
D.器皿上沾有的精盐没全部转移到称量纸上【解析】(1)滤纸折叠过程中,不能出现缝隙,否则会使液体从缝隙流下,导致过滤失败;(2)为避免蒸发过程中食盐固体飞溅,还可以来回移动酒精灯或间隔性加热;
(3)食盐未全部溶解即过滤、蒸发时食盐飞溅、精盐没有全部转移称量,都会导致称量结果比理论值偏低,导致制得率偏低。精盐潮湿会导致称量结果偏大,导致制得率偏大。
答案:(1)D (2)蒸发皿 来回移动酒精灯
(3)A、B、D
2.初步学会使用过滤、蒸发的方法对混合物进行分离。蒸馏水、粗盐;托盘天平、烧杯、玻璃棒、蒸发皿、坩埚钳、酒精灯、漏斗、药匙、量筒、滤纸、剪刀、铁架台(带铁圈)。
【友情提示】加热操作应避免灼伤人体、损坏仪器,应严格遵守操作规范。1.溶解:用_____量取10 mL水,倒入烧杯中,称取3.0 g粗盐,
加入水中,用_______搅拌,直至粗盐不再溶解为止。得到的
液体呈浑浊状态。量筒玻璃棒2.过滤:将烧杯中的液体沿玻璃棒倒入过滤器,如图所示进行
过滤。若滤液仍浑浊,应___________。再过滤一次漏斗边缘滤纸边缘玻璃棒三层滤纸处烧杯内壁3.蒸发:如图所示,将蒸发皿放到铁圈上,倒入滤液,用酒精灯
加热,用_______搅拌;待蒸发皿中出现较多晶体时,即
_________;用_______将蒸发皿中的晶体转移到指定的容器
内。玻璃棒停止加热玻璃棒(1)过滤操作中为什么要求做到“一贴二低三靠”?
提示:“一贴”即滤纸与漏斗紧贴在一起,这样可避免滤纸和漏斗之间的气泡影响过滤速度;“二低”指滤纸边缘要低于漏斗边缘和液面低于滤纸边缘,这样可避免浑浊液体进入滤液;“三靠”指盛浑浊液体的烧杯要与玻璃棒靠在一起,玻璃棒的下端要与三层滤纸一边靠在一起,漏斗的末端管口要与烧杯内壁靠在一起,这样可防止液体溅出,防止玻璃棒将滤纸捅破。(2)经过滤所得的滤液仍浑浊,可能的原因是什么?下一步应采取什么措施?
提示:滤液仍浑浊,可能的原因有滤纸破损;过滤时液面高于滤纸边缘;仪器不干净等。一次过滤所得的滤液仍浑浊时,应再过滤一次,如果过滤两次后滤液仍然浑浊,需重新制作过滤器再次过滤。
(3)在进行蒸发操作时,为什么看到大量晶体析出时就停止加热?
提示:这样做的目的是防止持续加热造成固体飞溅。(4)在以上几步实验操作中,有几处用到了玻璃棒,分别起了什么作用?
提示:溶解、过滤、蒸发等操作中,都用到了玻璃棒。在溶解中,玻璃棒起加速溶解的作用;在过滤时,玻璃棒起引导液体流下的作用;蒸发时,可用玻璃棒搅拌防止液体暴沸,停止加热后,可用玻璃棒将晶体转移到指定的容器内,此时玻璃棒起转移固体的作用。1.(2012·漳州中考)粗盐提纯中,蒸发时不需要用到的仪器是( )
【解析】选C。蒸发操作时,滤液应在蒸发皿中加热,不需要用到的仪器是烧杯。2.在粗盐提纯的实验中,最后进行氯化钠溶液的蒸发时,一般有如下操作:①固定铁圈位置,②放置蒸发皿,③放置酒精灯,④加热并搅拌,⑤停止加热,借余热蒸干。正确的操作顺序是
( )
A.①②③④⑤ B.①③②④⑤
C.③①②④⑤ D.③②①④⑤
【解析】选C。在进行氯化钠溶液的蒸发操作时,安装仪器的顺序为由下向上,即先放置酒精灯,根据酒精灯的高度确定铁圈的高度,再放置蒸发皿。 3.(2013·金山区二模)粗盐提纯实验中,不合理的操作是
( )
A.用天平称得11.7 g食盐 B.用适量水充分溶解食盐
C.过滤除去不溶性杂质 D.加热至水分全部蒸干为止
【解析】选D。天平的精确度为0.1 g,A合理;溶解食盐时水的量不宜过多或过少,B合理;过滤能除去不溶性杂质,C正确;加热至大部分晶体析出时就可停止加热,利用余热蒸干,D不合理。4.小明在家做“粗盐提纯”的实验,下列对其做法的认识中,错误的是( )
A.将粗盐放入玻璃杯中加水溶解——粒子在不断运动
B.溶解时用筷子搅拌——加快溶解速度
C.用自制净水器过滤粗盐水——过滤后的溶液中溶质只有食盐
D.实验时不用一次性塑料杯或纸杯——保护环境要从身边小事做起【解析】选C。用自制净水器过滤粗盐水只是将溶液中的不溶性固体杂质除去,溶液中仍含有氯化镁、氯化钙等可溶性杂质。5.下列是关于“粗盐提纯”实验的几种说法,其中正确的是
( )
A.为加快过滤速度,应用玻璃棒不断搅拌过滤器内的液体
B.如果经两次过滤滤液仍浑浊,则应检查实验装置并分析原因
C.蒸发滤液时要用玻璃棒不断搅拌,用酒精灯持续加热直到蒸干为止
D.为了节约蒸发时间,蒸发皿里应盛满溶液【解析】选B。用玻璃棒在过滤器内搅拌很容易弄破漏斗中的滤纸,而使实验失败,A操作不正确;经两次过滤滤液仍浑浊,可能是滤纸破损或盛接滤液的烧杯不洁净等,应检查实验装置并分析原因,B是正确的;直到蒸发皿中的液体蒸干再停止加热,会导致灼热的氯化钠固体飞溅,造成事故,C操作不正确;倒入蒸发皿中溶液的量不能超过其容积的2/3,如过多,加热时易逬溅,D操作也不正确。6.(2013·咸宁中考)用下列实验操作可完成两个实验。甲实验为粗盐中难溶性杂质的去除,乙实验为配制溶质的质量分数为10%的氯化钠溶液。下列说法中,正确的是( )A.甲实验的步骤是①④⑤,其中去除杂质的关键步骤是蒸发
B.甲实验各步操作中,玻璃棒的作用都是相同的
C.乙实验若按照②③①的步骤进行操作,则配制的溶液浓度偏大(ρ水=1 g·cm-3)
D.乙实验中,若①所用的烧杯内壁沾有水,对配制的溶液浓度无影响【解析】选C。粗盐中难溶性杂质的去除的步骤是溶解、过滤、蒸发结晶,故步骤为①④⑤,其中去除杂质的关键步骤是过滤;甲实验各步操作中玻璃棒的作用不同,分别为搅拌、引流、搅拌;配制氯化钠溶液时,量取液体体积时,视线偏高,造成量取液体体积偏少,故导致配制的溶液浓度偏大;若①所用的烧杯内壁沾有水,造成溶剂的质量偏大,使配制的溶液浓度偏小。7.(2013·河北中考)某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50 g 5%的氯化钠溶液。
实验一:下图是同学们做粗盐提纯实验的操作示意图。 请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是 。
(2)操作⑥中的错误是 。
(3)粗盐提纯实验的操作顺序为(填操作序号) 、称量精盐并计算产率。(4)操作④中,当观察到 时,停止加热。
实验二:用提纯得到的精盐配制了50 g 5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有 (填序号)。
①氯化钠固体仍然不纯
②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数
④装瓶时,有少量溶液洒出【解析】实验一:(1)玻璃棒在溶解的过程中起到了搅拌加速溶解的作用。(2)过滤操作过程中应该用玻璃棒引流;操作⑥中的错误是没有用玻璃棒引流。(3)粗盐提纯实验的操作顺序为取粗盐进行称量,倒入烧杯中加水,搅拌溶解后过滤,最后蒸发结晶得到精盐,称量精盐,计算产率,故步骤为①⑤②③⑥④。(4)蒸发过程中,蒸发皿中出现较多固体时,停止加热,利用余热将剩余的少量液体蒸干。实验二:所配溶液的溶质质量分数偏小,原因可能是溶质少、溶剂多或两种情况同时存在,氯化钠固体仍然不纯,称得氯化钠比需要的少,称量时砝码端忘垫质量相同的纸片使得称出的氯化钠减少,量取水时,仰视读数,水的体积比需要的多,都会造成所得溶液中溶质的质量分数偏小。装瓶时,有少量溶液洒出,不影响溶液中溶质的质量分数。答案:实验一:(1)加速溶解
(2)未用玻璃棒引流
(3)①⑤②③⑥④
(4)出现较多固体
实验二:①②③8.(2012·自贡中考)氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程:(1)操作③中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是 (填序号)。(2)操作④中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到 等仪器。该操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌外,你认为还可采取 等措施。(3)实验结束后称量获得的精盐,并计算精盐的制得率,发现制得率较低,其可能原因是 (填序号)。
A.食盐没有全部溶解即过滤
B.蒸发时食盐飞溅剧烈
C.蒸发后,所得精盐很潮湿
D.器皿上沾有的精盐没全部转移到称量纸上【解析】(1)滤纸折叠过程中,不能出现缝隙,否则会使液体从缝隙流下,导致过滤失败;(2)为避免蒸发过程中食盐固体飞溅,还可以来回移动酒精灯或间隔性加热;
(3)食盐未全部溶解即过滤、蒸发时食盐飞溅、精盐没有全部转移称量,都会导致称量结果比理论值偏低,导致制得率偏低。精盐潮湿会导致称量结果偏大,导致制得率偏大。
答案:(1)D (2)蒸发皿 来回移动酒精灯
(3)A、B、D
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
