1.4气体 学案 (1)
文档属性
| 名称 | 1.4气体 学案 (1) |

|
|
| 格式 | zip | ||
| 文件大小 | 420.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 物理 | ||
| 更新时间 | 2016-12-27 00:00:00 | ||
图片预览



文档简介
1.4气体
学案
【学习目标导航】
目标定位
核心提示
1.知道什么是等温变化及描述气体的三个状态参量.2.通过实验探究得出玻意耳定律,并掌握定律的内容.学会利用等温变化的规律解决有关问题.3.明确p—V图象中,等温变化的图线及其物理意义.
重点:玻意耳定律的理解及应用.难点:等温变化的p—V图象的理解.考纲:气体实验定律
I
【课前基础梳理】
一、探究气体等温变化的规律
1.状态参量:研究气体的性质时,用________、_______、_________这三个物理量来描述气体的状态,这三个物理量被称为气体的状态参量.
2.等温变化:一定质量的气体,在________不变时其压强随体积发生的变化.
3.实验条件:在探究气体等温变化规律的实验过程中,必须保证气体的________、_______不变.
4.实验数据的收集:课本演示实验中,注射器内封闭气体的压强可以从仪器上方的_________读出,空气柱的长度可以在玻璃管侧的__________上读出.空气柱的长度l与______________的乘积就是它的体积V.
5.实验数据的处理:用p-V图象处理数据时,得到的图线是___________,用p-1/V图象处理数据时,得到的图线是过_____________,图线的斜率表示_____,且保持不变.
二、玻意耳定律
1.内容:一定_______的某种气体,在___________的情况下,压强p与体积V成________
2.公式:pV=C,或_______________.
三、气体等温变化的p-V图象
一定质量的气体发生等温变化时的p-V图象如图所示.图线的形状为___________由于它描述的是温度不变时的p-V关系,因此称它为_________一定质量的气体,不同温度下的等温线是________的.
四、实验注意事项
1.保证气体质量温度变,所以应该密封气体.并且不能用手触摸注射器,由于柱塞对气体做功,实验中应该缓慢推拉柱塞,目的是不改变气体的温度.
2.气体体积等于L与S的乘积,我们的目的是定性探究温度不变时,P与V的关系,V等于L与S的乘积,所以只要知道P与S的关系即可,没有必要求S.
3.
p1V1=p2V2计算时,等式两边相同的物理量单位可以不用国际单位,但必须一致.
【课堂互动探究】
一、封闭气体压强的计算
1.液体封闭气体的情况
(2)容器加速运动时封闭气体压强的计算
当容器加速运动时,通常选与气体相关联的液柱为研究对象进行受力分析,然后由牛顿第二定律列方程,求出封闭气体的压强.
2.活塞汽缸结构封闭气体的情况
通常以活塞(汽缸)为研究对象,利用动力学知识求解.
若活塞(汽缸)处于平衡状态,求解时列平衡方程即可;若处于加速状态,求解时列牛顿第二定律方程即可.
【典例1】求图中被封闭气体A的压强.其中(1)、(2)、(3)图中的玻璃管内都灌有水银,(4)图中的小玻璃管浸没在水中.大气压强p0=76
cmHg.(p0=1.01×105Pa,g=10
m/S2,ρ水=1×103kg/m3)
【自主解答】
【变式训练】如图所示,活塞的质量为m,缸套的质量为M,通过弹簧吊在天花板上,汽缸内封有一定质量的气体,缸套和活塞间无摩擦,活塞面积为S,大气压强为p0,则封闭气体的压强为( )
A.p=p0+
B.p=p0+
C.p=p0-
D.p=
二、对玻意耳定律的理解
1.成立条件:玻意耳定律p1V1=p2V2是实验定律.只有在气体质量一定、温度不变的条件下才成立.
2.恒量的定义:p1V1=p2V2=恒量C该恒量C与气体的种类、质量、温度有关,对一定质量的气体,温度越高,该恒量C越大.
3.等温变化的图象
(1)p-V图
①一定质量的气体,在温度不变的情况下p与V成反比,因此等温过程的p-V图象是双曲线的一支.
②一定质量的气体,温度越高,气体压强与体积的乘积必然越大,在p-V图上的等温线就越高,图中,T1(2)p-图
一定质量的气体,温度不变时,pV=恒量,p与V成反比,p与就成正比,在p-图上的等温线应是过原点的直线,直线的斜率即为p与V的乘积,斜率越大,pV乘积越大,温度就越高,图中,T2>T1.
4.利用玻意耳定律解题的基本思路
(1)确定研究对象:根据题意,确定所研究的气体.
(2)明确初、末状态:找出气体变化前后的初、末状态,并确定初、末状态的p、V值.
(3)列方程求解:根据玻意耳定律列方程,必要时还应由力学或几何知识列出辅助方程;求解时注意同一物理量的单位要统一.
(4)检验结果:有时列方程求解会得到两个结果,应通过合理性的检验决定取舍.
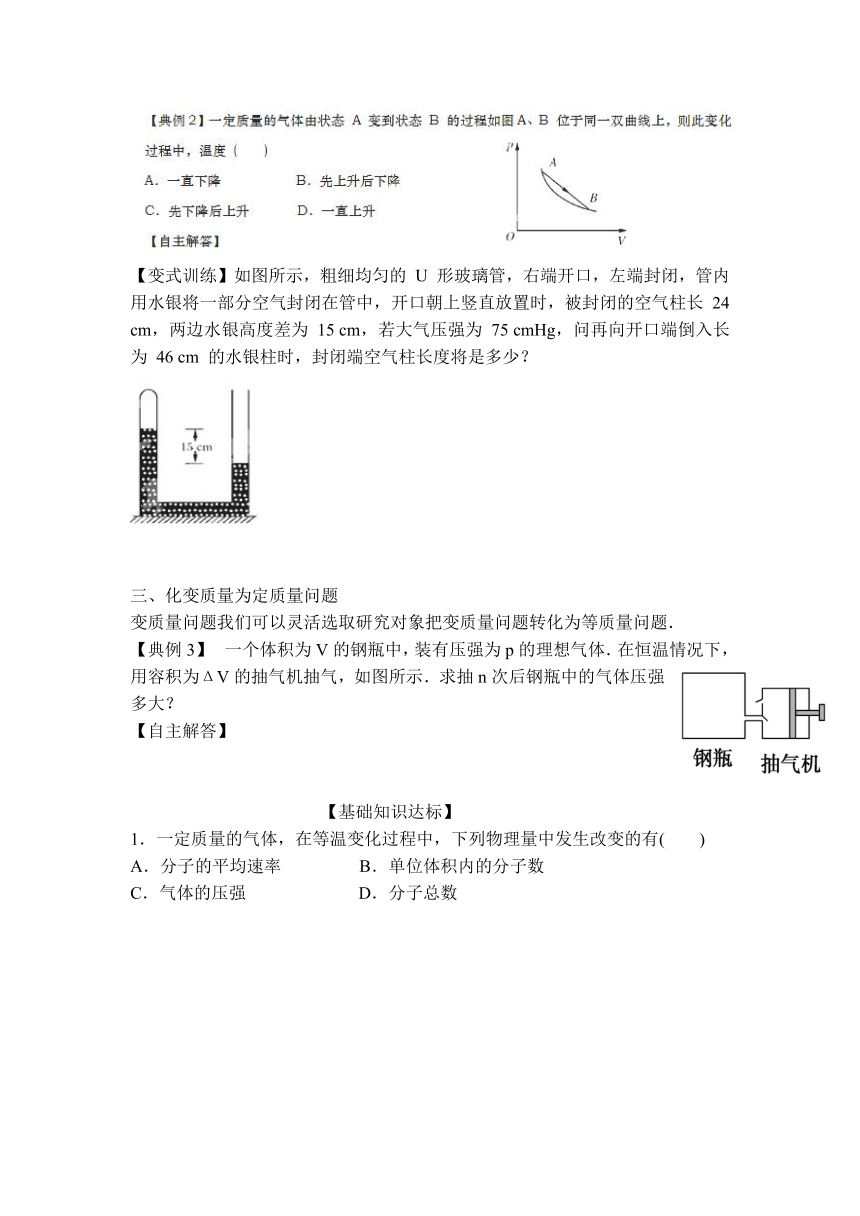
【变式训练】如图所示,粗细均匀的
U
形玻璃管,右端开口,左端封闭,管内用水银将一部分空气封闭在管中,开口朝上竖直放置时,被封闭的空气柱长
24
cm,两边水银高度差为
15
cm,若大气压强为
75
cmHg,问再向开口端倒入长为
46
cm
的水银柱时,封闭端空气柱长度将是多少?
三、化变质量为定质量问题
变质量问题我们可以灵活选取研究对象把变质量问题转化为等质量问题.
【典例3】 一个体积为V的钢瓶中,装有压强为p的理想气体.在恒温情况下,用容积为ΔV的抽气机抽气,如图所示.求抽n次后钢瓶中的气体压强多大?
【自主解答】
【基础知识达标】
1.一定质量的气体,在等温变化过程中,下列物理量中发生改变的有( )
A.分子的平均速率
B.单位体积内的分子数
C.气体的压强
D.分子总数
4.各种卡通形状的氢气球,受到孩子们的喜欢,特别是年幼的小孩,小孩一不小心松手,氢气球会飞向天空,上升到一定高度会胀破,是因为( )
A.球内氢气温度升高
B.球内氢气压强增大
C.球外空气压强减小
D.以上说法均不正确
5.如图水银柱上面封闭一段气体,管内外水银面高度差h=72cm,大气压强为76cmHg,下列说法正确的是( )
A.将管稍上提,h不变
B.将管稍上提,h变大
C.将管下插至管顶与管外水银面高度差为70cm时,管内外水银面高度差也是70cm
D.将管下插至C项所述位置时,管内外水银面高度差小于70cm
【知能巩固作业】
1.已知两端开口的“”型管,且水平部分足够长,一开始如右图所示,若将玻璃管稍微上提一点,或稍微下降一点时,被封闭的空气柱的长度分别会如何变化( )
A.变大;变小
B.变大;不变
C.不变;不变
D.不变;变大
2.在室内,将装有5atm的6L气体的容器的阀门打开后,从容器中逸出的气体相当于(设室内大气压强p0=1atm)( )
A.5atm,3L
B.1atm,24L
C.5atm,4.8L
D.1atm,30L
3.容积为20L的钢瓶内,贮有压强为1.5×107Pa的氧气.打开钢瓶的阀门,让氧气分装到容积为5L的氧气袋中(袋都是真空的),充气后的氧气袋中氧气压强都是1.0×106Pa,设充气过程不漏气,环境温度不变,则这瓶氧气最多可分装( )
A.60袋
B.56袋
C.50袋
D.40袋
5.如图所示,粗细均匀的弯曲玻璃管A、B两端开口,管内有一段水银柱,右管内气体柱长为39
cm,中管内水银面与管口A之间气体柱长为40
cm.先将B端封闭,再将左管竖直插入水银槽中,设整个过程温度不变,稳定后右管内水银面比中管内水银面高2
cm,(大气压强p0=76
cmHg)求:
(1)稳定后右管内的气体压强p;
(2)左管A端插入水银槽的深度h.
【课后小结提升】
第1节
气体的等温变化(答案)
第1节
气体的等温变化
【基础自主梳理】
【课堂互动探究】
【典例1】【解析】(1)pA=p0-ph=76
cmHg-10
cmHg=66
cmHg.
(2)pA=p0-ph=76
cmHg-10×sin30°
cmHg=71
cmHg.
(3)pB=p0+ph2=76
cmHg+10
cmHg=86
cmHg,
pA=pB-ph1=86
cmHg-5
cmHg=81
cmHg.
(4)pA=p0+ρ水gh
=1.01×105
Pa+1×103×10×(1.2-0.8)
Pa
=1.05×105
Pa
【答案】(1)66
cmHg
(2)71
cmHg
(3)86
cmHg
(4)1.05×105
Pa
【变式训练】【解析】选C.对气缸和活塞整体由平衡条件得F-(M+m)g=0,对活塞由平衡条件得,解得p=p0-,C正确.
【变式训练】【解析】倒入水银前对封闭端的气体有:V1=SL1=24S,p1=(75-15)
cmHg=60
cmHg倒入水银后,左端水银面将上升,右端水银面将下降,设左端水银面上升
x,则此时封闭端气柱长
L2=L1-x=24-x
此时两边水银面的高度差Δh2=46-(15+2x)=2L2-17此时封闭端气体的压强
p2=75+Δh2=58+2L2
根据玻意耳定律
p1V1=p2V2
得
24×60=L2×(58+2
L2)
即
L22+29L2-720=0
解得:L2=-45
cm(舍去),L2=16
cm.
【答案】16cm
【典例3】【解析】由于每一次抽气均为等温变化过程,可根据玻意耳定律得
第一次抽气:pV=p1(V+ΔV)
可得p1=
第二次抽气:p1V=p2(V+ΔV)
可得p2==p2
……则第n次抽气后气体压强为pn=pn.
【答案】pn
【知能巩固作业】1.【解析】选D.上提时空气柱压强不变,空气柱的长度不变;下降时空气柱压强变小,空气柱长度变大,所以D选项正确.
2.【解析】BC.当气体从阀门跑出时,温度不变,所以p1V1=p2V2,当p2=1atm时,得V2=30L,逸出气体30L-6L=24L,B正确.据p2(V2-V1)=p1V1′得V1′=4.8L,所以逸出的气体相当于5atm下的4.8L气体.C正确,故应选B、C.
3.【解析】选B.设可分装n袋,取全部气体研究,据玻意耳定律有:p1V=p2V+np2V0
1.5×107Pa×20L=1.0×106Pa×20L+n×1.0×106Pa×5L,解得n=56,B选项正确.
4.【解析】选B.题图中试管在水下某深度处于静止状态,浮力(等于排开水的重力)与试管重力相平衡.当试管中空气压强稍大些,即试管稍下移或向广口瓶中加水时,试管内的空气被压缩,浮力将减小,试管将下沉,在下沉的过程中,空气所受压强越来越大,浮力越来越小,试管将加速下沉.
5.(1)插入水银槽后右管内气体:由玻意耳定律得:
p0l0S=pS,
得p=78
cmHg.
(2)插入水银槽后左管压强:
p′=p+ρgΔh=80
cmHg,
左管内外水银面高度差h1==4
cm,
中、左管内气体由玻意耳定律得p0l=p′l′,代入数据解得l′=38
cm,
故左管插入水银槽深度h=l+-l′+h1=7
cm.
【答案】(1)78
cmHg (2)7
cm
学案
【学习目标导航】
目标定位
核心提示
1.知道什么是等温变化及描述气体的三个状态参量.2.通过实验探究得出玻意耳定律,并掌握定律的内容.学会利用等温变化的规律解决有关问题.3.明确p—V图象中,等温变化的图线及其物理意义.
重点:玻意耳定律的理解及应用.难点:等温变化的p—V图象的理解.考纲:气体实验定律
I
【课前基础梳理】
一、探究气体等温变化的规律
1.状态参量:研究气体的性质时,用________、_______、_________这三个物理量来描述气体的状态,这三个物理量被称为气体的状态参量.
2.等温变化:一定质量的气体,在________不变时其压强随体积发生的变化.
3.实验条件:在探究气体等温变化规律的实验过程中,必须保证气体的________、_______不变.
4.实验数据的收集:课本演示实验中,注射器内封闭气体的压强可以从仪器上方的_________读出,空气柱的长度可以在玻璃管侧的__________上读出.空气柱的长度l与______________的乘积就是它的体积V.
5.实验数据的处理:用p-V图象处理数据时,得到的图线是___________,用p-1/V图象处理数据时,得到的图线是过_____________,图线的斜率表示_____,且保持不变.
二、玻意耳定律
1.内容:一定_______的某种气体,在___________的情况下,压强p与体积V成________
2.公式:pV=C,或_______________.
三、气体等温变化的p-V图象
一定质量的气体发生等温变化时的p-V图象如图所示.图线的形状为___________由于它描述的是温度不变时的p-V关系,因此称它为_________一定质量的气体,不同温度下的等温线是________的.
四、实验注意事项
1.保证气体质量温度变,所以应该密封气体.并且不能用手触摸注射器,由于柱塞对气体做功,实验中应该缓慢推拉柱塞,目的是不改变气体的温度.
2.气体体积等于L与S的乘积,我们的目的是定性探究温度不变时,P与V的关系,V等于L与S的乘积,所以只要知道P与S的关系即可,没有必要求S.
3.
p1V1=p2V2计算时,等式两边相同的物理量单位可以不用国际单位,但必须一致.
【课堂互动探究】
一、封闭气体压强的计算
1.液体封闭气体的情况
(2)容器加速运动时封闭气体压强的计算
当容器加速运动时,通常选与气体相关联的液柱为研究对象进行受力分析,然后由牛顿第二定律列方程,求出封闭气体的压强.
2.活塞汽缸结构封闭气体的情况
通常以活塞(汽缸)为研究对象,利用动力学知识求解.
若活塞(汽缸)处于平衡状态,求解时列平衡方程即可;若处于加速状态,求解时列牛顿第二定律方程即可.
【典例1】求图中被封闭气体A的压强.其中(1)、(2)、(3)图中的玻璃管内都灌有水银,(4)图中的小玻璃管浸没在水中.大气压强p0=76
cmHg.(p0=1.01×105Pa,g=10
m/S2,ρ水=1×103kg/m3)
【自主解答】
【变式训练】如图所示,活塞的质量为m,缸套的质量为M,通过弹簧吊在天花板上,汽缸内封有一定质量的气体,缸套和活塞间无摩擦,活塞面积为S,大气压强为p0,则封闭气体的压强为( )
A.p=p0+
B.p=p0+
C.p=p0-
D.p=
二、对玻意耳定律的理解
1.成立条件:玻意耳定律p1V1=p2V2是实验定律.只有在气体质量一定、温度不变的条件下才成立.
2.恒量的定义:p1V1=p2V2=恒量C该恒量C与气体的种类、质量、温度有关,对一定质量的气体,温度越高,该恒量C越大.
3.等温变化的图象
(1)p-V图
①一定质量的气体,在温度不变的情况下p与V成反比,因此等温过程的p-V图象是双曲线的一支.
②一定质量的气体,温度越高,气体压强与体积的乘积必然越大,在p-V图上的等温线就越高,图中,T1
一定质量的气体,温度不变时,pV=恒量,p与V成反比,p与就成正比,在p-图上的等温线应是过原点的直线,直线的斜率即为p与V的乘积,斜率越大,pV乘积越大,温度就越高,图中,T2>T1.
4.利用玻意耳定律解题的基本思路
(1)确定研究对象:根据题意,确定所研究的气体.
(2)明确初、末状态:找出气体变化前后的初、末状态,并确定初、末状态的p、V值.
(3)列方程求解:根据玻意耳定律列方程,必要时还应由力学或几何知识列出辅助方程;求解时注意同一物理量的单位要统一.
(4)检验结果:有时列方程求解会得到两个结果,应通过合理性的检验决定取舍.
【变式训练】如图所示,粗细均匀的
U
形玻璃管,右端开口,左端封闭,管内用水银将一部分空气封闭在管中,开口朝上竖直放置时,被封闭的空气柱长
24
cm,两边水银高度差为
15
cm,若大气压强为
75
cmHg,问再向开口端倒入长为
46
cm
的水银柱时,封闭端空气柱长度将是多少?
三、化变质量为定质量问题
变质量问题我们可以灵活选取研究对象把变质量问题转化为等质量问题.
【典例3】 一个体积为V的钢瓶中,装有压强为p的理想气体.在恒温情况下,用容积为ΔV的抽气机抽气,如图所示.求抽n次后钢瓶中的气体压强多大?
【自主解答】
【基础知识达标】
1.一定质量的气体,在等温变化过程中,下列物理量中发生改变的有( )
A.分子的平均速率
B.单位体积内的分子数
C.气体的压强
D.分子总数
4.各种卡通形状的氢气球,受到孩子们的喜欢,特别是年幼的小孩,小孩一不小心松手,氢气球会飞向天空,上升到一定高度会胀破,是因为( )
A.球内氢气温度升高
B.球内氢气压强增大
C.球外空气压强减小
D.以上说法均不正确
5.如图水银柱上面封闭一段气体,管内外水银面高度差h=72cm,大气压强为76cmHg,下列说法正确的是( )
A.将管稍上提,h不变
B.将管稍上提,h变大
C.将管下插至管顶与管外水银面高度差为70cm时,管内外水银面高度差也是70cm
D.将管下插至C项所述位置时,管内外水银面高度差小于70cm
【知能巩固作业】
1.已知两端开口的“”型管,且水平部分足够长,一开始如右图所示,若将玻璃管稍微上提一点,或稍微下降一点时,被封闭的空气柱的长度分别会如何变化( )
A.变大;变小
B.变大;不变
C.不变;不变
D.不变;变大
2.在室内,将装有5atm的6L气体的容器的阀门打开后,从容器中逸出的气体相当于(设室内大气压强p0=1atm)( )
A.5atm,3L
B.1atm,24L
C.5atm,4.8L
D.1atm,30L
3.容积为20L的钢瓶内,贮有压强为1.5×107Pa的氧气.打开钢瓶的阀门,让氧气分装到容积为5L的氧气袋中(袋都是真空的),充气后的氧气袋中氧气压强都是1.0×106Pa,设充气过程不漏气,环境温度不变,则这瓶氧气最多可分装( )
A.60袋
B.56袋
C.50袋
D.40袋
5.如图所示,粗细均匀的弯曲玻璃管A、B两端开口,管内有一段水银柱,右管内气体柱长为39
cm,中管内水银面与管口A之间气体柱长为40
cm.先将B端封闭,再将左管竖直插入水银槽中,设整个过程温度不变,稳定后右管内水银面比中管内水银面高2
cm,(大气压强p0=76
cmHg)求:
(1)稳定后右管内的气体压强p;
(2)左管A端插入水银槽的深度h.
【课后小结提升】
第1节
气体的等温变化(答案)
第1节
气体的等温变化
【基础自主梳理】
【课堂互动探究】
【典例1】【解析】(1)pA=p0-ph=76
cmHg-10
cmHg=66
cmHg.
(2)pA=p0-ph=76
cmHg-10×sin30°
cmHg=71
cmHg.
(3)pB=p0+ph2=76
cmHg+10
cmHg=86
cmHg,
pA=pB-ph1=86
cmHg-5
cmHg=81
cmHg.
(4)pA=p0+ρ水gh
=1.01×105
Pa+1×103×10×(1.2-0.8)
Pa
=1.05×105
Pa
【答案】(1)66
cmHg
(2)71
cmHg
(3)86
cmHg
(4)1.05×105
Pa
【变式训练】【解析】选C.对气缸和活塞整体由平衡条件得F-(M+m)g=0,对活塞由平衡条件得,解得p=p0-,C正确.
【变式训练】【解析】倒入水银前对封闭端的气体有:V1=SL1=24S,p1=(75-15)
cmHg=60
cmHg倒入水银后,左端水银面将上升,右端水银面将下降,设左端水银面上升
x,则此时封闭端气柱长
L2=L1-x=24-x
此时两边水银面的高度差Δh2=46-(15+2x)=2L2-17此时封闭端气体的压强
p2=75+Δh2=58+2L2
根据玻意耳定律
p1V1=p2V2
得
24×60=L2×(58+2
L2)
即
L22+29L2-720=0
解得:L2=-45
cm(舍去),L2=16
cm.
【答案】16cm
【典例3】【解析】由于每一次抽气均为等温变化过程,可根据玻意耳定律得
第一次抽气:pV=p1(V+ΔV)
可得p1=
第二次抽气:p1V=p2(V+ΔV)
可得p2==p2
……则第n次抽气后气体压强为pn=pn.
【答案】pn
【知能巩固作业】1.【解析】选D.上提时空气柱压强不变,空气柱的长度不变;下降时空气柱压强变小,空气柱长度变大,所以D选项正确.
2.【解析】BC.当气体从阀门跑出时,温度不变,所以p1V1=p2V2,当p2=1atm时,得V2=30L,逸出气体30L-6L=24L,B正确.据p2(V2-V1)=p1V1′得V1′=4.8L,所以逸出的气体相当于5atm下的4.8L气体.C正确,故应选B、C.
3.【解析】选B.设可分装n袋,取全部气体研究,据玻意耳定律有:p1V=p2V+np2V0
1.5×107Pa×20L=1.0×106Pa×20L+n×1.0×106Pa×5L,解得n=56,B选项正确.
4.【解析】选B.题图中试管在水下某深度处于静止状态,浮力(等于排开水的重力)与试管重力相平衡.当试管中空气压强稍大些,即试管稍下移或向广口瓶中加水时,试管内的空气被压缩,浮力将减小,试管将下沉,在下沉的过程中,空气所受压强越来越大,浮力越来越小,试管将加速下沉.
5.(1)插入水银槽后右管内气体:由玻意耳定律得:
p0l0S=pS,
得p=78
cmHg.
(2)插入水银槽后左管压强:
p′=p+ρgΔh=80
cmHg,
左管内外水银面高度差h1==4
cm,
中、左管内气体由玻意耳定律得p0l=p′l′,代入数据解得l′=38
cm,
故左管插入水银槽深度h=l+-l′+h1=7
cm.
【答案】(1)78
cmHg (2)7
cm
