人教版化学选修四第三章第四节《 难溶电解质的溶解平衡》课件
文档属性
| 名称 | 人教版化学选修四第三章第四节《 难溶电解质的溶解平衡》课件 |

|
|
| 格式 | zip | ||
| 文件大小 | 145.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-01-07 00:00:00 | ||
图片预览







文档简介
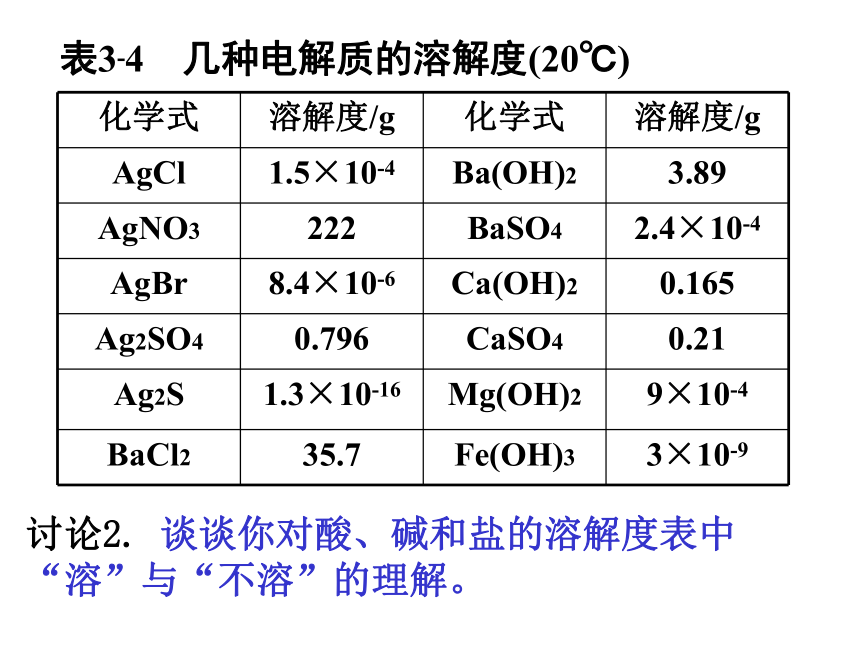
课件24张PPT。第三章 水溶液中的离子平衡第四节 难溶电解质的溶解平衡讨论:(1)如何判断某NaCl溶液是否已经达到饱和?实验:在饱和NaCl溶液中加入浓盐酸,观察。(2)饱和的NaCl溶液中NaCl是否不再溶解了呢?实验探究(3)NaCl能不能和盐酸反应? (4)要使NaCl饱和溶液中析出NaCl固体,还可以采取什么措施?加热浓缩、降温、加入钠离子浓度更大的其它溶液 可溶的电解质溶液中存在溶解平衡,难溶的电解质在水中是否也存在溶解平衡呢?一、Ag+和Cl-的反应真能进行到底吗?思考与交流:阅读课本P65~66 我们知道,溶液中有难溶于水的沉淀生成是离子反应发生的条件之一。例如,AgNO3溶液与NaCl溶液混合,生成白色沉淀AgCl:Ag++Cl-=AgCl↓,如果上述两种溶液是等物质的量浓度、等体积的,一般认为反应可以进行到底。一、Ag+和Cl-的反应真能进行到底吗?Ag+ + Cl-== AgCl↓讨论1.当AgNO3与NaCl反应生成难溶AgCl时,溶液中是否含有Ag+和Cl-? 表3-4 几种电解质的溶解度(20℃)讨论2. 谈谈你对酸、碱和盐的溶解度表中“溶”与“不溶”的理解。大于10 g,易溶
1 g~10 g,可溶
0.01 g~1 g,微溶
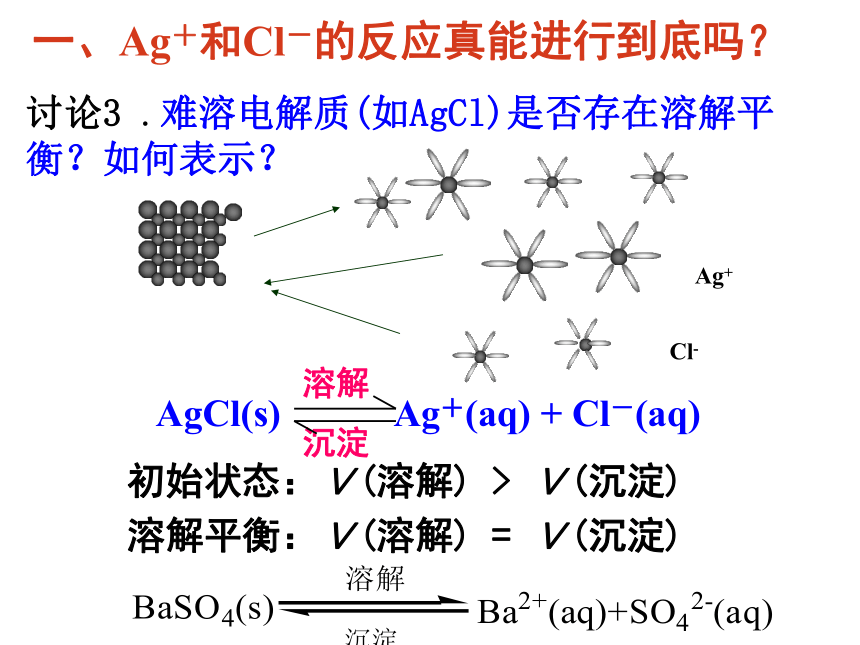
小于0.01 g,难溶20℃时,溶解度:讨论3 .难溶电解质(如AgCl)是否存在溶解平衡?如何表示? 一、Ag+和Cl-的反应真能进行到底吗?初始状态:V(溶解) > V(沉淀) 溶解平衡:V(溶解) = V(沉淀) 1、生成沉淀的离子反应能发生的原因生成物的溶解度很小2、溶解平衡的建立1)概念:
在一定条件下,难溶电解质电解质溶解成离子的速率等于离子重新结合成沉淀的速率,溶液中各离子的浓度保持不变的状态。(也叫沉淀溶解平衡)
2)表达式:练习:书写碘化银、氢氧化镁溶解平衡的表达式小结3、溶解平衡的特征逆、等、动、定、变4、生成难溶电解质的离子反应的限度难溶电解质的溶解度小于0.01g,离子反应生成难溶电解质,离子浓度小于1×10-5mol/L时,认为反应完全,但溶液中还有相应的离子。1. 石灰乳中存在下列平衡:
Ca(OH)2(s) Ca2+(aq)+2OH-(aq),加入下列溶液,可使Ca(OH)2减少的是
A、Na2CO3溶液 B、AlCl3溶液
C、NaOH溶液 D、CaCl2溶液课堂练习二、沉淀反应的应用1、沉淀的生成(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。(阅读课本P66~68)(2)方法①调节溶液pH值:如:工业原料氯化铵中混有氯化铁,加氨水调pH值至7-8Fe3+ + 3NH3?H2O=Fe(OH)3↓+3NH4+②加入沉淀剂:如沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂Cu2++S2-=CuS↓Hg2++S2-=HgS↓1、如果要除去某溶液中的SO42-,你选择加入钡盐还是钙盐?为什么?加入钡盐,因为BaSO4比CaSO4更难溶,使用钡盐可使SO42-沉淀更完全思考与交流2、以你现有的知识,你认为判断沉淀能否生成可从哪方面考虑?是否可能使要除去的离子通过沉淀反应全部除去?说明原因。从溶解度方面可判断沉淀能否生成不可能使要除去的离子通过沉淀完全除去2. 要除去MgCl2酸性溶液中少量的FeCl3,不宜选用的试剂是( ).
A、MgO B、MgCO3
C、NaOH D、Mg(OH)2课堂练习2、沉淀的溶解原理:设法不断移去溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动。(1) 生成弱电解质使沉淀溶解CaCO3(s) Ca2++CO32-+H+如:CaCO3、FeS、Al(OH)3、Cu(OH)2 、CaC2O4溶于强酸思考与交流用平衡移动的原理分析Mg(OH)2溶于盐酸和NH4Cl溶液的原因固体无明显溶解现象迅速溶解逐渐溶解(2) 加入某些盐促进沉淀溶解[实验3-3] 解释在溶液中存在Mg(OH)2的溶解平衡:加入NH4Cl时,解释2: NH4+水解,产生的H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解。Mg(OH)2(s) Mg2+(aq)+2OH-(aq)解释1: NH4+直接结合OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解。小结:难溶电解质溶解的规律不断减小溶解平衡体系中的相应离子,平衡就向沉淀溶解的方向移动,从而使沉淀溶解。 3. 牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:
Ca5(PO4)3OH(s) 5Ca2++3PO43-+OH- 进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是 .
。课堂练习 生成的有机酸能中和OH-,使平衡向脱矿方向移动,加速腐蚀牙齿 4.试用平衡移动原理解释下列事实
1)FeS不溶于水,但却能溶于稀盐酸中。
CaCO3难溶于稀硫酸,但却能溶于醋酸中。
2)分别用等体积的蒸馏水和0.010 mol/L硫酸洗涤
3)BaSO4沉淀,用水洗涤造成的BaSO4的损失量大于用稀硫酸洗涤造成的损失量。课堂练习3、沉淀的转化有白色沉淀析出白色沉淀转化为黄色黄色沉淀转化为黑色有白色沉淀析出白色沉淀变红褐色红褐色沉淀析出溶液褪至无色(实验3-4、3-5 沉淀转化)(1)沉淀转化的实质
沉淀转化的实质是沉淀溶解平衡移动。一般溶解度小的沉淀转化成溶解度更小的沉淀容易实现。在含有沉淀的溶液中加入另一种沉淀剂,使其与溶液中某一离子结合成更难溶的物质,引起一种沉淀转变成另一种沉淀的现象,叫沉淀的转化。(2)沉淀转化的应用
沉淀的转化在科研和生产中具有重要的应用价值。思考:如果将上述两个实验中沉淀生成和转化的操作步骤颠倒顺序,会产生什么结果?锅炉中水垢中含有CaSO4 ,可先用Na2CO3溶液处理,使 之转化为疏松、易溶于酸的CaCO3。CaSO4 SO42- + Ca2+ +
CO32-CaCO3②对一些自然现象的解释①锅炉除水垢CaSO4(s)+ Na2CO3 = CaCO3(s)+ Na2SO4【小结】:沉淀的生成、溶解、转化本质上都是沉淀溶解平衡的移动问题,其基本依据主要有:
①浓度:加水,平衡向溶解方向移动。
②温度:升温,多数平衡向溶解方向移动。
③加入相同离子,平衡向沉淀方向移动。
④加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子。使平衡向溶解的方向移动。
1 g~10 g,可溶
0.01 g~1 g,微溶
小于0.01 g,难溶20℃时,溶解度:讨论3 .难溶电解质(如AgCl)是否存在溶解平衡?如何表示? 一、Ag+和Cl-的反应真能进行到底吗?初始状态:V(溶解) > V(沉淀) 溶解平衡:V(溶解) = V(沉淀) 1、生成沉淀的离子反应能发生的原因生成物的溶解度很小2、溶解平衡的建立1)概念:
在一定条件下,难溶电解质电解质溶解成离子的速率等于离子重新结合成沉淀的速率,溶液中各离子的浓度保持不变的状态。(也叫沉淀溶解平衡)
2)表达式:练习:书写碘化银、氢氧化镁溶解平衡的表达式小结3、溶解平衡的特征逆、等、动、定、变4、生成难溶电解质的离子反应的限度难溶电解质的溶解度小于0.01g,离子反应生成难溶电解质,离子浓度小于1×10-5mol/L时,认为反应完全,但溶液中还有相应的离子。1. 石灰乳中存在下列平衡:
Ca(OH)2(s) Ca2+(aq)+2OH-(aq),加入下列溶液,可使Ca(OH)2减少的是
A、Na2CO3溶液 B、AlCl3溶液
C、NaOH溶液 D、CaCl2溶液课堂练习二、沉淀反应的应用1、沉淀的生成(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。(阅读课本P66~68)(2)方法①调节溶液pH值:如:工业原料氯化铵中混有氯化铁,加氨水调pH值至7-8Fe3+ + 3NH3?H2O=Fe(OH)3↓+3NH4+②加入沉淀剂:如沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂Cu2++S2-=CuS↓Hg2++S2-=HgS↓1、如果要除去某溶液中的SO42-,你选择加入钡盐还是钙盐?为什么?加入钡盐,因为BaSO4比CaSO4更难溶,使用钡盐可使SO42-沉淀更完全思考与交流2、以你现有的知识,你认为判断沉淀能否生成可从哪方面考虑?是否可能使要除去的离子通过沉淀反应全部除去?说明原因。从溶解度方面可判断沉淀能否生成不可能使要除去的离子通过沉淀完全除去2. 要除去MgCl2酸性溶液中少量的FeCl3,不宜选用的试剂是( ).
A、MgO B、MgCO3
C、NaOH D、Mg(OH)2课堂练习2、沉淀的溶解原理:设法不断移去溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动。(1) 生成弱电解质使沉淀溶解CaCO3(s) Ca2++CO32-+H+如:CaCO3、FeS、Al(OH)3、Cu(OH)2 、CaC2O4溶于强酸思考与交流用平衡移动的原理分析Mg(OH)2溶于盐酸和NH4Cl溶液的原因固体无明显溶解现象迅速溶解逐渐溶解(2) 加入某些盐促进沉淀溶解[实验3-3] 解释在溶液中存在Mg(OH)2的溶解平衡:加入NH4Cl时,解释2: NH4+水解,产生的H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解。Mg(OH)2(s) Mg2+(aq)+2OH-(aq)解释1: NH4+直接结合OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解。小结:难溶电解质溶解的规律不断减小溶解平衡体系中的相应离子,平衡就向沉淀溶解的方向移动,从而使沉淀溶解。 3. 牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:
Ca5(PO4)3OH(s) 5Ca2++3PO43-+OH- 进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是 .
。课堂练习 生成的有机酸能中和OH-,使平衡向脱矿方向移动,加速腐蚀牙齿 4.试用平衡移动原理解释下列事实
1)FeS不溶于水,但却能溶于稀盐酸中。
CaCO3难溶于稀硫酸,但却能溶于醋酸中。
2)分别用等体积的蒸馏水和0.010 mol/L硫酸洗涤
3)BaSO4沉淀,用水洗涤造成的BaSO4的损失量大于用稀硫酸洗涤造成的损失量。课堂练习3、沉淀的转化有白色沉淀析出白色沉淀转化为黄色黄色沉淀转化为黑色有白色沉淀析出白色沉淀变红褐色红褐色沉淀析出溶液褪至无色(实验3-4、3-5 沉淀转化)(1)沉淀转化的实质
沉淀转化的实质是沉淀溶解平衡移动。一般溶解度小的沉淀转化成溶解度更小的沉淀容易实现。在含有沉淀的溶液中加入另一种沉淀剂,使其与溶液中某一离子结合成更难溶的物质,引起一种沉淀转变成另一种沉淀的现象,叫沉淀的转化。(2)沉淀转化的应用
沉淀的转化在科研和生产中具有重要的应用价值。思考:如果将上述两个实验中沉淀生成和转化的操作步骤颠倒顺序,会产生什么结果?锅炉中水垢中含有CaSO4 ,可先用Na2CO3溶液处理,使 之转化为疏松、易溶于酸的CaCO3。CaSO4 SO42- + Ca2+ +
CO32-CaCO3②对一些自然现象的解释①锅炉除水垢CaSO4(s)+ Na2CO3 = CaCO3(s)+ Na2SO4【小结】:沉淀的生成、溶解、转化本质上都是沉淀溶解平衡的移动问题,其基本依据主要有:
①浓度:加水,平衡向溶解方向移动。
②温度:升温,多数平衡向溶解方向移动。
③加入相同离子,平衡向沉淀方向移动。
④加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子。使平衡向溶解的方向移动。
