【寒假作业】假期培优解决方案 寒假专题突破练 高二化学(鲁科版)专题7 化学平衡的图像分析
文档属性
| 名称 | 【寒假作业】假期培优解决方案 寒假专题突破练 高二化学(鲁科版)专题7 化学平衡的图像分析 |
|
|
| 格式 | zip | ||
| 文件大小 | 365.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-01-13 00:00:00 | ||
图片预览



文档简介
专题7 化学平衡的图像分析
题组1 速率-时间图像
1.汽车净化的主要原理为2NO(g)+2
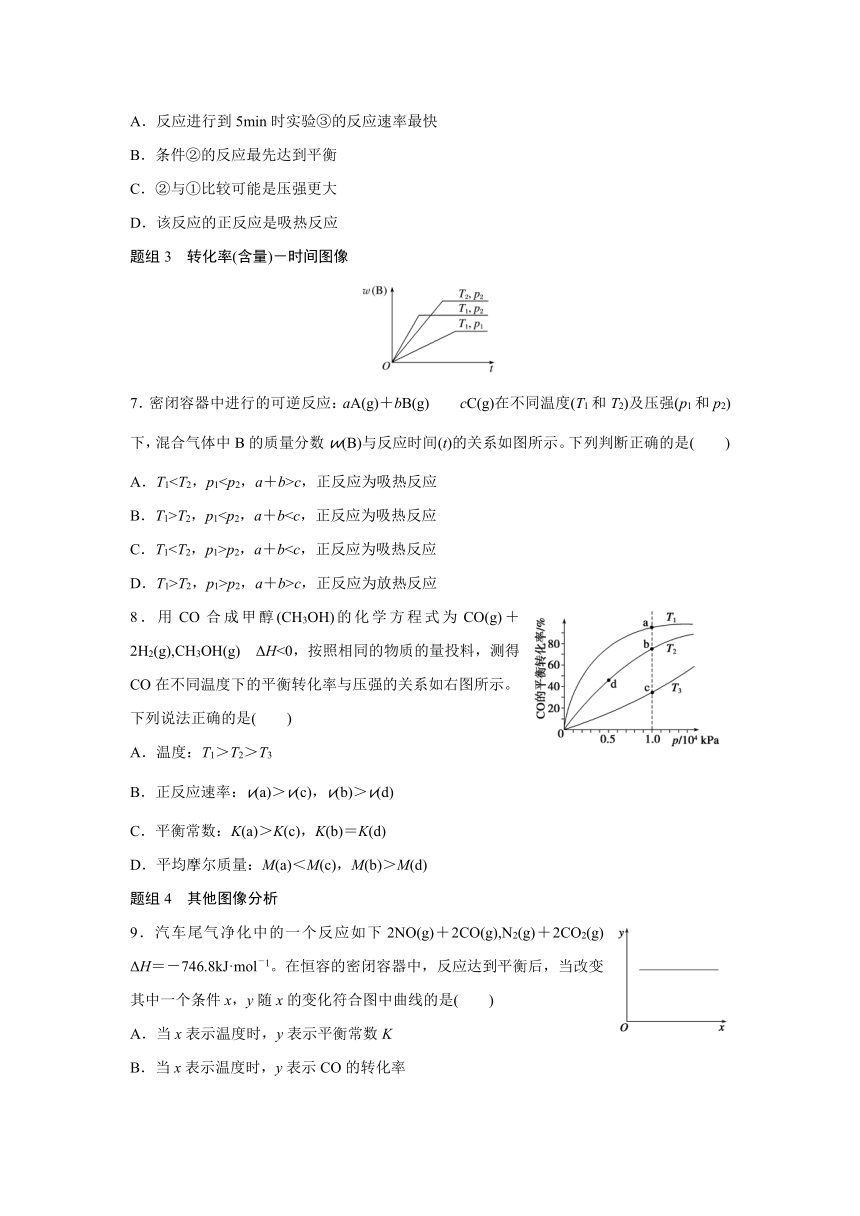
( http: / / www.21cnjy.com )CO(g)2CO2(g)+N2(g) ΔH<0。若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是( )
2.一密闭容器中发生反应:2SO2(g)+
( http: / / www.21cnjy.com )O2(g),2SO3(g) ΔH<0,如图表示该反应的速率(v)在某一时间内的变化。则下列时间段中,SO3的百分含量最高的是( )
A.t0→t1B.t2→t3C.t3→t4D.t5→t6
3.一定条件下,在某密闭容器中进行如下反应
( http: / / www.21cnjy.com ):mA(g)+nB(g),pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图所示,则对该反应的叙述正确的是( )
A.正反应是吸热反应
B.逆反应是放热反应
C.m+nD.m+n>p+q
题组2 物质的量(或浓度等)-时间图像
4.可逆反应aA(g)+bB(g),cC(g)+dD(g) ΔH,同时符合下列两图中各曲线的是( )
A.a+b>c+d T1>T2 ΔH>0
B.a+b>c+d T1C.a+bT2 ΔH>0
D.a+b5.将3molO2加入到V
( http: / / www.21cnjy.com )L的反应器中,在高温下放电,经t1s建立了平衡体系:3O2,2O3,此时测知O2的转化率为30%。下列图像能正确表示气体的物质的量(n)与时间(t)的关系的是( )
6.溶液中的反应X+Y,2Z分别在①、
( http: / / www.21cnjy.com )②、③三种不同实验条件下进行,它们的起始浓度为c(X)=c(Y)=0.100mol·L-1及c(Z)=0mol·L-1,反应物X的浓度随时间变化如图所示。②、③与①比较只有一个实验条件不同,下列说法不正确的是( )
A.反应进行到5min时实验③的反应速率最快
B.条件②的反应最先达到平衡
C.②与①比较可能是压强更大
D.该反应的正反应是吸热反应
题组3 转化率(含量)-时间图像
7.密闭容器中进行的可逆反应:aA
( http: / / www.21cnjy.com )(g)+bB(g)??cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是( )
A.T1c,正反应为吸热反应
B.T1>T2,p1C.T1p2,a+bD.T1>T2,p1>p2,a+b>c,正反应为放热反应
8.用CO合成甲醇(CH3OH)的
( http: / / www.21cnjy.com )化学方程式为CO(g)+2H2(g),CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示。下列说法正确的是( )
A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c),v(b)>v(d)
C.平衡常数:K(a)>K(c),K(b)=K(d)
D.平均摩尔质量:M(a)<M(c),M(b)>M(d)
题组4 其他图像分析
9.汽车尾气净化中的一个反应如下2NO(g)
( http: / / www.21cnjy.com )+2CO(g),N2(g)+2CO2(g) ΔH=-746.8kJ·mol-1。在恒容的密闭容器中,反应达到平衡后,当改变其中一个条件x,y随x的变化符合图中曲线的是( )
A.当x表示温度时,y表示平衡常数K
B.当x表示温度时,y表示CO的转化率
C.当x表示N2的物质的量时,y表示NO的转化率
D.当x表示NO的物质的量时,y表示平衡常数K
10.将I2溶于KI溶液中
( http: / / www.21cnjy.com ),能配制成浓度较大的碘水,主要是发生了反应:I2(aq)+I-(aq)??I(aq)。该平衡体系中,I的物质的量浓度与温度(T)的关系如图所示(曲线上的任何一点都代表平衡状态)。下列说法正确的是( )
A.反应速率:vM>vP
B.平衡常数:KNC.M、N两点相比,M点的[I-]大
D.Q点时,v正>v逆
11.一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(s)+CO(g),MgO(s)+CO2(g)+SO2(g)
ΔH>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
选项
x
y
A
温度
容器内混合气体的密度
B
CO的物质的量
CO2与CO的物质的量之比
C
SO2的浓度
平衡常数K
D
MgSO4的质量(忽略体积)
CO的转化率
题组5 图像题的综合应用
12.某温度时,在体积为
( http: / / www.21cnjy.com )5L的密闭容器中加入2molFe(s)与1molH2O(g),t1秒时,H2的物质的量为0.20mol,到第t2秒时恰好达到平衡,此时H2的物质的量为0.35mol。
(1)t1~t2这段时间内的化学反应速率v(H2)=________________。
(2)若继续加入2molFe(s),则
( http: / / www.21cnjy.com )逆反应速率________(填“增大”、“减小”或“不变”,下同),继续通入1molH2O(g),则正反应速率______________,H2的物质的量________。
(3)该反应的逆反应速率随时间变化的关
( http: / / www.21cnjy.com )系如图所示。t1时改变了某种条件,改变的条件可能是________________________、________________________(填写2项)。
13.已知NO2和N2O4可以相互转化:2NO2(g),N2O4(g)
ΔH<0。现将一定量NO2和N2O4的混合气体通入体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图所示:
(1)图中共有两条曲线X和Y,其中
( http: / / www.21cnjy.com )曲线________表示NO2浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是________。下列不能说明该反应已达到平衡状态的是________(填字母序号)。
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均相对分子质量不随时间变化而改变
(2)①前10min内用NO2表示的化学反应速率v(NO2)=________mol·L-1·min-1。
②0~15min,反应2NO2(g),N2O4(g)的平衡常数K(b)=____________。
(3)反应25min时,若只改变了某一个
( http: / / www.21cnjy.com )条件,使曲线发生如上图所示的变化,该条件可能是______________________(用文字表达);其平衡常数K(d)____K(b)(填“>”“=”或“<”)。
(4)若要达到使NO2(g)的百分含
( http: / / www.21cnjy.com )量与d点相同的化学平衡状态,在25min时还可以采取的措施是________________________(填字母序号)。
A.加入催化剂
B.缩小容器体积
C.升高温度
D.加入一定量的N2O4
答案解析
1.B [由于是绝热、恒容密闭体系,随着反应的进行,体系的温度升高,K不断减小,当K不变时,即温度保持不变,该反应达到平衡状态。]
2.A [分析图像可知,t2→t3是原
( http: / / www.21cnjy.com )平衡逆向移动后建立的平衡,SO3的百分含量降低;t3→t4和t2→t3两个时间段内,SO3的百分含量相同;t5→t6是平衡再次逆向移动后建立的平衡,SO3的百分含量再次降低。]
3.C [升高温度,由图像判断
( http: / / www.21cnjy.com )平衡向逆反应方向移动,则正反应为放热反应,逆反应为吸热反应,A、B不正确;增大压强,由图像判断平衡向逆反应方向移动,即逆反应气体体积减小,C正确,D不正确。]
4.B [图1中T2先达到平衡,则T2
( http: / / www.21cnjy.com )>T1,T2→T1时,生成物浓度增大,说明温度降低平衡向正反应方向移动,则正反应为放热反应,ΔH<0;图2中达到平衡(v正=v逆)后增大压强,v正>v逆,说明平衡向正反应方向移动,则该反应的正反应为气体分子数减小的反应,则a+b>c+d,B对。]
5.C [O2为反应物,随着反应的进行浓度
( http: / / www.21cnjy.com )逐渐减小;O3为生成物,随着反应的进行浓度逐渐增大。达到平衡时n(O2)=2.1
mol>n(O3)=0.6
mol。]
6.C [由图像看出,5
m
( http: / / www.21cnjy.com )in时,实验③中的c(X)变化量最大,A项正确;条件②的反应最先达到平衡,B项正确;②与①比较,只有反应速率不同,达到的平衡状态相同,可能为加入催化剂,在溶液中进行的反应,压强对反应速率没有影响,C项错误;条件③比条件①先达到平衡,说明条件③反应速率比条件①反应速率快,但反应的限度要大于条件①,可能为升温所致,则该反应为吸热反应,D项正确。]
7.B [当图像中有三个变量时,先确定
( http: / / www.21cnjy.com )一个量不变,再讨论另外两个量的关系,这叫做“定一议二”。解答该题要综合运用“定一议二”和“先拐先平”的原则。由(T1,p1)和(T1,p2)两条曲线可以看出:①温度相同(T1),但压强为p2时达到平衡所需的时间短,即反应速率大,所以p2>p1;②压强较大(即压强为p2)时对应的w(B)较大,说明增大压强平衡逆向移动,则a+bT2;②温度较高(即温度为T1)时对应的w(B)较小,说明升高温度平衡正向移动,故正反应为吸热反应。]
8.C [温度升高平衡逆向移动,CO的
( http: / / www.21cnjy.com )平衡转化率降低,所以温度为T19.D [温度升高,平衡向逆反应方向移动
( http: / / www.21cnjy.com ),平衡常数减小,CO的转化率降低,A、B错误;增大N2的浓度,平衡向逆反应方向移动,NO的转化率降低,C错误;平衡常数仅与温度有关,D正确。]
10.D [A项,温度越高,反应速率越大,v
( http: / / www.21cnjy.com )MKP;C项,M、N两点相比,M点温度低于N点温度,升温,平衡左移,所以M点的[I-]小。]
11.A [正反应为吸热反应,升高温
( http: / / www.21cnjy.com )度,平衡正向移动,容器内混合气体质量增加,而容器体积不变,故容器内混合气体的密度随温度升高而增大,A项正确;增加CO的物质的量,平衡虽正向移动,但因正反应为气体体积增大的反应,故达到新平衡时CO的转化率较原来的低,所以变小,B项错误;反应的平衡常数只与温度有关,因此SO2的浓度变大,反应平衡常数K不变,C项错误;MgSO4为固态,因此增加MgSO4的质量(忽略体积),其他反应物的浓度不变,平衡不移动,CO的转化率不变,D项错误。]
12.(1)mol·L-1·s-1 (2)
不变 增大 增大
(3)加入催化剂 升高温度
13.(1)X b和d B (2)①0.04 ②mol-1·L
(3)增大NO2的浓度 = (4)BD
解析 (1)在10
min内X曲线表示
( http: / / www.21cnjy.com )的物质浓度改变了0.4
mol·L-1,而Y曲线表示的物质浓度改变了0.2
mol·L-1,则X曲线表示NO2浓度随时间的变化;当曲线处于水平时(此时所表示的物质的浓度不变),表示反应已达平衡,故只有b、d两点处于平衡状态。该反应体系中全部是气体,其质量不变,体积不变,气体密度是恒量,与反应是否达到平衡无关。
(2)①v(NO2)==0.04
mol·L-1·min-1。
②平衡常数K(b)===mol-1·L。
(3)由曲线看出25
min时,NO2的浓度突然增大,可知改变的条件为增大NO2的浓度。温度不变,化学平衡常数不变。
(4)因在25
min时,增大了NO2的
( http: / / www.21cnjy.com )浓度,相当于增大了压强,平衡右移,d点时NO2的百分含量小于b点时NO2的百分含量,要使25
min时改变条件达到使NO2(g)的百分含量与d点相同的化学平衡状态,可加压或降温等,加入一定量的N2O4,也相当于加压。
题组1 速率-时间图像
1.汽车净化的主要原理为2NO(g)+2
( http: / / www.21cnjy.com )CO(g)2CO2(g)+N2(g) ΔH<0。若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是( )
2.一密闭容器中发生反应:2SO2(g)+
( http: / / www.21cnjy.com )O2(g),2SO3(g) ΔH<0,如图表示该反应的速率(v)在某一时间内的变化。则下列时间段中,SO3的百分含量最高的是( )
A.t0→t1B.t2→t3C.t3→t4D.t5→t6
3.一定条件下,在某密闭容器中进行如下反应
( http: / / www.21cnjy.com ):mA(g)+nB(g),pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图所示,则对该反应的叙述正确的是( )
A.正反应是吸热反应
B.逆反应是放热反应
C.m+n
题组2 物质的量(或浓度等)-时间图像
4.可逆反应aA(g)+bB(g),cC(g)+dD(g) ΔH,同时符合下列两图中各曲线的是( )
A.a+b>c+d T1>T2 ΔH>0
B.a+b>c+d T1
D.a+b
( http: / / www.21cnjy.com )L的反应器中,在高温下放电,经t1s建立了平衡体系:3O2,2O3,此时测知O2的转化率为30%。下列图像能正确表示气体的物质的量(n)与时间(t)的关系的是( )
6.溶液中的反应X+Y,2Z分别在①、
( http: / / www.21cnjy.com )②、③三种不同实验条件下进行,它们的起始浓度为c(X)=c(Y)=0.100mol·L-1及c(Z)=0mol·L-1,反应物X的浓度随时间变化如图所示。②、③与①比较只有一个实验条件不同,下列说法不正确的是( )
A.反应进行到5min时实验③的反应速率最快
B.条件②的反应最先达到平衡
C.②与①比较可能是压强更大
D.该反应的正反应是吸热反应
题组3 转化率(含量)-时间图像
7.密闭容器中进行的可逆反应:aA
( http: / / www.21cnjy.com )(g)+bB(g)??cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是( )
A.T1
B.T1>T2,p1
8.用CO合成甲醇(CH3OH)的
( http: / / www.21cnjy.com )化学方程式为CO(g)+2H2(g),CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示。下列说法正确的是( )
A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c),v(b)>v(d)
C.平衡常数:K(a)>K(c),K(b)=K(d)
D.平均摩尔质量:M(a)<M(c),M(b)>M(d)
题组4 其他图像分析
9.汽车尾气净化中的一个反应如下2NO(g)
( http: / / www.21cnjy.com )+2CO(g),N2(g)+2CO2(g) ΔH=-746.8kJ·mol-1。在恒容的密闭容器中,反应达到平衡后,当改变其中一个条件x,y随x的变化符合图中曲线的是( )
A.当x表示温度时,y表示平衡常数K
B.当x表示温度时,y表示CO的转化率
C.当x表示N2的物质的量时,y表示NO的转化率
D.当x表示NO的物质的量时,y表示平衡常数K
10.将I2溶于KI溶液中
( http: / / www.21cnjy.com ),能配制成浓度较大的碘水,主要是发生了反应:I2(aq)+I-(aq)??I(aq)。该平衡体系中,I的物质的量浓度与温度(T)的关系如图所示(曲线上的任何一点都代表平衡状态)。下列说法正确的是( )
A.反应速率:vM>vP
B.平衡常数:KN
D.Q点时,v正>v逆
11.一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(s)+CO(g),MgO(s)+CO2(g)+SO2(g)
ΔH>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
选项
x
y
A
温度
容器内混合气体的密度
B
CO的物质的量
CO2与CO的物质的量之比
C
SO2的浓度
平衡常数K
D
MgSO4的质量(忽略体积)
CO的转化率
题组5 图像题的综合应用
12.某温度时,在体积为
( http: / / www.21cnjy.com )5L的密闭容器中加入2molFe(s)与1molH2O(g),t1秒时,H2的物质的量为0.20mol,到第t2秒时恰好达到平衡,此时H2的物质的量为0.35mol。
(1)t1~t2这段时间内的化学反应速率v(H2)=________________。
(2)若继续加入2molFe(s),则
( http: / / www.21cnjy.com )逆反应速率________(填“增大”、“减小”或“不变”,下同),继续通入1molH2O(g),则正反应速率______________,H2的物质的量________。
(3)该反应的逆反应速率随时间变化的关
( http: / / www.21cnjy.com )系如图所示。t1时改变了某种条件,改变的条件可能是________________________、________________________(填写2项)。
13.已知NO2和N2O4可以相互转化:2NO2(g),N2O4(g)
ΔH<0。现将一定量NO2和N2O4的混合气体通入体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如图所示:
(1)图中共有两条曲线X和Y,其中
( http: / / www.21cnjy.com )曲线________表示NO2浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是________。下列不能说明该反应已达到平衡状态的是________(填字母序号)。
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均相对分子质量不随时间变化而改变
(2)①前10min内用NO2表示的化学反应速率v(NO2)=________mol·L-1·min-1。
②0~15min,反应2NO2(g),N2O4(g)的平衡常数K(b)=____________。
(3)反应25min时,若只改变了某一个
( http: / / www.21cnjy.com )条件,使曲线发生如上图所示的变化,该条件可能是______________________(用文字表达);其平衡常数K(d)____K(b)(填“>”“=”或“<”)。
(4)若要达到使NO2(g)的百分含
( http: / / www.21cnjy.com )量与d点相同的化学平衡状态,在25min时还可以采取的措施是________________________(填字母序号)。
A.加入催化剂
B.缩小容器体积
C.升高温度
D.加入一定量的N2O4
答案解析
1.B [由于是绝热、恒容密闭体系,随着反应的进行,体系的温度升高,K不断减小,当K不变时,即温度保持不变,该反应达到平衡状态。]
2.A [分析图像可知,t2→t3是原
( http: / / www.21cnjy.com )平衡逆向移动后建立的平衡,SO3的百分含量降低;t3→t4和t2→t3两个时间段内,SO3的百分含量相同;t5→t6是平衡再次逆向移动后建立的平衡,SO3的百分含量再次降低。]
3.C [升高温度,由图像判断
( http: / / www.21cnjy.com )平衡向逆反应方向移动,则正反应为放热反应,逆反应为吸热反应,A、B不正确;增大压强,由图像判断平衡向逆反应方向移动,即逆反应气体体积减小,C正确,D不正确。]
4.B [图1中T2先达到平衡,则T2
( http: / / www.21cnjy.com )>T1,T2→T1时,生成物浓度增大,说明温度降低平衡向正反应方向移动,则正反应为放热反应,ΔH<0;图2中达到平衡(v正=v逆)后增大压强,v正>v逆,说明平衡向正反应方向移动,则该反应的正反应为气体分子数减小的反应,则a+b>c+d,B对。]
5.C [O2为反应物,随着反应的进行浓度
( http: / / www.21cnjy.com )逐渐减小;O3为生成物,随着反应的进行浓度逐渐增大。达到平衡时n(O2)=2.1
mol>n(O3)=0.6
mol。]
6.C [由图像看出,5
m
( http: / / www.21cnjy.com )in时,实验③中的c(X)变化量最大,A项正确;条件②的反应最先达到平衡,B项正确;②与①比较,只有反应速率不同,达到的平衡状态相同,可能为加入催化剂,在溶液中进行的反应,压强对反应速率没有影响,C项错误;条件③比条件①先达到平衡,说明条件③反应速率比条件①反应速率快,但反应的限度要大于条件①,可能为升温所致,则该反应为吸热反应,D项正确。]
7.B [当图像中有三个变量时,先确定
( http: / / www.21cnjy.com )一个量不变,再讨论另外两个量的关系,这叫做“定一议二”。解答该题要综合运用“定一议二”和“先拐先平”的原则。由(T1,p1)和(T1,p2)两条曲线可以看出:①温度相同(T1),但压强为p2时达到平衡所需的时间短,即反应速率大,所以p2>p1;②压强较大(即压强为p2)时对应的w(B)较大,说明增大压强平衡逆向移动,则a+b
8.C [温度升高平衡逆向移动,CO的
( http: / / www.21cnjy.com )平衡转化率降低,所以温度为T1
( http: / / www.21cnjy.com ),平衡常数减小,CO的转化率降低,A、B错误;增大N2的浓度,平衡向逆反应方向移动,NO的转化率降低,C错误;平衡常数仅与温度有关,D正确。]
10.D [A项,温度越高,反应速率越大,v
( http: / / www.21cnjy.com )M
11.A [正反应为吸热反应,升高温
( http: / / www.21cnjy.com )度,平衡正向移动,容器内混合气体质量增加,而容器体积不变,故容器内混合气体的密度随温度升高而增大,A项正确;增加CO的物质的量,平衡虽正向移动,但因正反应为气体体积增大的反应,故达到新平衡时CO的转化率较原来的低,所以变小,B项错误;反应的平衡常数只与温度有关,因此SO2的浓度变大,反应平衡常数K不变,C项错误;MgSO4为固态,因此增加MgSO4的质量(忽略体积),其他反应物的浓度不变,平衡不移动,CO的转化率不变,D项错误。]
12.(1)mol·L-1·s-1 (2)
不变 增大 增大
(3)加入催化剂 升高温度
13.(1)X b和d B (2)①0.04 ②mol-1·L
(3)增大NO2的浓度 = (4)BD
解析 (1)在10
min内X曲线表示
( http: / / www.21cnjy.com )的物质浓度改变了0.4
mol·L-1,而Y曲线表示的物质浓度改变了0.2
mol·L-1,则X曲线表示NO2浓度随时间的变化;当曲线处于水平时(此时所表示的物质的浓度不变),表示反应已达平衡,故只有b、d两点处于平衡状态。该反应体系中全部是气体,其质量不变,体积不变,气体密度是恒量,与反应是否达到平衡无关。
(2)①v(NO2)==0.04
mol·L-1·min-1。
②平衡常数K(b)===mol-1·L。
(3)由曲线看出25
min时,NO2的浓度突然增大,可知改变的条件为增大NO2的浓度。温度不变,化学平衡常数不变。
(4)因在25
min时,增大了NO2的
( http: / / www.21cnjy.com )浓度,相当于增大了压强,平衡右移,d点时NO2的百分含量小于b点时NO2的百分含量,要使25
min时改变条件达到使NO2(g)的百分含量与d点相同的化学平衡状态,可加压或降温等,加入一定量的N2O4,也相当于加压。
