人教版九上化学第五单元课题1质量守恒定律课题公开课教学课件(33张PPT)
文档属性
| 名称 | 人教版九上化学第五单元课题1质量守恒定律课题公开课教学课件(33张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 241.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-01-16 00:00:00 | ||
图片预览








文档简介
课件33张PPT。课题1 质量守恒定律 1、通过实验探究认识质量守恒定律,了解常见化学反应中的质量关系;
2、能够从宏观和微观的角度理解质量守恒定律;
3、能够运用质量守恒定律解释一些实验现象。
拉瓦锡
参加化学反应的各物质的质量总和( )反应后生成的各物质的质量总和 等于二、猜想与假设实验设计操作要点:实验前后质量的称量
(要求称出实验药品及仪器的质量) 实验:分类研究1、反应前后都没有气体
2、只有气体生成
3、只有气体 参加4、反应前后都有气体三、验证与推理[实验要求]
(1)观察反应物的颜色、状态;
(2)混合后有什么现象?
(3)反应前和反应后物质的总质量有没有变化?
(3)将试管内的溶液倒入烧杯(试管仍留在烧杯中),使二者反应,观察实验现象产生蓝色沉淀(4)称量烧杯及烧杯内物质的总质量(1)将装有蓝色硫酸铜溶液的小试管放入
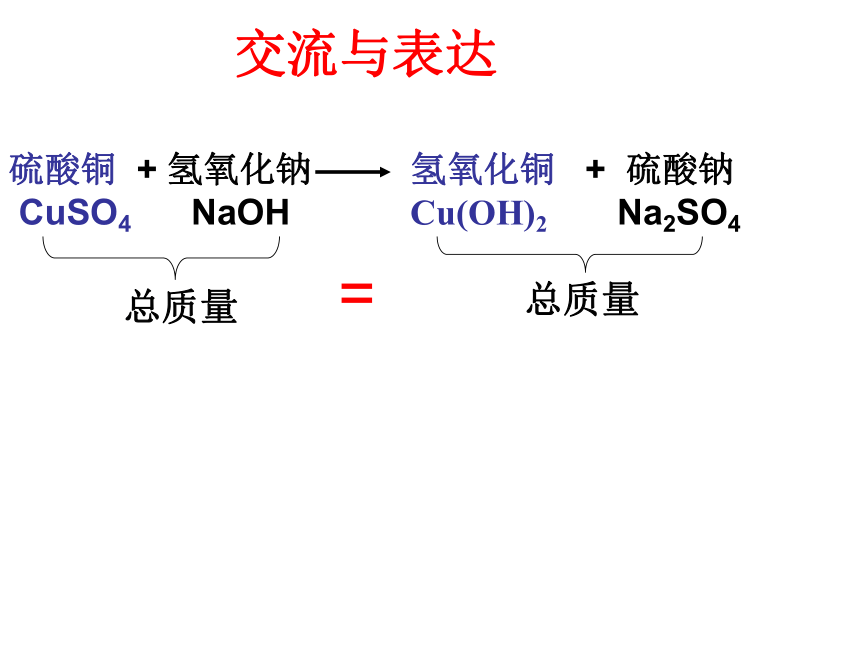
装有氢氧化钠溶液的烧杯中(2)称量烧杯及烧杯内物质的总质量(5)比较反应前后物质总质量的变化实验一:=总质量总质量交流与表达实验:分类研究2、只有气体生成
三、验证与推理实验二:
大理石与稀盐酸反应前后质量的变化 (1)将稀盐酸倒入锥形瓶中,将大理石放入气球中,然后将气球套在锥形瓶上 □ (2)称量锥形瓶及锥形瓶内物质的总质量 (3)将气球内的大理石倒入锥形瓶(气球仍套在锥形瓶上),使二者反应,观察实验现象(4)称量烧杯及烧杯内物质的总质量 (5)比较反应前后物质总质量的变化有气泡产生装置: 稀盐酸 + 碳酸钙 氯化钙+ 水 + 二氧化碳总质量总质量=交流与表达 HCl CaCO3 CaCl2 H2O CO2实验:分类研究3、只有气体 参加三、验证与推理 实验三:红磷燃烧前后质量的变化(1)在备好的锥形瓶中放一些红磷(2)称量锥形瓶及瓶内物质的总质量(3)点燃红磷,观察实验现象(4)称量锥形瓶及瓶内物质的总质量(冷却)(5)比较反应前后物质总质量的变化剧烈燃烧,放热,产生大量白烟(气球先膨胀后缩小)交流与表达实验:分类研究4、反应前后都有气体三、验证与推理实验四:蜡烛燃烧前后质量的变化交流与表达石蜡 + O2 CO2 + H2O总质量总质量=四、发现规律实验三:磷燃烧后有白烟生成即生成了五氧化二磷,但反应前后物质的总质量还是不变。实验二:大理石与稀盐酸反应,有气泡产生,反应前后物质的总质量仍然不变。实验一:无色的氢氧化钠溶液与蓝色的硫酸铜溶液反应,生成蓝色沉淀,反应前后物质的总质量不变。实验四:蜡烛燃烧后生成生成了二氧化碳和水,但反应前后物质的总质量还是不变。结论:反应前物质的总质量 反应后物质的总质量=一、质量守恒定律参加化学反应的各物质的质量总和,
等于生成物的各物质质量的总和。参加。(化学反应是按一定的质量比进行的,不一定所有的物质都参加了反应)质量守恒。(不是体积和分子个数的守恒)总和。(不能忽略反应物或生成物中的气体)例1,下列 变化可用质量守恒定律进行解释的是( )
10g水变成10g冰
物质升华时要吸收热量
9g水完全电解成1g氢气和8g氧气
5g糖放入25g水总得到30g糖水随堂练习:C2、实验表明,镁条在空气中燃烧后,生成物的质量比原来镁条的质量大.这一实验事实符合质量守恒定律吗?为什么?答:符合.因为有氧气参加了该反应. 为什么物质在发生化学变化前后,各物质的质量总和相等呢?分 子原 子新物质新分子H2O2H2O从分子、原子的角度解释质量守恒定律元素种类元素质量物质的总质量原子种类原子数目原子质量物质的种类分子的种类分子的数目可能改变质量守恒定律的应用1.根据质量守恒定律驳斥伪科学 “法轮功”邪教组织的头目李洪志说,他发功能使铝发生化学反应,变成铜和金,请你根据所学化学知识,指出这种说法违反科学之处。根据质量守恒定律,化学变化前后元素种类不变,没有金元素参加反应,不会生成金.2.推测一些物质的组成碳、氢氧.3.应用反应前后物质总质量不变解题
将27.5克高锰酸钾粉末加热,完全反应后 剩余固体物质的质量为17.9克,则生成氧气的质量为( )
A、9.6克 B、12.6克
C、6.6克 D、14.9克A4、推断某反应物或生成物的化学式 在化学反应2X2 +3Y2 = 2R 中,若用 X、Y表示R的化学式,其中正确的是( )
A、X2Y3 B、X2Y
C、X3Y4 D、XY2A 某化合物(X 表示其化学式)燃烧的化学方程式为2 X + 5 O2 = 4CO2 +2 H2O,则X的化学式( )
C2H4 B. CH4
C. C2H2 D. C6H6C课堂小结 1、通过实验探究从宏观角度得出并 验证了质量守恒定律;
2、用分子和原子的有关知识从微观角度分析了质量守恒的原因;
3、应用质量守恒定律解决一些问题
2、能够从宏观和微观的角度理解质量守恒定律;
3、能够运用质量守恒定律解释一些实验现象。
拉瓦锡
参加化学反应的各物质的质量总和( )反应后生成的各物质的质量总和 等于二、猜想与假设实验设计操作要点:实验前后质量的称量
(要求称出实验药品及仪器的质量) 实验:分类研究1、反应前后都没有气体
2、只有气体生成
3、只有气体 参加4、反应前后都有气体三、验证与推理[实验要求]
(1)观察反应物的颜色、状态;
(2)混合后有什么现象?
(3)反应前和反应后物质的总质量有没有变化?
(3)将试管内的溶液倒入烧杯(试管仍留在烧杯中),使二者反应,观察实验现象产生蓝色沉淀(4)称量烧杯及烧杯内物质的总质量(1)将装有蓝色硫酸铜溶液的小试管放入
装有氢氧化钠溶液的烧杯中(2)称量烧杯及烧杯内物质的总质量(5)比较反应前后物质总质量的变化实验一:=总质量总质量交流与表达实验:分类研究2、只有气体生成
三、验证与推理实验二:
大理石与稀盐酸反应前后质量的变化 (1)将稀盐酸倒入锥形瓶中,将大理石放入气球中,然后将气球套在锥形瓶上 □ (2)称量锥形瓶及锥形瓶内物质的总质量 (3)将气球内的大理石倒入锥形瓶(气球仍套在锥形瓶上),使二者反应,观察实验现象(4)称量烧杯及烧杯内物质的总质量 (5)比较反应前后物质总质量的变化有气泡产生装置: 稀盐酸 + 碳酸钙 氯化钙+ 水 + 二氧化碳总质量总质量=交流与表达 HCl CaCO3 CaCl2 H2O CO2实验:分类研究3、只有气体 参加三、验证与推理 实验三:红磷燃烧前后质量的变化(1)在备好的锥形瓶中放一些红磷(2)称量锥形瓶及瓶内物质的总质量(3)点燃红磷,观察实验现象(4)称量锥形瓶及瓶内物质的总质量(冷却)(5)比较反应前后物质总质量的变化剧烈燃烧,放热,产生大量白烟(气球先膨胀后缩小)交流与表达实验:分类研究4、反应前后都有气体三、验证与推理实验四:蜡烛燃烧前后质量的变化交流与表达石蜡 + O2 CO2 + H2O总质量总质量=四、发现规律实验三:磷燃烧后有白烟生成即生成了五氧化二磷,但反应前后物质的总质量还是不变。实验二:大理石与稀盐酸反应,有气泡产生,反应前后物质的总质量仍然不变。实验一:无色的氢氧化钠溶液与蓝色的硫酸铜溶液反应,生成蓝色沉淀,反应前后物质的总质量不变。实验四:蜡烛燃烧后生成生成了二氧化碳和水,但反应前后物质的总质量还是不变。结论:反应前物质的总质量 反应后物质的总质量=一、质量守恒定律参加化学反应的各物质的质量总和,
等于生成物的各物质质量的总和。参加。(化学反应是按一定的质量比进行的,不一定所有的物质都参加了反应)质量守恒。(不是体积和分子个数的守恒)总和。(不能忽略反应物或生成物中的气体)例1,下列 变化可用质量守恒定律进行解释的是( )
10g水变成10g冰
物质升华时要吸收热量
9g水完全电解成1g氢气和8g氧气
5g糖放入25g水总得到30g糖水随堂练习:C2、实验表明,镁条在空气中燃烧后,生成物的质量比原来镁条的质量大.这一实验事实符合质量守恒定律吗?为什么?答:符合.因为有氧气参加了该反应. 为什么物质在发生化学变化前后,各物质的质量总和相等呢?分 子原 子新物质新分子H2O2H2O从分子、原子的角度解释质量守恒定律元素种类元素质量物质的总质量原子种类原子数目原子质量物质的种类分子的种类分子的数目可能改变质量守恒定律的应用1.根据质量守恒定律驳斥伪科学 “法轮功”邪教组织的头目李洪志说,他发功能使铝发生化学反应,变成铜和金,请你根据所学化学知识,指出这种说法违反科学之处。根据质量守恒定律,化学变化前后元素种类不变,没有金元素参加反应,不会生成金.2.推测一些物质的组成碳、氢氧.3.应用反应前后物质总质量不变解题
将27.5克高锰酸钾粉末加热,完全反应后 剩余固体物质的质量为17.9克,则生成氧气的质量为( )
A、9.6克 B、12.6克
C、6.6克 D、14.9克A4、推断某反应物或生成物的化学式 在化学反应2X2 +3Y2 = 2R 中,若用 X、Y表示R的化学式,其中正确的是( )
A、X2Y3 B、X2Y
C、X3Y4 D、XY2A 某化合物(X 表示其化学式)燃烧的化学方程式为2 X + 5 O2 = 4CO2 +2 H2O,则X的化学式( )
C2H4 B. CH4
C. C2H2 D. C6H6C课堂小结 1、通过实验探究从宏观角度得出并 验证了质量守恒定律;
2、用分子和原子的有关知识从微观角度分析了质量守恒的原因;
3、应用质量守恒定律解决一些问题
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
