人教化学九年级下册 11.2 化学肥料 课件 (共36张PPT)
文档属性
| 名称 | 人教化学九年级下册 11.2 化学肥料 课件 (共36张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2017-02-01 00:00:00 | ||
图片预览










文档简介
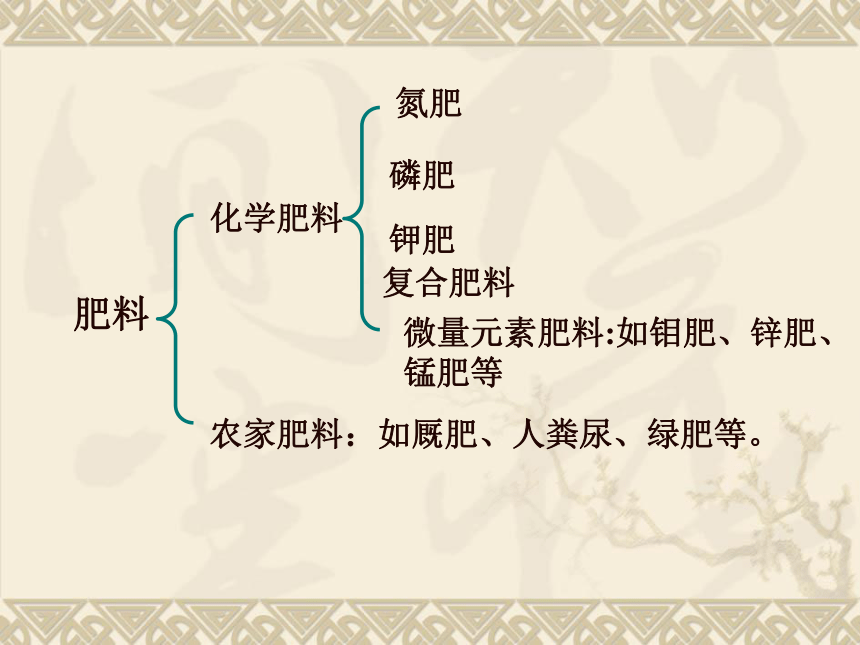
课件36张PPT。化学肥料 “庄稼一枝花,全靠肥当家”,你都认识哪些化学肥料?说说看:肥料化学肥料农家肥料:如厩肥、人粪尿、绿肥等。氮肥磷肥钾肥复合肥料微量元素肥料:如钼肥、锌肥、锰肥等一、氮肥2、氮肥的主要作用:
氮是作物体内蛋白质,核酸和叶绿素的重要成分,氮肥能促使作物的茎、叶生长茂盛,叶色浓绿。1、主要物质
尿素 铵盐(如:硝酸铵、硫酸铵、氯化铵、碳酸氢铵)
氨水 硝酸盐(如:硝酸钾、硝酸钙)3、缺乏时的表现
植株矮小瘦弱,叶片发黄,严重时叶脉呈淡棕色缺氮的棉花缺氮的玉米缺氮的马铃薯思考:我们知道空气中有大量的氮气,植物能不能吸收氮气并使之转化为氮肥呢?氮的固定:①空气中虽然含有大量的氮气,但植物通常只能吸收化合物中氮元素,不能直接吸收空气中的氮气。②根部有根瘤菌的豆科植物能把氮气转化为含氮的化合物而吸收。 ③将氮气转化为氮的化合物的方法叫做氮的固定。
自然界中氮的固定:
途径一:有根瘤菌的豆科植物途径二:雷雨肥庄稼铵盐的检验观察实验:
1、把氯化铵固体和氢氧化钙固体在研钵中混合研磨,闻放出的气味。
2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑
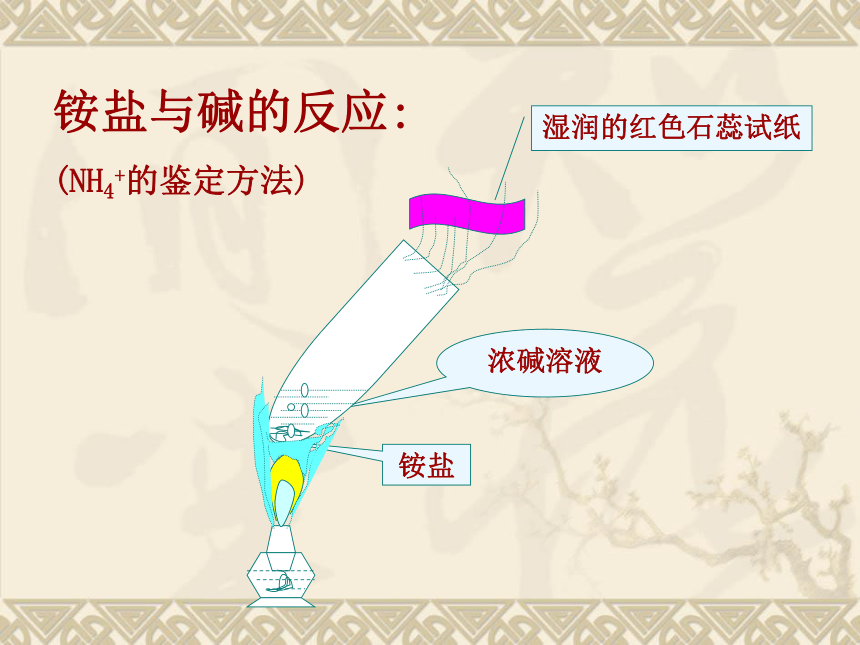
2、在一支试管中放入硫酸铵固体,加入氢氧化钠浓溶液并加热,在试管口放一片湿润的红色石蕊试纸,观察红色石蕊试纸颜色的改变情况。
(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑ 铵盐与碱的反应:
(NH4+的鉴定方法)湿润的红色石蕊试纸2NH4CI+Ca(OH)2=CaCI2+2H2O+2NH3↑铵盐和碱的反应原理:注意!施用铵盐时不要和碱性物质一起施用二、磷肥1、磷肥的主要作用:
磷肥能促进作物根系发达,增强抗寒抗旱能力,还能促进作物提早成熟,穗粒增多,籽粒饱满。
2、主要物质
磷矿粉、钙镁磷肥、过磷酸钙
3、缺乏时的表现
植株特别矮小,叶片呈暗绿色,并出现紫色
正常与缺磷的小麦和玉米正常与缺磷的水稻三、钾肥1、钾肥的主要作用
钾肥能促使作物生长健壮,茎秆粗硬 ,增强对病虫害和倒伏的抵抗能力,并能促进糖分和淀粉的生成。
2、主要物质
硫酸钾、氯化钾、碳酸钾
3、缺乏时的表现
茎干软弱,容易倒伏,叶片的边缘和尖端呈褐色,并焦枯。
棉花缺钾叶片棉花缺钾叶片土壤供钾水平不同对水稻的影响大豆缺钾叶片玉米缺钾症状缺钾使柑桔变小四、复合肥料同时含有两种或两种以上的营养元素,能同时均匀地供给多种养分,有效成分高。
如:磷酸二氢铵、磷酸氢二铵、硝酸钾等讨论:
化肥的使用是利大于弊还是弊大于利?
化学产品(如化肥、农药)的使用,对人类文明的发展作出了巨大贡献;
同时,不当使用也对人类健康和生态
环境产生危害。化肥与环境1. 有利:提高农作物产量
2. 不利:
(1)一些重金属元素、有毒有机物和放射性物质,污染土壤;
(2)因某些成分的积累、流失或变化,引起土壤酸化、水体的富营养化和大气环境的污染。
3. 注意合理使用农药和化肥。污染地下水源,污染生活饮用水。除了化肥之外,农药对农业的高产丰收也具有重要的作用。
但农药也是有毒物质,在杀灭病虫害的同时也带来了对自然环境的污染和对人体健康的危害。
P82 图11-12 农药在自然界中的转移对比化学肥料和农家肥料的一些特点五、农家肥P79 活动与探究白色
晶体白色
晶体灰白色
粉末灰白色
粉末白色
晶体白色
晶体明显刺鼻
氨味无气味无气味无气味无气味无气味溶于水溶于水不
溶于水溶于水溶于水部分
溶于水NH4HCO3常温下就能分解: NH4HCO3=NH3↑+H2O+CO2↑2. 有氨味有氨味无气味无气味无气味3、怎样区别氮肥、磷肥和钾肥3. 初步区分氮肥、磷肥和钾肥的步骤和方法:
(1)观察样品的颜色和气味:
颜色为灰白色粉末且不易溶于水的为磷肥;
有明显氨臭味的是碳酸氢铵。
(2)加熟石灰研磨:
能放出有刺激性气体的为铵态氮肥(铵盐)。二、化肥的简易鉴别1.氮肥的简易鉴别氮肥硫酸铵、氯化铵、硝酸铵尿素加碱有氨味无氨味加硝酸钡溶液硫酸铵氯化铵、硝酸铵有白色沉淀无白色沉淀加硝酸银溶液氯化铵硝酸铵有白色沉淀无白色沉淀常见化肥的种类与作用小结
氮是作物体内蛋白质,核酸和叶绿素的重要成分,氮肥能促使作物的茎、叶生长茂盛,叶色浓绿。1、主要物质
尿素 铵盐(如:硝酸铵、硫酸铵、氯化铵、碳酸氢铵)
氨水 硝酸盐(如:硝酸钾、硝酸钙)3、缺乏时的表现
植株矮小瘦弱,叶片发黄,严重时叶脉呈淡棕色缺氮的棉花缺氮的玉米缺氮的马铃薯思考:我们知道空气中有大量的氮气,植物能不能吸收氮气并使之转化为氮肥呢?氮的固定:①空气中虽然含有大量的氮气,但植物通常只能吸收化合物中氮元素,不能直接吸收空气中的氮气。②根部有根瘤菌的豆科植物能把氮气转化为含氮的化合物而吸收。 ③将氮气转化为氮的化合物的方法叫做氮的固定。
自然界中氮的固定:
途径一:有根瘤菌的豆科植物途径二:雷雨肥庄稼铵盐的检验观察实验:
1、把氯化铵固体和氢氧化钙固体在研钵中混合研磨,闻放出的气味。
2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑
2、在一支试管中放入硫酸铵固体,加入氢氧化钠浓溶液并加热,在试管口放一片湿润的红色石蕊试纸,观察红色石蕊试纸颜色的改变情况。
(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑ 铵盐与碱的反应:
(NH4+的鉴定方法)湿润的红色石蕊试纸2NH4CI+Ca(OH)2=CaCI2+2H2O+2NH3↑铵盐和碱的反应原理:注意!施用铵盐时不要和碱性物质一起施用二、磷肥1、磷肥的主要作用:
磷肥能促进作物根系发达,增强抗寒抗旱能力,还能促进作物提早成熟,穗粒增多,籽粒饱满。
2、主要物质
磷矿粉、钙镁磷肥、过磷酸钙
3、缺乏时的表现
植株特别矮小,叶片呈暗绿色,并出现紫色
正常与缺磷的小麦和玉米正常与缺磷的水稻三、钾肥1、钾肥的主要作用
钾肥能促使作物生长健壮,茎秆粗硬 ,增强对病虫害和倒伏的抵抗能力,并能促进糖分和淀粉的生成。
2、主要物质
硫酸钾、氯化钾、碳酸钾
3、缺乏时的表现
茎干软弱,容易倒伏,叶片的边缘和尖端呈褐色,并焦枯。
棉花缺钾叶片棉花缺钾叶片土壤供钾水平不同对水稻的影响大豆缺钾叶片玉米缺钾症状缺钾使柑桔变小四、复合肥料同时含有两种或两种以上的营养元素,能同时均匀地供给多种养分,有效成分高。
如:磷酸二氢铵、磷酸氢二铵、硝酸钾等讨论:
化肥的使用是利大于弊还是弊大于利?
化学产品(如化肥、农药)的使用,对人类文明的发展作出了巨大贡献;
同时,不当使用也对人类健康和生态
环境产生危害。化肥与环境1. 有利:提高农作物产量
2. 不利:
(1)一些重金属元素、有毒有机物和放射性物质,污染土壤;
(2)因某些成分的积累、流失或变化,引起土壤酸化、水体的富营养化和大气环境的污染。
3. 注意合理使用农药和化肥。污染地下水源,污染生活饮用水。除了化肥之外,农药对农业的高产丰收也具有重要的作用。
但农药也是有毒物质,在杀灭病虫害的同时也带来了对自然环境的污染和对人体健康的危害。
P82 图11-12 农药在自然界中的转移对比化学肥料和农家肥料的一些特点五、农家肥P79 活动与探究白色
晶体白色
晶体灰白色
粉末灰白色
粉末白色
晶体白色
晶体明显刺鼻
氨味无气味无气味无气味无气味无气味溶于水溶于水不
溶于水溶于水溶于水部分
溶于水NH4HCO3常温下就能分解: NH4HCO3=NH3↑+H2O+CO2↑2. 有氨味有氨味无气味无气味无气味3、怎样区别氮肥、磷肥和钾肥3. 初步区分氮肥、磷肥和钾肥的步骤和方法:
(1)观察样品的颜色和气味:
颜色为灰白色粉末且不易溶于水的为磷肥;
有明显氨臭味的是碳酸氢铵。
(2)加熟石灰研磨:
能放出有刺激性气体的为铵态氮肥(铵盐)。二、化肥的简易鉴别1.氮肥的简易鉴别氮肥硫酸铵、氯化铵、硝酸铵尿素加碱有氨味无氨味加硝酸钡溶液硫酸铵氯化铵、硝酸铵有白色沉淀无白色沉淀加硝酸银溶液氯化铵硝酸铵有白色沉淀无白色沉淀常见化肥的种类与作用小结
同课章节目录
